Ионообменное концентрирование неорганических анионов из водных растворов
Автор: Бондарева Л.П., Кунахова Е.Н., Никулина А.В.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Фундаментальная и прикладная химия, химическая технология
Статья в выпуске: 4 (70), 2016 года.
Бесплатный доступ
Мониторинг природных вод в настоящее время - трудоемкий процесс, на точность которого влияет множество факторов: состав воды, наличие примесей и «мешающих» компонентов - поэтому процесс пробоподготовки воды достаточно часто включает в себя стадию концентрирования и выделения определяемых ионов. Наиболее универсальным, эффективным и по-этому часто применяемым методом концентрирования неорганических анионов из водных растворов является ионообменное сорбционное концентрирование, которое при различном исходном составе природных вод приводит к требуемому для иден-тификации и количественного определения содержанию анионов в элюате. В работе сравнены сорбционные характеристики высокоосновных анионообменных смол АВ-17 и Purolite А430 по отношению к хлорид-, нитрат- и сульфат-ионам. Значения констант протолиза обоих ионообменников АВ 17 и Purolite A430 совпадают и равны 0,037 ± 0,002. Величина полной обмен-ной емкости (ПОЕ) Purolite A430 составила 4,3 ммоль/г, АВ 17 - 3,4 ммоль/г. Изучаемые ионообменники имеют одинаковый тип ионогенных групп - четвертичные аммониевые, но их количество различается и выше в Purolite A430, соответственно количество поглощенных анионов для этого ионита выше. Значения динамической обменной емкости (ДОЕ) ионита Purolite A430 выше, чем у АВ-17 и равны 1,48 ± 0,03 ммоль/дм3 для хлорид-иона, 1,50 ± 0,03 ммоль/дм3 для нитрат-иона,1,62 ± 0,03 ммоль/дм3 сульфат-иона. Полученные значения ПОЕ и ДОЕ анионообменных смол Purolite А430 и АВ-17 и характеристики индивидуальной сорбции хлорид-, нитрат-, сульфат-ионов показали преимущество Purolite в концентрировании анионов. Уста-новлено, что при сорбции анионов из тройных растворов на Purolite A430 времена сорбции существенно различаются, а на анионообменнике АВ-17 близки, что доказывает возможность количественного разделения и концентрирования рассмотрен-ных анионов на смоле Purolite A430..
Анионы, ионообменная смола, полная обменная емкость, динамическая обменная емкость, выходная кривая сорбции, концентрирование, количественное определение
Короткий адрес: https://sciup.org/140229654
IDR: 140229654 | DOI: 10.20914/2310-1202-2016-4-222-227
Ion-exchange concentration of inorganic anions from aqueous solution
Monitoring of natural waters in the present time - consuming process, the accuracy of which is influenced by many factors: the composition of water, the presence of impurities and "interfering" components. The water sample preparation process includes the step of concentration and separation of ions determined. The most versatile, efficient, and frequently used method is the concentration of inorganic anions from aqueous solutions by ion exchanger, which can optimize the composition of water to the optimal for identification and quantitative determination of anions. The characteristics of sorption chloride, nitrate and sulfate ions of basic anion exchange resin AВ-17 and Purolite A430 were compared in the article. The constants of protolysis of ion exchangers both AB 17 and Purolite A430 are the same and equal 0.037 ± 0,002. The value of total capacity (POE) Purolite A430 was 4.3 mmol/g, AB 17 - 3.4 mmol/g. The studied ion exchangers have the same type of ionic groups - quaternary ammonium, but their number and denotes differ. The number of quaternary ammonium groups is higher in Purolite A430, respectively the number of absorbed anions of these ion exchanger is higher. The values of dynamic exchange capacity (DOE) of ion exchanger Purolite A430 is higher than these values of AB-17 and equal to 1.48 ± 0.03 mmol / dm3 for chloride ion, 1.50 ± 0.03 mmol / dm3 for nitrate ion, 1.62 ± 0.03 mmol / dm3 for sulfate ion. The values ??of the POE and DOE of anion-exchange resins Purolite A430 and AV-17 and the characteristics of the individual sorption of chloride, nitrate, sulfate ions showed an advantage of the Purolite for the concentrationing of anions. It is found that times of anions sorption from triple-anion solutions by Purolite A430 are significantly different for different anions, and these times are close for anion-exchanger AV-17. It proves the possibility of quantitative separation and concentration by anion-exchanger Purolite A430
Текст научной статьи Ионообменное концентрирование неорганических анионов из водных растворов
Анализ природных вод – это одно из наиболее развивающихся направлений химического анализа, проводимого лабораториями. От качества природной воды зависит не только здоровье живых организмов, населяющих ее, но и людей, а также деятельность предприятий, которые используют природную воду в технологических процессах. Эффективный количественный химический анализ природных и сточных вод на сегодняшний день является актуальным
направлением аналитической химии, позволяет оперативно и достаточно точно проводить оценку не только качества природных и технологических вод, но и являться несомненно важным критерием при оценке состояния экосистемы данной местности в целом.
Мониторинг природных вод в настоящее время – трудоемкий процесс, на точность которого влияет множество факторов, в том числе и входящие в состав воды примеси – «мешающие» компоненты. Еще одной проблемой при проведении
анализа воды является малое содержание определяемых ионов при одновременном присутствии значительных количеств макропримесей. Поэтому процесс пробоподготовки воды достаточно часто включает в себя стадию концентрирования и выделения определяемых ионов. Наиболее универсальным, эффективным и поэтому часто применяемым методом концентрирования неорганических анионов из водных растворов является ионообменное сорбционное концентрирование, которое при различном исходном составе природных вод приводит к требуемому для идентификации и количественного определения содержанию анионов в элюате.
Таким образом, целью работы стало установление эффективных условий концентрирования и разделения анионов из водных растворов на анионообменных смолах.
Объекты и методы исследования
Концентрирование хлорид-, нитрат-, сульфат-ионов из водных сред проводили на ионообменных смолах АВ-17 и Purolite А430. Анионит АВ-17 является монофункциональным высокоосновным сорбентом полимериза-ционного типа, обладает хорошей осмотической стабильностью, высокой химической стойкостью к воздействию щелочей, кислот, окислителей; нерастворим в воде и органических растворителях. Широко применяется для умягчения и обессоливания воды, а также очистки оборотных и сточных вод [1]. Анионит Purolite А430 – гелевый сорбент с полистироль-ной матрицей и функциональными группами четвертичного аммония [2] – является новым промышленным сорбентом, применяемым для снижения уровня желчных кислот и уменьшения содержания холестерина в крови.
Кондиционирование и перевод в рабочую форму анионообменников проводили последовательной обработкой раствором гидроксида натрия с концентрацией 0,5 моль/дм3, затем дистиллированной водой, затем раствором соляной кислоты с концентрацией 0,5 моль/дм3, и снова дистиллированной водой. Каждый реагент брался в двух-, трехкратном избытке по сравнению с содержанием обменных групп в обрабатываемом образце . Таким образом, получали анионообменники в рабочей ОН-форме.
Для определения констант кислотно-основного равновесия и полной обменной емкости (ПОЕ) анионообменников применяли титрование образцов OH-формы методом отдельных навесок в статических условиях. В мерные колбы вводили возрастающие объемы 0,05 моль/дм3 раствора НСl и по 0,100 г. исследуемого сорбента
(в расчете на сухое вещество). Равновесие в растворе устанавливалось в течение 20 дней при условии неизменного рН внешнего раствора. При расчете обменной емкости положение скачка титрования устанавливали в дифференциальных координатных осях.
Для проведения сорбции в динамических условиях 10,00 г. ионообменника в рабочей форме помещали в колонку с внутренним диаметром 13 мм и высотой 30 см и оставляли на несколько часов для набухания. После этого через колонку пропускали раствор каждого из определяемых ионов с концентрацией 0,03 моль/дм3 со скоростью 0,033 см3/с или смесь анионов с суммарной концентрацией 0,1 моль/дм3 и получали выходные кривые ионного обмена. Для этого через определенные промежутки времени проводили отбор проб фильтрата на выходе из колонки и определяли в них концентрацию определяемых ионов.
Определение концентраций хлорид-ионов проводили методом аргентометрического титрования, нитрат-ионов – потенциометрического титрования с ион-селективным электродом. Концентрацию сульфат-ионов определяли осаждением слаборастворимого сульфата бария с последующим растворением осадка в растворе трилона Б в аммиачной среде и титровании избытка трилона Б раствором, содержащим ионы магния, с эриохромовым черным Т в качестве индикатора [3]. Фильтрацию раствора через сорбент прекращали, когда содержание насыщающего иона в фильтрате становилось равным его содержанию в исходном растворе.
Динамическую обменную емкость (ДОЕ) анионообменников по исследуемым ионам рассчитывали по формуле:
Z ( С о -С ) V
ДОЕ= , m где Со – исходная концентрация хлорид-ионов, моль/дм3; С– концентрация хлорид-ионов в каждой пробе фильтрата, моль/дм3; V – объем раствора хлорида натрия, пропущенного через слой сорбента до «проскока» поглощаемого иона, дм3; m– масса анионобменника в слое, г.
Для исследования сорбции анионов из раствора, содержащего NaCl, NaNO 3 , Na 2 SO 4 с концентрацией каждого компонента 0,033 моль/дм3, смесь пропускали через колонку со скоростью, равной 0,015 см3/с, отбирали пробы фильтрата и определяли в них концентрации анионов описанными выше методами.
Определение концентрации анионов в фильтрате и элюате многокомпонентного раствора проводили методом капиллярного электрофореза. Система капиллярного электрофореза «КАПЕЛЬ-104Т» управляется с лицевой панели с помощью встроенной клавиатуры и дисплея через систему меню, результат анализа выводится на внешний компьютер. Обработка результатов проводится с помощью программного обеспечения «МультиХром», которое, кроме управления прибором, позволяет собирать и обрабатывать электрофоретические данные.
Обсуждение результатов
-
1.1 Определение полной обменной емкости и констант кислотно-основного равновесия анионообмеников
Анионообменник АВ-17 давно и широко применяется, поэтому его характеристики описаны в литературе. Purolite A430 только начинает выходить на рынок, поэтому в работе определены некоторые его характеристики экспериментально. Кривая кислотно-основного титрования, приведенная на рисунке 1, имеет типичный для сильнокислотного сорбента вид и позволяет рассчитать показатель константы кислотно-основного равновесия (р К а) и параметр n , связанный с электростатическим взаимодействием функциональных групп. Для этого применяли уравнение Гендерсона-Хассельбаха [4]:
рКа = рН + n lg .
1 - а
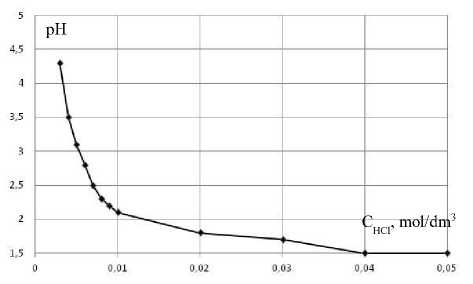
Рисунок 1. Кривая кислотно-основного титрования ионообменника PuroliteA430 в ОН-форме
Figure1. The curve of the acid-base titration, ion exchanger Purolite A430 in the form of OH
Значения констант протолиза обоих ионообменников АВ 17 и Purolite A430 совпадают и равны 0,037 ± 0,002. Величина ПОЕ Purolite A430 составила 4,3 ммоль/г, АВ 17 – 3,4 ммоль/г. Таким образом, изучаемые ионообменник имеют одинаковый тип ионогенных групп – четвертичные аммоние-вые, но их количество выше в Purolite A430.
-
1.2 Сорбция индивидуальных ионов
По результатам исследования сорбции индивидуальных анионов в динамических условиях построены выходные кривые, отражающие зависимость концентрации ионов в фильтрате от объема попущенного очищаемого раствора, примеры которых показаны на рисунках 2 и 3.
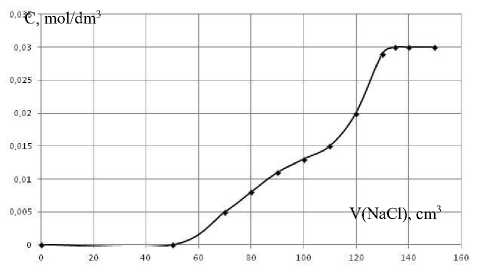
Рисунок 2. Выходная кривая сорбции хлорид-ионовна АВ-17
Figure2. Output curve of sorptionchloride ions on AB-17
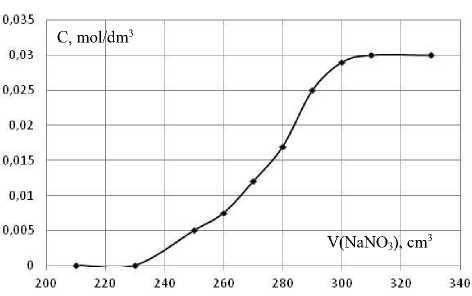
Рисунок 3. Выходная кривая сорбции нитрат-ионовна Purolite А 430
-
Figure3. Output curve of sorption nitrate ions to Purolite A 430
Полученные в работе выходные кривые сорбции анионов на обоих ионообменниках имеют вид «полуволн». Начальный участок для нитрат- и хлорид-ионов размыт, а конечный заострен, что может свидетельствовать о преобладании внешнедиффузионного лимитирования в кинетике процесса, то есть реализации «пленочного механизма» [5,6]. При сорбции сульфат-ионов кривые имеют размытые начальный и конечный фронты, что характеризует смешанно-диффузионную кинетику, то есть обмен достаточно большого аниона контролируется внутренней и внешней диффузией.
Изучение сорбции индивидуальных анионов позволило установить и сравнить времена «проскока» и рассчитать динамические обменные емкости анионообменников по каждому определяемому иону.
Таблица 1.
Характеристики сорбции анионов в динамических условиях
Table 1.
Anions sorption characteristics under dynamic conditions
|
Характеристика / Characteristic |
Аноны / Annonas |
||
|
Cl- |
NO 3 - |
SO 4 2- |
|
|
АВ-17 AV-17 |
|||
|
Динамическая обменная емкость, ммоль/дм3 Dynamic exchange capacity, mmol/dm3 |
1,06 ± 0,02 |
0,95 ± 0,01 |
1,42 ± 0,03 |
|
Время проскока (мин) при скорости пропускания 0,033 см3/с Breakthrough time (min) at a flow rate of 0.033 cm3/s |
10 |
40 |
50 |
|
Максимальное время концентрирования, мин Maximum concentration, min |
112 |
142 |
178 |
|
Purolite A430 |
|||
|
Динамическая обменная емкость, ммоль/дм3 Dynamic exchange capacity, mmol/dm3 |
1,48 ± 0,03 |
1,50 ± 0,03 |
1,62 ± 0,03 |
|
Время проскока (мин) при скорости пропускания 0,033 см3/с Breakthrough time (min) at a flow rate of 0.033 cm3/s |
120 |
||
|
Максимальное время концентрирования, мин Maximum concentration, min |
178 |
222 |
355 |
Результаты изучения индивидуальной сорбции анионов показывают, что ионообменная смола Purolite А430 является более эффективным сорбентом, чем АВ-17, для концентрирования хлорид-, нитрат- и сульфат-ионов из водных растворов за счет большей проницаемости и значения ДОЕ. Причины повышенной эффективности сорбции на Purolite А430 по сравнению с АВ-17 заключаются в более высокой полной обменной емкости и улучшенных гидродинамических характеристиках ионообменника.
-
1.3 Сорбция анионов из многокомпонент-ныхрастворов
Солевой состав природных вод определяется макрокомпонентами: катионами и анионами НСO3-, Сl-, SO 4 2-. Остальные анионы присутствуют в значительно меньших количествах и называются микрокомпонентами; они не определяют химический тип воды, к ним относятся гидроксид-, нитрит-, нитрат-, силикат-, фосфат- и фторид-ионы. В работе была приготовлена смесь, состоящая из двух макрокомпонентов хлорид- и сульфат-ионов, а также одного микрокомпонента нитрат-ионов. В работе проведено концентрирование анионов из трехкомпонентных растворов высокоосновными анионообменниками в динамических условиях.
Поскольку при использованной скорости пропускания индивидуальных ионов обменная емкость реализуется не полностью, то при исследовании тройных систем скорость пропускания уменьшили в 2 раза, и она составила 0,015 см3/с.
Изучение тройных растворов вели по методике, описанной выше. По полученным результатам строили выходные кривые сорбции, представленные на рисунках 4 и 5.
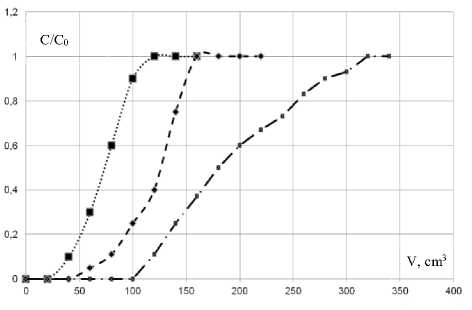
Рисунок 4. Выходные кривые сорбции:∙∙∙ – хлорид-ионов, – нитрат-ионов, -∙-∙ – сульфат-ионов на ионообменной смоле АВ-17измногокомпонентных растворов
-
Figure4. Sorptioncurves:∙∙∙ – chloride ions, nitrate ions –, – ∙ – ∙ – sulfate ions on the ion exchange resin AB-17 of a multi-component solution
Насыщение сорбентов хлорид-, нитрат- и сульфат-ионами происходит при разных объемах очищаемых растворов. На ионообменной смоле АВ-17 хлорид- и нитрат-ионы выходят при близких объемах, последним в фильтрате появляется сульфат-ион. Из смолы Purolite A430 хлорид-ионы выходят первыми, вторыми – нитрат-ионы и третьми – сульфат-ионы. Насыщение сульфат-ионами протекает полнее, чем другими ионами. Подтверждением данного предположения являются максимальные времена сорбции для каждого иона на обоих ионообменниках, представленные в таблице 1.
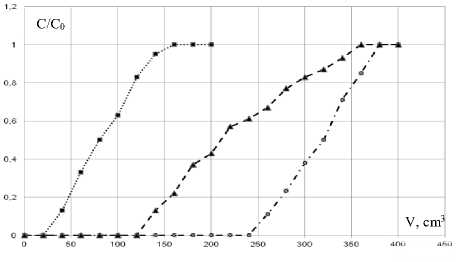
Рисунок 5. Выходные кривые сорбции: ∙∙∙ – хлорид-ионов, – нитрат-ионов, -∙-∙ – сульфат-ионов на ионообменной смоле PuroliteA430 из многокомпонентных растворов
-
Figure5. Sorption curves: ∙∙∙ – chloride ions, nitrate ions –, – ∙ – ∙ – sulfate ions on the ion exchange resin is Purolite A430 from multicomponent solutions
Установлено, что при сорбции анионов из тройных растворов на анионообменнике Purolite A430 времена сорбции различаются, а на анионообменнике АВ-17 близки и отсутствуют приемлемые области и индивидуальной идентификации ионов, что доказывает возможность количественного разделения изученных анионов на смоле Purolite A430.
Для подтверждения полученных результатов проведено сравнение определяемых концентраций в модельных смесях, содержащих три вида анионов. В качестве метода сравнения выбран капиллярный электрофорез. Результаты концентрирования и определения представлены в таблице 2.
Таблица 2.
Характеристики концентрирования анионов на Purolite A430
Table 2.
Characteristics of the concentrating of anions on Purolite A430
|
Анион Anion |
Концентрация в исходном растворе, мг/дм3 The concentration in the initial solution, mg/dm3 |
Концентрация в элюате, мг/дм3 The concentration in the eluate, mg/dm3 |
Коэффициент концентрирования The ratio of concentrationing |
Степень извлечения, % Recovery rate, % |
|
Cl- |
81 ±4 |
280 ±20 |
3,5 |
94 |
|
NO 3 - |
28 ±2 |
160 ±10 |
5,8 |
96 |
|
SО4 -2 |
130 ±10 |
1300 ±100 |
10,2 |
91 |
Согласно данным рисунка 5 и таблицы 2 более эффективно использовать сильноосновный анионообменник Purolite A430 в OH-форме для концентрирования анионов из водных растворов. Его применение на стадии подготовки пробы воды различного генезиса для анализа может решать одновременно как задачу концентрирования компонентов, так и их разделения.
Заключение
Полученные в работе значения полной обменной емкости и динамической обменной емкости анионообменных смол Purolite А430 и АВ-17 и характеристики индивидуальной сорбции
Список литературы Ионообменное концентрирование неорганических анионов из водных растворов
- Режим доступа: http://smoly.ru/anionit-av-17-8-harakteristiki.html Свободный. -Заглавие с экрана. -Яз.англ.
- Режим доступа: http://www.purolite.com/index Свободный. -Заглавие с экрана. -Яз.англ.
- ГОСТ 31940-2012. Вода питьевая. Методы определения содержания сульфатов. Введен 01.01.2014. М.: Межгосударственный стандарт: ИПК изд-во стандартов, 2014. 16 с.
- Математическая модель динамики сорбции в слое ионообменника/Т. С. Корниенко, Е. А.,Загорулько, Л. П. Бондарева//Сорбционные и хроматографические процессы. 2011. Т. 11, вып. 6. C.895-899.
- Риман В., Уолтон Х.Ф. Ионный обмен в аналитической химии: Международная серия монографий в аналитической химии. -Elsevier, 2013.
- Ганесан П., Камарадж Р., Васудеван С. Применение изотермы, кинетические и термодинамические модели для адсорбции ионов нитрата на графене из водного раствора//Журнал Тайваньского института инженеров-химиков. -2013. -Т. 44. -№. 5. -С. 808-814.


