Ишемическая болезнь сердца у пациентов с терминальной стадией хронической болезни почек: патофизиологические особенности и хирургическое наблюдение
Автор: Шенгелия Л.Д., Донаканян С.А., Фатулаев З.Ф., Абрамян М.В., Урко А.А., Коншина М.О.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Клинические наблюдения
Статья в выпуске: 4 т.18, 2023 года.
Бесплатный доступ
Пациенты с хронической болезнью почек (ХБП) имеют повышенный риск возникновения сердечно - сосудистых заболеваний, в то время как пациенты с терминальной стадией ХБП, получающие заместительную почечную терапию, которым показана реваскуляризация миокарда, представляют собой отдельную, более тяжелую группу пациентов, имеющую свои клинические и патофизиологические особенности. Реваскуляризация миокарда показана больным в терминальной стадии заболевания почек, однако риск смерти и развития интра- и послеоперационных осложнений при этом более высокий. Не смотря на значительные достижения эндоваскулярной хирургии, аортокоронарное шунтирование является преимущественным методом хирургического лечения ИБС у данной категории пациентов, демонстрируя более доказательные отдаленные результаты. В данном клиническом случае отражены патофизиологические особенности ИБС у пациента с терминальной стадией ХБП и продемонстрирована эффективность аортокоронарного шунтирования в лечении ИБС.
Хроническая болезнь почек, аортокоронарное шунтирование, реваскуляризация миокарда
Короткий адрес: https://sciup.org/140303486
IDR: 140303486 | DOI: 10.25881/20728255_2023_18_4_134
Ischemic heart disease in patients with end-stage chronic kidney disease: pathophysiological features and surgical treatment
Patients with chronic kidney disease have high risk of cardiovascular diseases, while patients with end-stage chronic kidney disease, initially on dialysis, whom myocardial revascularization is recommended, represent a separate, more severe group of patients with their own clinical and pathophysiological features. Myocardial revascularization is indicated for patients in the terminal stage of kidney disease, but the risk of death and the development of intra- and postoperative complications is higher. Despite the significant achievements of endovascular surgery, coronary artery bypass grafting is the preferred method of the surgical treatment of coronary heart disease in this category of patients, demonstrating more evidence-based long-term results. In this clinical case, the pathophysiological features of coronary heart disease in the patient with end-stage chronic kidney disease are reflected and the effectiveness of coronary artery bypass grafting in the treatment of coronary heart disease in the patient, who needs dialysis.
Текст научной статьи Ишемическая болезнь сердца у пациентов с терминальной стадией хронической болезни почек: патофизиологические особенности и хирургическое наблюдение
Сердечно-сосудистая патология является наиболее распространенной причиной смерти у пациентов, находящихся на заместительной почечной терапии [1]. По различным данным, каждый год у приблизительно 10% пациентов с ХБП диагностируется инфаркт миокарда, при этом 5% пациентов умирают по этой причине [2].
Течение ИБС и СН у пациентов с терминальной стадией ХБП имеют свои патофизиологические особенности
(Рис. 1). Как известно, потребность миокарда в кислороде определяется тремя основными факторами: напряжением стенки левого желудочка (ЛЖ), сократимостью миокарда ЛЖ и частотой сердечных сокращений. Для расчета напряжения стенки ЛЖ необходимо произведение значений давления и диаметра ЛЖ разделить на толщину стенки ЛЖ. У пациентов, находящихся на заместительной почечной терапии, отмечается повышенное артериальное давление и, соответственно, повышенное давление в ЛЖ. Перегрузка объемом приводит к увеличению объема и радиуса ЛЖ. Таким образом, у пациентов данной группы отмечается высокая потребность миокарда в кислороде, обусловливающая склонность миокарда к ишемии и инфаркту, и без наличия гемодинамически значимого поражения коронарных артерий.
Гипертония, хроническая перегрузка объемом и анемия приводят гипертрофии ЛЖ. Сама по себе гипертрофия миокарда повышает потребность миокарда в кислороде и приводит к относительной

Шенгелия Л.Д., Донаканян С.А., Фатулаев З.Ф. и др. ИШЕМИЧЕСКАЯ БОЛЕЗНЬ СЕРДЦА У ПАЦИЕНТОВ С ТЕРМИНАЛЬНОЙ СТАДИЕЙ ХРОНИЧЕСКОЙ БОЛЕЗНИ ПОЧЕК: ПАТОФИЗИОЛОГИЧЕСКИЕ ОСОБЕННОСТИ И ХИРУРГИЧЕСКОЕ НАБЛЮДЕНИЕ коронарной недостаточности. Еще одним патогенетическим звеном формирования ишемии является нарушение плотности капилляров, что создает дисбаланс между потреблением миокарда в кислороде и его доставкой. Наличие атеросклеротического поражения коронарных артерий при гипертрофированном миокарде ЛЖ также увеличивает риск развития ишемии. Ишемия миокарда приводит к апоптозу клеток, накоплению коллагена, фиброзу и в дальнейшем к увеличению жесткости ЛЖ, нарушению наполнения и диастолической дисфункции [3–5]. В конечном итоге ишемия может приводить к гибернации миокарда и систолической дисфункции ЛЖ [1].
Анемия, отмечаемая у пациентов с ХБП, также является патогенетическим компонентом несоответствия потребности миокарда в кислороде с его доставкой. По этой причине абсолютному большинству пациентов, находящихся на программной терапии, требуется терапия препаратами железа и стимуляторами эритропоэза [4].
Нарушение метаболизма кальция и фосфора представляет собой наиболее неблагоприятный синдром развивающейся хронической почечной недостаточности. Изменения фосфорно-кальци-евого обмена в конечном итоге приводят к кальцификации коронарных артерий и риску возникновения кардиоваскулярной смертности. Кроме того, нарушенный метаболизм углеводов является одними из факторов, приводящих к формированию атеросклеротических бляшек.
Существуют разные виды заместительной почечной терапии — гемодиализ, гемодиафильтрация, перитонеальный диализ. Длительность стандартной программной терапии составляет, как правило, около 720–800 минут/неделю, оказывая в том числе и воздействие на сердечно-сосудистую систему. Ультрафильтрация вызывает резкий сдвиг в объеме внутрисосудистой жидкости, опосредованно вызывая ишемию миокарда, за счет снижения артериального давления и перфузии, а также вызывая дисфункцию эндотелия.
Уремия, наблюдающаяся у пациентов с терминальной стадией ХБП, сопровождается запуском процессов ок-сидативного стресса и высвобождения свободных радикалов. Как известно, механизмы оксидативного стресса задействованы также в патогенезе атеросклероза — повреждения сосудистой стенки, формирования артеросклеротической бляшки, а также ее разрыва [1]. Доказа-
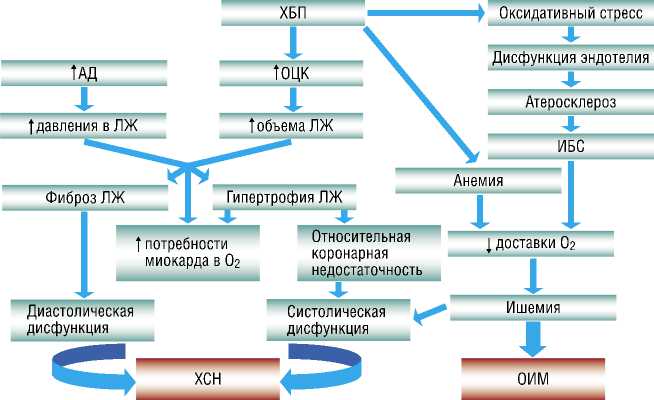
Рис. 1. Особенности патогенеза кардиальной патологии у пациентов с ХБП. Сокращения: АД — артериальное давление, ОЦК — объем циркулирующей крови, ХСН — хроническая сердечная недостаточность, ОИМ — острый инфаркт миокарда.
но, что гемодиализ увеличивает степень оксидативного стресса, развивающегося вследствие уремии. Одними из основных свободных радикалов, вырабатываемых при реперфузии являются гидроксильные радикалы. Они быстро вступают во взаимодействие с белками, фосфолипидами, тиолами и воздействуют на внутриклеточный уровень ионов кальция, а также на степень чувствительности сократительного аппарата к кальцию, таким образом влияя на сократительную функцию кардиомиоцитов. Таким образом, пациенты с терминальной стадией ХБП более подвержены риску развития инфаркта миокарда за счет ишемии, дисфункции эндотелия, атеросклероза, а также гипертрофии ЛЖ, что сопровождается более высокой смертностью данной категории больных [1; 7; 12].
Кроме того, довольно часто у пациентов, находящихся на диализе, клиническая картина ИБС может быть сглажена или вообще отсутствовать. Поэтому с целью предотвращения жизнеугрожающих осложнений и увеличения продолжительности жизни пациентов с почечной недостаточностью важными являются своевременная диагностика и лечение гемодинамически значимого поражения коронарных артерий. Случаи аортокоронарного шунтирования у пациентов, находящихся на заместительной почечной терапии, встречаются относительно редко и должны выполняться по показаниям и при оценке рисков интра- и послеоперационных осложнений [7]. В данной работе приведен пример хирургической реваскуляризации миокарда в объеме аортокоронарного шунтирования, у пациента, находящегося на заместительной почечной терапии.
Пациент Г. 67 лет поступил в отделение хирургического лечения интерактивной патологии НМИЦ ССХ им. А.Н. Бакулева МЗ РФ с жалобами на инспираторную одышку при минимальной физической нагрузке, давящие боли за грудиной при минимальной физической нагрузке, купирующиеся в течение двух минут после ее прекращения, головокружения.
Из анамнеза заболевания известно, что в течение 30 лет пациент страдает гипертонической болезнью, с максимальными цифрами артериального давления до 210/100 мм рт. ст. В 2004 г. перенес ОИМ по задней стенке ЛЖ, был госпитализирован в больницу по месту жительства, где была проведена диагностическая коронарография, по результатам которой выявлено многососудистое поражение. Оперативное лечение не проводилось, получал консервативную терапию. Также, известно, что пациент наблюдался у нефролога с выраженной клиникой пиелонефрита. В июле 2005 г. обнаружено уменьшение размеров правой почки. В мае 2007 г. при обследовании по данным лабораторных методов обследования: креатинин 265 мкмоль/л, рСКФ (CKD-EPI) 25 мл/мин./1.73 м2, мочевина 15,4 ммоль/л. Выставлен диагноз: вторично сморщенная правая почка
(нефункционирующая). Стационарного обследования в специализированном нефрологическом отделении не было. В дальнейшем отмечалось постепенное нарастание уровня креатинина. Пациент находился под наблюдением врача по месту жительства. В 2021 г. рСКФ снизилась до уровня 7 мл/мин./1.73 м2 (креатинин сыворотки 661 мкмоль/л), проведен консилиум по месту жительства, по результатам которого принято решение о начале проведения заместительной почечной терапии. Методом выбора коррекции ХБП стадии 5 стал перитонеальный диализ. В брюшную полость был имплантирован катетер. В вводном диализном периоде пациент отмечал стойкое снижение артериального давления до 100/60 мм рт. ст., слабость, головокружение, перебои в работе сердца, нарастание интенсивности ангинозных болей и одышки, снижение толерантности к физическим нагрузкам. Пациент обратился в НМИЦ ССХ им. А.Н. Бакулева МЗ РФ.
При поступлении состояние средней тяжести, дыхание жесткое, тоны сердца приглушены, ритмичные. Частота сердечных сокращений составила 70 уд/мин., артериальное давление 120/70 мм рт. ст. Диурез отсутствует.
По данным лабораторных методов обследования при поступлении в стационар гемоглобин составил
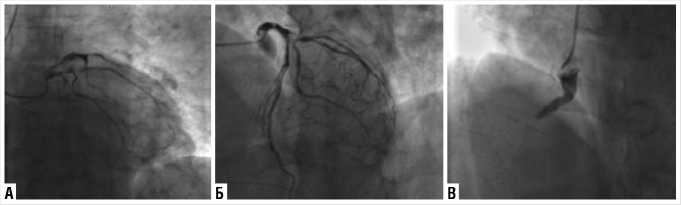
Рис. 2. Коронарография перед операцией. А,Б — система левой коронарной артерии. Визуализируются стенозы в передней межжелудочковой ветви левой коронарной артерии, огибающей и ветви тупого края. В — окклюзия правой коронарной артерии.
119 г/л; лейкоциты 8.58 х 109/л; тромбоциты 144 х 109/л; креатинин 985 мкмоль/л; мочевина 20,3 ммоль/л; альбумин 37 г/л; общий холестерин 3,98 ммоль/л; холестерин липопротеинов низкой плотности 1,59 ммоль/л; холестерин липопротеинов высокой плотности 0,7 ммоль/л; триглицериды 3,71 ммоль/л; натрий 138 ммоль/л; калий 4,6 ммоль/л.
При поступлении в стационар на ЭКГ регистрируется синусовый ритм с частотой сердечных сокращений 62 в минуту, нормальное положение электрической оси.
По данным ЭхоКГ фракция выброса ЛЖ была равна 53%, с конечным диастолическим объемом 120 мл, конечным систолическим объемом 56.0 мл по Симпсону. Недостаточность митрального клапана ишемического генеза до 2 степени.
Пациенту выполнена коронарография, по результатам которой выявлен стеноз 80% в проксимальной трети передней межжелудочковой ветви левой коронарной артерии, стеноз 90% в огибающей ветви, стеноз 90% ветви тупого края, правая коронарная артерия окклю-зирована (Рис. 2).
После выполнения комплекса диагностических процедур принято решение об оперативном лечении ИБС. В виду анатомических особенностей по- ражения правой коронарной артерии, выраженного кальциноза коронарных артерий, вероятность успешной эндоваскулярной реканализации низкая. В том числе учитывая многососудистый характер поражения, принято решение о хирургическом лечении ИБС — выполнении операции аортокоронарного шунтирования.
12.07.2022 г. выполнена операция реваскуляризации миокарда в объеме маммарокоронарного шунтирования передней межжелудочковой артерии, аортокоронарного шунтирования задней межжелудочковой ветви правой коронарной артерии, диагональной ветви и a.intermedia на работающем сердце в условиях искусственного кровообращения. После завершения хирургического этапа, проведена интраоперационная шунтография венозного шунта к ветви тупого края, диагональной ветви, a.int-ermedia, маммарного шунта к передней межжелудочковой ветви левой коронарной артерии с удовлетворительным ангиографическим результатом (Рис. 3).
На дооперационном периоде было принято решение о переводе пациента с перитонеального диализа на экстракорпоральную заместительную почечную терапию: проводились процедуры гемодиафильтрации с целью повышения клиренса процедуры заместительной почечной терапии. На дооперационном этапе в рамках подготовки пациента к операции проводилась коррекция анемии (препаратами железа, эритропоэтином), гипоальбуминемии, достижения сухого веса. Интраоперационно была выполнена ультрафильтрация, во избежание гиповолемии.
За период госпитализации выполнено 8 процедур продолжительностью 240–360 минут. В первые трое суток заместительная почечная терапия проводилась в режиме ежедневных процедур гемодиафильтрации, затем был выбран
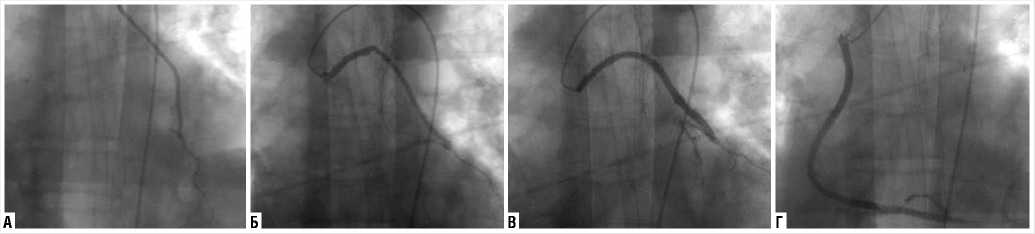
Рис. 3. Интраоперационная шунтография. А — анастомоз между левой внутренней грудной артерией и передней межжелудочковой артерией. Б — венозный анастомоз к ветви тупого края. В — венозный анастомоз к срединной артерии. Г — венозный анастомоз к правой коронарной артерии.
Шенгелия Л.Д., Донаканян С.А., Фатулаев З.Ф. и др. ИШЕМИЧЕСКАЯ БОЛЕЗНЬ СЕРДЦА У ПАЦИЕНТОВ С ТЕРМИНАЛЬНОЙ СТАДИЕЙ ХРОНИЧЕСКОЙ БОЛЕЗНИ ПОЧЕК: ПАТОФИЗИОЛОГИЧЕСКИЕ ОСОБЕННОСТИ И ХИРУРГИЧЕСКОЕ НАБЛЮДЕНИЕ протокол — проведения процедур гемодиафильтрации в режиме через день. Это позволило без осложнений провести послеоперационный период. Адекватно контролировались клинико-лабораторные показатели. Ультрафильтрация проводилась с учетом показателей гемодинамики (артериального давления, центрального венозного давления, конечно-диастолического объема левого желудочка), а также объема предполагаемой инфузионно-трансфузионной терапии. Использовался диализатор Leoceed 18 H (S = 1,8 м2).
В дальнейшем послеоперационный период протекал гладко, без особенностей. На вторые сутки после операции пациент переведен из отделения реанимации в палату интенсивной терапии. На третьи сутки пациенту удалены дренажи из полости перикарда и переднего средостения, пациент переведен в общую палату. По данным ЭКГ регистрировался синусовый ритм с частотой 70 ударов минуту. По данным анализов крови гемоглобин составил 97 г/л; креатинин 771 мкмоль/л; мочевина 14,4 ммоль/л, Сa 0,92 ммоль/л. На 12-е сутки пациент выписан под наблюдение кардиолога по месту жительства, перитонеальный диализ был далее продолжен.
Обсуждение
Первая процедура диализа выполнена в 1924 г. Г. Хаасом в Германии [8; 9]. Появление процедуры диализа внесло неоценимый вклад в лечение пациентов с терминальной стадией ХБП, позволив значительно увеличить продолжительность их жизни. Однако, основной причиной смерти среди данной категории больных являются сопутствующие сердечно-сосудистые заболевания и их осложнения. Учитывая ряд патогенетических данных, пациенты, находящихся на диализе, имеют более высокий риск развития артериальной гипертензии, сахарного диабета, дислипидемии, а также ИБС и ее осложнений. Несмотря на значительные достижения эндоваскулярной хирургии, аортокоронарное шунтирование остается предпочтительным методом хирургического лечения ИБС в том числе, и в этой категории пациентов.
Сам факт наличия у пациента ко-морбидности в виде терминальной стадии ХБП является фактором, который потенциально может существенно осложнить течение послеоперационного периода. Однако, наличие ишемической болезни сердца высокого риска жизнеугрожающих сердечно-сосудистых ослож- нений делает вопрос об оперативном лечении актуальным. К осложнениям послеоперационного периода у пациентов с терминальной стадии ХБП относятся: синдром низкого сердечного выброса, повышенная кровоточивость, высокий риск инфекционных осложнений, нарушения мозгового кровообращения, дыхательная недостаточность. Случаи сепсиса, а также абдоминальных осложнений после кардиохирургических вмешательства встречаются в группе [10–12].
В исследование A. Klvacek и соавт. вошла небольшая группа из 36 пациентов, находящихся на заместительной почечной терапии, которым выполнено кардиохирургическое вмешательство — изолированное аортокоронарное шунтирование в 21 случаев, в остальных — протезирование аортального, митрального клапанов, дуги аорты, операция «лабиринт» в сочетании с аортокоронарным шунтированием или без него. У 16 пациентов операция была выполнена в условиях ИК, 20 — на работающем сердце. Госпитальная летальность составила 11,1% — 4 пациента. Выживаемость через 1 год составила 77,8%. По мнению авторов предикторами неблагоприятного прогноза в средне-отдаленном периоде являются — сердечная недостаточность, наличие показаний к срочному или экстренному выполнению операции, сочетанное хирургическое вмешательство, синдром низкого сердечного выброса в раннем послеоперационном периоде [10].
Обсуждаемым является вопрос о выполнении операции аортокоронарного шунтирования у пациентов с терминальной стадией ХБП в условиях ИК или без него. В связи с меньшим системным воспалительным ответом более предпочтительным считается второй вариант. Проведение ИК также связано риском объемной перегрузки и застоя в малом круге кровообращения, а также риском кровотечений и усугубления степени анемии. Однако, оперирующему хирургу нужно понимать и иметь в виду известные случаи летальных исходов по причине возникновения жизнеугрожающих желудочковых нарушений ритма сердца при подъеме сердца для доступа к боковой стенке при выполнении аортокоронарного шунтирования на работающем сердце у данной группы пациентов [13]. В отдельных случаях, нарушения ритма не удается купировать, не смотря на конверсию и подключение аппарата ИК. Таким образом, несмотря на очевидные преимущества выполнения операции аортокоронарного шунтирования у пациентов с ХБП на работающем сердце без ИК, определяющими факторами являются гемодинамическая стабильность пациента, кардиальный статус и тяжесть поражения коронарных артерий.
Несмотря на то, что данные в отношении сравнительной оценки методов аортокоронарного шунтирования, стентирования и оптимальной консервативной терапии ИБС у пациентов с умеренной почечной недостаточностью варьируют, их сопоставление с группой пациентов с терминальной стадией ХБП не совсем уместно в связи с большей исходной тяжестью второй группы больных. А также выраженным развитием указанных ранее внутри- и внесердечных патофизиологических изменений, значительно увеличивающих риск развития интра- и послеоперационных изменений. Кроме того, сочетание хронической болезни почек с сахарным диабетом, делает выполнение аортокоронарного шунтирования более предпочтительным над эндоваскулярным подходом.
Вообще, выбор эндоваскулярного или открытого хирургического методов реваскуляризации у пациентов с ХБП и сравнение непосредственных и отдаленных результатов является предметом широкого обсуждения и анализа. Одним из ключевых моментов в выборе тактики лечения является частое наличие у пациентов с ХБП тяжелого, протяженного или диффузного поражения коронарных артерий, обусловленных как атеросклеротическим процессом , так и нарушением кальций-фосфорного обмена, а также их тонкий диаметр и часто многососудистый характер поражения. В подобных ситуациях технически затруднительным может являться и стентирование, и аортокоронарное шунтирование. Тем не менее, не смотря на более высокий риск осложнений, только указанные подходы могут улучшить качество жизни и ее продолжительность. Несмотря на то, что согласно Европейским рекомендациям по реваскуляризации миокарда предпочтение в указанной группе больных отдается аортокоронарному шунтированию, нередко сами пациенты выбирают стентирование по причине меньшей инва-зивности процедуры и более короткому послеоперационному периоду [11].
Общее число пациентов вошедших в мета-анализ K. Cui и соавт., посвященный сравнению аортокоронарного шунтирования и стентирования у пациентов с ИБС и ХБП, составило 26 441. Половина пациентов вошла в группу стентирова-
ния коронарных артерий, а другая половина — в группу аортокоронарного шунтирования. В исследование включались пациенты с многососудистым поражением или поражением ствола левой коронарной артерии. Первичной конечной точкой являлась смертность по любым причинам в отдаленном периоде, вторичные конечные точки — смертность в раннем послеоперационном периоде, инфаркт миокарда, инсульт, повторная реваскуляризация. Согласно исследованию в группе аортокоронарного шунтирования отмечалась меньшая смертность в отдаленном периоде, меньшее число случаев инфаркта миокарда и случаев повторных реваскуляризаций, по сравнению с группой эндоваскулярного лечения. Однако, в группе аортокоронарного шунтирования отмечалось больше число нарушений мозгового кровообращения в раннем послеоперационном периоде. Непосредственная летальность была одинаковой в обеих группах [14].
Как известно, случаи ИБС у пациентов с ХБП часто сопровождается тяжелым, диффузным, многососудистым поражением с выраженным кальцинозом коронарных артерий. При этом диаметр сосудов часто тоньше, чем у классических ишемических пациентов. Все вышеуказанные факторы делают технически сложным не только аортокоронарное шунтирование, но и стентирование. Наличие тяжелого кальциноза существенно затрудняет процесс имплантации и расположения стента в артерии, в то время как диффузный кальциноз сосудистой стенки создает технические трудности при наложении дистальных анастомозов [14].
Исследование EXCEL (Evaluation of XIENCE Versus Coronary Artery Bypass Surgery for Effectiveness of Left Main Revascularization trial) представляет собой международное, многоцентровое, рандомизированное исследование, посвященное сравнению стентирования и аортокоронарного шунтирования у пациентов с ИБС с поражением ствола левой коронарной артерии [18]. Одной из исследуемых целей было сравнение результатов в подгруппе пациентов с ХБП. Из 1869 пациентов, включенных в исследование, хроническая болезнь почек наблюдалась у 361. Согласно данным авторов у пациентов с ХБП отмечался более высокий риск послеоперационных осложнений, включая жизнеугрожающие нарушения ритма сердца, более частые случаи переливания крови, инфекции, в том числе раневые. При сравнении групп стентирования и аортокоронарного шунтирования авторы обнаружили меньшее число случаев манифестации почечной дисфункции в послеоперационном периоде и других крупных послеоперационных осложнений в группе стентирования, что логически объяснимо. При анализе отдаленных результатов не было обнаружено статистически значимых различий по числу инфарктов миокарда, нарушений мозгового кровообращения и смертности в исследуемых группах. Однако, число повторных, опосредованных ишемией реваскуляризаций было ниже в группе аортокоронарного шунтирования как у пациентов с ХБП, так и без нее [18]. Мы хотим также отметить, что данное исследование применимо к заданной нами тематике лишь частично. Это связано с тем, что пациенты, с терминальной стадией ХБП, которым показана реваскуляризация миокарда, представляют собой отдельную, более тяжелую группу пациентов, имеющую свои клинические и патофизиологические особенности, а также более высокие риски интра- и послеоперационных осложнений [15; 6].
Несомненно, проведение крупных, рандомизированных исследований позволило бы получить новые данные и сформировать более глубокое понимание в отношении тактики выбора открытой или эндоваскулярной методики реваскуляризации миокарда. Тем не менее, учитывая фактор частого наличия многососудистого поражения у данной категории пациентов, именно аортокоронарное шунтирование позволяет достичь полную реваскуляризацию коронарных артерий [17].
Заключение
Наличие ИБС у пациентов с ХБП встречается довольно часто, являясь основной причиной смертности в данной группе больных. Несмотря на то, что данная категория больных является клинически более тяжелой по сравнению с классическими пациентами с кардиальной патологией, аортокоронарное шунтирование является предпочтительным и более эффективным, по сравнению с эндоваскулярным подходом, демонстрируя более убедительные отдаленные результаты. Должная медикаментозная терапия на до- и послеоперационном периодах, а также возможность проведения заместительной почечной терапии, позволяют снизить риски послеоперационных осложнений. В данном клиническом случае отражены патогенетические особенности пациента с ишемической болезнью сердца, опосредованные закономерными осложнениями терминальной ХБП, на которые следует обратить внимание врачу для более глубокого понимания клинического статуса пациента, оценка рисков потенциальных осложнений и их механизмов, а также показана возможность, эффективность и целесообразность выполнения операции аортокоронарного шунтирования пациентов с указанной коморбидностью. Отсутствие ишемии, улучшение клинической картины, отсутствие ангинозных болей, улучшение функционального статуса и качества жизни, а также профилактика жизнеугрожающих осложнений являются основными целями хирургического лечения.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Ишемическая болезнь сердца у пациентов с терминальной стадией хронической болезни почек: патофизиологические особенности и хирургическое наблюдение
- Venkatesh K., Sudarshan B., Kunal C. Ischemic Heart Disease in Patients Undergoing Dialysis, Hospital Practice. 2012; 4: 33-39. doi: 10.3810/hp.2012.10.1001.
- Ther A. Patient Registration Committee, Japanese Society for Dialysis Therapy: An overview of regular dialysis treatment in Japan. 2004; 8: 358-382.
- Tanaka Y, Nobuhiko J, Hiroki H. Affiliations Ischemic Heart Disease in Patients with End-Stage Kidney Disease. 2015; 40(4): 332-6. doi: 10.1159/000441582.
- Herzog C, Asinger R, Berger A, Charytan D, Díez J, Hart R, et al. Cardiovascular disease in chronic kidney disease. A clinical update from Kidney Disease: Improving Global Outcomes (KDIGO). Kidney Int. 2011; 80: 572-586.
- Cerasola G, Nardi E, Palermo A, Mulè G, Cotone S. Epidemiology and pathophysiology of left ventricular abnormalities in chronic kidney disease: a review. 2011; 24: 1-10.
- Chu-Lin C, Te-Chao F. Coronary artery disease in dialysis patients: What is the optimal therapy? Tzu Chi Medical Journal. 2013; 25: 82-85. doi: 10.1016/j.tcmj.2013.02.002.
- Burton J, Jefferies H, Selby N, McIntyre C. Hemodialysis- induced repetitive myocardial injury results in global and segmental reduction in systolic cardiac function. Clin J Am Soc Nephrol. 2009; 4(12): 1925-1931.
- Sniderman A, Solhpour A, Alam A, Williams K, Sloand J. Cardio- vascular death in dialysis patients: lessons we can learn from AURORA. Clin J Am Soc Nephrol. 2010; 5(2): 335-340.
- Vienken J. Hemodialysis as an Experimental Therapy: Georg Haas and the First Clinical Treatment of a Human Kidney Patient. Dialysis. 2012; 43-50. doi: 10.1142/9789814289764_0007.
- Klváček A, Šantavý P, Zuščich O, Konečný М, Hájek R, Lonský V. Pětileté zkušenosti se srdečními operacemi u pacientů závislých na dialyze. Cor et Vasa. 2015; 57(2): e86-e90. doi: 10.1016/j.crvasa.2015.03.004.
- Соколова Н.Ю, Голухова Е.З. Реваскуляризация миокарда у больных стабильной ишемической болезнью сердца: стратификация периоперационных и отдаленных рисков // Креативная кардиология. — 2016. — №10 (1). — С.25-36. [Sokolova NYU, Goluhova EZ. Revaskulyarizaciya miokarda u bol’nyh stabil’noj ishemicheskoj bolezn’yu serdca: stratifikaciya perioperacionnyh i otdalennyh riskov. Kreativnaya kardiologiya; 2016; 10(1): 25-36. (In Russ.)] doi: 10.15275/kreatkard. 2016.01.03.
- Меликулов А.А., Мерзляков В.Ю., Ключников И.В., Скопин А.И., Мамедова С.К., Жалилов А.К., и др. Непосредственные результаты коронарного шунтирования на работающем сердце у пациентов высокого хирургического риска // Анналы хирургии. — 2017. — №22(6). — С.353-360. [Melikulov AA, Merzlyakov VYU, Klyuchnikov IV, Skopin AI, Mamedova SK, ZHalilov AK, et al. Neposredstvennye rezul’taty koronarnogo shuntirovaniya na rabotayushchem serdce u pacientov vysokogo hirurgicheskogo riska. Annaly hirurgii. 2017; 22(6): 353-360. (In Russ.)]
- Chung-Dann K, Yu-Jen Y. Coronary Artery Bypass Grafting in Patients with Dialysis-Dependent Renal Failure. Tex Heart Inst J. 2004; 31: 224-30.
- Cui K, Liu H, Yuan F, et al. Coronary artery bypass graft surgery versus stenting for patients with chronic kidney disease and complex coronary artery disease: a systematic review and meta-analysis. Therapeutic Advances in Chronic Disease. 2021; 12. doi: 10.1177/ 2040622321990273.
- Бочаров А.В., Сидоров Д.В., Попов Л.В. Трудности лечения острого коронарного синдрома у пациента с терминальной стадией хронической почечной недостаточности на программном гемодиализе (описание случая) // Клиническая практика. — 2020. — №11(3). — С.102-106. [Bocharov AV, Sidorov DV, Popov LV. Difficulties in Treatment of Acute Coronary Syndrome in a Patient with End-Stage Chronic Renal Failure on Program Hemodialysis (Case Description). Journal of Clinical Practice. 2020; 11(3): 102-106. (In Russ.)] doi: 10.17816/clinpract33946.
- Солдаткина А.О., Ярустовский М.Б., Абрамян М.В., Кудзоева З.Ф., Камардина Е.В., Назарова В.И. Особенности периоперационного ведения кардиохирургических пациентов с терминальной стадией хронической болезни почек // Актуальные аспекты экстракорпорального очищения крови в интенсивной терапии. — 2018. — С.70-71. [Soldatkina AO, Yarustovsky MB, Abramyan MV, Kudzoeva ZF, Kamardina EV, Nazarova VI. Features of perioperative management of the cardiac surgery patients with end-stage chronic kidney disease. Topical aspects of the extracorporeal blood purification in intensive care. 2018: 70-71. (In Russ.)]
- Ярустовский М.Б., Абрамян М.В., Солдаткина А.О., Муратов Р.М., Бокерия О.Л., Кудзоева З.Ф. и др. Особенности периоперационного ведения пациентов с терминальной стадией хронической болезни почек, нуждающихся в хирургической коррекции кардиоваскулярной патологии // Нефрология и диализ. — 2018. — №20(3). –С.281-289. [Yarustovsky MB, Abramyan MV, Soldatkina AO, Muratov RM, Bokeria OL, Kudzoeva ZF, et al. Features of perioperative management in patients with end-stage renal disease requiring surgical correction of cardiovascular pathology. Nephrology and dialysis. 2018; 20(3): 281-289. (In Russ.)]


