Искусственные геохимические барьеры для решения экологических и технологических задач
Автор: Баюрова Юлия Леонидовна, Макаров Дмитрий Викторович
Журнал: Горные науки и технологии @gornye-nauki-tekhnologii
Статья в выпуске: 2, 2013 года.
Бесплатный доступ
Показана возможность использования в качестве искусственных геохимических барьеров различных химически активных минералов. Смоделировано добавление вещества барьера в раствор, синтезированы искусственные гидросиликаты никеля. Проанализирована форма базальных рефлексов.
Искусственные геохимические барьеры, очистка сточных и природных вод
Короткий адрес: https://sciup.org/140215706
IDR: 140215706 | УДК: 628.32;
Текст научной статьи Искусственные геохимические барьеры для решения экологических и технологических задач
Одним из перспективных методов защиты и очистки природных водоемов и стоков от загрязнения является применение геохимических барьеров. Геохимические барьеры - это участки земной коры, в которых на коротком расстоянии происходит резкое уменьшение интенсивности миграции химических элементов и, как следствие, их концентрация.
На геохимических барьерах образуются рудные тела многих месторождений.
Учение о геохимических барьерах было разработано профессором А.И. Перельманом, выделяют девять типов геохимических барьеров: окислительный; восстановительный; щелочной; кислый; сульфидный (сероводородный); глеевый; сорбционный; испарительный и термодинамический [1].
Среди направлений использования искусственных геохимических барьеров, кроме очистки природных и сточных вод от тяжелых металлов, радиоактивных элементов, нефтепродуктов, могут быть выделены:
-
- доизвлечение ценных компонентов из природного и техногенного сырья методами физико-химической геотехнологии;
-
- гидроизоляция хвосто- и шламохранилищ, накопителей, отстойников и т.д.;
-
- закрепление грунтов в строительстве.
Геохимические барьеры могут применяться для решения различных задач:
-
- устройства антифильтрационных экранов;
-
- фильтрации растворов через барьер с осаждением загрязняющих веществ;
-
- добавления вещества барьеров в раствор (в природные водоемы, хвостохранилища, отстойники и т.д.).
В качестве материалов для искусственных геохимических барьеров могут использоваться:
-
- отходы горнопромышленного комплекса (вскрышные породы, хвосты обогащения), содержащие химически активные минералы;
-
- смеси химически активных или модифицированных различным образом минералов;
-
- продукты и отходы глубокой химико-металлургической переработки руд и концентратов.
В качестве материалов для создания геохимических барьеров можно использовать химически активные минералы, такие как серпофит Mg 5 Fe(OH) 8 [Si 4 O 10 ], тальк Mg 2.5 Fe 0.5 (OH) 2 [Si 4 O 10 ] и биотит
KMgFe 2 (OH) 2 [AlSi 3 O 10 ]. При взаимодействии растворов сульфатов цветных металлов с данными минералами происходит осаждение металлов. Эти процессы протекают в естественной геологической обстановке и при хранении отходов горнопромышленного комплекса. Они также могут быть искусственно интенсифицированы и использованы при очистке природных и сточных вод и в методах геотехнологической переработки техногенного сырья.
Данные минералы широко распространены. В частности, они входят в состав хвостов обогащения медно-никелевых руд Печенгского рудного поля.
В природе известны никелевые слоистые гидросиликаты:
-
- гарниерит Ni 6 Si 4 O 10 (OH) 8 ,
-
- пимелит Ni 3 Si 4 O 10 (OH) 2 .4H 2 O,
-
- виллемсеит Ni 3 Si 4 O 10 (OH) 2 .
Нами были поставлены эксперименты по моделированию добавления вещества геохимических барьеров к сульфатным растворам, содержащими ионы никеля, синтезу искусственных никельсодержащих гидросиликатов.
В опытах были использованы мономинеральные фракции антигорита офитового строения (серпофита) и талька из массива Пильгуярви, Печенгское рудное поле, а также биотита из жилы керамического пегматита месторождения Куруваара, Кольский полуостров.
Минералы измельчали до крупности -0.1 мм.
В опытах концентрация раствора сульфата никеля соответствовала 0.1 и 0.05N.
В ряде экспериментов растворы подкисляли серной кислотой.
Соотношение минерал : раствор составляло 1, 5, 10, 20, 40 г/л.
Минерал взаимодействовал с раствором при постоянном перемешивании в течение 3 часов, при этом через каждые 10 минут измеряли pH раствора.
Затем раствор фильтровали и проводили химический анализ жидкой фазы, твердую фазу исследовали методами РФА и ДТА.
Также проведены длительные опыты (2 месяца).
После взаимодействия с сульфатными растворами твердая фаза приобретает более яркую окраску. В ней появляется большое количество тонкодисперсного материала.
На графиках видно некоторое снижение рН, которое вероятно является следствием образования на поверхности минерала твердой фазы, препятствующей дальнейшему протеканию реакции, скорость которой контролируется диффузией раствора через пленку новообразований. Если скорость диффузии ниже скорости гидролиза растворенной соли, наблюдается снижение рН раствора. Резкое повышение рН соответствует, вероятно, этапу достижения равновесия в системе (рис. 1).
При взаимодействии растворов сульфата никеля с серпентиновыми минералами происходит ионообмен между твердой и жидкой фазами и устанавливается равновесие между ними.
Коэффициент распределения никеля и магния в твердой фазе и растворе находится в зависимости от величины водородного показателя раствора.
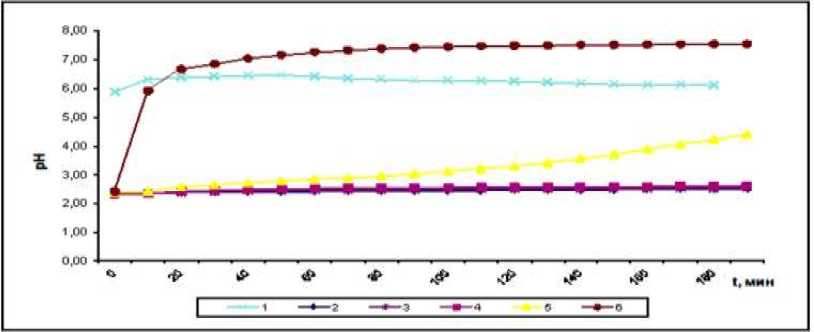
Рис. 1. Зависимость величины pH раствора от времени взаимодействия серпофита с раствором NiSO 4 : 1 - без подкисления, расход минерала 5 г/л, 2 – расход 1 г/л, 3 - расход 5 г/л, 4 – расход 10 г/л, 5 – расход 20 г/л, 6 – расход 40 г/л.
Если кислотность исходного раствора высокая (рН 1-3), то наряду с обменными реакциями MgоNi имеют место и процессы Mgо H или MgоН 3 О. Это приводит к образованию монтмориллонитоподобных (сапонитовых) слоев в серпентиновом минерале и, в конечном счете, к образованию пимелита Ni 3 Si 4 O 10 (OH) 2 .4H 2 O.
Вхождение никеля в биотит обусловлено обменными реакциями 2KоNi, MgоNi и, в меньшей мере, FeоNi. При этом никель может входить как в октаэдрические слои, так и занимать места межслоевых катионов. Состав тетраэдрических слоев практически не меняется. В случае биотита зависимость коэффициента распределения никеля и магния в твердой фазе и растворе от величины рН отсутствует. По-видимому, это обусловлено присутствием, как в растворе, так и в твердой фазе других катионов – калия и, в меньшей мере, железа.
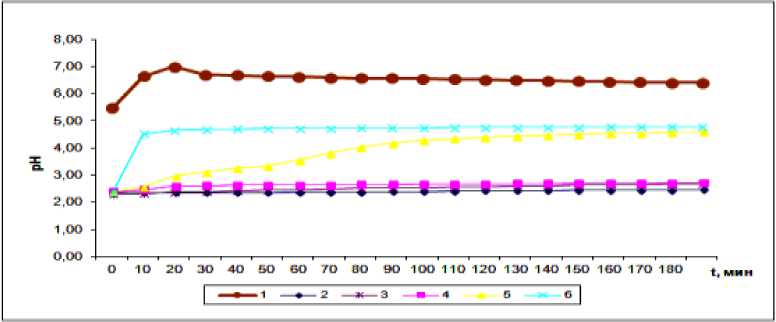
Рис. 2. Зависимость величины pH раствора от времени взаимодействия биотита (фр. -0,1) с 0.1N раствором сернокислого никеля: 1 - без подкисления (расход 5 г/л), 2 – расход 1 г/л, 3 - расход 5 г/л,4 – расход 10 г/л, 5 – расход 20 г/л, 6 – расход 40 г/л.
Механизм взаимодействия растворов сульфата никеля с тальком в основном сводится к обменным процессам типа MgоNi и приводит к образованию виллемсеита (Ni 3 Si 4 O 10 (OH) 2 ). Имеется зависимость между коэффициентом распределения содержания никеля и магния от рН.
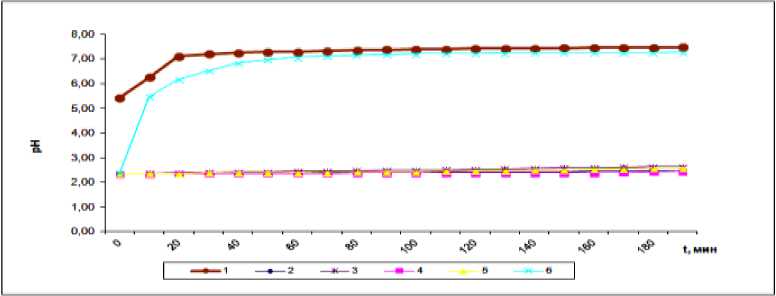
Рис. 3. Зависимость величины pH раствора от времени взаимодействия талька (фр. -0,1) с 0.1N раствором сернокислого никеля: 1 - без подкисления (расход 5 г/л), 2 – расход 1 г/л, 3 - расход 5 г/л,4 – расход 10 г/л, 5 – расход 20 г/л, 6 – расход 40 г/л.
7,00
6,00
5,00
t, мин
3,00
2,00
1,00
0,00
Рис. 4. Изменение pH расствора во времени при взаимодействии талька с 0,05 N раствором сернокислого никеля: 1 – с подкислением (расход 10г/л, степень извлечения никеля 22,17 %), 2 – без подкисления (расход 10 г/л, степень извлечения никеля 6,79%).
В долговременном опыте с тальком значение pH постепенно росло (рис. 4).
Рассмотрим обоснование механизма замещения MgоNi на примере серпофита и талька с использованием метода РФА. Съемку вели со скоростью 0.5 град./мин в интервале углов 29 от 6 о до 60 о для талька (рис. 5) и от 4о до 40о для серпофита (рис. 6).
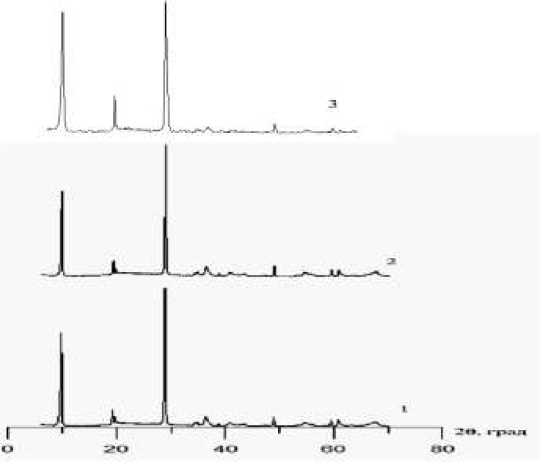
Рис. 5. Дифрактограммы талька: 1 – тальк после взаимодействия с 0.05N раствором сульфата никеля без подкисления; 2 – тальк после взаимодействия с 0.05N подкисленным раствором сернокислого никеля; 3 – тальк исходный.
Таблица 1.
Форма базальных рефлексов талька до и после взаимодействия с 0.05 N раствором сульфата никеля без подкисления (1) и с подкислением (2).
|
Параметр |
Образцы |
||
|
Исходный |
1 |
2 |
|
|
H/b 006 |
19,38 |
10,92 |
12,87 |
|
H/b0010 |
2,58 |
1,01 |
1,28 |
|
H/b 0012 |
1,00 |
0,56 |
0,96 |
|
I 006 /I 0010 |
19,375 |
16,620 |
13,353 |
|
I 0012 /I 0010 |
0,625 |
0,647 |
0,662 |
|
A 006 |
0,818 |
1,467 |
1,571 |
|
A 0010 |
0,950 |
1,182 |
1,250 |
|
A 0012 |
1,000 |
0,867 |
0,846 |
На дифрактограммах талька видно изменение кристаллической решетки, проявляющиеся в усилении асимметричности базальных рефлексов 006 и 0010 (табл. 1).
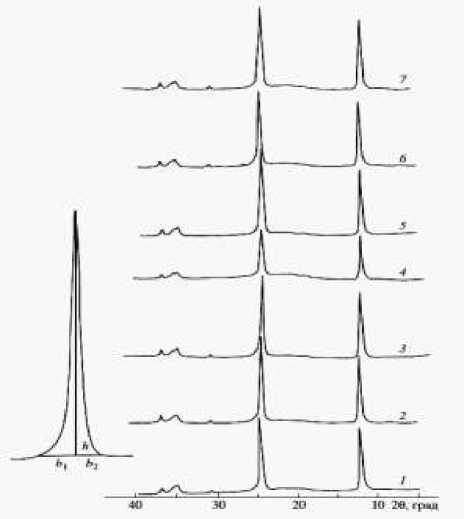
Рис. 6. Дифрактограммы серпофитов: 1- исходный минерал; 2 – после взаимодействия с дистиллированной водой; 3 – с 0.05 N раствором NiSO4, с 0.05 N подкисленными растворами NiSO4: 4 – pHисх 1.0, 5 – pHисх 2.0, 6 – pHисх 3.0, 7 – pHисх 4.85
На дифрактограммах серпофита фиксируется появление монтмориллонитоподобных слоев, беспорядочно чередующихся с серпентиновыми. Это проявляется в уширении и усилении асимметричности базальных рефлексов 001 и 002, что видно из данных табл. 2. Характерных для других слоистых силикатов дополнительных линий не наблюдается. Судя по характеру фона аморфной фазы нет. При большем соотношении минерал: раствор происходит упорядочение структуры, но при меньших соотношениях роль монтмориллонитоподобных слоев снова возрастает.
Таблица 2.
Форма базальных рефлексов серпофита до и после взаимодействия с 0.05 N раствором сульфата никеля
(расход серпофита: 1 – 15 г/л, 2 – 10 г/л, 3 – 6 г/л, 4 – 2 г/л).
|
Параметр |
Образцы |
||||
|
Исходный |
1 |
2 |
3 |
4 |
|
|
H/b 001 |
5.95 |
8.00 |
7.09 |
6.02 |
6.33 |
|
H/b 002 |
6.06 |
7.75 |
5.92 |
6.08 |
5.49 |
|
H/b 003 |
0.88 |
1.69 |
1.83 |
1.21 |
1.40 |
|
I 001 /I 002 |
0.848 |
0.862 |
0.902 |
0.830 |
0.812 |
|
I 003 /I 002 |
0.051 |
0.066 |
0.072 |
0.066 |
0.080 |
|
A 001 |
0.39 |
0.52 |
0.42 |
0.38 |
0.33 |
|
A 002 |
1.421 |
1.5 |
1.31 |
1.32 |
1.38 |
Термограммы талька после взаимодействия с подкисленным и без подкисления никельсодержащим раствором различаются. После взаимодействия талька с сульфатным раствором никеля без подкисления характерен широкий слабовыраженный эндоэффект в интервале 140о -380оС, и интенсивный эндоэффект с двумя минимумами при 977оС и 1008оС. При общей потере массы 4,91 мас. %, в низкотемпературной области теряется 0,35% (рис. 7).
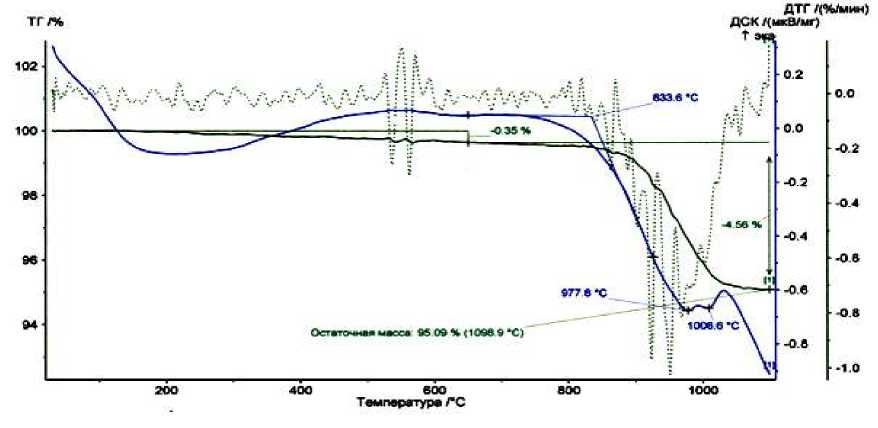
Рис. 7. Дериватограмма талька после взаимодействия с 0,05 N без подкисленния раствором сернокислого никеля.
Для талька после взаимодействия с 0,05 N раствором сернокислого никеля с подкислением наблюдается слабый низкотемпературный эффект 150о-220оС, интенсивный эндоэффект с минимумом при 941оС. Наблюдается широкий экзоэффект с максимумом при 500оС. Общая потеря массы составила 4,42 мас. % (рис. 8).
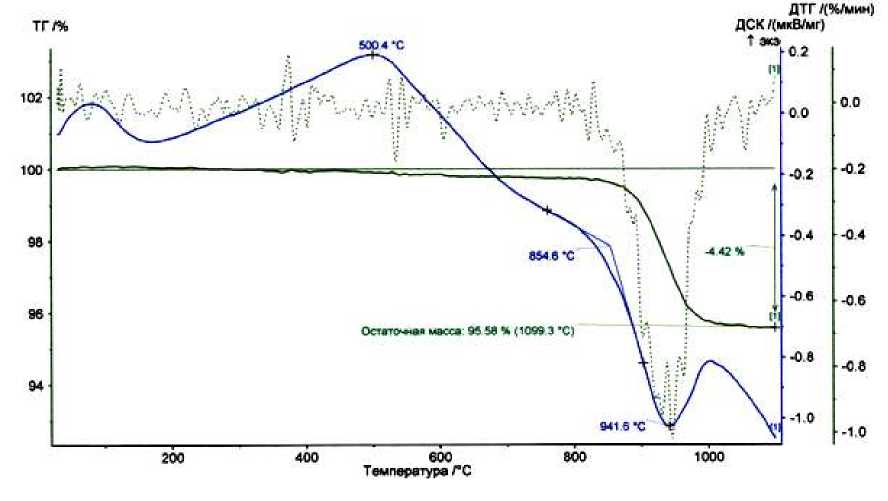
Рис. 8. Дериватограмма талька после взаимодействия с 0,05 N раствором сернокислого никеля с подкислением.
Для осаждения никеля из раствора использовали минералы фракции -0.1 мм с различным соотношением минерал : раствор. Исходная концентрация никеля в растворе - 2.93 г/л. Извлечение никеля растет с увеличением расхода минералов (табл. 3).
Таблица 3.
Концентрация никеля после взаимодействия с минералами.
|
Расход, г/л |
1 |
5 |
10 |
20 |
40 |
|
Тальк |
|||||
|
С Ni , г/л |
2.48 |
2.24 |
2.35 |
2.52 |
2.10 |
|
Извлечение, % |
15.36 |
23.55 |
19.80 |
13.99 |
28.33 |
|
Серпофит |
|||||
|
С Ni , г/л |
2.44 |
2.50 |
2.25 |
2.18 |
1.94 |
|
Извлечение, % |
16.72 |
14.68 |
23.21 |
25.60 |
33.79 |
|
Биотит |
|||||
|
С Ni , г/л |
2.52 |
2.35 |
2.37 |
2.21 |
1.88 |
|
Извлечение, % |
13.99 |
19.80 |
19.11 |
24.57 |
35.84 |
Заключение.
Поставлены эксперименты по моделированию добавления вещества геохимических барьеров к сульфатным растворам, содержащими ионы никеля, синтезу искусственных никельсодержащих гидросиликатов.
При взаимодействии раствора сернокислого никеля с минералами значение pH росло с увеличением расхода минерала. Значение pH росло значительней при добавлении серпофита.
Взаимодействие растворов сульфата никеля при рН=1-3 с серпентиновыми минералами приводит к образованию пимелитов (Ni 3 Si 4 O 10 (OH) 2 .4H 2 O). При меньшей кислотности растворов образуются минералы типа гарниерита Ni6Si4O10(OH)8.
Взаимодействие растворов сульфата никеля с тальком приводит к образованию виллемсеита (Ni 3 Si 4 O 10 (OH) 2 ).
При взаимодействии растворов сульфата никеля с биотитом практически не происходит изменения состава тетраэдрических слоев. Наблюдается образование минералов типа пимелитов
(Ni 3 Si 4 O 10 (OH) 2 .4H 2 O).
Извлечение никеля закономерно растет с увеличением соотношения минерал : раствор.
Использование искусственных геохимических барьеров позволит целенаправленно формировать концентраты цветных металлов с одновременным снижением нагрузки на окружающую среду.
Список литературы Искусственные геохимические барьеры для решения экологических и технологических задач
- Перельман А.И. Геохимия. -М.: Высшая школа, 1989. -582 с.


