Использование электрохимического способа мицеллирования водно-солевого раствора ионами металлов 1-й и 2-й групп для создания основы противоопухолевых препаратов
Автор: Наумова Галина Алексеевна, Фомичев Валерий Тарасович, Борисанова Яна Андреевна, Синельникова Юлия Юрьевна
Журнал: НБИ технологии @nbi-technologies
Рубрика: Технико-технологические инновации
Статья в выпуске: 1 (20), 2016 года.
Бесплатный доступ
В работе рассмотрены варианты использования противоопухолевых препаратов на основе растворов мицеллированных ионами металлов. Рассмотрены работы молодых ученых, работающих в ведущих российских лабораториях, и варианты поддержки их работ со стороны государства. Предложен эффективный и малозатратный способ мицеллирования ионами металлов водно-солевого раствора и результаты его анализа. Изучены результаты первых опытов воздействия раствора, полученного в процессе неорганического синтеза, на живые клетки. Предпринята попытка расширения исследовательской базы с целью продвижения данного проекта.
Мицеллирование, наноструктурированный раствор, электрохимический способ, ионы металла, противоопухолевый препарат
Короткий адрес: https://sciup.org/14968421
IDR: 14968421 | УДК: 544.6 | DOI: 10.15688/jvolsu10.2016.1.7
Use of electrochemical method of water-salt solutions micellization by ions of metals of 1st and 2nd groups for creation of basis for anticancer agent
Today active work on search of new drugs with more sharp selectivity and various range of antineoplastic action is conducted. Modern researches of scientists in the field of creation of antineoplastic preparations have passed to a nanolevel. Works on creation of the antioncological preparations based on use of properties of nanodimensional particles of metals are conducted in many laboratories and the oncological centers of the world. For this purpose connections practically of all biogenous elements are offered: Na, Mg, K, Ca, V, Cr, Mn, Fe, Co, Ni, Cu, Zn, Mo. It is well known that ions of many metals exert impact on a condition of immune system, being necessary metabolic components for all its links. Mechanisms of action of the existing onkopreparat on the basis of platinum metals, their pharmacokinetics, features of interaction with DNA currently are up to the end not studied. Refer their toxicity and not selectivity of action to the main shortcomings. For the purpose of reduction of toxicity of this class of onkopreparat and a minimizirovaniye of risk of injury of healthy cells of an organism, and also decrease in quantity of side effects new dosage forms of preparations are developed. In work options of use of antineoplastic preparations on the basis of solutions the mitsellirovannykh are considered by ions of metals. Works of the young scientists working in the leading Russian laboratories and options of support of their works are considered from the state. The effective and low-cost method of a mitsellirovaniye by ions of metals of water-salt solution and results of its analysis is offered. Results of the first experiences of impact of the solution received in the course of inorganic synthesis on living cells are studied. An attempt of expansion of research base for the purpose of promotion of this project is made.
Текст научной статьи Использование электрохимического способа мицеллирования водно-солевого раствора ионами металлов 1-й и 2-й групп для создания основы противоопухолевых препаратов
DOI:
Мицелла (новолат. micella, уменьшительное от лат. mica – «крошка, крупинка») – отдельная частица дисперсной фазы золя, то есть высокодисперсной коллоидной системы с жидкой дисперсионной средой. Мицелла состоит из ядра кристаллической или аморфной структуры и поверхностного слоя, включающего сольватно связанные молекулы окружающей жидкости [4].
Более половины населения всего земного шара живет в странах, где онкологические заболевания – одна из главных проблем национального здравоохранения. Ущерб, наносимый обществу и экономике, для некоторых народов разрушителен. Потери, которые наносят злокачественные опухоли здоровью человечества, по некоторым оценкам составляют до десяти процентов потерь от всех болезней [14].
Ежегодно в мире регистрируется более миллиона людей с онкологическими заболеваниями, из которых 61 % приходится на развитые страны. В России с начала 90-х годов прошлого века идет постоянный прирост случаев заболеваемости. Заболеваемость раком повышается во всех возрастных группах, однако наиболее быстро онкозаболеваемость растет у мужчин после 60 лет и у женщин после 50 лет. Рост заболеваемости у женщин в два раза выше, нежели у мужчин. По локализации опухолей наиболее распространены: трахея, бронхи, легкие (13,3 %), кожа (12,5 %, включая меланому), желудок (10,2 %), молочная железа (10,1 %) [19].
Задача поиска эффективного противоопухолевого препарата не является проблемой одного государства или народа. Многие развитые страны, такие как США, Япония и Германия, проводят активную политику в области исследований противоопухолевых препаратов. Ведущие онкологи обмениваются опытом и результатами своих исследований на международных конференциях и съездах, вовлекая в свои исследования молодых перспективных ученых [23].
В России в 2014 г. фонд содействия развитию малых форм предприятий в научно-технической сфере федерального конкурса молодых исследователей «УМНИК» поддержал работу по исследованию наночастиц биогенных металлов и их применение в медицине, которая выполняется в Южном федеральном университете [11]. Фонд является государственной некоммерческой организацией в форме федерального государственного бюджетного учреждения. По заверениям авторов работы, средства выигранного гранта дадут возможность довести проект до коммерческого продукта уже в 2016 году. Команде проекта удалось получить лекарственные наночастицы металлов разных размеров, форм и составов и вплотную перейти к работе над созданием стабильного раствора.
В 2015 г. стипендии Президента России были удостоены ученые и аспиранты Дальневосточного федерального университета за разработку инновационных противоопухолевых препаратов. Вообще по итогам всероссийского открытого публичного конкурса на получение стипендий Президента РФ наград были удостоены 585 исследователей в возрасте до 35 лет. Все они выполняют перспективные научные разработки по приоритетным направлениям модернизации российской экономики [20].
В большинстве своем препараты для лечения онкологических заболеваний – препараты, задерживающие развитие клеток злокачественных опухолей и перерожденных форменных элементов крови при заболеваниях крови, а также тканей, близких по темпам клеточного деления к тканям злокачественных опухолей.
Противоопухолевые препараты, получившие практическое применение в онкологии, принято делить на следующие группы:
-
1. Гормональные препараты (половые гормоны, кортикостероиды).
-
2. Алкилирующие агенты: хлорэтилами-ны («Эмбихин», «Новэмбихин», «Сарколизин»,
-
3. Антиметаболиты: антагонисты пурина («6-меркаптопурин»), антагонисты пиримидина («5-фторурацил»), антагонисты фолиевой кислоты («Метотрексат»).
-
4. Вещества растительного происхождения: винка-алкалоиды («Винбластин», «Винк-ристин»), колхамин.
-
5. Противоопухолевые антибиотики (актиномицины С и D, «Хризомаллин», «Рубомицин»).
-
6. Прочие препараты («Натулан») [12].
«Допан», «Дегранол»), этиленимины («Тиофосфамид», «Дипин», «Тиодипин»), метансульфониды («Миелосан»).
На сегодняшний день ведется активная работа по поиску новых лекарств с более высокой избирательностью и различным спектром противоопухолевого действия. Современные исследования ученых в области создания противоопухолевых препаратов перешли на наноуровень. Работы по созданию проти-воонкологических препаратов, основанных на использовании свойств наноразмерных частиц металлов, ведутся во многих лабораториях и онкологических центрах мира. Для этой цели предлагаются соединения практически всех биогенных элементов: Na, Mg, K, Ca, V, Cr, Mn, Fe, Co, Ni, Cu, Zn, Mo.
Хорошо известно, что ионы многих металлов оказывают влияние на состояние иммунной системы, являясь необходимыми метаболическими компонентами для всех ее звеньев [1]. Влияние вновь синтезированных металлосодержащих наночастиц на функции иммунной системы, в частности на структурное и функциональное состояние ее органов, описано в работах [1; 2; 3; 13; 21].
На сегодняшний день в клинической практике широко используются следующие основные типы металлосодержащих противоопухолевых препаратов:
-
1. Препараты на основе комплексов платины (II) и платины (IV) (цисплатин, карбоплатин и др.).
-
2. Препараты на основе комплексных соединений других металлов (Re, Ru, Os, Co, Cu, Fe, Ni и др.) – металлоинтеркаляторы.
Механизмы действия существующих онкопрепаратов на основе платиновых металлов, их фармакокинетика, особенности взаимодействия с ДНК на настоящий момент до конца не изучены. К основным недостаткам относят их токсичность и неизбирательность действия. С целью уменьшения токсичности данного класса онкопрепаратов и минимизирования риска повреждения здоровых клеток организма, а также снижения количества побочных эффектов разрабатываются новые лекарственные формы препаратов.
Спектр онкопрепаратов из второй группы очень широк. Синтезируются и исследуются комплексы металлов с органическими лигандами, обладающие противоопухолевой активностью. Такие комплексы – металлоин-теркаляторы – состоят из центрального иона металла, окруженного ароматическими гетероциклическими планарными кольцами, способными встраиваться между парами оснований ДНК за счет электростатического, ионного, гидрофобного взаимодействия. Метал-лоинтеркаляторы хорошо растворяются в воде, что является важным свойством в фармакологии [3].
Один из наиболее простых и эффективных способов «доставки» лекарства в организм человека – трансдермальный (через кожу), который подходит для большинства биологически активных соединений, вне зависимости от их молекулярной массы (размеров) или физико-химических свойств. Считается, что лучшие «переносчики» – неорганические наночастицы. К ним относятся соединения оксида кремния, а также различных металлов (золото, серебро, платина). Такая наночастица имеет внешнюю оболочку и кремниевое ядро. Внешняя оболочка сформирована атомами металла. Использование металлов позволяет создавать переносчики, обладающие рядом уникальных свойств. Так, их активность (и, в частности, высвобождение терапевтического агента) может быть модулирована термическим воздействием (инфракрасное излучение), а также изменением магнитного поля [5].
Разработка новых низкомолекулярных металлосодержащих противоопухолевых соединений ведется и в научно-исследовательском институте механики при МГУ им. Ломоносова. Идея предлагаемого проекта заключается в разработке принципиально нового подхода (с использованием стратегии медицинской химии: «выбор валидированной мишени – компьютерный молекулярный дизайн – направленный синтез – скрининг») к созданию соединений металлов с противоопухолевым действием, базирующегося на двух основных принципах. Первый принцип построен на модификации молекулы органической субстанции известного препарата (лонидамин, бекса-ротин, фторурацил) путем введения металла с доказанной фармакологической активностью с целью повышения эффективности действия по отношению к опухолевым клеткам. Второй принцип: исследования модификации молекулы известного металлосодержащего препарата путем введения протекторных органических групп (токоферол, мексидол) с целью снижения общей неспецифической токсичности по отношению к здоровым клеткам организма. Предложенные подходы позволят решить важную задачу создания новых нетривиальных по структуре и биомолекулярному механизму действия соединений металлов, обладающих более высокой эффективностью и более низкой токсичностью по сравнению с известными препаратами. Задачей проекта является разработка новой стратегии создания оригинальных физиологически активных комплексов Au, Sn и Ru, обладающих анти-пролиферативной и/или антиметастатической активностью in vitro и in vivo, и получение экспериментальных образцов соединений-лидеров для ранних доклинических испытаний. Основное внимание будет сконцентрировано на подавлении возможности неограниченного деления клеток, а также на подавлении процесса ангиогенеза. Будет осуществлено компьютерное молекулярное моделирование и молекулярный дизайн металлосодержащих структур [13].
В 2009 г. научными сотрудниками Ростовского научно-исследовательского онкологического института были представлены научному сообществу результаты экспериментального исследования действия наночастиц металлов (Zn, Cu, Fe и их сплава) на рост перевиваемых опухолей мышей [24]. В ходе проведения проекта было доказано, что наночастицы обладают выраженным противоопухолевым эффектом, вызывая регрессию опухоли, повышая процент погибших и дистрофически измененных опухолевых клеток, что способствует значительному увеличению продолжительности жизни подопытных мышей.
В работе были использованы наночастицы размером 300–1000 Å, представляющие собой ультрадисперсные порошки металлов Cu, Zn, Fe и их сплава. Для исследовани брались белые беспородные мыши массой 18– 20 г, которым прививались саркомы 37 и 180. В случае опухоли С37 после введения наночастиц установлено резкое подавление накопления асцитической жидкости и снижение количества в ней живых опухолевых клеток. На модели опухоли С180 показано, что введение наночастиц способствует полной регрессии опухоли, наиболее быстро развивающейся при введении наночастиц сплава и приводящей к существенному (3–4-кратному) повышению продолжительности жизни мышей. При этом в исследуемом препарате были задействованы наночастицы ультрадисперсных порошков металлов (Cu, Zn, Fe и их сплава), которые синтезировались на Саратовском плазмохимическом комплексе ФГУП РФ ГНЦ ГНИИХТЭОС.
В дальнейшем, в 2010–2013 гг., ФГУ «Ростовский научно-исследовательский онкологический институт» Росмедтехнологий для проведения аналогичных экспериментов на белых мышах с привитой саркомой использовал водно-солевые мицеллированные металлами (Zn, Cu, Cd) растворы, предоставленные волгоградскими учеными. Растворы были приготовлены электрохимическим способом по уникальной технологии, защищенной патентами РФ [18].
Технология получения мицеллированных растворов посредством электролиза относится в частности к способу электрохимического получения раствора гипохлоритов магния и меди. Способ включает электролиз основной базы, полученной растворением природного бишофита в непроточном бездиафрагменном электролизере с медными электродами, на которые подают электрический ток определенного напряжения при соответсвующей температуре электролита. Электролиз осуществляют в течение 0,25–0,5 часа. Техническим результатом является увеличение выхода гипохлоритов меди и магния на 18–20 % и снижение затрат электрической энергии на получение единицы продукта на треть.
Известен способ получения раствора гипохлоритов магния, включающий электролиз раствора хлоридов металлов с использо- ванием нерастворимого анода, при этом электролизу подвергают раствор, содержащий хлорид магния в виде бишофита, борную кислоту, сульфат магния и сульфат кальция при рН 4,5–6,0 в электролизере без диафрагмы с анодом из графита и катодом из титана при плотности тока 8–12 А/дм2 и температуре 20– 50 °С [16]. Недостатком такого способа является отсутствие растворимого анода. На используемом в качестве анода графите протекают реакции окисления хлорид-ионов с генерацией гипохлорит-ионов, что приводит к увеличению плотности тока. В остальном ионный состав используемого раствора остается неизменным. Недостатком такого способа являются высокие плотности тока, используемые в способе, и длительное осуществление процесса с дополнительным интенсивным перемешиванием раствора.
Также известен способ получения раствора гипохлорита магния, включающий электролиз водного раствора хлоридов магния в виде бишофита в электролизере с анодом из угольного графита и катодом из стали, на постоянном токе при плотности тока 0,1– 1,5 А/дм2 и температуре электролита 20 °С [15], недостатком которого является использование в качестве анода графита. Такой способ позволяет получать только один продукт – гипохлорит магния.
Существует способ получения гипохлоритов магния и меди, включающий электролиз водного раствора хлоридов магния, полученных растворением природного бишофита в непроточном бездиафрагменном электролизере с медными электродами, на которые подают постоянный ток напряжением 1–25 В плотностью 1–10 A/дм2, при концентрации электролита 0,5–2 % и температуре 20–25 °С, процесс электролиза осуществляют в течение 0,5 часа [17]. Недостатком этого способа является использование постоянного тока. В результате за счет постоянства токового режима происходит поляризация электродов. В итоге для получения единицы продукта (гипохлоритов магния и меди) расходуется излишнее количество электрической энергии и уменьшается выход по току получаемой продукции.
С целью повышения производительности процесса на медные электроды подается импульсный ток средней плотности, с соот- ветствующей частотой и скважностью импульсов, при определенной концентрации электролита и его кислотности. Процесс электролиза осуществляется в течение 0,25–0,5 часа. Это позволяет увеличить выход по току продукта гипохлорита магния и меди при плотностях тока, значения которых равны плотностям постоянного тока. Заявляемый способ может быть реализован в электролизере с неразделенными анодным и катодным пространствами непрерывного или периодического действия с медным катодом в растворе минерала бишофита. Примеры конкретного исполнения представлены в таблицах 1 и 2, где показано влияние плотности, скважности на выход по току ионов меди и активного хлора.
Использование постоянного тока (см. табл. 1) позволяет при концентрации электролита 10 % получать при плотности тока 0,5 А/дм2 выход по току для гипохлорита меди 55,3 %, гипохлорита магния – 45,1 %. Применение импульсного тока частотой 100 Гц той же плотности при скважности 2 (см. табл. 2) увеличивает выход гипохлорита меди до 65,0 %. В диапазоне используемых равных плотностей тока увеличение плотности импульсного тока до 1,0 А/дм2 (скважность 2) приводит к возрастанию выхода по току гипохлорита меди с 61,0 для постоянного до 69,4 % (увеличение на 13,8 %). Увеличение скважности импульсного тока частотой 100 Гц от 2 до 3 при одинаковых значениях плотностей тока (см. табл. 2) из растворов электролита одинаковой концентрации приводит к большему выходу по току гипохлорита меди, чем при использовании постоянного тока. При плотности 0,75 А/дм2 увеличение скважности от 2 до 3 и 4 соответственно по отношению к постоянному току составляет: 2 – 14 %, 3 – 16,4 %, 4 – 16,5 %.
Использование импульсного тока частотой 200 Гц (см. табл. 2) при равных с постоянным током плотностях и концентрации электролита 5 % также приводит к большему выходу гипохлорита меди. Например: при плотности тока 0,5 А/дм2 увеличение скважности от 2 до 4 приводит к увеличению выхода продукта, по сравнению с постоянным током, на проценты: 2 – 20,5 %, 3 – 18 %, 4 – 17 %. Применение импульсного тока частотой 100 Гц скважностью 2, 3, 4 при одинаковых с посто-
Таблица 1
Влияние концентрации электролиза и плотности постоянного тока на выход по току
|
Плотность тока, А/дм² |
Концентрация электролита, % |
Выход по току, % |
|
|
Гипохлорит меди |
Гипохлорит магния |
||
|
0,5 |
10 |
55,3 |
45,1 |
|
0,75 |
10 |
58,1 |
47,2 |
|
1,0 |
10 |
61,0 |
48,2 |
|
0,5 |
5 |
44,3 |
27,1 |
|
0,75 |
5 |
51,0 |
29,0 |
|
1,0 |
5 |
54,7 |
30,0 |
Таблица 2
Влияние концентрации электролиза и плотности импульсного тока на выход по току (1, 2, 3 – скважности)
|
Плотность тока, А/дм² |
Концентрация электролита, % |
Выход по току, % |
|||||||||||
|
при импульсном токе 100 Гц |
при импульсном токе 200 Гц |
||||||||||||
|
Гипохлорит меди |
Гипохлорит магния |
Гипохлорит меди |
Гипохлорит магния |
||||||||||
|
2 |
3 |
4 |
2 |
3 |
4 |
2 |
3 |
4 |
2 |
3 |
4 |
||
|
0,5 |
10 |
65,0 |
65,8 |
66,2 |
35,0 |
34,2 |
35,3 |
66,1 |
66,4 |
67,2 |
33,9 |
33,6 |
32,8 |
|
0,75 |
10 |
67,5 |
67,6 |
67,7 |
32,5 |
32,7 |
32,3 |
67,3 |
67,1 |
67,4 |
32,7 |
32,9 |
32,6 |
|
1,0 |
10 |
69,4 |
69,0 |
68,8 |
30,6 |
31,0 |
31,2 |
68,2 |
67,9 |
67,8 |
31,8 |
32,1 |
32,2 |
|
0,5 |
5 |
52,4 |
52,3 |
52,2 |
47,6 |
47,7 |
47,8 |
53,4 |
52,5 |
52,1 |
46,6 |
47,5 |
47,9 |
|
0,75 |
5 |
52,0 |
52,1 |
52,7 |
48,0 |
47,9 |
47,3 |
51,0 |
51,7 |
52,1 |
49,0 |
48,3 |
47,9 |
|
1,0 |
5 |
55,7 |
55,0 |
54,8 |
44,3 |
45,0 |
45,2 |
53,0 |
53,4 |
53,4 |
47,0 |
46,5 |
46,6 |
янным током плотностях тока приводит к сокращению затрат электрической энергии на единицу массы продукта. Например, при плотности тока 0,5 А/дм2 в электролите с концентрацией 10 % удельные затраты энергии составляют 5,1 кВт • ч/кг, при импульсном токе 100 Гц и, соответственно, скважностях 2, 3, 4 затраты составляют: 2 – 4,1 кВт • ч/кг (24 % выигрыша), 3 – 4,3 кВт • ч/кг (18,6 % выигрыша), 4 – 4,6 кВт • ч/кг (4,1 % выигрыша). При использовании тока частотой 200 Гц при тех же скважностях и плотности тока 1,0 А/дм2: 2 – 4,2 кВт • ч/кг (73,8 % выигрыша), 3 – 4,6 кВт • ч/кг (58,7 % выигрыша), 4 – 4,9 кВт • ч/кг (48,9 % выигрыша).
Приведенные примеры по влиянию плотности тока, формы, частоты и скважности импульсного тока в сравнении с постоянным током одинаковой плотности тока показывают, что выход по току продукта электролиза увеличивается. Это позволяет в процессе электролиза раствора бишофита при замене постоянного тока импульсным током при тех же плотностях тока увеличить выход по току гипохлоритов меди и снизить расход электрической энергии.
Анализ мицеллированного водно-солевого раствора, полученного в процессе элек- тролиза с целью подтверждения появления в ионном растворе гетерогенных нанораз-мерных структур, выполнялся в лабораториях СГУ.
Процесс измерений происходил следующим образом.
Из сосуда с образцом проводился отбор пробы объемом 1 мл, после чего проба вносилась в U-образную капиллярную кювету для измерения электрического потенциала. Кювета помещалась в анализатор, и проводилось термостатирование пробы при температуре 25 °С в течение 2 мин. После этого анализировался гранулометрический состав и измерялся дзета-потенциал образцов.
В образце после отстаивания обнаружены частицы размером от 0,3 единицы мкм. В первом измерении присутствует единственный пик в области 20 нанометров. В последующих измерениях данный пик исчезает.
В распределении по размерам для образца после интенсивного перемешивания зафиксированы пики от 2 до 6 мкм. После воздействия ультразвука положение пиков сместилось к 0,8 мкм и не менялось в течении нескольких измерений. В обоих образцах дзета-потенциал поменял свой знак на положитель- ный и его средняя величина составила 1,95 и 1,84 мВ соответственно.
После центрифугирования в образце присутствует только один пик с максимумом в области 0,62 нм (рис. 1). При этом положение пика не менялось ни во время (несколько последовательных измерений), ни при увеличении длительности центрифугирования. В процессе построения распределения частиц по размерам был получен высокий индекс полидисперсности, который свидетельствует о присутствии ассоциатов и частиц больших размеров, однако их концентрация оказалась незначительной, и такие частицы не повлияли на распределение. Выдержка во времени приводит к образованию коагуляционных структур различной плотности (рис. 2). Средняя величина дзета-потенциала центрифугированного образца составила -0,2 мВ, при этом меняясь от +3,96 мВ в первом измерении до -5,36 мВ в последнем, что может объясняться высокой электрокинетической инер- ционностью ассоциатов, присутствующих в пробе (рис. 1, 2).
Для предварительной оценки взаимодействия полученных структур на клеточном уровне на примере растительных клеток изучался эффект проникновения мицеллярных структур в основу клетки. Эксперимент проводился в лаборатории аналитической микроскопии испытательного центра «Центр коллективного пользования» Российского университета дружбы народов. В ходе исследования были изучены микропрепараты срезов корней пшеницы, пророщенной с использованием мицеллированного раствора (бишофита) и обычного ионного раствора бишофита. Оценка интенсивности флюоресценции (в относительных единицах) срезов корней проводилась с помощью программы EZ-C1. Флюоресценция в образцах ионного раствора практически не наблюдалась (см. рис. 3).
Интенсивность флюоресценции после использования мицеллированного водно-со-
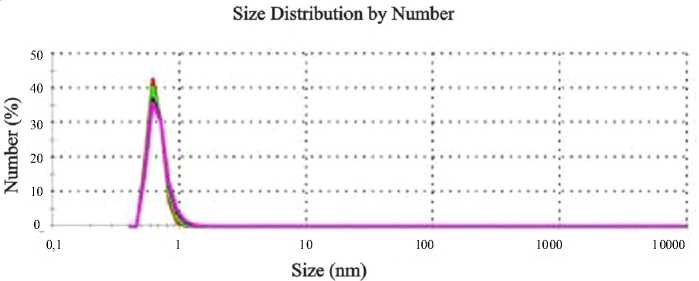
Рис. 1. Гранулометрический состав образцов водно-солевого мицеллированного раствора
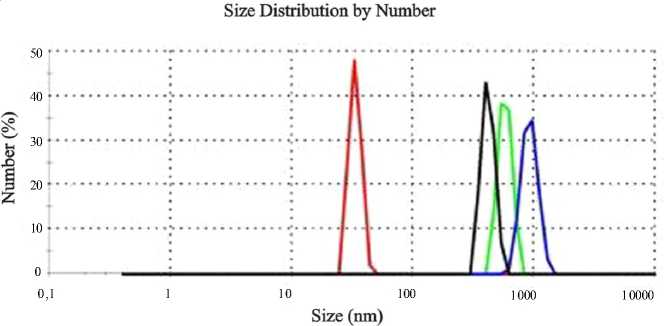
Рис. 2. Гранулометрический состав образцов водно-солевого мицеллированного раствора после центрифугирования
левого раствора значительно увеличилась (рис. 4).
По технологии получения растворов ионов меди были разработаны системы с ионами цинка и кадмия. Мицеллированные электрохимическим способом растворы исследовались в лабораториях ФГУ Ростовского научно-исследовательского онкологическо- го института на предмет изучения цитотоксического эффекта ионов меди и цинка на крысах и белых беспородных мышах с привитой саркомой. Ставилась задача определения влияния мицеллы на рост перевиваемых опухолей in vivo, а также на жизнеспособность различных клеток при инкубации in vitro. Результаты первых опытов были предоставлены
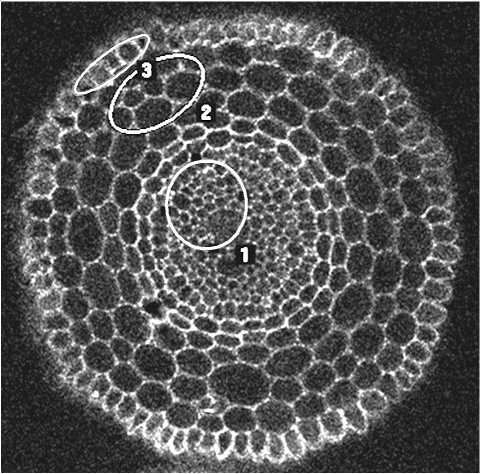
Рис. 3. Общая картина флюоресценции среза корня пшеницы, пророщенной с помощью ионного раствора: 1 – фрагмент осевого цилиндра; 2 – фрагмент коры; 3 – фрагмент эпидермы
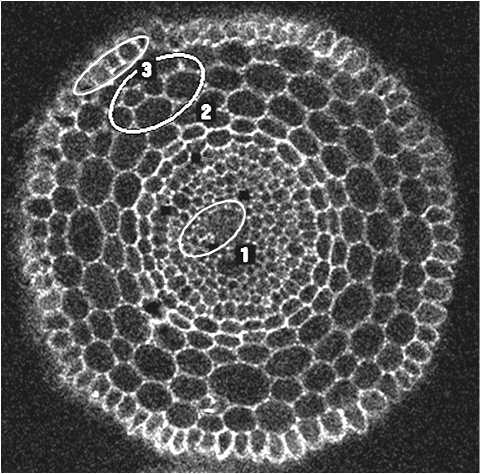
Рис. 4. Общая картина флюоресценции среза корня пшеницы, пророщенной с использованием мицеллированного раствора бишофита: 1 – фрагмент осевого цилиндра; 2 – фрагмент коры; 3 – фрагмент эпидермы
сотрудниками лаборатории для анализа разработчикам мицеллированного раствора.
Первая серия опытов проводилась с мицеллами, которые содержали Zn, Cu и базу. В результате первых экспериментов по оценке действия мицелл на культуры опухолевых клеток было выявлено, что мицеллы Zn и Cu способствуют повышению гибели опухолевых клеток и лимфоцитов в 2–10 раз при кратковременной инкубации in vitro (30–60 мин). Результат зависел в первую очередь от исходного состояния культуры, а также от концентрации мицелл. В ходе исследования оказалось, что база тоже цитотоксична. Из-за этого факта затрудняется определение эффекта самого мицеллированного раствора.
Опыты in vivo проводились на основе уже другой базы. Вторую серию мицелл испытывали на двух видах перевиваемых опухолей. Мышам вводили внутрибрюшинно саркому 37, а крысам подкожно лимфосаркому Плисса. Вводили ежедневно, опухоли измеряли еженедельно. Животные переносили введение этих мицелл без видимых проявлений токсичности.
Результаты были видны уже через 2– 3 недели. Из пяти мышей, которым вводили опухоль С37, у двух животных продолжался рост, а у трех развилась регрессия с уменьшением объема в 6–19 раз. Несмотря на то, что регрессия происходила не сразу, на первой недели саркома продолжала увеличиваться, уже в течение 2–3-й недели начиналась регрессия. Затем мыши были забиты для морфологического исследования опухоли и других органов. На саркоме 37 изучали действие мицеллы цинка.
На крысах был опробован эффект мицелл цинка, меди и кадмия. При введении мицелл цинка были получены следующее результаты: из пяти крыс у четырех опухоль росла; они погибли через один месяц. Только у одной крысы началась регрессия через два месяца, но и она сопровождалась явлениями некроза.
После введения мицелл меди все подопытные животные погибли через 1,5 месяца в результате роста опухоли. В ходе исследования у некоторых особей происходило торможение роста опухоли, но потом он опять возобновлялся.
При введении мицелл кадмия через 20 дней у двух из пяти крыс наступила рег- рессия, позже – еще у одной крысы (через 1,5 месяца), у двух опухолевый рост продолжался, через 20 дней они погибли. На 1-й и 2-й неделе объем опухоли у крыс этой группы был в 10 и в 3 раза меньше соответственно. Продолжительность жизни этих животных составила 2 месяца.
Однако немногочисленность и неоднозначность данных не позволяет сделать определенного заключения о противоопухолевом действии мицелл, и тем более о его механизмах. Обобщив эксперименты, можно сделать выводы, что мицеллы, содержащие металлы, проявляют цитотоксичность по отношению к различным клеткам. Мицеллы на основе металлов способны вызывать торможение или регрессию перевиваемых опухолей у лабораторных животных. В этом плане представляет интерес дальнейшее исследование растворов мицеллированных металлами электрохимическим способом.
Используемая в данном случае технология мицеллирования растворов позволяет значительно уменьшить стоимость противоопухолевых препаратов в сравнении с ранее рассмотренными решениями, в которых использовались дорогостоящие компоненты или трудоемкий процесс производства. Предлагаемая технология использования неорганических соединений синтеза позволяет существенно упростить процесс производства, не снижая при этом эффективность и результативность противоопухолевых лекарств. Учеными показано влияние наночастиц металлов на опухолевые процессы, но поиск идеальной формулы препарата на их основе только начинаются. Разработчики проекта производства электрохимически мицеллированной базы готовы предоставить свои образцы всем заинтересованным лабораториям для дальнейшего изучения ее состава и механизма действия с целью создания новых эффективных противоопухолевых препаратов.
Список литературы Использование электрохимического способа мицеллирования водно-солевого раствора ионами металлов 1-й и 2-й групп для создания основы противоопухолевых препаратов
- Златник, Е. Ю. Особенности морфофункционального состояния тимуса мышей при введении наночастиц различных металлов/Е. Ю. Златник, Л. В. Передреева, О. Ф. Евстратова//Известия высших учебных заведений. Северо-Кавказский регион. Серия «Естественные науки». -2011. -№ 1 (161). -С. 106-109.
- Кудрин, А. В. Микроэлементы в иммунологии и онкологии/А. В. Кудрин, О. М. Громова. -М.: Издат. группа «ГЭОТАР-Медиа», 2007. -544 с.
- Металлы в живых организмах: учеб. пособие для лекционного курса «Основы бионеорганической химии»/Н. А. Улахович, Э. П. Медянцева, С. С. Бабкина, М. П. Кутырева, А. Р. Гатаулина. -Казань: Казан. ун-т, 2012. -102 с.
- Мицелла//Большая научная библиотека. -Электрон. дан. -Режим доступа: http://bse.sci-lib.com/article077147.html (дата обращения: 25.03.2016). -Загл. с экрана.
- Наночастицы в медицине и фармацевтике//Фонд «Вечная молодость»: . Статьи. -05.10.2009. -Электрон. текстовые дан. -Режим доступа: http://vechnayamolodost.ru/articles/?PAGEN_2=2&PAGEN_1=331 (дата обращения: 20.03.2016). -Загл. с экрана.
- Наумова, Г. А. Инновационная технология повышения биологической активности раствора минерала бишофита/Г. А. Наумова, В. Фомичев, О. Ахременко//Вестник Волгоградского государственного университета. Серия 10, Инновационная деятельность. -2013. -№ 1. -С.131-137. - DOI: 10.15688/jvolsu10.2013.1.24
- Наумова, Г. А. Современные модели оценки эффективности инновационных проектов с учетом инвестиционных рисков на ранних стадиях pre-seed и seed/Г. А. Наумова, О. Ю. Ахременко//Вестник Волгоградского государственного университета. Серия 10, Инновационная деятельность. -2013. -№ 2 (9). -С. 27-33. - DOI: 10.15688/jvolsu10.2013.2.4
- Наумова, Г. А. Интерактивные формы открытого научно-образовательного семинара/Г. А. Наумова, Я. А. Борисанова, А. Ю. Арзамасцева//Вестник Волгоградского государственного университета. Серия 10, Инновационная деятельность. -2014. -№ 6 (15). -С. 15-24. - DOI: 10.15688/jvolsu10.2014.6.2
- Наумова, Г. А. Оценка инвестиционной привлекательности инновационных проектов на различных стадиях коммерциализации/Г. А. Наумова, Я. А. Белоножко//Вестник Волгоградского государственного университета. Серия 10, Инновационная деятельность. -2013. -№ 2 (9). -С. 34-42. - DOI: 10.15688/jvolsu10.2013.2.5
- Наумова, Г. А. Построение интеграционной модели оценки эффективности инновационных проектов/Г. А. Наумова, О. Ю. Ахременко, Ю. Ю. Синельникова//Вестник Волгоградского государственного университета. Серия 10, Инновационная деятельность. -2015. -№ 4 (19). -С. 20-28. - DOI: 10.15688/jvolsu10.2015.4.3
- Погонцева, Е. Студентка ЮФУ работает над созданием лекарства от рака на основе наночастиц биогенных металлов/Е. Погонцева//Фармацевтический вестник. -2015. -Электрон. дан. -Режим доступа: http://www.pharmvestnik.ru/publs/lenta/v-rossii/studentka-jufu-rabotaet-nad-sozdaniem-lekarstva-ot-raka-na-osnove-nanochastits-biogennyx-metallov.html (дата обращения: 20.03.2016). -Загл. с экрана.
- Противоопухолевые средства//Медицинская энциклопедия. -Электрон. дан. -2011. -Режим доступа: http://www.medical-enc.ru/15/protivoopuholevye-sredstva.shtml (дата обращения: 20.03.2016). -Загл. с экрана.
- Разработка новых низкомолекулярных металлосодержащих противоопухолевых соединений. Компьютерный молекулярный дизайн, направленный синтез и скрининг: /Милаева Е. Р. (рук. НИР) //Истина. -2014. -Электрон. дан. -Режим доступа: http://istina.msu.ru/projects/7884582/(дата обращения: 20.03.2016). -Загл. с экрана.
- Рак -проблема века//Медицина: научно-популярный журнал. -2016. -Электрон. текстовые дан. -Режим доступа: http://www.medjour.ru/meditsina-segodnya/32-problemy-veka (дата обращения: 12.03.2016). -Загл. с экрана.
- Способ получения гипохлорита: пат. 2238348 Рос. Федерация: МПК С25В 1/26, 1/18/Фомичев В. Т., Куликова И. А., Лебедев Д. Н., Бурдова Н. Г., Геращенко А. А.; патентообладатель Государственное образовательное учреждение высшего профессионального образования «Волгоградский государственный архитектурно-строительный университет» (ВолгГАСУ). -Заявл. 30.07.2003; опубл. 20.10.2004.
- Способ получения раствора смеси хлората и гипохлорита магния: а. с. 1624057 СССР: МПК С25В 1/26/Лецких Е. С., Коробицын А. С., Обозюк В. И., Большакова Е. В.; заявитель и патентообладатель Предприятие ПЯА-7125. -Заявл. 06.01.1987; опубл. 30.01.1991, Бюл. № 4.
- Способ получения фунгицидов меди: пат. 2361016 Рос. Федерация: MПK С25В 1/00/Фомичев В. Т., Лаврикова Н. А.; патентообладатель Государственное образовательное учреждение высшего профессионального образования «Волгоградский государственный архитектурно-строительный университет» (ВолгГАСУ). -№ 2008101270/15; заявл. 09.01.2008; опубл. 10.07.2009.
- Способ электрохимического получения раствора гипохлоритов магния и меди: пат. 2466214 Рос. Федерация: МПК C25B 1/26/Фомичев В. Т., Наумова Г. А.; заявитель и патентообладатель ИП Богданов С.А. -№ 2011127199/02; заявл. 01.07.2011; опубл. 10.11.2012, Бюл. № 31. -7 с.
- Статистика заболеваемости раком//Книга медика. -Электрон. текстовые дан. -2016. -Режим доступа: http://www.knigamedika.ru/novoobrazovaniya-onkologiya/statistika-zabolevaemosti-rakom.html#ixzz42xtUyDkP (дата обращения: 12.03.2016). -Загл. с экрана.
- Стипендиатов Президента России наградили на Ученом совете ДВФУ//Лента новостей Владивостока. -Электрон. дан. -2015. -Режим доступа: http://vladivostok-news.net/other/2015/03/26/60202.html (дата обращения: 05.04.2016). -Загл. с экрана.
- Структурно-функциональные и биохимические изменения в органах иммунной системы при противоопухолевом действии наночастиц меди в эксперименте/Е. В. Шалашная, И. А. Горошинская, П. С. Качесова, Г. В. Жукова //Бюллетень экспериментальной биологии и медицины. -2011. -Т. 152, № 11. -С. 552-556.
- Хаитов, Р. М. Современные иммуномодуляторы: основные принципы их применения/Р. М. Хаитов, Б. В. Пинегин//Иммунология. -2000. -№ 5. -С. 4-7.
- Шелепко, С. Мировой рынок противоопухолевых препаратов/С. Шелепко//Российская Фармацевтика. Эффективность, безопасность, качество. -Электрон. текстовые дан. -2015. -Режим доступа: http://pharmapractice.ru/116836 (дата обращения: 05.04.2016). -Загл. с экрана.
- Экспериментальное исследование влияния наночастиц металлов на опухолевый рост/Ю. С. Сидоренко, Е. Ю. Златник, Л. В. Передреева, В. Б. Бородулин//Конференция «Нанотехнологии в онкологии 2009», г. Москва, 9-10 окт. 2009 г. -М., 2009.


