Использование картриджей для твердофазной экстракции при анализе органических соединений в природных водах
Автор: Потурай В.А.
Журнал: Региональные проблемы @regionalnye-problemy
Рубрика: Геоэкология
Статья в выпуске: 3 т.28, 2025 года.
Бесплатный доступ
В статье излагаются основные этапы процесса твердофазной экстракции как метода пробоподготовки природных, в частности, термальных и минеральных холодных вод к последующему инструментальному анализу органического вещества средней летучести методом газовой хроматографии в сочетании с масс-спектрометрией. Применение стандартных картриджей, оборудованных фриттами, несет в себе большой риск загрязнения экстракта сторонними примесями, которые проявляются в виде отдельных пиков на хроматограмме. В работе рассмотрены картриджи двух основных производителей: DSC-18 Supelco и StrataC18-EPhenomenex. Дихлорметан (хлористый метилен), используемый в качестве элюирующего растворителя, вступает в реакцию со стенками картриджа, результатом которой являются экстракция н-алканов и силоксанов из полипропилена, из которого изготовлен картридж. Замена дихлорметана на метанол, с одной стороны, помогает снизить количество и интенсивность пиков такого рода инструментального загрязнения, но, с другой стороны, несет в себе риск неэффективного извлечения из сорбента неполярных органических соединений средней летучести и причинение вреда капиллярной газовой колонке, которая применяется в газовой хроматографии. Использование самодельных стеклянных картриджей, оборудованных деактивированной стекловатой в качестве фритт, помогает избежать вышеперечисленных недостатков. Дихлорметан не экстрагирует из стеклянных стенок самодельных картриджей сторонние примеси и успешно извлекает неполярные и слабополярные органические соединения средней летучести из сорбента С18. Анализ природной воды из непроточного водоема г. Биробиджана с применением самодельного стеклянного картриджа показал наличие в экстракте большого количества разнообразных органических соединений (115 компонентов) бактериального и растительного генезиса при полном отсутствии посторонних примесей. К доминирующим соединениям относятся терпены, гетероароматические углеводороды, кислородсодержащие соединения и нормальные алканы, происхождение которых связано с биогенными процессами. К соединениям, указывающим на техногенное загрязнение, относятся эфиры фталевой кислоты с относительным содержанием около 9%.
Твердофазная экстракция, полипропиленовый картридж, стеклянный картридж, дихлорметан, метанол, сорбент с18
Короткий адрес: https://sciup.org/143185082
IDR: 143185082 | УДК: 543.381:550.461 | DOI: 10.31433/2618-9593-2025-28-3-19-33
The use of cartridges for solid-phase extraction in the analysis of organic compounds in natural waters
The article presents the main stages of the solid-phase extraction process as a method of sample preparation of natural thermal and mineral cold waters for subsequent instrumental analysis of medium volatility organic matter by gas chromatography, in combination with mass spectrometry. The use of standard polypropylene cartridges, equipped with frits, has a high risk of the extract contamination with adventitious impurities, which appear as separate peaks on the chromatogram. The paper examines cartridges from two major manufacturers: DSC-18 Supelco and Strata C18-E Phenomenex. Dichloromethane (methylene chloride), used as an eluting solvent, reacts with the walls of the cartridge, resulted in the extraction of n-alkanes and siloxanes from the polypropylene the cartridge is made of. Replacing dichloromethane with methanol, on the one hand, helps to reduce or completely prevent the occurrence of this type of instrumental contamination, but, on the other hand, it carries the risk of ineffective extraction of non-polar organic compounds of medium volatility from the sorbent and causing damage to the capillary gas column, which is used in gas chromatography. The use of homemade glass cartridges, equipped with deactivated glass wool as frits, helps to avoid the above-mentioned disadvantages. Dichloromethane does not extract unwanted impurities from glass walls of homemade cartridges and successfully extracts non-polar and weakly polar organic compounds of medium volatility from the C18 sorbent. The natural water analyzes from a stagnant reservoir in the town of Birobidzhan, when using a homemade glass cartridge have shown in the extract a large number of various organic compounds (115 components) of bacterial and plant origin, with a complete absence of foreign impurities. The dominant compounds include terpenes, heteroaromatic hydrocarbons, oxygen-containing compounds and normal alkanes, the origin of which is associated with biogenic processes. The man-made pollution compounds are presented there by phthalic acid esters, with a relative content of about 9%.
Текст научной статьи Использование картриджей для твердофазной экстракции при анализе органических соединений в природных водах
Институт комплексного анализа региональных проблем ДВО РАН, ул. Шолом-Алейхема 4, г. Биробиджан, 679016, e-mail: ,
как в результате инструментального загрязнения,
Исследование органических микропри- так и в ходе стандартного хроматографического месей в природных водах, проводимое на сверх- анализа. Кроме этого, угрозу контаминации несут чувствительном оборудовании, всегда сопрово- в себе все стадии пробоподготовки. В последние ждается риском появления сторонних пиков на годы изучение органических соединений в при-хроматограмме. Эти примеси могут появляться родных водах привлекает внимание множества ис
следователей [1, 2, 5, 6, 17–19, 22, 24–34, 36–39]. При этом для пробоподготовки преимущественно используют два метода: жидкостно-жидкостная экстракция и твердофазная экстракция (ТФЭ). Основные достоинства и недостатки этих методов описаны в работе [12]. Наиболее популярный и подходящий для анализа органического вещества (ОВ) в природных водах метод пробоподготовки – твердофазная экстракция [3, 20, 21, 23]. Суть этого метода заключается в разделении интересующих исследователя целевых компонентов между твердым телом (фазой) и жидкостью. Происходит это в результате загрузки образца на твердую фазу. Соединения, удерживаемые на твердой фазе, далее переводятся в органический растворитель, который уже и анализируется различными высокочувствительными методами. Картриджи являются наиболее распространенным одноразовым форматом, содержащим твердую фазу, он появился более 40 лет назад (первые картриджи датируются 1978 годом) [20]. При помощи картриджа осуществляется процесс пробоподготовки, а именно: смена исходной матрицы, концентрирование аналитов и удаление мешающих примесей. Однако, при всех своих достоинствах картриджи для ТФЭ могут нести и определенные риски привноса примесей в экстракт, поскольку изготовлены из органического материала. В настоящей работе будут рассмотрены основные типы картриджей для ТФЭ, примеси, которые могут поступать в экстракт в результате их использования, а также предложен способ устранения этого недостатка метода ТФЭ. Кроме этого, на примере реального природного объекта показан результат анализа с использованием модифицированного картриджа.
Методика анализа
Нами уже полтора десятилетия проводятся исследования ОВ в природных водах. Их объектами выступают преимущественно термоминеральные воды [7–11, 14–16]. Для процесса пробо-подготовки использовался метод ТФЭ, при этом применялись различные картриджи. В настоящей работе будут рассмотрены картриджи двух основных производителей: фирмы Supelco (Sigma Aldrich) DSC-18 и Strata C18-E Phenomenex. В обоих типах картриджей использован сорбент С18. В процессе пробоподготовки картриджи последовательно кондиционировались 2 мл гексана, метанола и хлористого метилена, а затем высушивались в токе газа аргон в течение 10 минут. Непосредственно перед ТФЭ в картридж вносились 2 мл дистиллированной воды, а затем уже 100 мл анализируемой воды. Скорость потока 1 мл/мин. После оконча- ния фильтрации в сорбент снова вносились 2 мл дистиллированной воды – для удаления примесей. Перед элюированием сорбент сушился в токе газа аргон 10–15 минут. Органические соединения снимались с сорбента 500 мкл дихлорметана.
Для регистрации органических соединений использовался метод капиллярной газовой хрома-то-масс-спектрометрии [4, 13, 35]. Анализ проводился на газовом хромато-масс-спектрометре Shimadzu GCMS-QP2010 Ultra, оборудованном автосэмплером AOC-5000. Разделение осуществлялось на кварцевой капиллярной колонке HP-5MS (неподвижная фаза – (5%-фенил)-метилполиси-локсан). Скорость потока газа-носителя (гелий марки 60) 1 мл/мин. Объем вводимого экстракта 2 мкл. Режим ввода с делением потока. Коэфициент деления – 5.0. Температура инжектора 320 ºС, температура ионного источника 250 ºС, температура интерфейса 310 ºС. Программирование термостата колонки: начальная температура 40 ºС, выдержка в течение 4 мин с последующим подъемом температуры со скоростью 7 ºС/мин до 300 ºС, выдержка при температуре 300 ºС в течение 15 мин. Сбор данных выполнялся в режиме полного сканирования в диапазоне отношения массы к заряду (m/z) от 50 до 550 дальтон, с частотой дискретизации 2с, с использованием программного обеспечения GCMS RealTime Analysis. Пики идентифицировались по масс-спектрам с помощью программного обеспечения GCMS Postrun Analysis посредством сравнения с базой данных библиотеки NIST-17 и собственной базой данных. При идентификации пиков использовались индексы удерживания – индекс Ковача, который рассчитывали на основе анализа стандарта линейных алканов С7–С40 в гексане компании Supelco.
Результаты и их обсуждение
Картриджи для ТФЭ представляют собой полипропиленовый или полиэтиленовый тубус, в котором сорбент, способный удерживать аналиты, упакован между двумя пористыми дисками (фриттами). Количество сорбента варьируется от миллиграмма до нескольких граммов в зависимости от применяемого объема образца. Жидкая фаза (вода) проходит через картридж либо за счет положительного давления (например, давление газа), либо за счет отрицательного давления (разрежение, создаваемое вакуумным насосом). ТФЭ может удерживать приблизительно 5% от массы сорбента без значительного прорыва. Мы использовали картриджи с массой сорбента 50 и 100 мг. Для определения примесей, которые поступают в ходе ТФЭ, мы использовали последнюю порцию дихлорметана, который являлся заключительным растворителем в ходе кондиционирования картриджа. Растворитель был профильтрован через чистый сорбент и содержит, соответственно, только те соединения, которые поступают из стенок картриджа.
Для выявления пиков, появившихся в ходе ТФЭ, необходимо отделить их от пиков, которые могут поступать в ходе анализа чистого растворителя и возникать в результате уноса фазы из колонки. Пики, характеризующие унос фазы, определяются по m/z 73, 207, 253, 281. Перед проведением анализов картриджей был осуществлен холостой анализ колонки (без ввода пробы) и анализ растворителя (дихлорметан), который используется при элюировании. На рис. 1 и 2 представ-
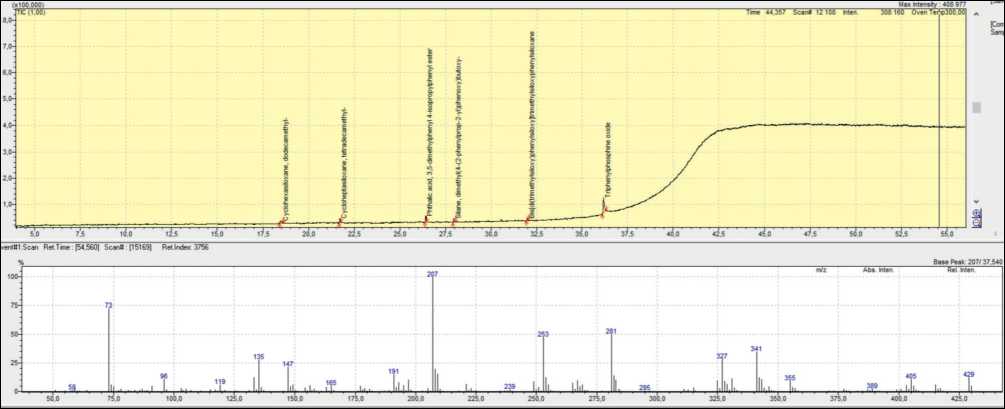
Рис. 1. Скриншот хроматограммы TIC (вверху) и масс-спектра фона (внизу) холостого анализа колонки (без ввода пробы)
Fig. 1. Blank column run (without sample injection) screenshot of the TIC chromatogram (top) and background mass spectrum (bottom)
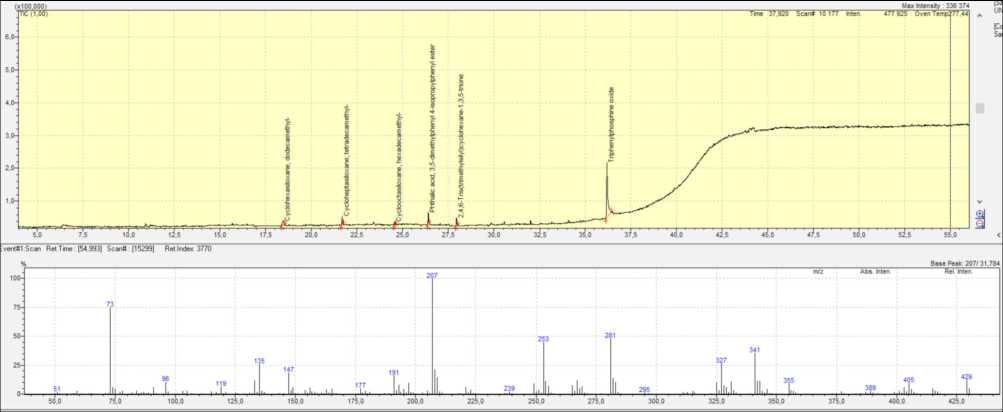
Рис. 2. Скриншот хроматограммы TIC (вверху) и масс-спектра фона колонки (внизу) анализа чистого дихлорметана (элюирующий растворитель)
Fig. 2. Screenshot of TIC chromatogram (top) and column background mass spectrum (bottom) of pure dichloromethane (eluting solvent) analysis лены скриншоты хроматограмм и масс-спектра колонки и дихлорметана. Как видно, растворитель и колонка чистые, фиксируются незначительные пики силоксанов (4 соединения) и пик фталата, а также один пик с большой интенсивностью, характерный для трифенилфосфин оксида. Внизу представлен масс-спектр фона колонки.
Стандартный картридж Supelco DSC-18
На рис. 3 представлен скриншот хроматограммы дихлорметана, который был загружен в чистый прокондиционированный полипропиленовый картридж DSC-18 (Supelco). Здесь уже фиксируется большое количество пиков веществ, которые экстрагированы из стенок картриджа. Всего идентифицировано 33 компонента. Большая часть представлена различными силоксанами и н-алка-нами, причем среди н-алканов присутствуют в основном четные углеводороды состава С12, С14, С16, С18, С20, С22 и один нечетный н-алкан С11. Внизу представлен масс-спектр н-алкана. При использовании такого картриджа при исследовании ОВ природных вод пики картриджа, с одной стороны, будут закрывать пики целевых соединений, а с другой пики четных н-алканов картриджа станут накладываться на пики н-алканов, которые растворены в воде (а н-алканы являются распространенными компонентами природных вод, которые постоянно фиксируются на хроматограммах). Это искажает реальную картину и зачастую приводит к неверным выводам, так как молекулярно-мас- совое распределение н-алканов используется для определения генезиса ОВ. Среди мешающих компонентов, поступивших из стенок картриджа, есть и ароматические углеводороды, которые также играют важную роль в геохимическом облике природных вод.
Стандартный картридж Strata C18-E Phenomenex
Другой, часто используемый картридж при анализе природных вод, – картридж Strata C18-E Phenomenex. В принципе, это абсолютно одинаковые картриджи, только изготавливаемые разными производителями, соответственно стенки картриджа также могут быть изготовлены из различных материалов. На рис. 4 представлен скриншот хроматограммы дихлорметана, профильтрованный через чистый прокондиционированный картридж Strata. Здесь также были зафиксированы различные соединения, преимущественно силоксаны. Однако интенсивность пиков гораздо выше, чем это было для картриджа Supelco. Отдельно, красной линией, выведена хроматограмма по m/z 57 (характерный ион для н-алканов). Хорошо видны большие пики н-алканов как четного, так и нечетного рядов и целый спектр более мелких пиков, соответствующие изоалканам. Реальные соединения, которые растворены в природной воде, на таком картридже гораздо труднее определить, поскольку пики картриджа будут полностью подавлять пики аналитов.
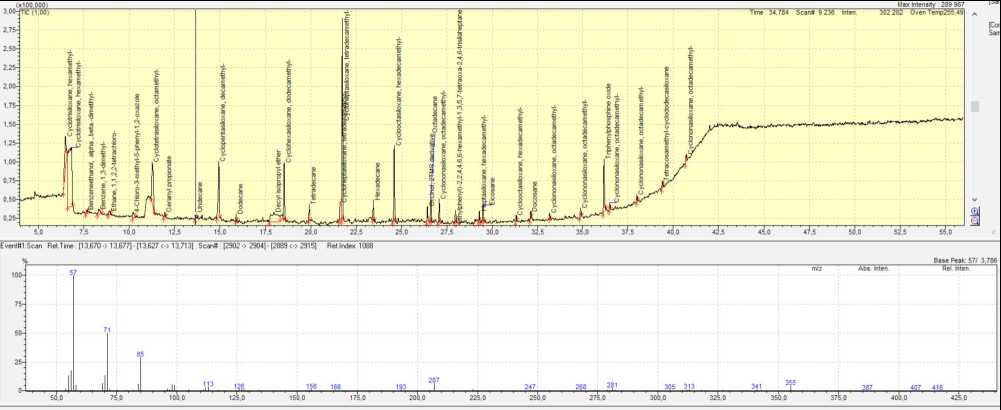
Рис. 3. Скриншот хроматограммы TIC (вверху) и масс-спектра н-алкана (внизу) анализа дихлорметана, профильтрованного через стандартный картридж DSC-18 (Supelco)
Fig. 3. Screenshot of TIC chromatogram (top) and n-alkane mass spectrum (bottom) of dichloromethane analysis filtered through a standard DSC-18 cartridge (Supelco)
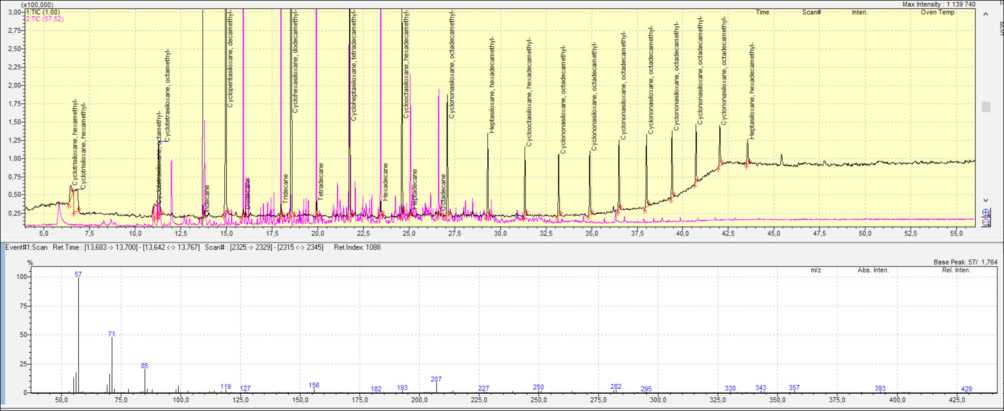
Рис. 4. Скриншот хроматограммы TIC (вверху) и масс-спектра н-алкана (внизу) анализа дихлорметана, профильтрованного через стандартный картридж Strata C18
Fig. 4. Screenshot of TIC chromatogram (top) and n-alkane mass spectrum (bottom) analysis of dichloromethane filtered through a standard Strata C18 cartridge
Выбор растворителя для элюирования органических соединений
Сорбент С18 представляет собой частицы силикагеля с привитыми октадецильными группами (C18H37), создающими гидрофобную поверхность. Он используется для удержания неполярных и слабополярных веществ (ПАУ, углеводороды, кислородсодержащие компоненты) из полярной среды (воды). Таким образом, сорбент С18 наиболее подходит для анализа органических соединений в природных водах. При элюировании неполярных и слабополярных органических соединений из сорбента С18 наиболее подходящим растворителем является дихлорметан, так как он обладает высокой элюирующей силой. Однако этот растворитель является очень агрессивным соединением и способен вступать в реакцию со многими видами пластика, в том числе и с полипропиленом, из которого изготовлены картриджи для ТФЭ, разрушая стенки картриджа и экстрагируя посторонние примеси. Результат такого взаимодействия хорошо виден на предыдущих скриншотах – появление на хроматограммах большого количества мешающих соединений, таких как силоксаны и н-алканы.
В качестве замены дихлорметана для элюирования органических компонентов природных вод из сорбента С18 можно использовать метанол или ацетонитрил, являющиеся менее агрессивными растворителями. Полипропилен, из которого изготовлены картриджи для ТФЭ, устойчив и к метанолу, и к ацетонитрилу. Это видно на скриншоте хроматограммы метанола, он был профильтрован через полипропиленовый катридж DSC-18 (рис. 5). Здесь зафиксировано гораздо меньше пиков, что говорит о сравнительной безопасности использования метанола для картриджей. Конечно, ряд соединений вымывается метанолом, в основном силоксаны и один н-алкан (ундекан), но их количество и интенсивность ниже, чем для дихлорметана.
Однако метанол и ацетонитрил – не совсем подходящие растворители для анализа органических веществ в природных водах, так как они способны элюировать только полярные соединения. Неполярные компоненты эти растворители элюируют гораздо хуже, чем дихлорметан. При использовании метанола в качестве элюирующего растворителя есть риск упустить многие вещества, которые растворены в природных водах и были удержаны сорбентом. Если цель исследования – анализ конкретных соединений в природных водах, то метанол и ацетонитрил – это хороший выбор при условии, что аналиты обладают сродством с этими растворителями. При анализе всего спектра органических компонентов, растворенных в воде, которые удерживаются сорбентом С18, лучше использовать дихлорметан. Кроме этого, метанол и ацетонитрил, являясь полярными растворителями, не подходят для использования с неполярными ка-
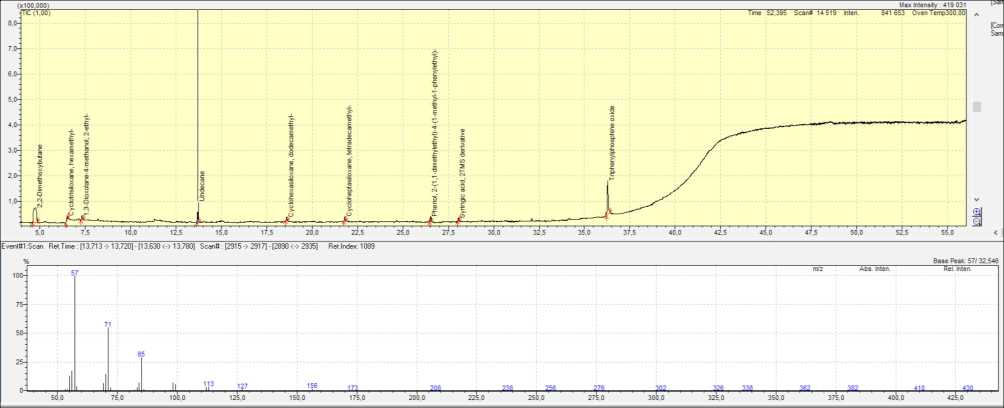
Рис. 5. Скриншот хроматограммы TIC (вверху) и масс-спектра н-алкана (внизу) анализа метанола, профильтрованного через стандартный картридж DSC-18 (Supelco)
Fig. 5. Screenshot of TIC chromatogram (top) and n-alkane mass spectrum (bottom) analysis of methanol filtered through a standard DSC-18 cartridge (Supelco)
пиллярными колонками, поскольку будут способствовать быстрому их износу и разрушению.
Самодельный стеклянный картридж для ТФЭ
Цель наших исследований органического вещества в природных водах, в частности в термоминеральных, состоит в определении всех органических соединений средней летучести, которые растворены в воде. Для этого лучше всего подходит сорбент С18 ТФЭ, который удерживает неполярные и слабополярные компоненты. Полярные вещества могут не фиксироваться этим сорбентом, но для генетических построений и характеристики ОВ природных вод наиболее интересны как раз неполярные и слабополярные соединения. Выбор между метанолом и дихлорметаном был сделан в пользу последнего, поскольку, как уже было сказано, именно этот растворитель способен элюировать все вещества из сорбента, минимизируя потери, и может продлить срок службы неполярной капиллярной колонки. Однако перед нами стояла задача найти способ, при котором дихлорметан не будет разрушать стенки картриджа, экстрагируя посторонние примеси силоксанов и н-алканов. Один из таких способов – это вычитание площадей пиков н-алканов картриджа из площади пиков н-алканов природных вод. Силоксаны в таком случае вообще не учитываются, а площадь н-алканов пересчитывается. Однако такой способ не помо- гает избежать «зашумления» колонки сторонними пиками и, как следствие, потерю пиков искомых соединений, так как они рискуют оказаться «закрытыми» пиками из картриджа.
Второй способ решения этой проблемы заключается в замене стандартного полипропиленового картриджа на другой картридж, который будет полностью инертен к дихлорметану и не станет вступать с ним в реакцию. Наиболее подходящий материал, на наш взгляд, – стекло. В качестве стеклянных тубусов были использованы градуированные пипетки на 2 мл. Они были обрезаны таким образом, чтобы их объем составил примерно 0.6–0.8 мл. В качестве фритт, то есть дисков, которые удерживают сорбент и препятствуют его загрязнению, использовалась деактивированная стекловата, которая используется для набивки лайнеров в газовой хроматографии (рис. 6). В доказательство инертности стекловаты и стеклянного тубуса был проэлюирован длихлормета-ном стеклянный картридж со стекловатой, но без сорбента (рис. 7). Как видно, никаких сторонних пиков не зафиксировано, кроме тех, что есть в самом растворителе и колонке. Причем интенсивность этих пиков такая же, как и интенсивность пиков на хроматограмме растворителя и колонки (рис. 1 и 2).
Из стандартных картриджей был извлечен

Рис. 6. Фотографии картриджей для ТФЭ.
На фото а) представлены стандартный полипропиленовый картридж DSC-18 (слева) и самодельный стеклянный картридж (справа). На фото б) представлен самодельный стеклянный картридж, где хорошо виден сорбент, зажатый между стекловатой
-
Fig. 6. Photos of SPE cartridges. The photo a) shows a standard DSC-18 polypropylene cartridge (left) and a homemade glass cartridge (right). The photo б) shows a homemade glass cartridge, where the sorbent is clearly visible, sandwiched between glass wool
стекловатой. Картридж был также стандартно прокондиционирован и последняя порция дихлор-метана при кондиционировании взята на анализ. На рис. 8 представлен скриншот хроматограммы дихлорметана после стеклянного картриджа. Как видно, хроматограмма стеклянного картриджа и ее интенсивность полностью совпадает с хроматограммами холостого анализа колонки, растворителя и стекловаты. Никаких сторонних примесей, как это было для стандартных картриджей, не зафиксировано. Применение самодельного стеклянного картриджа подходит при использовании дихлорметана в качестве элюирующего растворителя для анализа органических соединений природных вод.
Применение самодельных стеклянных картриджей для ТФЭ при анализе ОВ в непроточном водоеме г. Биробиджана Самодельные стеклянные картриджи собственного изготовления были использованы нами на многих объектах наших исследований. Это геотермальные месторождения Камчатки (Мут-новский, Паратунский и Узонский геотермальные районы) и континентальной части Дальнего Востока (Кульдурское, Анненское и Тумнинское
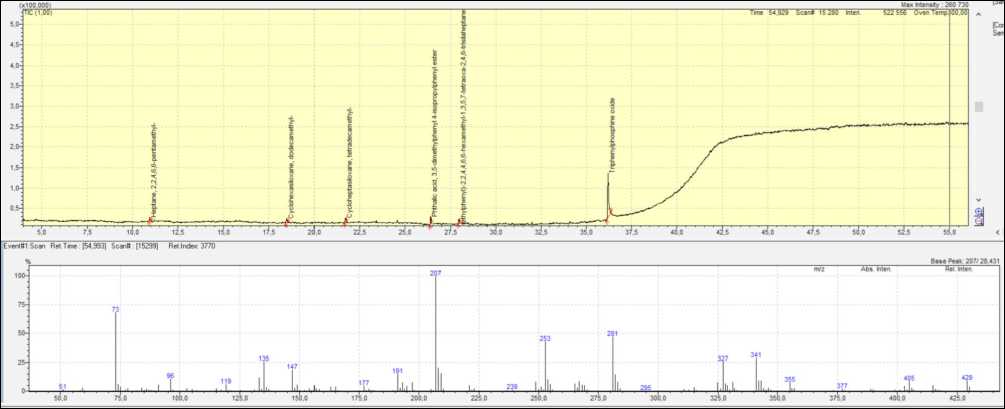
Рис. 7. Скриншот хроматограммы TIC (вверху) и масс-спектра фона колонки (внизу) анализа дихлрметана, профильтрованного через пустой стеклянный тубус с деактивированной стекловатой (без сорбента)
-
Fig. 7. Screenshot of TIC chromatogram (top) and column background mass spectrum (bottom) analysis of dichloromethane filtered through an empty glass tube with deactivated glass wool (without sorbent)
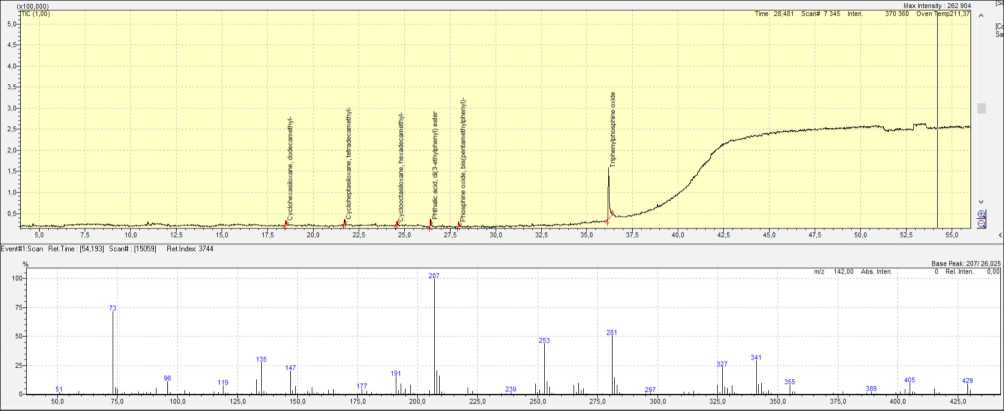
Рис. 8. Скриншот хроматограммы TIC (вверху) и масс-спектра фона колонки (внизу) анализа дихлорметана, профильтрованного через самодельный стеклянный картридж с сорбентом DSC-18
Fig. 8. Screenshot of TIC chromatogram (top) and column background mass spectrum (bottom) analysis of dichloromethane filtered through a homemade glass cartridge with DSC-18 sorbent геотермальные месторождения). Во всех случаях эти картриджи показали высокую эффективность, фиксируя аналиты и удаляя мешающие примеси. В настоящей работе в качестве примера приведен результат анализа ОВ в непроточном водоеме, который находится в пределах г. Биробиджана (карьер). Географические координаты точки отбора: 48.773173, 132.886470. Сезон (июнь) и объект (карьер в городской застройке) были выбраны таким образом, чтобы проба воды содержала большое количество взвешенных частиц. Сделано это было с целью оценить возможность полевой установки для ТФЭ [12] профильтровать пробу воды через самодельный стеклянный картридж. С помощью этой установки нам удалось создать необходимое давление (скорость потока 1 мл/мин), и 100 мл воды прошли через сорбент за 1 час 40 минут. Скриншот хроматограммы реальной пробы воды представлен на рис. 9. Гомологические ряды установленных органических соединений сведены в табл. 1.
Всего в исследуемом водоеме зафиксировано 115 органических компонентов средней летучести, которые относятся к 13 гомологическим рядам (15 рядов, если считать алкены, алкины и изомеры отдельно). Преобладают терпены (38% от состава ОВ), происхождение которых связано с биогенными процессами, так как терпены ши- роко распространены в живых организмах. Гете-роароматические УВ также имеют высокое относительное содержание, к ним преимущественно относятся бензоаты, происхождение которых, вероятно, связано с вкладом растительности. Кислородсодержащие вещества (карбоновые кислоты и их эфиры, альдегиды, кетоны и спирты) широко представлены в биосфере и также, по-видимому, имеют биогенный генезис. Наличие фталатов, возможно, связано с техногенным загрязнением, так как эти эфиры являются широко известными пластификаторами и содержатся практически во всех видах пластмасс и резины.
Молекулярно-массовое распределение н-алканов также указывает на преимущественно биогенный генезис установленного ОВ (табл. 2). Здесь преобладают низко- и среднемолекулярные н-алканы состава н-С9–С22, среди которых доминируют четные углеводороды, что указывает на их бактериальное происхождение. Доля высокомолекулярных н-алканов также значительна, при этом индексы нечетности (CPI и OEP) выше единицы, что говорит о вкладе наземной растительности в происхождении ОВ в исследуемом водном объекте.
Заключение
В результате проведенного исследования установлено, что стандартные полипропиленовые
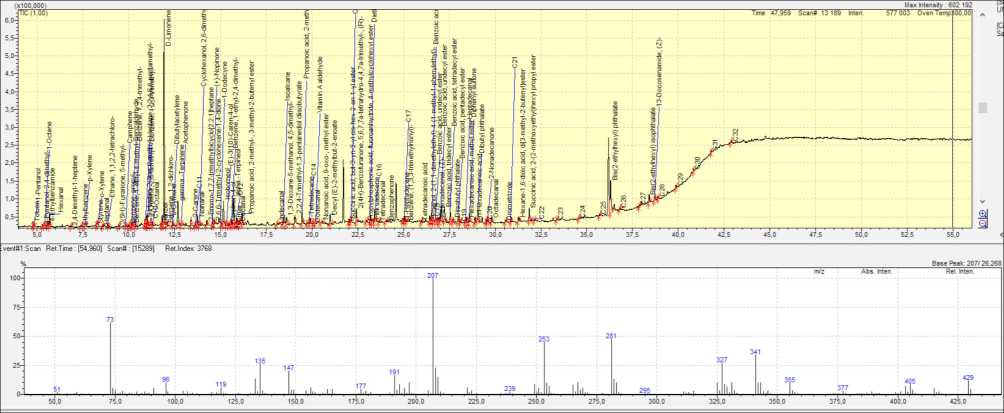
Рис. 9. Скриншот хроматограммы TIC (вверху) и масс-спектра фона колонки (внизу) анализа экстракта природной воды из водоема г. Биробиджан в дихлорметане, с использованием самодельного стеклянного картриджа с сорбентом DSC-18
Fig. 9. Screenshot of the TIC chromatogram (top) and the mass spectrum of the column background (bottom) analysis of natural water extract from the Birobidzhan reservoir, made in dichloromethane, using a homemade glass cartridge with DSC-18 sorbent
Таблица 1
Гомологические ряды органических соединений, идентифицированных в экстракте природной воды из водоема г. Биробиджана
Homologous series of organic compounds, found in the extract from a stagnant reservoir natural water in Birobidzhan
Table 1
|
№ п/п |
Наименование ряда |
Площадь пика в ед. прибора, у.е. |
Доля, % |
Количество соединений |
|
1 |
н-Алканы |
567386 |
9.2 |
26 |
|
2 |
Изоалканы |
124286 |
2.0 |
3 |
|
3 |
Алкены, алкины и их изомеры |
212522 |
3.5 |
8 |
|
4 |
Арены |
340657 |
5.5 |
13 |
|
5 |
Гетероароматические УВ |
806791 |
13.1 |
15 |
|
6 |
Карбоновые кислоты |
60069 |
0.9 |
2 |
|
7 |
Эфиры |
599287 |
9.7 |
12 |
|
8 |
Альдегиды |
370271 |
6.0 |
12 |
|
9 |
Кетоны |
61367 |
1.0 |
2 |
|
10 |
Спирты |
124721 |
2.0 |
4 |
|
11 |
Азотсодержащие соединения |
31234 |
0.5 |
1 |
|
12 |
Терпены |
2343640 |
37.9 |
13 |
|
13 |
Фталаты |
539680 |
8.7 |
4 |
|
Итого |
6181911 |
100.0 |
115 |
Таблица 2
Молекулярно-массовое распределение н-алканов в природной воде из водоема г. Биробиджана
Table 2
Molecular mass distribution of n-alkanes in natural water from the reservoir in Birobidzhan
Использование самодельных стеклянных картриджей, изготовленных из градуированных пипеток и деактивированной стекловаты в качестве фритт, доказало свою эффективность. При элюировании дихлорметаном на хроматограмме не фиксируются пики посторонних примесей, а сорбент в этом картридже не теряет своих свойств и способен удерживать широкий спектр неполярных и слабополярных органических соединений.
Результат анализа органического вещества природной воды из непроточного водоема г. Биробиджана с использованием самодельного стеклян- ного картриджа показал наличие в экстракте большого количества разнообразных органических соединений (115 компонентов) бактериального и растительного происхождения.
Исследование выполнено в рамках государственного задания Института комплексного анализа региональных проблем ДВО РАН.


