Использование метода масс-спектрометрии микробных маркеров в этиологической диагностике гнойно-воспалительных заболеваний кисти
Автор: Крайнюков П.Е., Моисеев Д.Н., Жиленкова О.Г., Кокорин В.В., Попов П.А., Колодкин Б.Б., Ким Д.Ю., Кондаков Е.В.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4 т.15, 2020 года.
Бесплатный доступ
Представлен опыт применения метода газовой хроматографии с масс-селективной детекцией ионов (ГХ-МС) для определения маркеров потенциальных возбудителей в качестве метода этиологической диагностики при гнойно-воспалительных заболеваниях кисти. В группу исследования были включены 63 пациента с указанной патологией кисти. Метод ГХ-МС позволил выявить присутствие в исследуемом биологическом материале (раневое отделяемое, капиллярная кровь) бактериальные маркеры представителей кишечной микрофлоры, что подтверждает представление о транслокации бактериальных токсинов и микроорганизмов в очаг воспаления. Определены маркеры трудно культивируемых, посредством классических культуральных бактериологических методов исследований, облигатных анаэробов представителей эндогенной микробиоты.
Гнойно-воспалительные заболевания кисти, газовая хроматография масс-спектрометрия, микробиом, бактериальная транслокация, микробные маркеры
Короткий адрес: https://sciup.org/140260060
IDR: 140260060 | DOI: 10.25881/BPNMSC.2020.25.88.010
Use of microbial marker mass spectrometry method in etiological diagnostics of purulent-inflammatory hand diseases
The article presents the experience of using the method of gas chromatography with mass-selective detection of ions (GC-MS) to determine markers of potential pathogens as a method of etiological diagnosis in purulent-inflammatory diseases of the hand. The study group included 63 patients with the indicated hand pathology. The GC-MS method revealed the presence of bacterial markers of representatives of the intestinal microflora in the biological material under study (wound separable, capillary blood), which confirms the idea of translocation of bacterial toxins and microorganisms into the focus of inflammation. Markers of difficult-to-cultivate, through classical culture bacteriological research methods, obligate anaerobes of endogenous microbiota representatives have been identified.
Текст научной статьи Использование метода масс-спектрометрии микробных маркеров в этиологической диагностике гнойно-воспалительных заболеваний кисти
Вопросы этиологической диагностики и лечения гнойно-воспалительных заболеваний кисти продолжают волновать практикующих хирургов, несмотря на многолетнюю историю изучения этой медикосоциальной проблемы. За последнее десятилетие частота встречаемости среди пациентов не имеет тенденции к снижению, а тяжесть течения самого гнойновоспалительного процесса нередко возрастает [1; 2]. Среди всех нагноительных процессов мягких тканей и костей гнойные заболевания кисти по-прежнему занимают первое место, составляя 15% случаев у пациентов впервые обратившихся за медицинской помощью [3; 4].
Одними из факторов определяющими эффективность лечебных мероприятий при гнойновоспалительных заболеваниях являются время и качество определения этиологического фактора. Существующие фенотипические методы идентификации, основанные на культивировании микроорганизмов на питательных средах, обладают недостатками (низкая скорость и относительно низкая информативность), не позволяющими вовремя сформировать мнение о видовом составе микрофлоры патологического очага, что в свою очередь затрудняет своевременную постановку клинического диагноза и назначение адекватной антибактериальной терапии.
Возникает необходимость поиска и внедрения новых диагностических технологий, которые могли бы

Крайнюков П.Е., Моисеев Д.Н., Жиленкова О.Г. и др.
ИСПОЛЬЗОВАНИЕ МЕТОДА МАСС-СПЕКТРОМЕТРИИ МИКРОБНЫХ МАРКЕРОВ В ЭТИОЛОГИЧЕСКОЙ ДИАГНОСТИКЕ ГНОЙНО-ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ КИСТИ обеспечить высокую скорость (не более нескольких часов), большую производительность, достаточную чувствительность и экономическую доступность клиникомикробиологического анализа. Важным требованием к методам диагностики является возможность получения достоверных результатов при работе с полимикробными биологическими образцами, содержащими смесь различных микроорганизмов [5].
В настоящее время тенденция персонифицированной медицины предполагает большее использование в рутинной практике лабораторной диагностики Омикс-технологий (геномика, транскриптомика, протеомика, метаболомика) наиболее перспективными из которых, в свете вышеизложенных задач, являются метаболомные методы исследования с использованием хромато-масс-спектрометрии.
ГХ-МС позволяет детектировать в исследуемых образцах биологического материала маркеры — компоненты микробной клетки и её метаболитов (жирные кислоты, альдегиды, спирты и стерины) — как эндогенной так и экзогенной микрофлоры, без предварительного выделения чистой культуры микроорганизмов, что особенно актуально принимая во внимание факт трудности культивирования анаэробов. Отличительные преимущества метода являются скорость анализа и возможность количественной оценки содержания маркера [6].
Цель работы выявить маркеры микроорганизмов методом ГХ-МС у пациентов с гнойно-воспалительными заболеваниями кисти посредством параллельного измерения концентраций микробных маркеров в крови и содержимым гнойного очага (раневом отделяемом).
Материалы и методы
Произведено оперативное лечение 63 пациентов с гнойно-воспалительными заболеваниями кисти. Средний возраст пациентов — 40,2 года. Преимущественно отмечалось поражение правой кисти у лиц мужского пола, трудоспособного возраста. Среднее количество суток до обращения за медицинской помощью составило — 3,2. Антибактериальная терапия, до готовности результатов ан-тибиотикограммы, проводилась, исходя из эмпирического принципа ее назначения. Группой выбора препаратов для антибактериальной терапии была цефалоспорины III поколения, первый прием назначали в день госпитализации, после изъятия биологического материала для микробиологического исследования классическими культуральными методами и химического анализа методом ГХ-МС.
Перед операцией все пациенты комплексно обследованы клинически, инструментально и с использованием лабораторных методов диагностики. Хирургическое лечение выполняли под проводниковой анестезией, на уровне локтевого сустава. Объем оперативного лечения включал: вскрытие, санацию и дренирование гнойного очага, с использованием отжимного жгута на уровне предплечья. Во время операции производился забор содержимого гнойного очага стерильным хлопчатобумажным тампоном на пластиковой палочке от пробир-
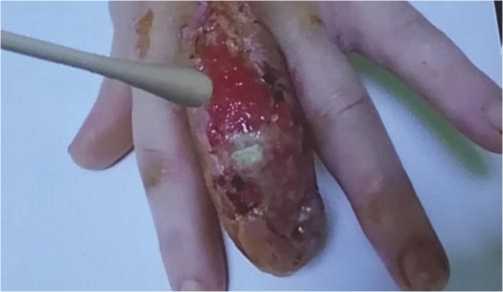
Рис. 1. Забор содержимого гнойного очага стерильным хлопчатобумажным тампоном.

Рис. 2. Газовый хроматограф с масс-спектометром.
ки для микробиологических исследований без наполнителя (Рис. 1). Изымалась капиллярная кровь в пробирки с ЭТДА объемом 2 мл. Повторный забор биологического материала проводили на 3 сутки после операции.
Так же проводилось классическое микробиологическое исследование, путем посевов на твердые питательные среды (желточно-солевой агар, кровяной агар, среда Эндо, среда Сабуро). Определение антибиотико-чувствитель-ности проводили по стандартной методике [7].
С целью обнаружения маркеров потенциальных возбудителей, в данных биологических образцах, было проведено исследование вышеуказанного материала посредством физико-химического анализа методом ГХ-МС с последующим алгоритмом автоматическим расчета, предложенным Г.А. Осиповым [8] (Рис. 2).
Принадлежность маркеров к конкретным микроорганизмам определялась посредством базы данных Национального института стандартов и технологий (NIST, USA), и входящим в алгоритм программ прибора Шерлок (MINI Inc, Delaware, USA) для хроматографической идентификации микроорганизмов по жирно-кислотным компонентам.
Результаты исследования
В раневом отделяемом и крови пациентов при анализе методом ГХ-МС обнаружены жирные кислоты, гидроксикислоты, циклопропановые кислоты, стерины являющиеся компонентами фосфолипидного бислоя бактериальной клеточной стенки и мембран, а также результатом метаболизма микрофлоры и макроорганизма.
В исследуемых образцах биологического материала, выявили более чем двукратное превышение концентраций следующих веществ: 7 гексадеценовая кислота (компонент клеточной стенки), 10-оксисте-ариновая и 10-оксидеценавая кислоты (продукты ферментативного гидролиза тканей макроорганизма ферментами микробов), изодеканавая и изодеценовые кислоты. По этим кислотам детектируют представителей клостридий ( Clostridium propionicom, Сl.ramosum, Cl.difficile, Cl.Hystolyticum, Cl.perfringens ). Цис-вактеновая кислота ( Lactobacillus spp. ), Октадеценовый альдегид ( Bifidobacterium spp. ), транс-9, 10-гексдеценовая кислота ( Nocardia asteroides ), 3-гидрокси-изопентадекановая кислота ( Prevotella spp. ), антеизо-нонадекановая кислота ( Staphylococcus spp. ), изогептадеценовая кислота ( Campylobacter mucosalis ), изо-пентадекановый альдегид ( Propionibacterium freudenreichii ), циклогептадекановая кислота (семейство Enterobacteriaceae , при отсутствии псевдоманад), дегидрохолестерол ( Eubacterium ), изо-гексадекановый альдегид ( Eggerthella lenta ), антеизотри-декановая кислота ( Bacillus cereus ) (Рис. 3).
В крови определялись эти же соединения, но в значительно меньшей концентрации (выше пределов детекции).
При классическом бактериологическом исследовании, содержимого гнойного очага, полученного при первичной операции из 63 (100%) посевов, в 4 (6,35%) рост микробной флоры не был обнаружен, в 40 (63,5%) определился Staphylococcus aureus , в 9 (14,3%) — Streptococcus pyogenus , в 5 (7,8%) — Staphylococcus еpidermidis , в 2 (3,17%) — Escherichia coli , в 2 (3,17%) — Staphylococcus «Koa-» , 1 (1,58%) — Enterococcus faecalis (Рис. 4, 5). При анализе результатов классического бактериологического исследования отмечено, что микроорганизмы преимущественно определяются в виде монокультуры. В нашем исследовании было зафиксировано 38 (66,6%) случая микст инфекции который состоит из следующих микроорганизмов: 1) St.aureus +Srt. Pyogenes ; 2) St.aureus
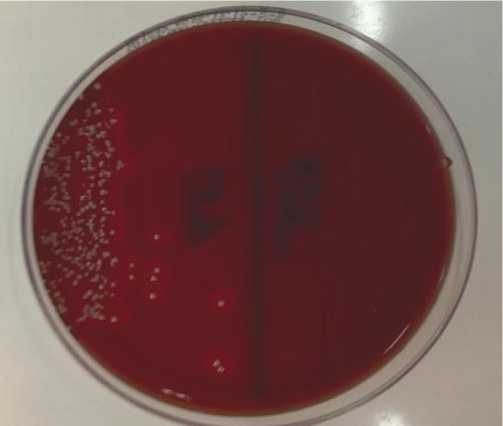
Рис. 4. Колонии St. aureus.
кл/гх 10*5
|
Ns Микроорганизм |
Проба |
Норма |
|
|
1 |
Staphylococcus spp. |
710 |
45 |
|
2 |
Eggerthella lenta |
285 |
40 |
|
3 |
bacillus cereus |
348 |
41 |
|
4 |
Nocardia spp. |
1125 |
94 |
|
5 |
Clostridium propionicom |
217 |
94 |
|
6 |
Clostridium ramosum |
2925 |
992 |
|
7 |
Staphylococcus epidermidis |
78 |
0 |
|
8 |
Lactobacillus spp. |
3455 |
659 |
|
9 |
Campylobacter mucosalis |
38 |
0 |
|
10 |
Clostridium spp. (группа C. tetani) 597 |
245 |
|
|
11 |
Clostridium difficile |
151 |
0 |
|
12 |
Prevotella spp. |
35 |
10 |
|
13 |
Eubacterium spp. |
4497 |
565 |
|
14 Staphylococcus aureus |
720 |
30 |
|
|
15 |
Bifidobacterium spp. |
1422 |
225 |
|
16 Clostridium perfringens |
950 |
84 |
|
|
17 |
Enterococcus spp. |
105 |
0 |
|
18 Propionibacterium freudenreichii |
2088 |
243 |
|
|
19 |
Nocardia asteroides |
267 |
40 |
|
20 |
Blautia coccoides |
192 |
0 |
|
Сумма |
20206 |
3406 |
|
0 500 1500 2500 3500 4500
-
1 —
-
2 -
-
3 ~
-
4 —
-
5 ‘
-
6 ЕЕ
-
8 =
ю Е-
11 :
13=7~
15 ~
16 :—
18 Е
20 ~
Проба
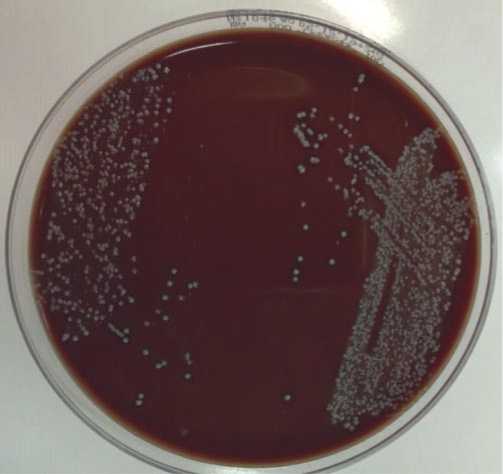
Рис. 5. Колонии St. еpidermidis.
Рис. 3. Графический пример результата исследования раневого отделяемого физико-химического анализа методом ГХ-МС.

Крайнюков П.Е., Моисеев Д.Н., Жиленкова О.Г. и др.
ИСПОЛЬЗОВАНИЕ МЕТОДА МАСС-СПЕКТРОМЕТРИИ МИКРОБНЫХ МАРКЕРОВ В ЭТИОЛОГИЧЕСКОЙ ДИАГНОСТИКЕ ГНОЙНО-ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ КИСТИ
В полученных результатах методом ГХ-МС также выявлено присутствие четырех предполагаемых возбудителей ( St.aureus, St. еpidermidis, Escherichia coli, Str. spp. ) в очаге воспаления, которых нам удалось получить культуральными методами, что подтверждает его состоятельность как экспресс метода диагностики. Данные о составе микробиоты позволяют утверждать о лидирующей роли аутофлоры, преимущественно анаэробной природы, в поддержании очага гнойного воспаления, появившейся в нем посредством транслокации кишечной микрофлоры. Анаэробные бактерии являются значимыми составляющими нормального микробиома человека, большая часть заселяет биотоп толстой кишки 10 10 -10 12 КОЕ/гр.
Большинство определяемых видов микроорганизмов либо трудно культивируемые, либо некультивируе-мые. R.Berg определил бактериальную транслокацию как прохождение жизнеспособных бактерий и их токсинов из желудочно-кишечного тракта через слизистую оболочку в экстраинтестинальные участки макроорганизма (мезентериальные лимфоузлы, печень, селезенку, кровоток) [9].
Роль этого феномена в патогенезе хирургической инфекции подробно описана в трудах Н.И. Никитенко [10]. Компоненты клеточных мембран микроорганизмов в крови появляются в результате фагоцитоза, ферментативного лизиса белковым комплементом крови или автолиза. Наличие микробных маркеров в крови отражает состав микробных консорциумов тела человека, независимо от места обитания микроорганизмов или очага воспаления [11]. Определение в крови маркеров микроорганизмов не дает оснований для предположений о наличии генерализованного септического процесса, хотя и детектируются в соизмеримых концентрациях с ведущим этиологическим объектом.
Выводы
-
1. Таким образом метод ГЗ-МС позволяет определить наличие бактериальной транслокации кишечных микроорганизмов в очаг гнойного воспаления.
-
2. Выявление маркеров микроорганизмов одновременно в крови и очаге гнойного воспаления позволяет определить их как потенциально этиологические агенты.
-
3. Преобладание анаэробной микрофлоры в очаге воспаления подчеркивает необходимость применения антибактериальных препаратов, активных в отношении анаэробной флоры.
-
4. Скорость проведения исследования материала методом ГХ-МС является неоспоримым преимуществом (не более 4 часов) этого метода, позволяющего использовать его в качестве экспресс метода изучения состава микробиоты биотопов.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Использование метода масс-спектрометрии микробных маркеров в этиологической диагностике гнойно-воспалительных заболеваний кисти
- Ерюхин И.А., Гельфанд Б.Р., Шляпников С.А. Хирургические инфекции. — СПб. — 2003. — 853 с. [Eryuhin IA, Gel'fand BR, SHIyapnikov SA. Hirurgicheskie infekcii. SPb; 2003. 853 p. (In Russ).]
- Гринев М.В., Гринев К.М. Некротизирующий фасциит в структуре хирургических инфекций мягких тканей. Стационарозамещающие технологии // Амбулаторная хирургия. — 2005. — №3 (19). — С. 6-8. [Grinev MV., Grinev KM. Nekrotiziruyushchij fasciit v strukture hirurgich-eskih infekcij myagkih tkanej. Stacionarozameshchayushchie tekhnologii. Ambulatornaya hirurgiya. 2005; 3(19): 6-8. (In Russ).]
- Крайнюков П.Е, Матвеев С.А Этиопатогенетические аспекты формирования гнойных заболеваний кисти // Вестник Национального медико-хирургического Центра им. Н.И. Пирогова — 2012. — Т.7, №2. — С. 46-49. [Krajnyukov PE, Matveev SA. Etiopatogeneticheskie aspekty formirovaniya gnojnyh zabolevanij kisti. Vestnik Nacional'nogo mediko-hir-urgicheskogo Centra im. N.I. Pirogova. 2012; 7(2): 46-49. (In Russ).]
- Рутенберг Д.Г., Конычев А.В., Кокорев О.В. Этиологические аспекты гнойно-воспалительных заболеваний верхней конечности // Актуальные вопросы гнойно-септических заболеваний и осложнений в хирургии, травматологии и интенсивной терапии»: материалы VII научно-практической конференции РАСХИ; Москва, 27-28 ноября 2008. Инфекция в хирургии. — Т.6. С. 59. [Rutenburg DG, Konychev AV, Kokorev OV. Etiologicheskie aspekty gnojno-vospalitel'nyh zabolevanij verhnej konechnosti. Aktual'nye voprosy gnojno-septicheskih zabolevanij i oslozhnenij v hirurgii, travmatologii i intensivnoj terapii»: materialy VII na-uchno-prakticheskoj konferencii RASSI; Moscow, 27-28 November 2008. Infekciya v hirurgii. (6): 59 p. (In Russ).]
- Бочарова Ю.А., Чеботарь И.В., Маянский Н.А. Возможности, проблемы и перспективы масс-спектрометрических технологий в медицинской микробиологии (обзор литературы) // Клиническая лабораторная диагностика. — 2016. — 61(4). — С. 249-256. [Bocharova YUA, CHebotar' IV, Mayanskij NA. Vozmozhnosti, problemy i perspektivy mass-spektro-metricheskih tekhnologij v medicinskoj mikrobiologii (obzor literatury). Klinicheskaya laboratornaya diagnostika. 2016; 61(4): 249-256. (In Russ).]
- Осипов Г.А. Хромато-масс-спектрометрический анализ микроорганизмов и сообществ в клинических пробах при инфекциях и дисбиозах. Химический анализ в медицинской диагностике. — М.: Наука, 2010. — С. 293-368. [Osipov GA. Hromato-mass-spektrometricheskij analiz mikroorganizmov i soobshchestv v klinicheskih probah pri infekciyah i disbiozah. Himicheskij analiz v medicinskoj diagnostike. Moscow: Nauka; 2010: 293-368. (In Russ).]
- Семенова А.Н., Резван С.П., Видьмина Е.А. МУК 4.2.1890-04 Определение чувствительности микроорганизмов к антибактериальным препаратам. Методические указания. [Semenova A.N., Rezvan S.P., Vid'mina E.A. MUK 4.2.1890-04 Opredelenie chuvstvitel'nosti mikroorganizmov k antibakterial'nym preparatam. Methodological guidelines. (In Russ).]
- Осипов Г.А., Новикова В.П., Методика масс-спектрометрии микробных маркеров как способ оценки пристеночной кишечной микробиоты при заболеваниях органов пищеварения. Учебно-методическое пособие. — СпБ, 2013. — 83 с. [Osipov GA, Novikova VP, Metodika mass-spektr-ometrii mikrobnyh markerov kak sposob ocenki pristenochnoj kishechnoj mikrobioty pri zabolevaniyah organov pishchevareniya. Teaching Manual. SPb; 2013: 83 p. (In Russ).]
- Berg. RD. Bacterial translocation from the intestine. Jikken Dobutsu. 1985; 34(1): 1-16.
- Никитенко Н.И., Захаров В.В., Бородин А.В. Роль транслокации бактерий в патогенезе хирургической инфекции // Хирургия. — 2001. — Т.2. — С. 63-66. [Nikitenko NI, Zaharov VV, Borodin AV. Rol' transl-okacii bakterij v patogeneze hirurgicheskoj infekcii. Hirurgiya. 2001; (2): 63-66. (In Russ).]
- Beloborodova NV., Osipov GA. Small molecules originating from microbes (SMOM) and their role in microbes-host relationship. Microbial Ecologyin Healthand Disease. 2000; (12): 12-21.


