Использование метода самовозгорания для получения замещенного алюминием гексаферрита бария
Автор: Чернуха Александр Сергеевич, Зверева Анастасия Александровна, Зирник Глеб Михайлович, Мустафина Карина Эльвировна, Пашнин Денис Рафаэлевич, Дюкова Ольга Вадимовна, Малв Егор Викторович, Вепрева Анастасия Владимировна, Крошнина Валерия Вячеславовна, Некорыснова Надежда Сергеевна, Живулин Владимир Евгеньевич, Мосунова Татьяна Владимировна, Винник Денис Александрович
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Физическая химия
Статья в выпуске: 3 т.13, 2021 года.
Бесплатный доступ
Оксидные материалы традиционно привлекают внимание исследователей по всему миру. Это обусловлено широкой областью их применения: электротехника, электроника, специальные покрытия, химические технлогии и т. д. Широко распространено легирование оксидных материалов различными элементами, такими как Al, Bi, Zn, Co, Sn, Ti, B, Sb и другими с целью тонкой настройки их физико-химических свойств. В частности, отдельный интерес представляет легирование гексаферрита бария алюминием, так как это позволяет изменять такие важнейшие параметры, как намагниченность насыщения (σ S ), коэрцитивную силу ( HC ), коэффициент прямоугольности петли гистерезиса ( K ), а также влиять на поле анизотропии и микроволновые свойства материала. Так как в случае получения BaAl x Fe12-x O19 классическим керамическим методом требуется тщательное перетирание исходных материалов, проведение предварительного спекания, высокая температура (выше 1300 °C) и длительность синтеза, было решено опробовать альтернативный метод получения замещенного алюминием гексаферрита бария. В качестве такового нами был выбран метод самовозгорания (self-combustion method). В ходе синтеза готовился раствор нитратов соответствующих металлов с лимонной кислотой. После нейтрализации и упаривания раствора, полученная масса нагревалась в муфельной печи для проведения процесса самовозгорания и удаления остаточного углерода. Финальное спекание образцов состава BaAl x Fe12-x O19 (при х = 0, 1, 2 и 3) проводилось в муфельной печи с презиционным регулятором температуры при 1100 °С в течение 4 часов. Полученные образцы исследовались методами порошковой дифрактометрии, сканирующей электронной микроскопии и рентгеноспектрального микроанализа. Установлено, что метод самовозгорания позволяет получить гомогенные образцы замещенного алюминием гексаферрита бария при более низкой температуре по сравнению с классическим керамическим методом. Также были установлены параметры структуры полученных образцов. Опробованный метод не только позволяет получать замещенный алюминием гексаферрит бария при меньших температурах, но и дает возможность легирования ферритов высоколетучими элементами.
Гексаферрит бария, замещение алюминием, baalxfe12-xo19, метод самовозгорания
Короткий адрес: https://sciup.org/147235330
IDR: 147235330 | УДК: 544.228 | DOI: 10.14529/chem210312
Application of self-combustion method for synthesis of aluminum-substituted barium hexaferrite
Oxide materials have traditionally attracted the attention of researchers around the world. This is due to their wide range of applications: electrical engineering, electronics, special coatings, chemical technologies, etc. Doping of oxide materials with various elements such as Al, Bi, Zn, Co, Sn, Ti, B, Sb and others is widespread in order to fine-tune their physicochemical properties. In particular, doping of barium hexaferrite with aluminum is of particular interest, since this allows one to change such important parameters as saturation magnetization (σS), coercive force (HC), squareness coefficient of the hysteresis loop (K), as well as to influence the anisotropy field and microwave properties of the material. Since the preparation of BaAlxFe12-xO19 by the classical ceramic method requires thorough grinding of the starting materials, preliminary sintering, high temperature (above 1300 °C) and duration of the synthesis, it was decided to test an alternative method for obtaining aluminum-substituted barium hexaferrite. As such, we have chosen the self-combustion method. During the synthesis a solution of nitrates of the corresponding metals with citric acid was prepared. After neutralization and evaporation of the solution, the resulting mass was heated in a muffle furnace to carry out the spontaneous combustion process and remove residual carbon. The final sintering of samples with the composition BaAlxFe12-xO19 (for x = 0, 1, 2, and 3) was carried out in a muffle furnace with a precision temperature controller at 1100 °C for 4 hours. The obtained samples were studied by the powder diffractometry method, scanning electron microscopy, and X-ray spectral microanalysis. It has been established that the self-ignition method makes it possible to obtain homogeneous samples of barium hexaferrite substituted with aluminum at a lower temperature compared to the classical ceramic method. The parameters of the structure of the obtained samples were also determined. The tested method not only makes it possible to obtain aluminum-substituted barium hexaferrite at lower temperatures, but also makes it possible to dope ferrites with highly volatile elements.
Текст научной статьи Использование метода самовозгорания для получения замещенного алюминием гексаферрита бария
Оксидные материалы привлекают внимание ученых по всему миру, несмотря на свою давнюю историю и обилие исследовательских работ на данную тему. Простые и сложные оксиды интересны в сфере очистки воды и поверхностей как перспективные материалы для сенсоров и фотовольтаических устройств, а также в области водородной энергетики [1–8]. Оксиды, в особенности сложного состава, занимают важнейшее место в электротехнике – при производстве постоянных магнитов, интерференционных фильтров, радиопоглощающих покрытий, устройств крайне высоких и сверхвысоких частот [9–16].
Гексаферриты со структурой магнетоплюмбита не исключение [10, 14]. Важнейшим представителем этого семейства является гексаферрит бария (BaFe12O19), что обусловлено уникальным сочетанием его свойств. Он и ряд ферритов на его основе относятся к числу магнитотвердых материалов, имеют высокую намагниченность насыщения (σ S ), большую коэрцитивную силу ( H C ), превосходную химическую стабильность и механическую прочность [17–20]. В частности, высокое значение HC позволяет использовать BaFe12O19 в качестве постоянных магнитов [19].
Вместе с тем, данное соединение характеризуется высокой одноосной анизотропией и способно поглощать микроволновое излучение в ходе возникновения ферромагнитного резонанса [17–22]. Последнее обстоятельство обуславливает использование гексаферрита бария в качестве компонента СВЧ-устройств [19, 20, 22]. Гексаферриты M-типа, в частности BaFe 12 O 19 , легируют различными элементами с целью тонкой настройки магнитных свойств. Так влиять на намагниченность насыщения позволяет легирование такими металлами, как висмут, галлий и цинк, а также такими неметаллами, как бор, сурьма и мышьяк [23–25]. Легирование также позволяет эффективно воздействовать на значение коэрцитивной силы и температуры Кюри [19, 23, 26, 27]. Кроме того, широкое распространение получило совместное легирование двумя металлами: Co-Ti, Zn-Ti, Co-Sn, Zn-Nb и пр. [19, 23, 25, 28]. Перспективным видится легирование литием и ниобием, так как позволяет влиять на частоту ферромагнитного резонанса, что имеет большое значение для СВЧ-техники [23].
Особое место среди семейства замещенных гексаферритов занимают твердые растворы системы BaFe 12 O 19 ‒BaAl 12 O 19 . Дело в том, что для увеличения рабочих частот устройств миллиметрового диапазона (при сохранении адекватных значений внешнего магнитного поля) необходимо использование материалов с высоким полем анизотропии [22]. Благодаря этому возникает возможность уменьшения веса и размера СВЧ-устройств [22]. Увеличение поля анизотропии может быть достигнуто путем замещения магнитных ионов Fe3+ на немагнитные ионы Al3+ [29]. Кроме того, замещение ионов железа немагнитными ионами позволяет влиять на намагниченность насыщения в сторону заметного снижения [24]. Легирование алюминием также находит применение при улучшении свойств тонких пленок ферритов [17, 22, 29]. Последние являются привлекательным кандидатом для перпендикулярной магнитной записи сверхвысокой плотности [17, 18]. К сожалению, BaFe 12 O 19 демонстрирует низкий коэффициент прямоугольности петли гистерезиса и не очень высокую коэрцитивную силу, что не позволяет достигнуть приемлемого соотношения сигнал-шум [17]. Получение тонких пленок замещенного алюминием гексаферрита бария позволяет решить эту проблему и получать перспективные материалы для устройств миллиметрового диапазона нового поколения [22].
Исследования в области получения BaAl x Fe 12‒ x O 19 показали, что в данной системе нет непрерывного ряда твердых растворов. Область несмешиваемости лежит в интревале значений x от 6 до 7,2 [30]. Значительное количество работ посвящено получению и изучению свойств BaAl x Fe 12‒ x O 19 при небольших степенях замещения (до x = 2) [17, 18, 20, 22, 23, 29].
При получении чистого и замещенного алюминием гексаферрита бария, как правило, используется керамический метод [23, 29–31]. Данный подход предполагает тщательное перемешивание карбоната бария, оксида железа (III) и оксида алюминия. Это приводит к невысокой степени гомогенности получаемых образцов, а также вызывает необходимость неоднократного спекания и перетирания [23]. Также недостатком данного метода является необходимость достижения высоких температуры и продолжительности синтеза [23, 29]. Так авторы [29] проводили получение BaAl x Fe12‒ x O19 при температурах до 1300 °C и рентгеновский фазовый анализ показывал загрязненность данных образцов, в том числе, исходными компонентами. Дальнейшее увеличение температуры синтеза, помимо роста энергозатрат, приводит к другим нежелательным последствиям. Во-первых, при спекании выше 1300 °C возможно частичное восстановление трехвалентного железа до двухвалентного, что ухудшает магнитные свойства получаемого материала. Это вынуждает проводить спекание в атмосфере кислорода. Во-вторых, высокие температуры синтеза исключают получение гексаферритов, легированными также легколетучими элементами. В качестве альтернатив твердофазному синтезу оксидных материалов предложены методы: гидротермальный, микроволновый, соосаждения и контролируемого горения [32–41]. Преимущества последнего перед керамическим: более высокая степень однородности образцов в силу распределения компонентов на ионном уровне, большая удельная поверхность, а также значительное снижение температуры синтеза [39–40, 42]. Это дает принципиальную возможность получать ряд твердых растворов при более низких температурах с большим содержанием легирующего элемента, синтезировать оксидные материалы с развитой поверхностью и легировать их легколетучими элементами. Данный метод также имеет преимущества перед другими альтернативами: нет
Чернуха А.С., Зверева А.А., Использование метода самовозгорания
Зирник Г.М. и др. для получения замещенного алюминием гексаферрита бария нужды в сложном оборудовании (автоклавах, микроволновых печах и т. д.) и позволяет избежать потери части ионов с раствором (при соосаждении).
В рамках данного исследования проводилось получение и характеризация гексаферрита бария, замещенного алюминием при степенях замещения x от 0 до 3.
Экспериментальная часть
При получении образцов замещенного гексаферрита бария BaAl x Fe 12‒ x O 19 методом самовозгорания использовали нитрат бария (Ba(NO 3 ) 2 , «ч.д.а.»), девятиводный нитрат железа (III) (Fe(NO 3 ) 3 ·9H 2 O, «ч») и (Al(NO 3 ) 3 ·9H 2 O, «хч») (табл. 1).
Таблица 1
Химический состав исходной шихты, масс. %
|
Степень замещения |
Ba(NO 3 ) 2 |
Fe(NO 3 ) 3 ·9H 2 O |
Al(NO 3 ) 3 ·9H 2 O |
|
x = 0 |
5,11 |
94,89 |
0 |
|
x = 1 |
5,14 |
87,48 |
7,38 |
|
x = 2 |
5,17 |
79,98 |
14,85 |
|
x = 3 |
5,20 |
72,39 |
22,41 |
В рамках метода самовозгорания стехиометрические количества нитратов растворяли в 20 мл дистиллированной воды. После смешивания растворов к ним добавляли раствор лимонной кислоты (3 моль лимонной кислоты на 1 моль нитратов). Затем путем добавления раствора аммиака pH раствора доводили до 7 по универсальной индикаторной бумаге. Раствор упаривали в фарфоровой чашке до карамелевидного состояния. После упаривания препарат нагревали в сушильном шкафу при 150…200 °C в течение 4 часов. В ходе нагрева проходил процесс самовозгорания, в результате чего образовывался ксерогель. Далее ксерогель перетирали и прокаливали при 500 °C в течение 4 часов в муфельной печи. Окончательное спекание проводили при 1100 °C в течение 4 часов.
Химический состав полученных порошков определяли на растровом электронном микроскопе Jeol JSM-7001F с функцией микроанализа. Элементный состав образцов представлен в табл. 2. На рис. 1 представлены изображения образцов, полученные на электронном микроскопе во вторичных электронах.
Таблица 2
Элементный состав, ат. %
|
Образец |
Ba |
Al |
Fe |
Ba : Al : Fe |
|
x = 0 |
8,12 |
0 |
91,88 |
1,06 : 0 : 12 |
|
x = 1 |
7,84 |
8,75 |
83,40 |
1,02 : 1,14 : 10,86 |
|
x = 2 |
7,80 |
19,85 |
72,35 |
1,02 : 2,58 : 9,42 |
|
x = 3 |
7,97 |
21,44 |
70,59 |
1,04 : 2,80 : 9,20 |
Полученные образцы исследовали методом порошковой дифрактометрии. Регистрацию рентгенограмм проводили на многофункциональном дифрактометре Rigaku Ultima IV при скорости съемки 1°/мин. Результаты представлены на рис. 2. Видно, что при использовании метода самовозгорания образование гомогенного замещенного алюминием гексаферрита бария происходит при температуре 1100 °C, в то время как образцы, получаемые керамическим методом, содержат фазы Fe 2 O 3 и Al 2 O 3 вплоть до 1300 °C [29].
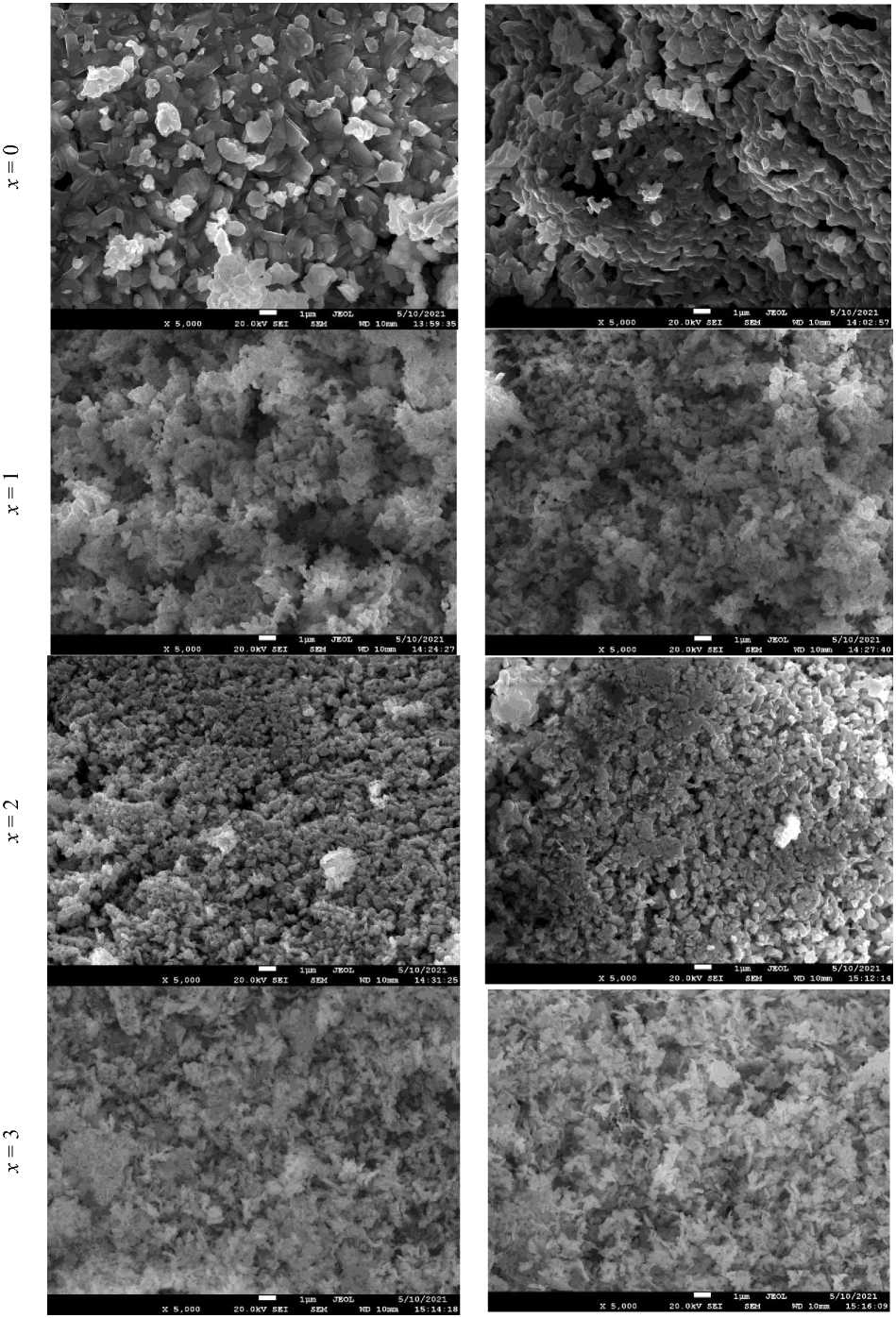
Рис. 1. Электронные изображения образцов BaAl x Fe 12- x O 19 во вторичных электронах
2,5
| BaFe12O19 [43]
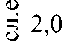
я
§ 1,5 о
Я
<и н я я я 1,0
л я о н я
О 0,5
0,0
20 30 40 50 60
2Θ, град
Рис. 2. Порошковые рентгенограммы образцов BaAl x Fe 12- x O 19 , полученных методом самовозгорания при 1100 °C, в сравнении с литературными данными [43]
В табл. 3 представлены рассчитанные параметры решетки полученных образцов чистого и замещенного алюминием гексаферрита бария.
Таблица 3
Параметры решетки и объем элементарной ячейки
|
Образец |
a , Å |
c , Å |
V , Å3 |
|
x = 0 |
5,892 |
23,210 |
697,8 |
|
x = 1 |
5,870 |
23,108 |
689,4 |
|
x = 2 |
5,847 |
23,044 |
682,2 |
|
x = 3 |
5,828 |
22,981 |
676,0 |
|
BaFe 12 O 19 [44] |
5,893 |
23,194 |
697,6 |
Выводы
Метод самовозгорания позволяет эффективно получать сложные оксиды, что было продемонстрировано на примере гексаферрита бария, замещенного алюминием. В результате проведенной серии экспериментов были получены монофазные образцы BaAl x Fe 12‒ x O 19 со степенями замещения железа до x = 3. Также был произведен расчет параметров структуры полученных образцов.
Благодаря большей степени гомогенности, достигаемой за счет перевода компонентов в раствор, и меньшему размеру образующихся частиц оксида, удалось снизить температуру синтеза материала с 1300 до 1100 °C. Снижение температуры синтеза позволит получать материалы с более развитой поверхностью и дает принципиальную возможность легирования легколетучими элементами.
Список литературы Использование метода самовозгорания для получения замещенного алюминием гексаферрита бария
- 1. Gratzel M. Mesoporous Oxide Junctions and Nanostructured Solar Cells. Curr. Opin. Colloid Interface Sci., 1999, vol. 4, pp. 314–321. DOI: 10.1016/S1359-0294(99)90013-4. 2. Hadei M., Mesdaghinia A., Nabizadeh R., Mahvi A.Н., Rabbani S., Naddafi K. A Comprehensive Systematic Review of Photocatalytic Degradation of Pesticides Using Nano TiO2. Environ. Sci. Pollut. Res., 2021, vol. 28, no. 11, pp. 13055–13071. DOI:10.1007/s11356-021-12576-8. 3. Serrà A., Philippe L., Perreault, Garcia-Segura S. Photocatalytic Treatment of Natural Waters. Reality or Hype? The Case of Cyanotoxins Remediation. Water Res., 2020, vol. 188. DOI: 10.1016/j.waters.2020.116543. 4. Medhi R., Marquez M.D., Lee T.R. Visible-Light-Active Doped Metal Oxide Nanoparticles: Review of their Synthesis, Properties, and Applications. ACS Appl. Nano Mater., 2020, vol. 3, no. 7., pp. 6156–6185. DOI: 10.1021/acsanm.0c01035. 5. Pascariu P., Homocianu M. ZnO-based Ceramic Nanofibers: Preparation, Properties and Applications. Ceramics International. Elsevier Ltd, 2019, vol. 45, no. 9, pp. 11158–11173. DOI: 10.1016/j.ceramint.2019.03.113. 6. Saad S.R., Mahmed N., Abdullah M.M.A.B., Sandu A.V. Self-Cleaning Technology in Fabric: a Review. IOP Conf. Ser. Mater. Sci. Eng., 2016, vol. 133, no. 1, 012028. DOI: 10.1088/1757-899X/133/1/0112028. 7. Verbič A., Gorjanc M., Simončič B. Zinc Oxide for Functional Textile Coatings: Recent Advances. Coatings, 2019, vol. 9, no. 9, 550. DOI: 10.3390/coatings9090550. 8. Montazer M., Amiri M.M. ZnO Nano Reactor on Textiles and Polymers : Ex-Situ and In-Situ Synthesis, Application and Characterization. J. Phys. Chem. B, 2014, vol. 118, no. 6, pp. 1453–1470. DOI: 10.1021/jp408532r. 9. Narang S.B., Pubby K. Nickel Spinel Ferrites: A review. J. Magn. Magn. Mater., 2020, vol. 519, 167163. DOI: 10.1016/j.jmmm.2020.167163. 10. de Julián Fernández C., Sangregorio C., de la Figuera J., Belec B., Makovec D., Quesada D. Progress and Prospects of Hard Hexaferrites for Permanent Magnet Applications. J. Phys. D. Appl. Phys., 2021, vol. 54, no. 15, 153001. DOI: 10.1088/1361-6463/abd272. 11. Thakur P., Chahar D., Taneja S., Bhalla N., Thakur A. A Review on MnZn ferrites: Synthesis, Characterization and Applications. Ceramics International. Elsevier Ltd, 2020, vol. 46, no. 10, pp. 15740–15763. DOI: 10.1016/j.ceramnit.2020.03.287. 12. Talaat A., Suraj M.V., Byerly K., Wang A., Wang Y., Leea J.K., Ohodnicki Jr P.R. Review on Soft Magnetic Metal and Inorganic Oxide Nanocomposites for Power Applications. J. Alloys Compd. Elsevier, 2021, vol. 870, 159500. DOI: 10.1016/j.jallcom.2021.159500. 13. Houbi A., Zharmenov A.A., Atassi Y., Bagasharova Z.T., Mirzalieva S., Kadyrakunov K. Microwave Absorbing Properties of Ferrites and their Composites: A Review. J. Magn. Magn. Mater., 2021, vol. 529, 167839. DOI: 10.1016/j.jmmm.2021.167839. 14. Chandel M, Singh V.P., Jasrotia R, Singha K., Kumar R. A Review on Structural, Electrical and Magnetic Properties of Y-type Hexaferrites Synthesized by Different Techniques for Antenna Applications and Microwave Absorbing Characteristic Materials. AIMS Mater. Sci., 2020, vol. 7, no. 3, рр. 244–268. DOI: 10.3934/matersci.2020.3.244. 15. Srinivasan G., Zavislyak I.V., Popov M., Sreenivasulu G., Fetisov Y.K. Ferrite-Piezoelectric Heterostructures for Microwave and Millimeter Devices: Recent Advances and Future Possibilities. J. Japan Soc. Powder Powder Metall., 2014, vol. 61, pp. S25–S29. DOI: 10.2497/jspm.61.s25. 16. Mallmann E.J.J., Sombra A.S.B., Goes J.C., Fechine P.B.A. Yttrium Iron Garnet: Properties and Applications Review. Solid State Phenom., 2013, vol. 202, pp. 65–96. DOI: 10.4028/www.scientific.net/ssp.202.65. 17. Feng J., Matsushita N., Murakoso T., Nakagawa S., Naoe M. (1999). Effects of Al Substitution for Fe in Ba Ferrite thin Films. J. Magn. Magn. Mater., 1999, vol. 193, no. 1–3, pp. 152–154. DOI:10.1016/s0304-8853(98)00421-1. 18. Feng J., Matsushita N., Watanabe K., Nakagawa S., Naoe M. A1 Substituted Ba Ferrite Films with High Coercivity and Excellent Squarneness for Low Noise Perpendicular Recording Layer. J. Appl. Phys., vol. 85, 1999, pp. 6139–6141. DOI:10.1063/1.3579262. 19. Zhou, X.Z., Morrish A.H., Yang Z., Zeng H.-X. Co-Sn Substituted Barium Ferrite Particles. J. Appl. Phys., 1994, vol. 75, no. 10, pp. 5556–5558. DOI:10.1063/1.355687.
- 20. Qiu J., Zhang Q., Gu M., Shen H. Effect of Aluminum Substitution on Microwave Absorption Properties of Barium Hexaferrite. J. Appl. Phys., 2005, vol. 98, no. 10, 103905. DOI: 10.1063/1.2135412. 21. Huang J., Li D., Li R., Chen P., Zhang Q., Liu H., Lv W., Liu G., Feng Y. One-Step Synthesis of Phosphorus/Oxygen Co-doped g-C3N4/Anatase TiO2 Z-scheme Photocatalyst for Significantly Enhanced Visible-Light Photocatalysis Degradation of Enrofloxacin. J. Hazard. Mater.., 2019, vol. 386, 121634. DOI:10.1016/j.jhazmat.2019.121634. 22. Ustinov A.B., Tatarenko A.S., Srinivasan G., Balbashov A.M. (2009). Al Substituted Ba-Hexaferrite Single-Crystal Films for Millimeter-Wave Devices. J. Appl. Phys., 2009, vol. 105, no. 2, 023908. DOI:10.1063/1.3067759. 23. Thongmee S., Osotchan T., Winotai P., Tang I.M. Fluctuations in the Local Fields Due to Al3+ Ions Substitution in the M-Type Barium Hexaferrites, BaFe12-xAlxO12. Int. J. Mod. Phys. B, 1998, vol. 12, no. 27–28, pp. 2847–2855. DOI:10.1142/S0217979298001666. 24. Albanese G., Asti G., Batti P. On the Effects of Partial Substitution of Fe by Ga in SrFe12O19. Nuovo Cimento B, 1968, vol. 58, no. 2, pp. 467–479. DOI:10.1007/bf02712001. 25. Kubo O., Ogawa E. Barium Ferrite Particles for High Density Magnetic Recording. J. Magn. Magn. Mater., 1994, vol. 134, no. 2–3, pp. 376–381. DOI:10.1016/0304-8853(94)00147-2. 26. Pavlova S.G., Balbashov A.M., Rybina L.N. Single Crystal Growth From the Melt and Magnetic Properties of Hexaferrites-Aluminates. J. Cryst. Growth., 2012, vol. 351, no. 1, pp. 161–164. DOI:10.1016/j.jcrysgro.2011.12.053. 27. Vinnik D.A., Ustinov A.B., Zherebtsov D.A., Vitko V.V., Gudkova S.A., Zakharchuk I., Lähderant E., Niewa R. Structural and Millimeter-Wave Characterization of Flux Grown Al Substituted Barium Hexaferrite Single Crystals. Ceram. Int. Elsevier Ltd., 2015, vol. 41, no. 10, pp. 12728–12733. DOI:10.1016/j.ceramint.2015.06.105. 28. Xu A., Yang M., Qiao R., Du H., Sun C. Activity and Leaching Features of Zinc-Aluminum Ferrites in Catalytic Wet Oxidation of Phenol. J. Hazard. Mater. Elsevier, 2007, vol. 147, no. 1–2, pp. 449–456. DOI: 10.1016/j.hazat.2007.01.026. 29.Wang S., Ding J., Shi Y., Chen Y.J. High Coercivity in Mechanically Alloyed BaFe10Al2O19. J. Magn. Magn. Mater., 2000, vol. 219, no. 2, pp. 206–212. DOI:10.1016/s0304-8853(00)00450-9. 30. Albanese G., Carbucicchio M., Deriu A., Substitution of Fe3+by Al3+in the Trigonal Sites of M-Type Hexagonal Ferrites. Nuovo Cimento B, 1973, vol. 15, no. 2, pp. 147–158. DOI:10.1007/bf02894778. 31. Albanese G. Mössbauer Investigation of Aluminium Substituted Barium Hexaferrite in the Paramagnetic State. 1995, J. Magn. Magn. Mater., vol. 147, no. 3, pp. 421–426. DOI:10.1016/0304-8853(95)00063-1. 32. Thakur P., Taneja S., Sindhu D., Lüders U., Sharma A., Ravelo B., Thakur A. Manganese Zinc Ferrites: a Short Review on Synthesis and Characterization. J. Supercond. Novel. Magn., 2020, vol. 33, no. 6, pp. 1569–1584. DOI: 10.1007/s10948-020-05489-z. 33. Zhang H., Kajiyoshi K. Hydrothermal Synthesis and Size-Dependent Properties of Multiferroic Bismuth Ferrite Crystallites. J. Am. Ceram. Soc., 2010, vol. 93, no. 11, pp. 3842–3849. DOI: 10.1111/j.1551-2916.2010.03953.x. 34. Chen M., Fun R.H, Liu G.F., Wang X.A., Sun K. Magnetic Properties of Barium Ferrite Prepared by Hydrothermal Synthesis. Key Eng. Mater., 2015, vol. 655, pp. 178–181. DOI:10.4028/www.scientific.net/kem.655.178. 35. Fariñas J. C., Moreno R., Pérez A., García M.A., García-Hernández M., Salvador M.D., Borrell A. Microwave-assisted Solution Synthesis, Microwave Sintering and Magnetic Properties of Cobalt Ferrite. J. Eur. Ceram. Soc., 2018. vol. 38, no. 5, pp. 2360–2368. DOI: 10.1016/j.jeurceramsoc.2017.12.052. 36. Lagashetty A., Muttin V., Patil M.K., Ganiger S.K. Synthesis, Characterization and Studies of BaFe2O4/PMMA Nanocomposite. J. Polym. Bull., 2020, pp. 1–17. DOI:10.1007/s00289-020-03403-0. 37. Belous A., Tovstolytkin A., Fedorchuk O., Shlapa Yu., Solopan S., Khomenko B. Al-doped Yttrium Iron Garnets Y3AlFe4O12: Synthesis and Properties. J. Alloys Compd., 2021, vol. 856, p. 158140. DOI:10.1016/j.jallcom.2020.158140. 38. Prabhu S., Geerthana M., Sohila S., Bhalerao G.M., Harish S., Navaneethan M., Hayakawa Y., Ramesh R. Preparation of Cr3+-Substituted NiFe2O4 Nanoparticles and its Microwave Absorption Properties. J. Supercond. Novel Magn., 2019, vol. 32, no. 5, pp. 1423–1429. DOI: 10.1007/s10948-018-4835-0.
- 39. Cobos M.A., de la Presa P., Llorente I., García-Escorial A., Hernando A., Jiménez J.A. Effect of Preparation Methods on Magnetic Properties of Stoichiometric Zinc Ferrite. J. Alloys Compd. Elsevier Ltd, 2020, vol. 849, 156353. DOI: 10.1016/j.jallcom.2020.156353. 40. Fan L., Zheng H., Zhou X., Zhang H., Wu Q., Zheng P., Zheng L., Zhang Y. A Comparative Study of Microstructure, Magnetic, and Electromagnetic Properties of Zn2W Hexaferrite Prepared by Sol–Gel and Solid-State Reaction Methods. J. Sol-Gel Sci. Technol. Springer US, 2020, vol. 96, no. 3, pp. 604–613. DOI: 10.1007/s10971-020-05364-2. 41. Del Toro R.S., Pinto-Castilla S., Cañizale E., Ávila E., Díaz Y., Gutiérrez B., Sifontes A.B. Synthesis of SrFe(Al)O3−δ–SrAl2O4 Nanocomposites Via Green Route. Nano-Structures & Nano-Object., 2020. vol. 22, pp. 100437. DOI:10.1016/j.nanoso.2020.100437. 42. Rekhila G., Trari M. Physical Properties of the Ferrites NiFe2−xMnxO4 (0 ≤ x ≤ 2) Prepared by Sol–Gel Method. J. Mater. Sci. Mater. Electron, 2021, vol. 32, no. 2, pp. 1897–1906. DOI: 10.1007/s10854-020-04958-4. 43. Shin H.S., Kwon S.-J. A Suggestion on the Standard X-ray Powder Diffraction Pattern of Barium Ferrite. Journal of Powder Diffraction, 1992, vol. 7, no. 4, pp. 212–214. DOI: 10.1017/S088571560001873X. 44. Townes W.D., Fang J.H., Perrotta A.J. The Crystal Structure and Refinement of Ferrimagnetic Barium Ferrite, BaFe12O19. Book Series of the Zeitschrift für Krist., 1967, vol. 125, pp. 437–449.


