Использование наноалмазов детонационного синтеза для определения фенола в водных средах
Автор: Ронжин Н.О., Пузырь А.П., Бондарь В.С.
Журнал: Вестник Красноярского государственного аграрного университета @vestnik-kgau
Рубрика: Биологические науки
Статья в выпуске: 2, 2017 года.
Бесплатный доступ
Проведена оценка применимости модифи-цированных наноалмазов (МНА) взрывного синтеза для диагностики фенола в водной среде с помощью реакции окислительного азо-сочетания (перекись водорода - 4-аминоантипирин - фенол). Содержание фе-нола оценивали по величине оптической плот-ности образующегося цветного продукта ка-тализируемой наночастицами реакции с по-мощью спектрального анализа водных проб. Исследован каталитический эффект МНА в реакции азосочетания после дополнительной адсорбции на поверхности наночастиц ионов железа и меди. Показано, что при выбранных условиях эксперимента повышение темпера-туры катализируемой МНА реакции азосоче-тания приводит к значительному (до 4,5 раза) увеличению выхода окрашенного продукта. Показано, что МНА обеспечивают линейный выход цветного продукта реакции в диапазоне концентраций фенола 0,05-10 мкг/мл. Полу-ченная линейная зависимость выхода продук-та реакции от концентрации аналита может быть использована в качестве калибровочной кривой при анализе содержания фенола в вод-ных средах. Установлено, что дополнитель-ная адсорбция ионов железа и меди на поверх-ности МНА сопровождается увеличением их каталитической активности в 2 и 1,7 раза соответственно. Продемонстрирована воз-можность многократного использования МНА для тестирования фенола в водной среде. По-казано, что при последовательном четырех-кратном применении частиц МНА для опреде-ления фенола в водных образцах с одинаковой концентрацией аналита наблюдается прак-тически одинаковый выход цветного продук-та. Результаты проведенных в работе иссле-дований имеют практическое значение и от-крывают перспективы разработки на основе МНА новых индикаторных средств многоразо-вого действия для выявления фенола и фе-нольных соединений в водных средах.
Наноалмазы, катализа-тор, фенол, системы индикации и диагности-ки, экологический мониторинг
Короткий адрес: https://sciup.org/14084840
IDR: 14084840 | УДК: 577.332.23:539.199
The use of nanodiamonds of detonation synthesis for the definition of phenol in water environments
The assessment of applicability of modified nanodiamonds (MND) of explosive synthesis for diagnostics of phenol in the water environment by means of reaction of an oxidizing azocoupling was carried out (hydrogen peroxide - 4-aminoantipirin - phenol). The content of phenol was estimated in the size of optical density of formed color product of the reaction catalyzed by nanoparticles by means of the spectral analysis of water tests. The catalytic effect of MND in reaction of azocoupling reaction after additional adsorption on the surface of nano-particles of ions of iron and copper was investigat-ed. It was shown that under chosen experimental conditions the temperature increase of the cata-lyzed MND of reaction of azocoupling resulted in considerable (4.5 fold) increase in the exit of paint-ed product. It was shown that MND provided a line-ar exit of a color product of reaction in the range of concentration of phenol of 0.05-10 mkg/ml. The received linear dependence of a product yield of reaction on concentration of analyte can be used as a calibration curve in the analysis of the content of phenol in water environments. It was established that additional adsorption of ions of iron and copper on the surface of MND was followed by the in-crease in their catalytic activity in 2 and 1.7 fold respectively. The possibility of repeated use of MND for testing of phenol in the water environment was shown. It was shown that at consecutive quad-ruple application of particles of MND for the defini-tion of phenol in water samples with identical con-centration of analyte almost identical exit of a color product was observed. The results of the research-es conducted in the study have practical value and open development prospects on the basis of MND of new indicator means of reusable action for identi-fication of phenol and phenolic connections in wa-ter environments.
Текст научной статьи Использование наноалмазов детонационного синтеза для определения фенола в водных средах
Введение. Одной из актуальных задач современной аналитики является разработка и создание новых методов и средств быстрого выявления токсикантов при экологическом мониторинге загрязнений окружающей среды [1– 5]. К числу наиболее распространенных во всем мире (в том числе в России) загрязняющих водные среды веществ относятся фенольные соединения [6–9]. Для создания новых эффективных средств диагностики фенолов интерес могут представлять модифицированные наноал- мазы (МНА) взрывного синтеза [10, 11]. Ранее нами была обнаружена каталитическая активность МНА в реакции окислительного азосочетания (Н2О2 – 4-аминоантипирин – фенол), которая сопровождается образованием цветного продукта [12, 13]. В этих исследованиях было установлено, что каталитическая функция МНА определяется наличием на поверхности наночастиц микропримесей ионов железа и меди и вероятным участием в катализе поверхностных кислородсодержащих функциональных групп [13]. Анализ полученных данных позволил высказать предположение о возможности использования МНА в создании новых систем экс-пресс-индикации фенола и его производных для экологического мониторинга загрязнений водных сред этими токсикантами.
Цель работы. Экспериментальная оценка применимости МНА для диагностики фенола в водной среде и возможности повышения каталитической эффективности наночастиц в реакции окислительного азосочетания.
Материалы и методы исследований. В работе использовали МНА со средним размером кластеров 49,6 нм (Zetasizer Nano ZS, Malvern Instruments Ltd., Англия), полученные из взрывных наноалмазов отечественного производства (ООО «Реал-Дзержинск», Россия) по разработанной ранее технологии [10,11] и обладающие высокой коллоидной стабильностью в дисперсионных средах. Для экспериментов использовали гидрозоли МНА с концентрацией наночастиц 10,0 г/л, которые готовили добавлением деионизованной воды к навеске порошка МНА. Деионизованную воду получали с помощью системы Milli-Q system (Millipore, США).
Применяемые реагенты: 4-аминоантипирин (1-фенил-2,3-диметил-4-аминопиразолон) (4-ААП) квалификации «чда» и соли двухвалентных металлов (FeSO 4 и CuSO 4 ) квалификации «хч» и «чда» (Реахим, Россия); фенол (Flucka, Германия); 3%-й раствор перекиси водорода (Галено Фарм™, Россия). Рабочие растворы реагентов готовили in situ в деионизованной воде.
При проведении реакции азосочетания с использованием МНА в качестве катализатора концентрация ингредиентов в объеме реакционной смеси 1 мл составляла: 0,03% H 2 O 2 ; 0,10 мг/мл 4-ААП; 0,56 мг/мл фенола. Реакцию запускали добавлением суспензии МНА (финальная концентрация наночастиц в пробе 0,5 мг/мл). После внесения всех компонентов образцы интенсивно перемешивали в течение 3
секунд на Vortex-Genie 2 g-560E (Scientific Industries, Inc., США) и инкубировали при температурах 20 или 40°С в течение 10 мин. После инкубации МНА удаляли из образцов центрифугированием (Centrifuge 5415R, Eppendorf, Германия) при 16000 g в течение 10 мин при 10°С. Для более полного осаждения наночастиц перед центрифугированием в образцы добавляли хлорид натрия до концентрации 100–120 мМ. Полученные супернатанты отбирали и проводили спектральную оценку образовавшегося окрашенного продукта реакции на спектрофотометре UV-1800 (Shimadzu, Япония) по величине оптической плотности при длине волны 506 нм.
Для проверки увеличения каталитической активности МНА в реакции окислительного азосочетания на их поверхность дополнительно адсорбировали ионы железа и меди. С этой целью к 1 мл водных растворов сульфата железа (или сульфата меди) с концентрацией 25 мМ добавляли 100 мкл гидрозоля МНА и после перемешивания инкубировали пробы в течение одного часа при комнатной температуре. После этого частицы МНА удаляли из образцов центрифугированием при указанных выше условиях. Супернатанты отбирали для спектральной оценки количества адсорбированных МНА ионов металлов. Расчеты проводили на основании спектральных данных исходных растворов металлов (контроль) и после их инкубации с МНА (опыт). Полученные осадки МНА дважды отмывали деионизованной водой с добавлением 100 мМ хлорида натрия для удаления неадсорбировав-шихся ионов металлов, каждый раз ресуспен-дируя наночастицы в новом объеме промывочного раствора и собирая центрифугированием. Отмытые МНА ресуспендировали в деионизованной воде до исходного объема (100 мкл) и использовали для оценки каталитической активности в реакции азосочетания.
Результаты исследований и их обсуждение. В исследованиях было показано, что повышение температуры реакции окислительного азосочетания, катализируемой частицами МНА, приводит к значительному увеличению выхода окрашенного продукта. Из полученных данных (рис. 1) следует, что при температуре 40°C наблюдается гораздо большее (в 3,5–4,5 раза) образование продукта, чем при температуре 20°С, и такая закономерность наблюдается при разном содержании аналита в пробе.
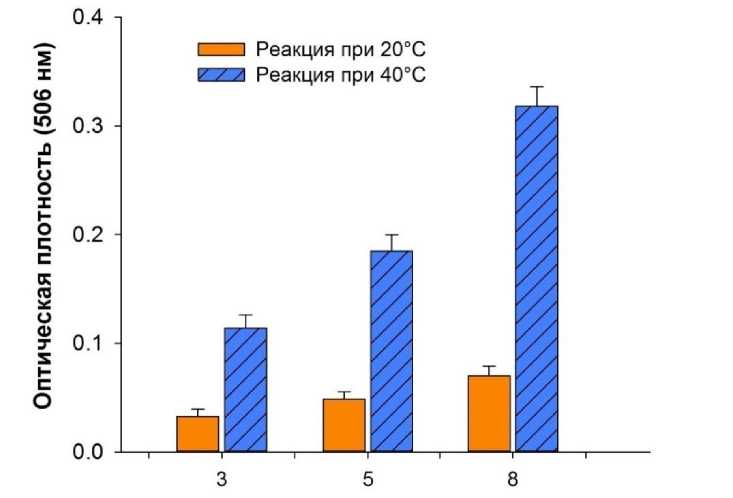
Содержание аналита в пробе (мкг)
Рис. 1. Выход окрашенного продукта реакции, катализируемой частицами МНА при разных температурах и разном содержании аналита в пробе (инкубация образцов 10 мин)
Экспериментально установлено (рис. 2), что использование МНА как катализатора реакции азосочетания обеспечивает линейный выход цветного продукта в широком интервале кон- центраций аналита. Из представленных данных видно, что прирост выхода продукта линейно возрастает в диапазоне концентраций фенола 0,05–10 мкг/мл. Полученная зависимость
(рис. 2) может быть использована в качестве калибровочной кривой при анализе содержания фенола и его соединений в водных средах.
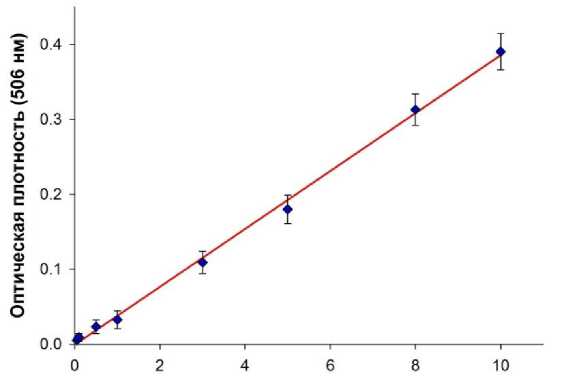
Концентрация фенола (мкг/мл)
Рис. 2. Калибровочная зависимость образования продукта реакции, катализируемой МНА, от концентрации фенола (инкубация образцов 10 мин, температура 40°C)
Ранее нами было выявлено, что каталитический эффект МНА в реакции окислительного азосочетания реализуется за счет микропримесей ионов железа и меди на их поверхности [13]. Для проверки увеличения каталитической активности МНА в настоящей работе была исследована возможность дополнительной адсорбции ионов железа и меди на поверхность наночастиц. Эксперименты показали (рис. 3), что обработка МНА водных растворов солей металлов сопровождается адсорбцией ионов железа и меди на наночастицы. Из расчетов, проведенных на основании спектральных данных контрольных (без инкубации с МНА) и опытных (после инкубации с МНА) растворов солей металлов, было показано следующее. При использованных экспериментальных условиях (концентрация ионов металлов в пробе, количество добавляемых наночастиц, время инкубации) на 1 мг МНА адсорбируется 0,19 мг ионов меди или 1,05 мг ионов железа соответственно.
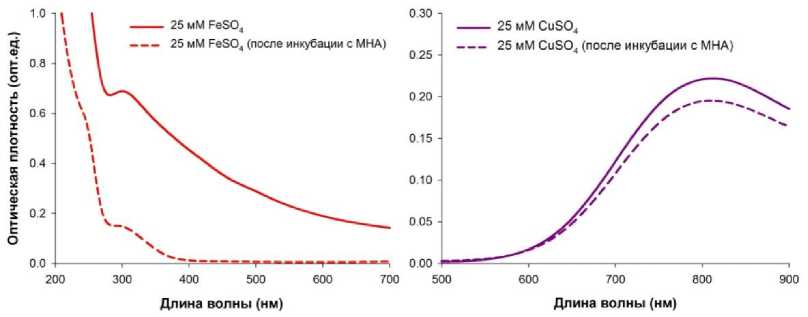
Рис. 3. Спектры поглощения водных растворов сульфата железа и меди без и после инкубации с частицами МНА
Как показали эксперименты (рис. 4), частицы (МНА-Fe) и меди (МНА-Cu) обладают большей
МНА с адсорбированными ионами железа каталитической активностью в реакции азосоче-
тания и обеспечивают больший выход продукта по сравнению с исходными наночастицами. Из представленных данных видно, что при использовании в качестве катализатора частиц МНА-Cu и МНА-Fe выход продукта увеличивается в 1,7 и 2 раза по сравнению с его образованием в реакции, катализируемой исходными МНА. Эти данные создают предпосылки для повышения эффективности систем индикации фенольных соединений, создаваемых на основе МНА.
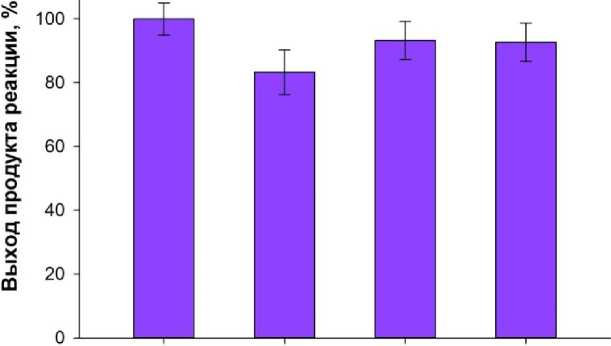
В исследованиях продемонстрирована возможность многократного использования МНА для тестирования фенола в водной среде (рис.5). Видно, что при последовательном четырехкратном применении частиц МНА для определения фенола в водных образцах с одинаковой концентрацией аналита наблюдается практически одинаковый выход цветного продукта. Эти данные имеют важное практическое значение и открывают перспективы разработки на основе МНА новых индикаторных средств многоразового действия для выявления фенола и фенольных соединений в водных средах.
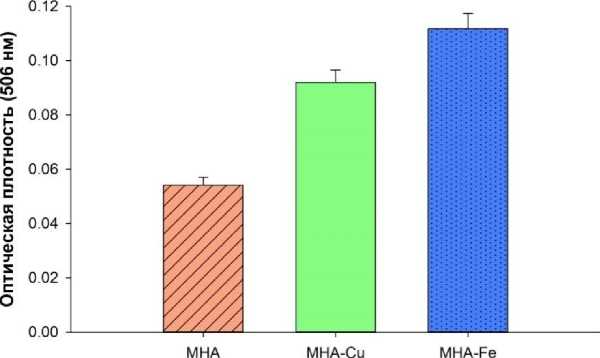
Образцы МНА, используемые в реакции
Рис. 4. Выход цветного продукта реакции, катализируемой исходными МНА и МНА, после дополнительной адсорбции на них ионов железа и меди
12 3 4
Номер измерения
Рис. 5. Выход цветного продукта реакции при четырехкратном использовании частиц МНА для индикации фенола в водных образцах с одинаковой концентрацией аналита
Заключение. Совокупность полученных в работе данных позволяет высказать несколько общих выводов. Экспериментально показано, что применение МНА в качестве катализатора реакции окислительного азосочетания (Н 2 О 2 – 4-ААП – фенол) обеспечивает линейный выход цветного продукта в широком диапазоне (0,05– 10 мкг/мл) концентраций аналита. Установлено, что каталитическая эффективность МНА при тестировании фенола может быть значительно увеличена за счет повышения температуры реакции (в 3,5–4,5 раза) и адсорбции на поверхности наночастиц ионов железа или меди, участвующих в катализе (в 2 и 1,7 раза соответственно). В модельных экспериментах продемонстрирована возможность многократного использования МНА для тестирования фенола в водных образцах. Это открывает перспективы создания на основе МНА новых эффективных индикаторных тест-систем многоразового действия для быстрой диагностики загрязнений водной среды фенолами.
Исследование выполнено при финансовой поддержке Российского фонда фундаментальных исследований, Правительства Красноярского края, Красноярского краевого фонда поддержки научной и научно-технической деятельности в рамках научного проекта № 16-43-243027.
Список литературы Использование наноалмазов детонационного синтеза для определения фенола в водных средах
- Hatamie A., Zargar B., Jalali A. Copper nano-particles: A new colorimetric probe for quick, naked-eye detection of sulfide ions in water samples//Talanta. -2014. -V. 121. -P. 234-238.
- Rapid colorimetric detection of melamine by H2O2-Au nanoparticles/M. Yin, L. Zhao, Q. Wei //RSC Advances. -2015. -V. 5. -P. 32897-32901.
- Wang Y., Hu S. Applications of carbon nano-tubes and graphene for electrochemical sens-ing of environmental pollutants//J. Nanosci. Nanotechnol. -2016. -V. 16. -№ 8. -P. 7852-7872.
- Real-time remote monitoring of water quality: a review of current applications, and advance-ments in sensor, telemetry, and computing technologies/H.B. Glasgow, J.M. Burkholder, R.E. Reed //J. Exp. Mar. Biol. Ecol. -2004. -V. 300. -P. 409-448.
- Rodriguez-Mozaz S., Lopes de Alda M.J., Barcelo D. Fast and simultaneous monitoring of organic pollutants in a drinking water treat-ment plant by a multi-analyte biosensor fol-lowed by LC-MS validation//Talanta. -2006. -V. 69. -№ 2. -P. 377-384.
- Другов Ю.С., Родин А.А. Мониторинг орга-нических загрязнений природной среды: практ. руководство. -М., 2013. -893 с.
- Сурсякова В.В., Бурмакина Г.В., Рубайло А.И. Разработка методик определения фе-нолов в питьевых и природных водах мето-дами капиллярного электрофореза и высо-коэффективной жидкостной хроматографии//Журнал СФУ. -2010. -Т. 3. -№ 3. -С. 268-277.
- Global water pollution and human health/R.P. Schwarzenbach, T. Egli, T.B. Hofstetter //Environment and Resources. -2010. -V. 35. -P. 109-136.
- Wasi S., Tabrez S., Ahmad M. Toxicological effects of major environmental pollutants: an overview//Environ. Monit. Assess. -2013. -V. 185. -№ 3. -P. 2585-2593.
- Bondar V.S., Puzyr A.P. Nanodiamonds for biological investigations//Phys. Solid State. -2004. -V. 46. -P. 716-719.
- Physical and chemical properties of modified nanodiamonds/A.P. Puzyr, V.S. Bondar, A.A. Bukayemsky //NATO Sci. Ser. II: Math. Phys. Chem. -2005. -V. 192. -P. 261-270.
- Каталитическая активность наноалмазных частиц в органических реакциях/В.С. Бон-дарь, К.В. Пуртов, А.П. Пузырь //ДАН. -2008. -Т. 418. -С. 267-169.
- Catalytic activity of nanodiamonds in azocoupling reaction/N.O. Ronzhin, A.P. Puzyr, A.E. Burov //J. Biomat. Nanobiotech. -2014. -V. 5. -P. 173-178.


