Использование принципов геоники в практике водоочистки
Автор: Лесовик Валерий Станиславович, Сапронова Жанна Ануаровна, Фетисов Роман Олегович, Ипанов Дмитрий Юрьевич
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Промышленная экология
Статья в выпуске: 5-3 т.14, 2012 года.
Бесплатный доступ
В работе рассмотрены эндогенные и экзогенные процессы образования природных вод, их очистка в естественных природных условиях. Описаны возможности использования техногенного сырья для очистки сточных вод с учетом принципов геоники – науки об использовании результатов исследования геологических процессов для решения различных технологических задач, в частности, проблемы водоочистки.
Геоника, геофизические и геохимические процессы, очистка, природные и сточные воды
Короткий адрес: https://sciup.org/148201604
IDR: 148201604 | УДК: 504.4:574(571.12)
Use the geonics principles in practice of water purification
In work endogenous and exogenous processes of natural waters formation, their cleaning in natural environment are considered. Possibilities of use the technogenic raw materials for a sewage disposal taking into account the geonics principles – sciences about use the results of research the geological processes for the solution of various technological tasks, in particular, water purification problems are described.
Текст научной статьи Использование принципов геоники в практике водоочистки
Ипанов Дмитрий Юрьевич, аспирант вещества находятся в виде молекул и ионов с размерами частиц, не превышающих 10-7 мм. Коллоидные же растворы включают в себя не отдельные молекулы, а группы молекул и ионов с размерами растворенных частиц от 10-1 до 10-5 мм. Проникая в почву, вода растворяет различные вещества, обогащаясь солями, органическими остатками и изменяя свой газовый состав. Согласно современным представлениям, подземные воды по происхождению могут быть как экзогенными (их источник – водные объекты на поверхности суши и влага атмосферы), так и эндогенные (их источник – недра Земли) [2].
Экзогенные подземные воды попадают в горные породы либо в процессе просачивания (инфильтрация) поверхностных вод и конденсации водяного пара, либо в результате седиментации (осадконакопления). Просачиваясь сквозь толщу земной коры, вода соприкасается с такими породами, как пески, глины, песчаники, мел, мергели, алевриты и др. Все эти породы в той или иной мере обладают адсорбционными, коагуляционными, ионообменными, флокуляцион-ными и другими свойствами, способствующими удалению из воды вредных примесей и обогащению многими микроэлементами. Вода, проникающая в нижние горизонты, по своему составу значительно отличается от поверхностных вод. В качестве примера можно привести минеральные воды некоторых месторождений (табл. 2). Согласно новейшим представлениям о видах воды в горных породах в настоящее время выделяются следующие основные виды: парообразная; прочносвязанная (адсорбированная, гигроскопическая) и рыхлосвязанная (вода поверхностных слоев, пленочная); капиллярная; свободная (гравитационная); твердая. Кроме того, в минералах установлена химически связанная вода (конституционная и кристаллизационная) [4].
Таблица 1. Состав воды р. Оскол и Тихая Сосна [1]
|
Вещество или показатель химического состава воды |
Единица из-мере-ния |
Концентрация веществ в водном объекте |
|
|
р. Оскол |
р. Тихая Сосна |
||
|
взвешенные вещества |
мг/дм3 |
4,484 |
10,2 |
|
хлориды |
мг/дм3 |
18,68 |
44,1 |
|
сульфаты |
мг/дм3 |
57,16 |
98,8 |
|
сухой остаток |
мг/дм3 |
- |
609,5 |
|
ХПК |
мг/дм3 |
14,61 |
15,2 |
|
БПК 5 |
мг/дм3 |
5,039 |
2,47 |
|
азот аммонийный |
мг/дм3 |
0,075 |
0,45 |
|
азот нитритный |
мг/дм3 |
0,03 |
0,09 |
|
азот нитратный |
мг/дм3 |
1,029 |
14,2 |
|
фосфаты по р |
мг/дм3 |
0,2 |
0,44 |
|
железо общее |
мг/дм3 |
0,07 |
0,21 |
|
нефтепродукты |
мг/дм3 |
0,098 |
0,04 |
|
СПАВ |
мг/дм3 |
0,0015 |
0 |
|
медь |
мг/дм3 |
0,0004 |
- |
Таблица 2. Составы минеральных вод [3]
|
Вещество или показатель химического состава воды |
Ед. изм. |
Концентрация веществ в минеральной воде |
|||||
|
Ессентуки № 4 |
Ессентуки № 17 |
Нарзан |
Боржоми |
Славяновская, Смирновская |
Лысогорская |
||
|
минерализация |
мг/дм3 |
8000-10000 |
12000-18500 |
1800-3000 |
5000-7500 |
3000-4000 |
13000-19000 |
|
гидрокарбонаты |
мг/дм3 |
3600-4500 |
6000-8000 |
1000-1500 |
3500-5000 |
1200-1500 |
400-1200 |
|
сульфаты |
мг/дм3 |
< 25 |
< 50 |
300-500 |
< 10 |
800-1000 |
5500-9000 |
|
хлориды |
мг/дм3 |
1500-1900 |
2200-4200 |
100-150 |
250-500 |
250-350 |
2200-3700 |
|
кальций |
мг/дм3 |
< 150 |
< 200 |
300-400 |
20-150 |
250-350 |
350-550 |
|
магний |
мг/дм3 |
< 75 |
< 300 |
80-120 |
20-150 |
< 50 |
500-900 |
|
натрий |
мг/дм3 |
130-200 |
1000-2000 |
||||
|
калий |
мг/дм3 |
130-200 |
1,0 |
||||
|
натрий+калий |
мг/дм3 |
2500-2900 |
3200-6000 |
600-800 |
2800-4500 |
||
В ходе эндогенных процессов под воздействием тепловой энергии, давления земных недр и геологических процессов происходит выделение воды из горных пород. В частности, выделение воды из кристаллогидратов можно продемонстрировать на примере следующих схем: t
CuSO 4 ∙ 5 H 2 O → CuSO 4 + 5 H 2 O;
t
CaSO 4 ∙ 2 H 2 O → CaSO 4 + 2 H 2 O;
t
Na 2 CO 3 ∙ 10 H 2 O → Na 2 CO 4 + 10 H 2 O;
t
Ca(HCO 3 ) 2 ∙ 5 H 2 O → CaCO 3 + CO 2 + H 2 O;
t
Mg(OH) 2 ∙ → MgO + H 2 O и др.
В момент своего образования в силу геохимических условий вода насыщена самыми разнообразными примесями, среди которых могут быть и токсичные. Просачиваясь сквозь слои разнообразных пород к поверхности земли, вода проходит многочисленные стадии фильтрации, адсорбции, ионного обмена и т.д. Таким образом, в ходе продвижения воды с поверхности вглубь земли и наоборот осуществляются естественные природные процессы очистки с участием различных пород, т.е. процессы, описываемые геоникой.
В отличие от бионики, идея которой заключается в применение знаний о живой природе для решения инженерных задач, цель геоники – разработка общих принципов управления развитием объектов неорганического мира. Реализация нового научного направления позволит не только расширить сырьевую базу и разработать новые технологии производства материалов и водоочистки, но и улучшить комфортность пребывания вида Homo Sapiens в системе «человек-материал-среда обитания». Геоника появилась в конце ХХ в. как одно из направлений кибернетики – науки общих законах управления в системах любой природы – биологической, технической, социальной [5, 6]. В частности, геоника может использовать результаты исследования геологических процессов для решения различных технологических задач. К одной из таких задач относится проблема очистки сточных вод, в особенности, использование в водоочистке отходов различных производств.
Как известно, проблема образования, накопления и возможности повторной переработки промышленных отходов обширна и многогранна. Для решения некоторых аспектов этой всеобъемлющей проблемы нами использованы принципы геоники, основные положения которой разработаны в Белгородском государственном технологическом университете им. В.Г. Шухова доктором технических наук, чл.-корр. РААСН В.С. Лесовиком [5, 6]. Мы рассматриваем образующиеся отходы, их возникновение, накопление, утилизацию и повторное использование как постоянное изменение и движение материи, как элемент эволюции окружающего мира. Многие твердые промышленные отходы обладают рядом физико-химических свойств, делающих их пригодными к использованию в водоочистке, применяя технологии, аналогичные процессам, протекающим в природе. Так, на кафедре промышленной экологии исследована возможность использования для очистки сточных вод таких отходов предприятий, как электросталеплавильный шлак и пыль электросталеплавильного цеха (ЭСПЦ) Оскольского электрометаллургического комбината, отход производства дисахаридов – дефекат, аспирационная пыль комбината строительных материалов (БКСМ). Все перечисленные отходы являются тонкодисперсными (рис. 1), имеют большую удельную поверхность (табл. 3), обладают высокоразвитой поверхностью (рис. 2) и имеют хорошие сорбционные свойства (табл. 3) [7-9]. Кроме того, благодаря своему сложному многокомпонентному химическому (табл. 4) и фазовому составу (рис. 3), они в определенных условиях способны проявлять реагентные, коагуляционные и флокуляционные свойства.
Таблица 3 . Удельная поверхность отходов промышленности их сорбционная емкость по метиленовому голубому
|
Наименование отхода |
Удельная поверхность, S уд , м2/кг |
Сорбционная емкость, мг/г |
|
шлак ОЭМК |
465,0 |
4,82 |
|
пыль ЭСПЦ |
556,7 |
3,92 |
|
дефекат |
872,5 |
3,49 |
|
пыль БКСМ |
933,7 |
4,12 |

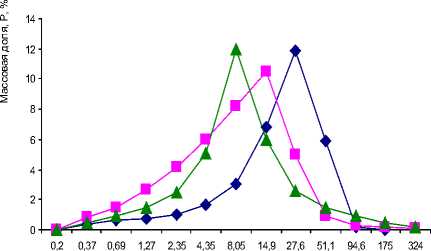
Диаметр частиц, D, мкм
—♦— шлак —■— пыль БКСМ —*— ТД
Рис. 1. Соответствие весовой доли частиц (Р, %) заданным значениям размеров частиц (D, мкм)
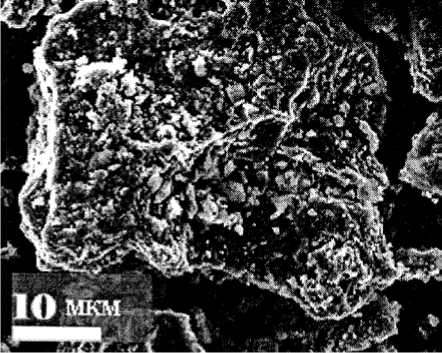

б)
Рис. 2. Микроструктура шлака ( а ) и термически модифицированного дефеката ( б )
Все эти характерные особенности делают возможным использование их для очистки сточных вод сложного состава. Так, в лабораторных и промышленных условиях нами установлена возможность достижения высокой эффективности очистки сточных вод от ионов Cr 2 O 7 2-, CrO 4 2-, Cu2+, Ni2+, Zn2+, Fe2+ и Fe3+ и других металлов с помощью пыли ЭСПЦ, шлака ОЭМК, пыли БКСМ, отхода производства дисахаридов – де-феката. Показано, что дефекат эффективен также при очистке сточных вод от жиров, нефтепродуктов, СПАВ, красителей. Во всех этих случаях в ходе очистки в растворах протекают процессы, аналогичные протекающим в земной коре при просачивании воды через многочисленные слои различных пород: адсорбция, коагуляция, флокуляция.
Таблица 4. Химический состав некоторых отходов
|
Вид |
Химический |
состав, |
% |
|||||||||
|
отхода |
CaO |
SiO 2 |
Al 2 O 3 |
FeO |
MnO |
MgO |
Cr 2 O 3 |
FeO общ |
C |
S |
Zn |
прочие |
|
шлак ОЭМК |
54,6 |
25,4 |
7,1 |
1,8 |
0,8 |
9,4 |
0,1 |
2,3 |
н/о |
н/о |
н/о |
0,3 |
|
пыль ЭСПЦ |
24,0 |
18,0 |
0,3 |
8,0 |
3,0 |
5,0 |
0,28 |
43,3 |
2,5 |
0,4 |
1,5 |
1,72 |
|
пыль БКСМ |
46,7 |
47,8 |
0,7 |
- |
- |
2,12 |
- |
0,2 |
- |
- |
- |
2,5 |
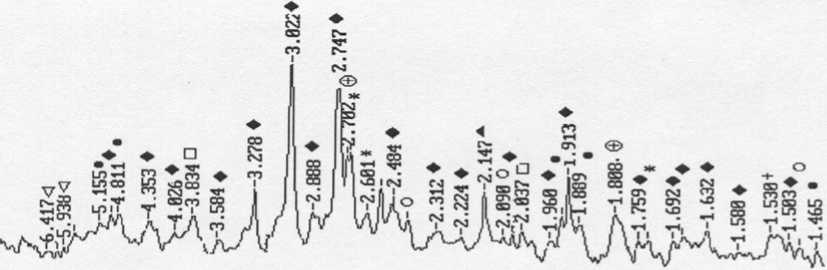
а)
Примечание: ♦ - y -2CaO - SiO 2 ; * - 3CaO^Al2O 3 ; + - 3CaO - MgO - SiO2; V - CaO^Al2O3; o - MgO; □ - CaCO3;
• - Ca(OH)2; < - FeO; ® - 3CaO - 2SiO 2 ;
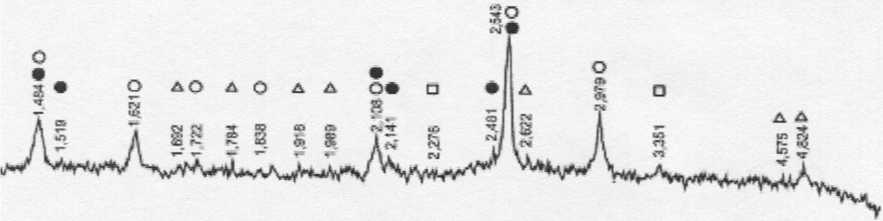
б)
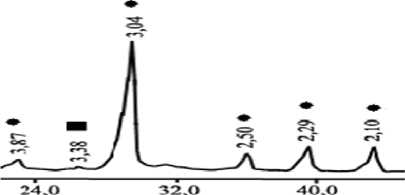
Примечание: • – СаСО 3; ■ – SiO 2 в)
Рис. 3. Рентгенофазовый анализ шлака воздушного охлаждения электросталеплавильного производства ( а ), пыли ЭСПЦ ( б ) и дефеката ( в )
Благодаря высокоразвитой поверхности, наличию пор и активных центров в местах дислокации кристаллов при добавлении вышеперечисленных отходов к модельным растворам и сточными водами протекают процессы адсорбции загрязняющих веществ (рис. 4).
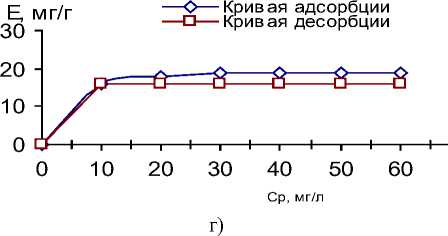
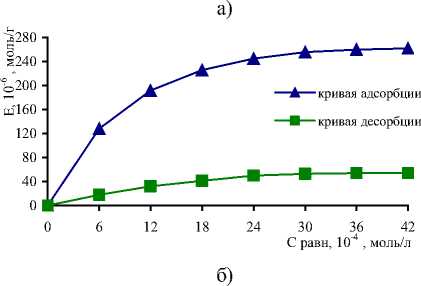
Рис. 4. Изотермы адсорбции и десорбции: а – ионов Ni2+, Cu2+ на поверхности дефеката; б – красителя ОR на поверхности дефеката; в – ионов Fe2+ на поверхности шлака; г – ионов Zn2+ на поверхности шлака
В связи с повышенной щелочностью водных вытяжек шлака ОЭМК, дефеката, пыли ЭСПЦ и БКСМ (рис. 5) в водных средах возможна реагентная очистка:
Men+ + n(OH-) →Me(OH) n ↓
120 J
100 J
80 J
40 J
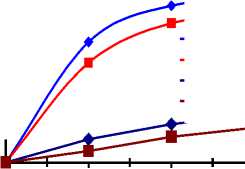
кривая адсорбции ионов Ni кривая адсорбции ионов Cu кривая десорбции ионов Ni кривая десорбции ионов Cu
Cравн, 10 -2 мол
При растворении шлака и пылей в подкисленной водной среде происходит растворение соединений Fe(II), Fe(III), Al и переход ионов Fe2+, Fe3+ и Al3+ в раствор. Известно, что данные ионы являются хорошими коагулянтами, поэтому при их гидролизе происходит коагуляция (слипание) взвешенных частиц в модельных растворах и сточных водах, что приводит к их быстрой седиментации и обеспечивает высокую эффективность очистки вод.
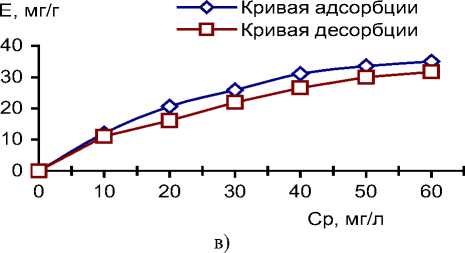
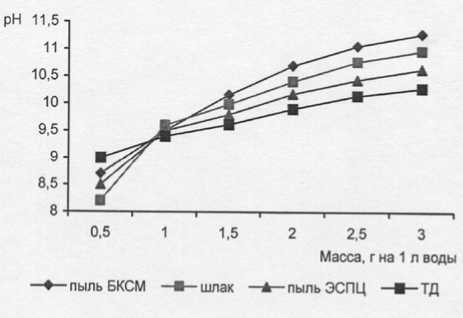
Рис. 5. Изменение рН водной среды при добавлении отходов промышленности (Ø частиц < 40 мкм)
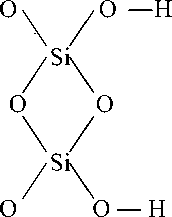
Вследствие присутствия в шлаке и пылях силикатов металлов в кислой среде в растворенное состояние переходят ионы SiO 3 2-, SiO 4 2- и другие ионы кремниевых кислот. Образующиеся кремнекислоты в водной среде диссоциируют и подвергаются реакции поликонденсации, вследствие чего их развитая поверхность приобретает отрицательный заряд.
СаSiO 3 + 2H+ → Ca2+ + H 2 SiO 3 ↓
H 2 SiO 3 ↔ Н+ + HSiO 3 -
Са 2 SiO 4 + 4H+ → 2Ca2+ + H 4 SiO 4 ↓
H O O HH
Si
H O OH
- 2H 2 O
H O OH
Si
H O O HH
H 4 SiO4 + ↔ Н+ + HSiO 4 3-
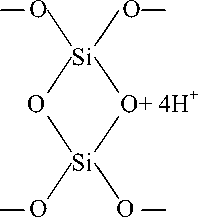
Коллоидные частицы поликислоты, благодаря своему поверхностному заряду, притягивают к себе ионы и дипольные молекулы и обратимо связывают их, поэтому этот процесс можно приравнять к действию ионитов.
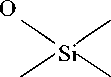
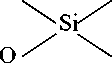
Fe2+, Zn2+ [FeOH]+, [ZnOH]+
Fe3+, [FeOH]2+
[Fe(OH) 2 ]+
H
H
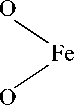
H O Fe
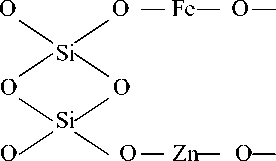
Выводы: принципы геоники позволяют успешно использовать закономерности геологических и геохимических процессов в практике водоочистки.
Список литературы Использование принципов геоники в практике водоочистки
- Состояние окружающей природной среды Белгородской области в 2011 году. -Белгород: Росприроднадзор, 2012. 132 с.
- Климентов, П.П. Общая гидрогеология/П.П. Климентов, Г.Я. Богданов. -М.: Недра, 1977. 357 с.
- Минеральные воды [Электронный ресурс]. -2012. -Режим доступа: http://мвж.рф.
- Михайлов, В.Н. Гидрология/В.Н. Михайлов, А.Д. Добровольский, С.А. Добролюбов. -М.: Высш. шк., 2007. 463 с.
- Лесовик, В.С. Геоника. Предмет и задачи. -Белгород: Изд-во БГТУ, 2012. 213 с.
- Лесовик, В.С. Генетические основы энергосбережения в промышленности строительных материалов//Изв. Вузов. Строительство. 1994. № 7, 8. С. 96-100.
- Кирюшина, Н.Ю. Шлаковые отходы в водоочистке/Н.Ю. Кирюшина, Г.И. Тарасова, С.В. Свергузова//Вестник БГТУ им. В.Г. Шухова. 2010. № 4. С. 140-145.
- Лупандина, Н.С. Использование производственных отходов для очистки сточных вод/Н.С. Лупандина, Н.Ю. Кирюшина, Ж.А. Свергузова, Д.А. Ельников//Экология и промышленность России. 2010. Май. С. 38-41.
- Свергузова, С.В. Использование отходов сталеплавильной промышленности и ГОКов для очистки сточных вод/С.В. Свергузова, Н.Ю. Кирюшина, О.В. Лашина//Вузовская наука -региону: материалы 6-й Всероссийской научно-технической конференции. -Вологда, 2008. Т. II. С. 438-441.


