Исследование аминокислотного состава кормовой добавки методом ионообменной хроматографии
Автор: Волнин А.А., Мишуров А.В., Михина А.А., Коротаева А.А., Севко А.В.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Пищевая биотехнология
Статья в выпуске: 1 (75), 2018 года.
Бесплатный доступ
Определение содержания аминокислот в кормах для сельскохозяйственных животных имеет большую научно-практическую значимость. Это необходимо для более точной детализации норм кормления и балансирования рационов животных по содержанию аминокислот и белка, а, следовательно, способствует повышению продуктивности животных. В данной работе рассмотрены вопросы применения ионообменной хроматографии с постколоночной дериватизацией проб нингидрином для исследования аминокислотного состава кормов для сельскохозяйственных животных. Определено общее содержание аминокислот (кроме триптофана) в кормовой добавке. Концентрация треонина составила 3,26 г/100г протеина, лейцина – 6,43, изолейцина – 3,24, валина – 4,77, метионина – 2,18, лизина – 2,90, фенилаланина – 3,16, гистидина – 2,03, тирозина – 2,33, суммы аспарагина и аспарагиновой кислоты – 6,76, серина – 3,97, суммы глутамина и глутаминовой кислоты – 12,04, глицина – 6,00, аланина – 6,71, аргинина – 6,93, пролина – 3,08, суммы цистина и цистеина – 1,38. Выполнена оценка полноценности добавки по содержанию незаменимых аминокислот в сравнении с референтным белком ФАО/ВОЗ и определены лимитирующие аминокислоты. Аминокислотный скор треонина составил 81,5%, лейцина – 91,9%, изолейцина – 81%, валина – 95,4%, лизина – 52,7%, суммы фенилаланина и тирозина – 91,5%, суммы метионина и цистеина – 101,7%. Определено соотношение незаменимых и заменимых аминокислот: 0,57. Установлена относительно низкая биологическая ценность (относительно референтного белка ФАО/ВОЗ) исследованной кормовой добавки по содержанию незаменимых аминокислот. Данная добавка может быть использована в кормлении сельскохозяйственных животных в комплексе с другими кормовыми компонентами, содержащими свободные аминокислоты и / или белки, в составе рациона, сбалансированного по содержанию незаменимых аминокислот.
Аминокислоты, ионообменная хроматография, аминокислотный скор, постколоночная дериватизация, кормовая добавка
Короткий адрес: https://sciup.org/140229959
IDR: 140229959 | DOI: 10.20914/2310-1202-2018-1-199-205
Determination of feedstuff amino acids composition by ion-exchange chromatography
Determination of animal feeds amino acids composition is the very important part of agricultural sciences and livestock management. This is necessary for normalization and balanced of farm animal’s diets parameters. Advances in husbandry techniques are making in response to the needs for rearing high genetic merit livestock. The nutrition of livestock has a critical role in these developments and is an element which needs to be continually updated as new scientific information becomes available. This article is devoted to the use of ion-exchange chromatography with post-colum derivatization by ninhydrin in the study of the amino acid composition and evaluation of the biological value of livestock feedstuff components. The amino acid composition (except tryptophan) of the livestock feed-stuff component is presented for threonine – 3.26 g/100g of protein, leucine – 6.43, isoleucine – 3.24, valine – 4.77, methionine – 2.18, lysine – 2.90, phenylalanine – 3.16, histidine – 2.03, tyrosine – 2.33, sum of asparagine and aspartate – 6.76, serine – 3.97, sum of glutamine and glutamic acid – 12.04, glycine – 6.00, alanine – 6.71, arginine – 6.93, proline – 3.08, sum of cystine and cysteine – 1.38. Biological value of feedstuff component compared with the "ideal" protein (FAO WHO) is estimated, limiting amino acids were found. The amino acid score was calculated: for threonine – 81.5%, leucine – 91.9%, isoleucine – 81%, valine – 95.4%, lysine – 52.7%, phenylalanine and tyrosine sum – 91.5%, methionine and cysteine sum – 101.7%. Feedstuff component had a low level of essential amino acids in compare with "ideal" protein (FAO WHO). Feedstuff component can be used for livestock nutrition as a component of essential amino-acid balanced diet.
Текст научной статьи Исследование аминокислотного состава кормовой добавки методом ионообменной хроматографии
Повышение потребности населения в продуктах питания является основным стимулом развития отрасли животноводства. При этом одной из тенденций является повышение продуктивности сельскохозяйственных животных за счет использования молекулярно-генетических методов селекции в сочетании с оптимизацией условий содержания, обеспечивающей наиболее полную реализацию высокого генетического потенциала животных. Повышение эффективности кормления является одним из решающих факторов в этой системе. Кормление животных в настоящее время динамично развивается благодаря поступлению новых экспериментальных данных о составе и качестве кормов и их конверсии в организме животных [1–3, 18, 19].
Аминокислоты являются одними из ключевых компонентов питания животных, как в составе белковой диеты, так и в качестве дополняющих продуктов [1, 4]. Считается, что белок не является питательным веществом. Животные нуждаются в аминокислотах, а не в белке как таковом. Качество кормового белка определяется его потенциалом для покрытия физиологических требований в отношении аминокислот на поддержание жизнедеятельности и продуктивность (рост, воспроизводство, моло-кообразование и т. д.). Потребность в кормовом белке зависит от вида животных, возраста, генотипа и пола. Отсюда следует, что существуют два важных фактора, определяющих качество белка, а) профиль аминокислот, который представляет собой соотношение незаменимых аминокислот в белке и b) их усвояемость [1]. В рационе животных возможен недостаток одной или нескольких незаменимых аминокислот, необходимых для поддержания оптимального роста и здоровья [1, 4]. Исследование аминокислотного состава кормов имеет крайне важную роль в оптимизации систем кормления, детализации и нормировании рационов сельскохозяйственных животных [5-7].
Наиболее распространенными методами количественного аминокислотного анализа являются высокоэффективная жидкостная хроматография (ВЭЖХ) и ионообменная хроматография с постколоночной дериватизацией проб нингидрином. Однако в практике рутинного анализа, при значительном количестве исследуемых проб метод ионообменной хроматографии имеет ряд существенных преимуществ по сравнению с ВЭЖХ: более высокая точность определения, воспроизводимость результата и надежность (высокая производительность этого метода является следствием того, что большинство загрязнений быстро перемещаться по колонке и выходят из системы, прежде чем начинается разделение аминокислот), а также более простая подготовка проб (по сравнению с методами предколоночной дериватизации) [8–14].
Метод ионообменной хроматографии с постколоночной дериватизацией проб нингидрином стандартизирован Международной организацией по стандартизации (EN ISO 13903), а также Регламентом Европейской Комиссии № 152/2009; рекомендован к использованию для анализа аминокислотного состава сырья и кормов, а также контроля полноценности аминокислотного питания животных Европейской федерацией производителей кормовых добавок и кормов для животных (FEFANA, фр. Fédération Européenne des Fabricants d’Adjuvants pour la Nutrition Animale) [1].
В данной работе рассмотрены вопросы применения ионообменной хроматографии с постколоночной дериватизацией проб нингидрином для исследования аминокислотного состава кормов для сельскохозяйственных животных. Определено общее содержание аминокислот (кроме триптофана) в кормовой добавке на основе продуктов переработки отходов мясной промышленности, выполнена оценка полноценности добавки по содержанию незаменимых аминокислот в сравнении с референтным белком ФАО/ВОЗ и определены лимитирующие аминокислоты.
Материалы и методы
Для подготовки проб использовали кислотный гидролиз в растворе 6 М соляной кислоты, с добавлением норлейцина в качестве внутреннего стандарта. Гидролиз выполняли в термостате при 110 °С в течении 24 ч. Для определения цистина и метионина пробы окисляли 50% раствором надмуравьиной кислоты, которую предварительно готовили из муравьиной кислоты и перекиси водорода, с добавлением фенола.
Определение содержания сырого протеина выполняли методом Кьельдаля [15].
Для расчёта аминокислотного скора белка аминокислотный скор каждой незаменимой аминокислоты в «идеальном» референтном белке ФАО/ВОЗ [16] принимали за 100%, а в исследуемом – определяли процент соответствия. Если значение скора для определенной аминокислоты ниже 100%, данную аминокислоту определяли как лимитирующую.
Результаты и обсуждение
Метод ионообменной хроматографии с постколоночной дериватизацией работает на основе того факта, что аминокислоты являются катионами при рН 2,2, удерживаются ионообменной смолой колонки и при элюировании градиентом с повышением рН смываются с нее согласно изоэлектрическим точкам молекул. На выходе с колонки разделившиеся аминокислоты вступают в специфическую реакцию с нингидрином, при высокой температуре, с образованием окрашенного продукта, который количественно определяют используя фотометрическое детектирование при 440 нм – для пролина и 570 нм – для всех других аминокислот [1, 10, 12].
Анализ аминокислот проводят после кислотного гидролиза белков (кроме триптофана). Для более полного нахождения метионина и цистеина (с димером последнего – цистином), кислотный гидролиз проводят с предварительно окисленными (количественно) серосодержащими радикалами аминокислотных остатков. В результате образуются соответствующие продукты окисления – метионинсульфон и цистеиновая кислота. Данный метод позволяет определить 17 протеиногенных аминокислот (за исключением триптофана, разрушающегося при кислотном гидролизе, аспарагина и глутамина, которые гидролизуются в аспарагиновую и глутаминовую кислоты, соответственно). Сумма определяемых аминокислот включает свободные аминокислоты и аминокислоты, которые были связанные в составе белка до гидролиза [12]. Схема аминокислотного анализатора представлена на рисунке 1.
В исследуемой кормовой добавке было установлено содержание сырого протеина: 18,29%. Было определено содержание незаменимых и заменимых аминокислот. Аминокислотный состав кормовой добавки представлен в таблице 1.
Был рассчитан аминокислотный скор, соотношение незаменимых и заменимых аминокислот и определены лимитирующие аминокислоты. Результаты исследования представлены в таблице 2.
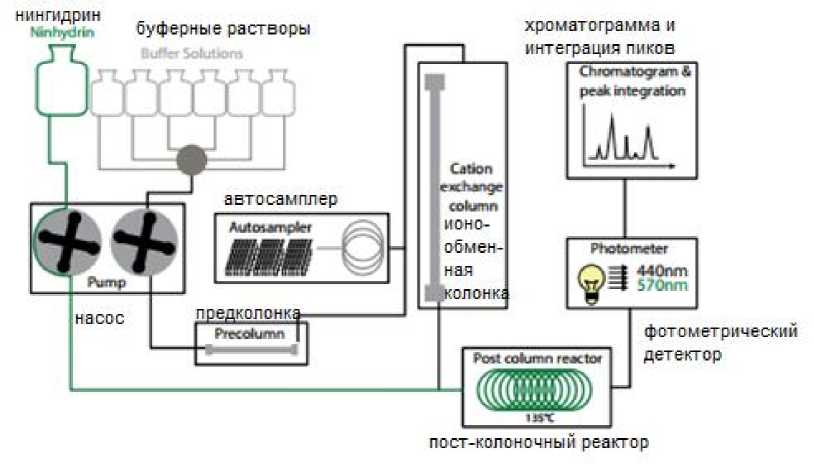
Рисунок 1. Общая схема аминокислотного анализатора [1]
Figure 1. The General scheme of amino acid analyzer [1]
Таблица 1.
Аминокислотный состав кормовой добавки, г/100 г. протеина
Amino acid composition of feed additive, g/100 g of protein
Table 1.
Незаменимые аминокислоты | Essential amino acids
|
THR |
LEU |
ILE |
VAL |
MET |
LYS |
PHE |
HIS |
|
|
3,26 |
6,43 |
3,24 |
4,77 |
2,18 |
2,90 |
3,16 |
2,03 |
|
|
Заменимые аминокислоты | Non-essential amino acids |
||||||||
|
TYR |
ASP |
SER |
GLU |
GLY |
ALA |
ARG |
PRO |
CYS |
|
2,33 |
6,76 |
3,97 |
12,04 |
6,00 |
6,71 |
6,93 |
3,08 |
1,38 |
Таблица 2.
Аминокислотный скор и соотношение незаменимых и заменимых аминокислот
Amino acid score and ratio of essential and non-essential amino acids
Table 2.
|
«Идеальный белок» ФАО/ВОЗ | «Ideal protein FAO/WHO»[9] |
Незамени- |
||||||
|
THR |
LEU |
ILE |
VAL |
MET 1 CYS |
LYS |
PHE 1 TYR |
мые/заменимые |
|
4 |
7 |
4 |
5 |
3,5 |
5,5 |
6 |
essential/non-es- |
|
Аминокислотный скор | Amino acid score, % |
sential |
||||||
|
81,5* |
91,9* |
81,0* |
95,4* |
101,7 |
52,7* |
91,5* |
0,57 |
* – лимитирующая аминокислота
Исходя из результатов очевидно, что исследуемая кормовая добавка наименее полноценна по содержанию лизина, скор этой аминокислоты составил 52,7%. Среди основных протеиногенных аминокислот, лизин является одной из ключевых незаменимых аминокислот [1]. Лизин необходим для синтеза гемоглобина и нуклеопротеидов [17].
Аминокислотный скор изолейцина, лейцина и валина составил 81; 91,9 и 95,4% соответственно. Изолейцин, лейцин и валин являются аминокислотами, имеющими разветвленные алифатические цепи в радикалах. Их метаболизм интересен тем, что данные аминокислоты имеют общие пути катаболизма и, следовательно, могут создавать помехи друг другу при усвоении. Лейцин является сильным регулятором катаболизма аминокислот с разветвленной цепью, поэтому избыток лейцина в рационе нежелателен для животных [1, 3–4]. Лейцин и изолейцин обладают сильно выраженным кетогенным свойством. Валин связан с обменом холестерола, каротиноидов, метилмасляных кислот, служит источником образования гликогена и кофермента А [17]. Аргинин является незаменимым для молодых животных [1]. Установлено, что кормовая добавка содержит аргинин в количестве 6,93 г./100г протеина. Аргинин, превращаясь в орнитин (орнитиновый цикл, совокупность процессов образования мочевины), участвует в обезвреживании конечных продуктов азотистого обмена (аммиак), связан с функцией паращитовидных желез, служит источником образования креатина и креатинина, играя важную роль в энергетическом обмене [17]. Аминокислотный скор треонина составил 81,5%. Треонин, превращаясь в глицин, используется для синтеза протопорфирина, холестерола, жирных кислот и углеводов. В обмене веществ он тесно связан с лейцином и является антагонистом метионина и серина [17]. Аминокислотный скор суммы фенилаланина и тирозина составил 91,5%. Фенилаланин и тирозин являются «взаимо-превращаемыми» аминокислотами, имеющиеся данные показывают, что тирозин может частично обеспечить потребность в фенилаланине и наоборот [1]. Фенилаланин и тирозин служат источником образования в организме таких гормонов как тироксин, адреналин и норадреналин, а также пигментов меланинов. Нарушение обмена этих аминокислот сопровождается тяжелыми расстройствами общего обмена веществ, приводящими не только к снижению продуктивности, но и к гибели животных [17].
В представленной добавке аминокислотный скор более 100% был установлен лишь у суммы метионина и цистеина. Метионин участвует в ряде важных биосинтетических процессов, участвуя в обмене холина, креатина и адреналина через высвобождение метильной группы [1, 17]. Метионин является первой аминокислотой, встраивающейся в рибосомы при биосинтезе полипептидных цепей белков в клетках [10]. В настоящее время гистидин рассматривается как незаменимая аминокислота [1]. Установленное содержание гистидина в исследованной кормовой добавке составило 2,03 г./100г протеина. Гистидин необходим для синтеза гемоглобина, входит в состав карнозина и ансерина, содержащихся в мышцах. При декарбоксилировании гистидина образуется гистамин, являющийся физиологически активным соединением [17].
Полученные результаты свидетельствуют об относительно низкой биологической ценности (относительно референтного белка ФАО/ВОЗ) исследованной кормовой добавки по содержанию незаменимых аминокислот. Данная добавка может быть использована в кормлении сельскохозяйственных животных в комплексе с другими кормовыми компонентами, содержащими свободные аминокислоты и/или белки, в составе рациона, сбалансированного по содержанию незаменимых аминокислот.
Заключение
Исследование аминокислотного состава кормовых компонентов имеет важное значение в рационализации норм кормления сельскохозяйственных животных и балансировании рационов. В данной работе выполнен анализ
Список литературы Исследование аминокислотного состава кормовой добавки методом ионообменной хроматографии
- Dalibard P., Hess V., Tutour L., Peisker M. et al. Amino Acids in Animal Nutrition//FEFANA Publication, FEFANA. Brussels, 2014.
- Эрнст Л.К., Зиновьева Н.А. Биологические проблемы животноводства в XXI веке. М., 2008.
- D’Mello J.P. Felix Amino acids in animal nutrition, Second Edition//CABI Publishing. 2003
- Karau A, Grayson I. Amino acids in human and animal nutrition//AdvBiochemEngBiotechnol. 2014. № 143. Р. 189-228 DOI: 10.1007/10_2014_269
- de Sousa Prado J.P., Oliveira Cavalheiro J.M., da Silva J.A., Cavalheiro T.B. et al. Amino acid profile and percent composition of meals and feeds used in shrimp farming//Gaia Scientia. 2016. № 10,4. Р. 347-360.
- Purwin C., Fija?kowska M., Lipi?ski K., Wierzbowska J. et al. Changes in amino acid composition during ensiling lucerne and red clover in round bales//J. Elem. 2015. № 20.4. P. 965-973. doi: 10.5601/jelem.2015.20.1.863.
- Adejumo I. O., Adetunji C. O., Ogundipe K., Osademe S. N. Chemical composition and amino acid profile of differently processed feather meal//Journal of Agricultural Sciences, 2016. № 61,3. P. 237-246 DOI: 10.2298/JAS1603237A
- Ween O., Stangeland J.K., Fylling T.S., Aas G.H. Nutritional and functional properties of fishmeal produced from fresh by-products of cod (Gadus morhua L.) and saithe (Pollachius virens)//Heliyon. 2017. № 3, 7 DOI: 10.1016/j.heliyon.2017.e00343
- Silvao C.F., Nunes A.J.P. Effect of dietary amino acid composition from proteins alternative to fishmeal on the growth of juveniles of the common snook, Centropomus undecimalis//R. Bras. Zootec. 2017. № l.46. Р. 7
- Шапошников М.Н., Севко А.В., Севко Д.А., Волнин А.А. и др. Анализ аминокислотного состава молока коров симментальской породы//Ветеринария, зоотехния и биотехнология. 2015. № 11. С. 70-75
- Volnin A.A., Sheraliev F.D., Shaposhnikov M.N., Zaitsev S.Y. et al. Amino acid score of milk proteins of the interspecific hybrids of argali and domestic sheeps//RJOAS. 2017. № 4,64. P. 240-247. 10.18551/RJOAS.2017-04.31 DOI: 10.18551/rjoas.2017–04.31
- Волнин А.А., Шералиев Ф.Д., Шапошников М.Н., Зайцев С.Ю. и др. Применение ионообменной хроматографии при оценке биологической ценности белков молока овец//Актуальные вопросы биологической физики и химии. 2017. № 1, 2. C./494-498./
- Jaji? I., Krstovi? S., Glamo?i? D., Jak?i? S. et al. Validation of an HPLC method for the determination of amino acids in feed//J. Serb. Chem. Soc. 2013. № 78, 6. P. 839-850.
- Dai Z, Wu Z, Jia S, Wu G Analysis of amino acid composition in proteins of animal tissues and foods as pre-column o-phthaldialdehyde derivatives by HPLC with fluorescence detection//J Chromatogr B AnalytTechnol Biomed Life Sci. 2014. № 27. Р. 964, 116. DOI: 10.1016/j.jchromb.2014.03.025
- ISO 5983-1:2005 Feeds, mixed feeds and raw material. Determination of mass fraction of nitrogen and calculation of mass fraction of crude protein. Part 1. Kjeldahl method
- FAO. Energy and protein requirements. Report of a Joint FAO/WHO/UNU Expert Consultation. Geneva: World Health Organization, 1985. 112 p.
- Алиев А.А. Обмен веществ у жвачных животных. М.: НИЦ «Инженер», 1997
- Дерканосова А. А., Коротаева А. А. Особенности российского рынка комбикормов и перспективы его развития//Экономика. Инновации. Управление качеством. 2013. № 3. С. 107.
- Дерканосова А.А. Анализ перспективы производства отечественных кормовых препаратов//Вестник Воронежского государственного университета инженерных технологий. 2012. № 2. С. 194-196.


