Исследование биоэлектрической активности мозга и характера сердечной деятельности при подавлении нистагма в процессе периодического светового воздействия
Автор: Усанова Татьяна Борисовна, Николенко Владимир Николаевич, Скрипаль Анатолий Владимирович
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Глазные болезни
Статья в выпуске: 1 т.7, 2011 года.
Бесплатный доступ
В работе приведены результаты исследования биоэлектрической активности мозга и характера сердечной деятельности пациентов с нистагмом глаз, при одновременной регистрации нистагмограмм, электроэнцефалограмм и электрокардиограмм. Показано, что при периодическом воздействии света на глаза пациента наблюдается взаимосвязанное уменьшение амплитуд спектральных составляющих спектров мощности электроэнцефалограмм и электрокардиограмм
Нистагм, офтальмология, спектральный анализ, электрокардиография, электроэнцефалография
Короткий адрес: https://sciup.org/14917220
IDR: 14917220
Текст научной статьи Исследование биоэлектрической активности мозга и характера сердечной деятельности при подавлении нистагма в процессе периодического светового воздействия
1Введение. Известно, что патологический нистагм (непроизвольные колебания движения глаз) может возникнуть при поражении вестибулярного аппарата, патологическом процессе в мозжечке, воспалительном процессе внутреннего уха, черепно-мозговой травме, инфекционных и токсических поражениях мозга, а также может быть следствием патологии зрительно-нервного анализатора [1-3].
В работах [4, 5] было показано, что периодическое световое воздействие способно изменять для ряда больных с нистагмом амплитуду и частоту колебательных движений в сторону уменьшения их амплитуды или полного исчезновения нистагма. При этом не обсуждались возможности взаимосвязи изменений функционирования других подсистем организма в момент подавления нистагма.
Представляет, в частности, интерес попытка исследовать взаимосвязь изменений биоэлектрической активности головного мозга и характера сердечной деятельности в момент подавления непроизвольных движений глаз.
Методы. В состав аппаратного комплекса входили: видеокамера ( 3 ), регистрирующая угловое смещение
Адрес: 410012, Саратов, ул. Астраханская, 83, СГУ, кафедра медицинской физики.
Тел.: (8452) 511430.
обоих глаз в орбите пациента ( 1 ), электроэнцефалограф ( 4 ) и электрокардиограф ( 5 ) (рис. 1), оцифрованные сигналы с которых вводились в компьютер ( 5 ). Голову пациента фиксировали в держателе, а с двух сторон от глаз обследуемого на расстоянии 50 см под углом 45˚ от линии взора (по горизонтали к нормалям глазных яблок) устанавливали два источника света ( 6 ) (60-ваттные лампы накаливания), которые выступали в роли раздражителя зрительной системы. Питание к лампам ( 6 ) от источника питания ( 8 ) подводилось с помощью электронного ключа ( 9 ) таким образом, чтобы в зависимости от положения электронного ключа загоралась попеременно то одна, то другая лампа. Ключ управлялся генератором импульсов ( 7 ), частоту следования которых можно было менять в пределах от 0,5 до 10 Гц с шагом 0,5 Гц.
Видеоизображение движущихся зрачков анализировалось с применением компьютерной программы VideoOculograph [6]. Одновременно с регистрацией видеоокулограммы происходила запись электрической активности коры головного мозга скальповыми электродами 21-канального электроэнцефалографа «Нейрон-Спектр-5», расположенными согласно стандартной методике по биполярной схеме [7, 8], и электрокардиограммы компьютерным электрокардиографом «Полиспектр 8/12», разработанным фирмой «Нейрософт» (г. Иваново). Электроэнцефало-
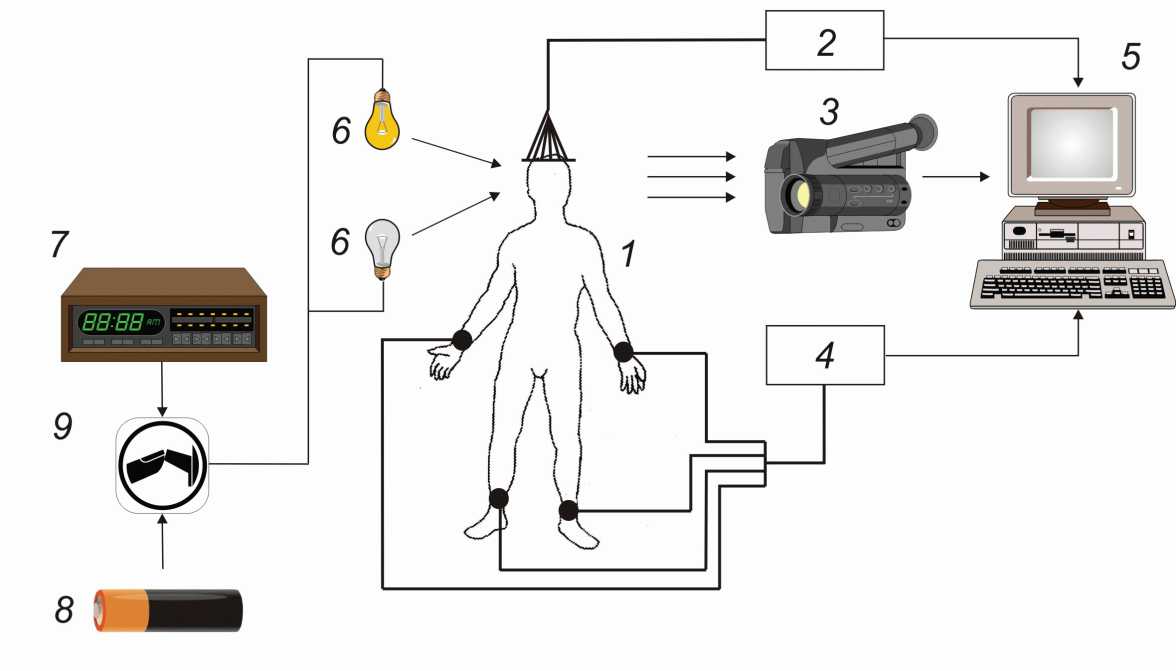
Рис. 1. Схема установки: 1 – пациент, 2 – электроэнцефалограф, 3 – цифровая видеокамера, 4 – электрокардиограф, 5 – персональный компьютер, 6 – лампы накаливания, 7 – задающий генератор импульсов с регулируемой частотой, 8 – источник питания, 9 – электронный ключ
граф и электрокардиограф подключались к одному компьютеру, что позволяло одновременно следить за процессом изменения нистагма, происходящего в результате воздействия на пациента периодически изменяющимся световым сигналом, и за параметрами электроэнцефалограммы (ЭЭГ) и электрокардиограммы (ЭКГ).
Результаты. Влияние световой модуляции на спектры ЭЭГ. В начале проведения исследований осуществляли запись электроэнцефалограммы (ЭЭГ) в покое, для этого пациент располагался на стуле в расслабленном состоянии в тихой затемненной комнате, чтобы исключить тем самым воздействие внешних артефактов.
На рис. 2 представлены спектры мощности S записи скальповой ЭЭГ с электрода O2-A2 при периодической световой стимуляции с частотой 3 Гц
(рис. 2 а) и 5 Гц (рис. 2 б). На приведенных электроэнцефалограммах отчетливо наблюдаются пики на частоте световой стимуляции. Относительная мощность этих спектральных компонент варьировалась в зависимости от локализации электродов: наибольшая мощность наблюдалась в затылочной доле и уменьшалась по мере приближения к лобной доле. Такая зависимость связана с тем, что именно в затылочной доле располагаются зрительные центры [4], и наиболее интенсивный отклик фиксируется именно в этих центрах. Подобные результаты наблюдались как у здоровых людей, добровольно участвовавших в эксперименте, так и у пациентов с нистагмом.
Каждый эксперимент представлял собой непрерывную серию из следующих этапов: отсутствие стимуляции, периодическая стимуляция (с подбором параметров светового воздействия до подавления
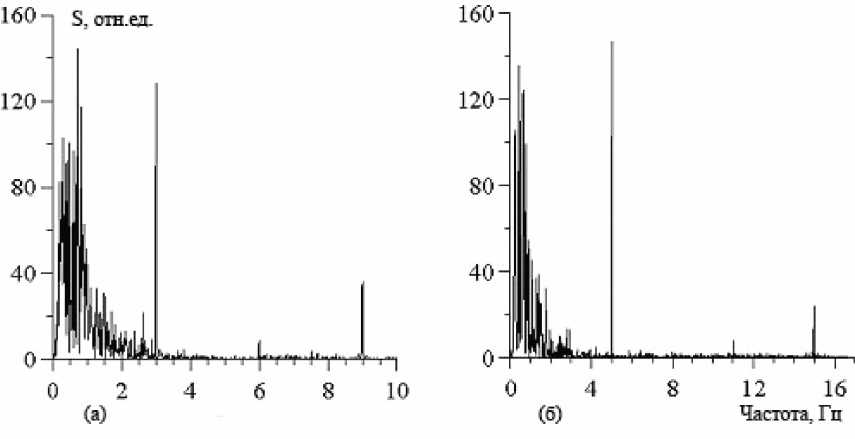
Рис. 2. Спектры мощности записи скальповой ЭЭГ с электрода O2-A2 при периодической световой стимуляции с частотой 3 Гц (а) и 5 Гц (б)
нистагма), прекращение стимуляции. В отсутствие стимуляции по нистагмограмме определялась частота нистагма и измерялась характерная для этого состояния ЭЭГ. При периодическом световом воздействии по нистагмограмме определялись параметры светового воздействия, при которых амплитуда нистагма значительно уменьшалась вплоть до полного подавления. После прекращения светового воздействия определялось отличие параметров нистагма от аналогичных до и после воздействия и соответствующее изменение спектра мощности ЭЭГ.
У пациента К. (12 лет) наблюдался нерегулярный маятникообразный нистагм с амплитудой 2 мм и частотой ~3 Гц. На рис. 3 и 4 приведены соответственно спектры мощности нистагмограммы пациента и электроэнцефалограммы с электрода О2-А2 в спокойном состоянии (а), при периодическом световом воздействии с частотой 3 Гц (б), 5 Гц (в) и после воздействия (г).
Нрегулярное движение глаз при нистагме и соответственно широкий спектр мощности имелись вблизи частоты 3,2 Гц (рис. 3 а).
При световом воздействии на пациента с частотой ~3 Гц движения глаз пациента становились более регулярными (рис. 3 б): спектральная составляющая на 3 Гц имела большую амплитуду по сравнению с аналогичной до светового воздействия, при этом подавления нистагма еще не наблюдалось. В спектре мощности ЭЭГ в окрестности частоты 3 Гц отмечался размытый максимум.
При увеличении частоты следования световых импульсов до 5 Гц у пациента наблюдалась остановка нистагма, о чем можно судить по спектру мощности нистагмограммы (рис. 3 в). В спектре мощности ЭЭГ появлялся ярко выраженный пик на частоте 5 Гц при значительном подавлении гармоник спектра на других частотах (рис. 4 в).
После прекращения светового воздействия у пациента некоторое время нистагм не восстанавливался (рис. 3 г). Спектр мощности ЭЭГ (рис. 4 г) при этом отличался от случая отсутствия светового воздействия наличием выраженных спектральных компонент на отдельных частотах с существенно меньшими, чем при нистагме, амплитудами.
Пациенту Г. (11 лет) был поставлен диагноз: «Нистагм, частичная атрофия зрительного нерва» (рис. 5: сверху спектр мощности нистагмограммы, а снизу ЭЭГ одного из отведений). На рис. 5 и 6 приведены соответственно спектры мощности нистагмограммы пациента Г. и электроэнцефалограммы с электрода О2-А2 в спокойном состоянии (а), при периодическом световом воздействии с частотой 5 Гц (б), 7 Гц (в) и 3 Гц (в) в той последовательности, в которой на пациента воздействовали.
В спектре нистагмограммы (рис. 5 а) прослеживается «собственная частота нистагма» около 2 Гц.
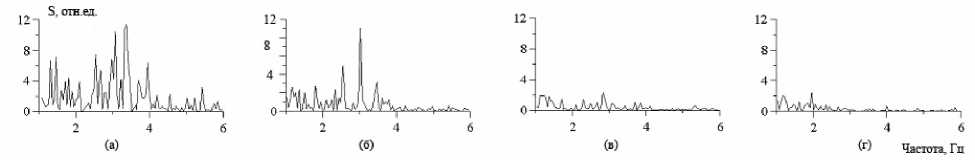
Рис 3. Спектры мощности нистагмограммы в спокойном состоянии (а), при периодической световой стимуляции с частотой 3 Гц (б), 5 Гц (в) и после стимуляции (г)
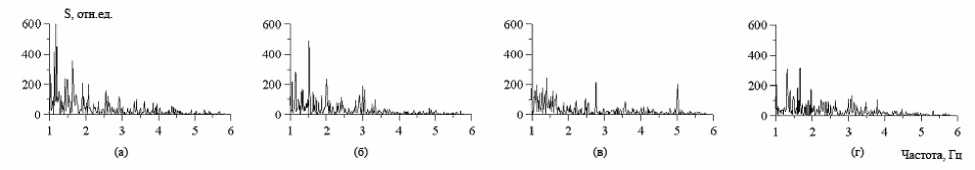
Рис 4. Спектры мощности записи ЭЭГ с электрода О2-А2 в спокойном состоянии (а); при периодической световой стимуляции с частотой 3 Гц (б); 5 Гц (в) и после стимуляции (г)
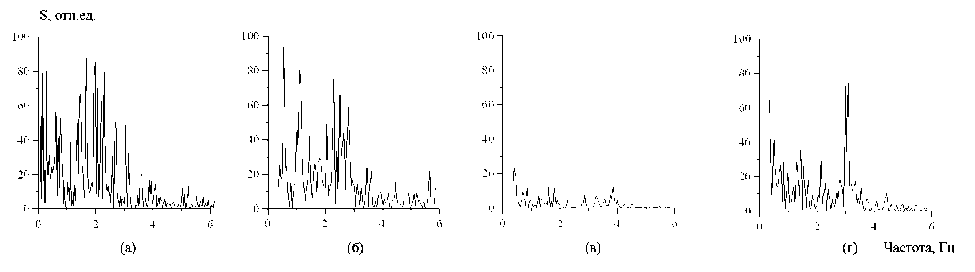
Рис. 5. Спектры мощности нистагмограммы: в спокойном состоянии (а); при периодической световой стимуляции с частотой 5 Гц (б); при периодической световой стимуляции с частотой 7 Гц (в); при периодической световой стимуляции с частотой 3 Гц (г)
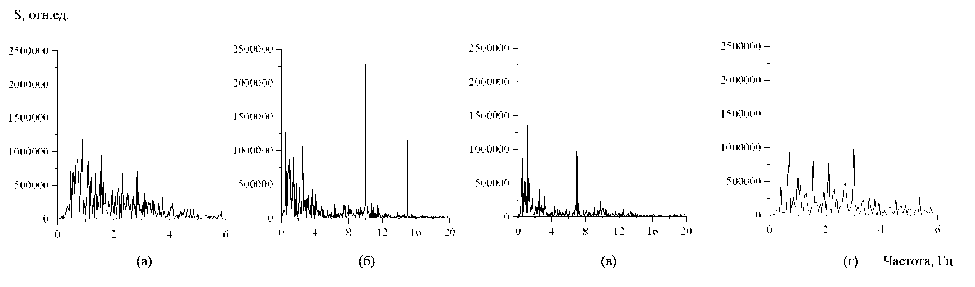
Рис. 6. Электроэнцефалограмма одного из отведений: в спокойном состоянии (а); при периодической световой стимуляции с частотой 5 Гц (б); при периодической световой стимуляции с частотой 7 Гц (в); при периодической световой стимуляции с частотой 3 Гц (г)
При периодическом световом воздействии с частотой 5 Гц уменьшения амплитуды нистагма не происходило (рис. 5 б) и в спектре мощности ЭЭГ на этой частоте не наблюдалось пика мощности (рис. 6 б).
При увеличении периодического светового воздействия до частоты 7 Гц наблюдалось уменьшение всех составляющих спектра нистагмограммы, что соответствовало случаю подавления нистагма (рис. 5 в). В спектре ЭЭГ в это время наблюдается значительное подавление всех спектральных составляющих, за исключением гармоники с частотой, равной частоте светового воздействия 7 Гц (рис. 6 в).
При уменьшении частоты периодического светового воздействия до значения ~3 Гц у пациента наблюдалось восстановление нистагма на частоте светового воздействия (рис. 5 г). В спектре мощности ЭЭГ появлялись спектральные составляющие в широком диапазоне значений с несколькими ярко выраженными пиками (рис. 6 г), но так же, как и в предыдущем случае, с уменьшенными амплитудами по сравнению с состоянием до светового воздействия.
Изменение характера сердечной деятельности при подавлении нистагма. Исследования проводились на шести пациентах одной возрастной группы от 7 до 14 лет с нистагмом, при их добровольном согласии. Фиксировались также параметры для пациентов без нистагма – контрольная группа.
Одновременно с регистрацией нистагмограммы происходила запись электрокардиограммы. На рис. 7 представлены ЭКГ до и в момент светового
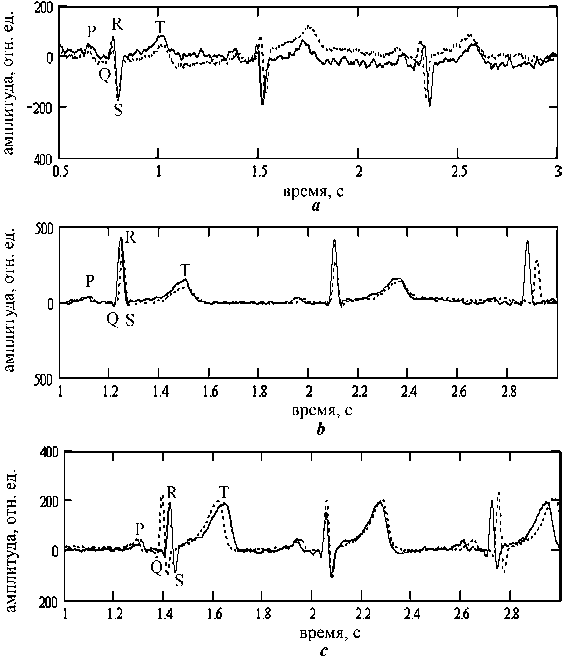
Рис. 7. Сигнал ЭКГ для трех пациентов до и во время светового воздействия (сплошная кривая – ЭКГ до воздействия, пунктирная – во время воздействия с частотой, близкой к частоте нистагма):
а – пациент А. 17 лет; b – пациент Д. 6 лет; с – пациент Л. 5 лет
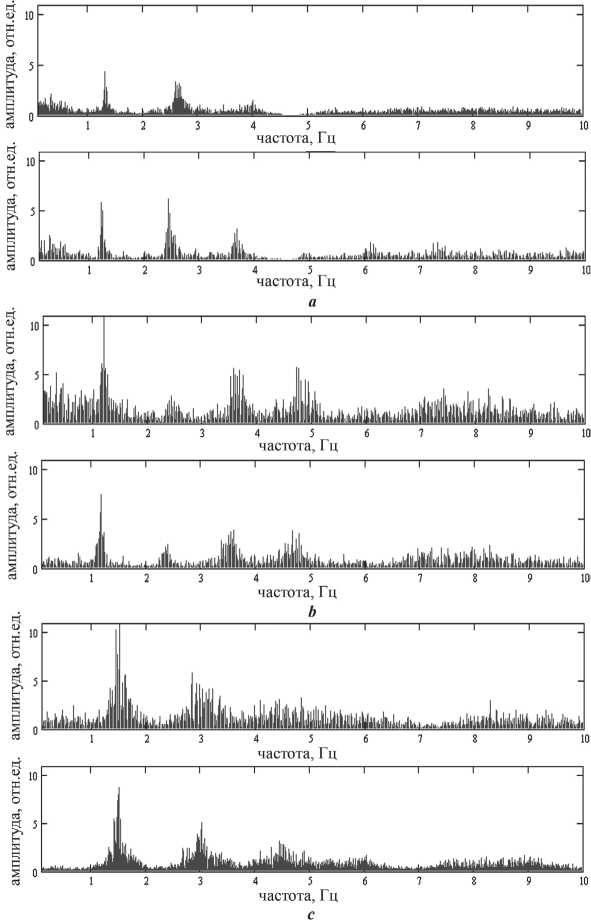
Рис. 8. Спектр ЭКГ для трех пациентов а – А., в – Д., с – Л.: верхний график – пациент в покое, нижний – во время светового воздействия
воздействия на пациентов с нистагмом, приводящего к изменению характеристик нистагма.
Как видно из рис. 7, форма электрокардиограммы, зафиксированной для пациента во время светового воздействия, несколько отличается от аналогичной ЭКГ в «нормальных» (без светового воздействия) условиях. В частности, у пациентов А. и Д. (соответственно ЭКГ рис. 7 а и b ) R-R-кардиоинтервалы значительно больше отличаются друг от друга по величине во время светового воздействия, чем R-R-кардиоинтервалы без светового воздействия. У пациентов Д. и Л. (соответственно ЭКГ рис. 7 b и с ) задержка между P- и Q-максимумами во время светового воздействия становится больше, чем эта же задержка без светового воздействия. Изменяется также форма самого кардиосигнала, что свидетельствует об измененном характере формирования электрических биопотенциалов в сердечной мышце.
Поскольку изменяется форма кардиосигнала до и во время воздействия света, интересно определить характер изменения спектра ЭКГ во время воздей- ствия, который для трех пациентов А., Д. и Л. (соответственно спектр ЭКГ рис. 8 а, b и с) представлен на рис 8. Из данного рисунка следует, что во время светового воздействия, приводящего к уменьшению амплитуды нистагма, наблюдается существенное уменьшение амплитуды шумовой составляющей спектра.
Для регистрации активности нервной вегетативной регуляции, проявляющейся в изменении показателей хронотропной структуры сердечного ритма, т.е. в изменении R-R-интервалов, определялись индексы Баевского [9, 10] до и во время светового воздействия. В таблице представлены усредненные индексы Баевского для пациентов с нистагмом и без него.
В таблице использованы следующие обозначения:
-
1) М, с – математическое ожидание (М), которое отражает конечный результат всех регуляторных влияний на сердце и систему кровоснабжения в целом. Этот показатель связан со средней частотой сердечных сокращений (ЧСС) и обладает наименьшей изменчивостью среди всех медико-статических
Индексы Баевского при воздействии света
Параметр
До воздействия, пациенты
Во время воздействия, пациенты
с нистагмом
без нистагма
с нистагмом
без нистагма
ЧСС, уд./мин
80
58
74
64
М, с
0,756
1,03
0,813
0,981
М0, с
0,766
1,03
0,817
0,968
АМо, %
40,7
39,3
55,6
27,1
ВР, с
0,243
0,334
0,135
0,947
ИВР, у.е.
167
118
412
28,6
ПАПР, у.е.
53,1
38,2
68
28
ВПР, у.е.
5,36
2,91
9,06
1,09
ИН, у.е.
109
57,2
252
14,8
показателей, и его отклонение от индивидуальной нормы обычно сигнализирует об увеличении нагрузки на аппарат кровообращения или о наличии патологических отклонений;
-
2) мода (М0) – наиболее часто встречающееся значение R-R-интервалов, указывающее на доминирующий уровень функционирования синусового узла. При симпатикотонии М0 меньше, при вагото-нии – больше;
-
3) вариационный размах (ВР), который вычисляется как разница между максимальным и минимальным значениями R-R. Он отражает степень вариабельности или размах колебаний значений кардиоинтервалов;
-
4) амплитуда моды (АМ0) – число кардиоинтервалов (в %), соответствующих диапазону моды, отражающее меру мобилизирующего влияния симпатического отдела;
-
5) индекс вегетативного равновесия (ИВР), который указывает на соотношение между активностью симпатического и парасимпатического отделов;
-
6) показатель адекватности процессов регуляции (ПАПР), который отражает соответствие между активностью симпатического отдела ВНС и ведущим уровнем функционирования синусового узла;
-
7) вегетативный показатель ритма (ВПР), который позволяет судить о парасимпатических сдвигах вегетативного баланса. Чем меньше ВПР, тем больше вегетативный баланс смещен в парасимпатическую сторону;
-
8) индекс напряжения (ИН) регуляторных систем, который отражает степень централизации управления сердечным ритмом.
Из таблицы следует, что при подавлении нистагма во время периодического светового воздействия средняя частота сердечных сокращений (ЧСС, уда-ров/минуту) у пациентов с нистагмом уменьшается, в то время как у пациентов контрольной группы частота в этих же условиях увеличивается. Изменение индекса М до и во время воздействия для пациентов без нистагма составило 0,049, а для пациентов с нистагмом 0,051, что может свидетельствать об увеличении нагрузки на регуляторный аппарат. Индекс М0 при периодическом световом воздействии для пациентов без нистагма уменьшается, а с нистагмом увеличивается, что позволяет говорить об активации симпатической нервной системы. Другие индексы, например АМ0, ВР, ИВР, ПАПР, ВПР, также свидетельствуют о смещении вегетативного баланса в симпатическую сторону для пациентов c нистагмом, для пациентов без нистагма – в парасимпатическую.
Обсуждение. Сравнение спектров мощности электроэнцефалограмм и электрокардиограмм свидетельствует о синхронном их поведении во время подавления нистагма, выражающемся в уменьшении амплитуд спектральных составляющих. При подавлении нистагма глаз, регистрируемом по уменьшению амплитуды спектральных составляющих нистагмограммы, в спектре мощности электроэнцефалограммы появляются ярко выраженные гармонические составляющие на частоте светового воздействия при одновременном уменьшении амплитуд остальных составляющих спектра, а в спектре мощности электрокардиограммы уменьшаются шумовые составляющие и изменяется длительность R-R-интервалов сердечного ритма, свидетельствующая об увеличении уровня тонуса симпатической нервной системы в регуляции сердечной активности.
Заключение. Таким образом, установлено, что при подавлении нистагма глаз наблюдается взаимосвязанное уменьшение амплитуд спектральных составляющих спектров мощности электроэнцефалограмм и электрокардиограмм.
Список литературы Исследование биоэлектрической активности мозга и характера сердечной деятельности при подавлении нистагма в процессе периодического светового воздействия
- Аветисов Э.С. Нистагм. М.: ГЭОТАР-МЕД, 2001. 96 с.
- Гиппенрейтер Ю.Б. Движения человеческого глаза. М.: Изд-во Моск. ун-та., 1978. 256 с.
- Филин В.А. Автоматия саккад. М: Изд-во МГУ, 2002. 240 с.
- Устойчивость эффекта уменьшения амплитуды нистагма у детей при периодическом световом воздействии/Т.П. Кащенко, Д.А. Усанов, И.Э. Рабичев [и др.]//Вестник офтальмологии. 2008. № 3. С. 46-47.
- Изменения параметров колебательных движений глазного яблока в результате периодического светового воздействия при сложном характере нистагма/Д.А. Усанов, Т.П. Кащенко, Ан.В. Скрипаль [и др.]//Известия высших учебных заведений. Прикладная нелинейная динамика. 2007. Т. 15, № 6. С. 45-56.
- Свидетельство о государственной регистрации программы для ЭВМ А.с. № 2008613235 «Компьютерная видеодиагностика параметров движений глаз «VideoOculograph»/Д.А. Усанов, Ал.В. Скрипаль, Ан.В. Скрипаль, А.В. Абрамов. заявл. 2008.
- Пенфилд В., Эриксон Т. Эпилепсия и мозговая локализация. М.: Медгиз, 1949. 451 с.
- Звенков Л.Р. Клиническая электроэнцефалография (с элементами эпилептологии). Таганрог: Изд-во ТРГУ 1996. 358 с.
- Анализ вариабельности ритма сердца в клинической практике/О.В. Коркушко, А.В. Писарук, В.Б. Шатило [и др.]. Киев, 2002. 192 с.
- Баевский РМ, Кириллов О.И., Клецкин С.З. Математический анализ изменений сердечного ритма при стрессе. М.: Наука, 1984.221 с.


