Исследование фазового перехода жидкость-кристалл в растворе KNO3 с использованием рамановской спектроскопии
Автор: Кряжев А.А., Камашев Д.В.
Журнал: Вестник геонаук @vestnik-geo
Рубрика: Научные статьи
Статья в выпуске: 6 (282), 2018 года.
Бесплатный доступ
С помощью рамановской спектроскопии исследуется фазовый переход жидкость-кристалл, метастабильная область в районе точки насыщения и предкристаллизационные кластеры в водно-солевом растворе KNO3. Показано существование довольно широкой метастабильной области раствора при изменении температуры, а сдвиги и уширения линий на рамановских спектрах связаны с наличием кластерных ассоциаций при фазовом переходе жидкость-кристалл.
Рамановская спектроскопия растворов, фазовый переход, предкристаллизационные кластеры
Короткий адрес: https://sciup.org/149128712
IDR: 149128712 | УДК: 544.344.01, | DOI: 10.19110/2221-1381-2018-6-25-29
Study of liquid-crystal phase transformation in KNO3 solution by Raman spectroscopy
Liquid-crystal phase transformation, metastable area around saturation point and precrystallization clusters in water-salt KNO3 solution are investigated by Raman spectroscopy. We presented the existence of a quite wide solution metastable area in case of the temperature change, and also line shifts and broadenings in the Raman spectra are related to the presence of cluster associations during liquid-crystal phase transformation.
Текст научной статьи Исследование фазового перехода жидкость-кристалл в растворе KNO3 с использованием рамановской спектроскопии
В настоящее время рамановская спектроскопия или спектроскопия комбинационного рассеяния (КР) света является мощным инструментом для исследования различных веществ. Свое широкое распространение она получила благодаря возможности неразрушающего изучения разнообразных объектов в различных агрегатных состояниях. КР спектроскопия с успехом используется в геологии и минералогии, геммологии, биологии и медицине, криминалистике, а также в различных отраслях промышленности.
Цель данной работы заключалась в исследовании фазового перехода жидкость—кристалл, определении метастабильной области в районе точки насыщения и выявлении предкристаллизационных кластеров в водно-солевом растворе в рамках кватаронной концепции самоорганизации вещества [1].
В качестве модельного объекта использовался основной раствор KNO 3 как чистый, так и смешанный с дополнительным раствором NaCl в пропорции 1:1. Выбор данных веществ обусловлен появлением мощных дополнительных пиков на спектре основного раствора в области от 500 см-1 до 1500 см-1, связанных с валентными колебаниями аниона NO3- и отсутствием полос в этой области у дополнительного раствора. В качестве растворителя использовалась дистиллированная вода.
Схема эксперимента
В данной работе все спектры комбинационного рассеяния света были получены при использовании модернизированного спектрометра ДФС-24 фирмы ЛОМО. Несмотря на некоторые недостатки, он обладает качественной оптической частью и, соответственно, высоким разрешением, не уступающим современ ным приборам и идеально подходит для исследования жидкостей. Используемый спектрометр представлял собой двойной монохроматор со сложением дисперсии. Диспергирующими элементами служили две одинаковые дифракционные решетки-реплики, с числом штрихов 1200 на 1 мм, вследствие чего вдвое увеличивалась линейная дисперсия и повышалась чистота спектра. На входе спектрометра устанавливалась осветительная система, предназначенная для работы с жидкими образцами. Геометрия осветительной системы позволяла установить дополнительное оборудование рядом с исследуемыми объектами.
Оптико-кинематическая схема спектрометра обеспечивала практически равномерную развертку спектра по длинам волн с точностью <0.01 нм. Для калибровки счетчика длин волн использовалась зеленая линия спектра ртутной лампы низкого давления с длиной волны 546.074 нм. С целью устранения эффекта нелинейности отсчета длин волн и повышения точности дополнительно вводились калибровочные поправки по нескольким известным длинам волн ртутной лампы. При использовании зеленого лазера такими точками калибровки служили линии ртути с длинами волн 531.669 нм, 567.586 нм, 607.264 нм. Результатом являлась калибровочная функция, с помощью которой рассчитывалась поправка для необходимого интервала длин волн.
В качестве источника возбуждающего излучения использовался зеленый полупроводниковый лазер 532 нм мощностью 50 мВт, обладающий полушириной спектральной линии <0.1 нм. Для подавления некогерентного излучения лазер проходил через три ирисовые диафрагмы, установленные до исследуемого образца. После прохождения диафрагм излучение лазера фокусировалось на исследуемом объекте. При исследовании 25
жидкостей в луч лазера вводилась кювета с вертикальным капилляром объемом 0.04 мл. Так же, непосредственно на кювету был приклеен цифровой термодатчик DS18B20, а на основание установлен автоматический PID регулируемый нагревательный элемент. Это позволяло поддерживать необходимую температуру исследуемой жидкости в интервале от комнатной до 80 °C с точностью < 0.1°С. Оптическая схема представлена на рис. 1.
Затем, рассеянное от образца излучение собиралось оптическими элементами и фокусировалось на входной щели первого монохроматора, далее проходя через центральную и выходную щели второго монохроматора. На выходе спектрометра установлен фотоэлектронный умножитель (ФЭУ), сигнал с которого через усилитель регистрировался с помощью ЭВМ. От качества источника возбуждающего излучения, ширины щелей и скорости сканирования зависит разрешение спектрометра. Оно может достигать <1 см-1 при использовании одномодовых, одночастотных лазеров, малых скоростей сканирования и точной юстировке.
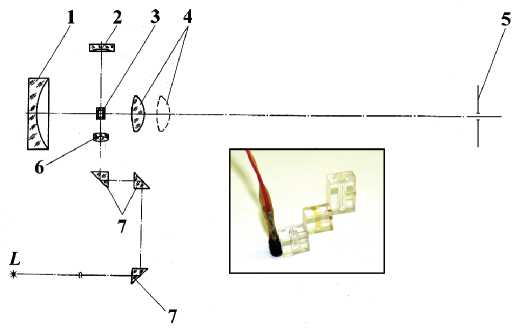
Рис. 1. Оптическая схема съемки КР спектра для жидкостей. 1, 2 — вогнутые отражатели, 3 — кювета с жидкостью, 4 — фокусирующая на щель линза, 5 — входная щель, 6 — фокусирующая на объект линза, 7 — 90° призмы ввода лазера, L — лазер
Fig. 1. Optical scheme for Raman spectroscopy of liquids. 1, 2 — concave reflectors, 3 — basin with liquid, 4 — slit focusing lens, 5 — entrance slit, 6 — object focusing lens, 7 — laser input 90° prisms, L — laser
Экспериментальные результаты и их обсуждение
Перед выбором модельного объекта дополнительно были исследованы различные жидкости: дистиллированная вода, растворы солей, водный раствор аммиака, спирты, тетраэтоксисилан (ТЭОС) и др. для оценки влияния компонент и температуры растворов на общий вид спектров. Так КР спектр дистиллированной воды, полученный при температуре T = 21.7°С, состоит из нескольких хорошо разрешимых пиков. Основными из них являются: деформационная полоса с максимумом около 1640 см-1, ассоциативная полоса с максимумом около 2130 см-1 и валентная полоса OH-групп с максимумом около 3420 см-1 [2, 3]. Дальнейшее увеличение температуры приводит к незначительному сдвигу и изменению формы валентной полосы, что связано с ослаблением водородных связей и увеличением частоты симметричных валентных колебаний [3].
Растворение в воде различных солей может значительно менять КР спектр. Например, NaCl слабо влияет на общую форму спектра, в то время как NaNO3 вызывает появление мощных дополнительных пиков в области от 500 до 1500 см-1, обусловленных валентными колебаниями аниона NO3-. В области валентных колебаний воды простой катион Na + оказывает такое же слабое влияние, как и в случае с NaCl. В растворе аммиака сложный катион NH 4+ , наоборот, оказывает влияние именно в области валентных колебаний воды. Если растворить соединение, состоящее из двух сложных ионов, то значительно изменятся обе области валентных колебаний.
Органические жидкости обычно имеют сложный КР спектр, состоящий из множества колебательных полос. Так, например, в спектре этилового спирта содержатся полосы деформационных колебаний групп C-C-О, валентных колебаний C-C и C-O, других видов колебаний молекул спирта, а также наиболее интенсивные полосы валентных симметричных колебаний CH2, валентных симметричных и асимметричных колебаний CH3 и небольшую валентную полосу OH-группы. Добавление воды в спирт приводит к сильному перераспределению интенсивности полос CH и OH-групп в спектре, благодаря чему можно определять концентрацию спирта с высокой точностью [4]. КР спектры различных спиртов сильно отличаются друг от друга, что дает возможность идентифицировать даже изомеры. Например, изопропиловый спирт имеет сложный спектр, на котором отдельно выделяется самый мощный пик С-С-С, при этом спектр его изомера — пропанола сильно отличается, обладая одинаковым с ним химическим составом.
После анализа спектров различных жидкостей в качестве модельного объекта для исследования фазового перехода жидкость—кристалл был выбран водный раствор KNO3. Необходимо было оценить влияние изменения температуры на форму линий в спектре модельного объекта и его исходных веществ, чтобы выяснить, связанны ли эти изменения только с температурой или с процессом кристаллизации. Так же, в качестве примеси, вводился дополнительный раствор NaCl, чтобы определить влияние “чужих” ионов на форму спектра.
Основной раствор KNO3 подготавливался путем взвешивания перекристаллизованной ХЧ соли и разбавлением в воде таким образом, чтобы точка его насыщения соответствовала температуре 20 и 40 °С. Затем соль полностью растворялась в дистиллированной воде при температуре ~ 80 °С. Аналогично подготавливался и дополнительный раствор NaCl, точка его насыщения соответствовала T = 20 °С. Подготовленные растворы вводились в кювету через шприцевой фильтр с диаметром пор 0.2 pm для фильтрации от возможных грубых загрязнений, при этом кювета и растворы предварительно нагревались до температуры ~ 80 °С чтобы избежать кристаллизации в процессе ввода. Измерения проводились при охлаждении одно- и двухкомпонентного растворов и их исходных веществ в интервале температур от ~ 60 до ~ 23 °С, с шагом ~ 10 °С по 5-ти различным значениям температуры в массиве (рис. 2).
Спектр кристаллического KNO3 состоит из трех основных пиков, главным из которых является пик 1049 см-1, причем перекристаллизация значительно улучшает качество исходного вещества. Для приготов-
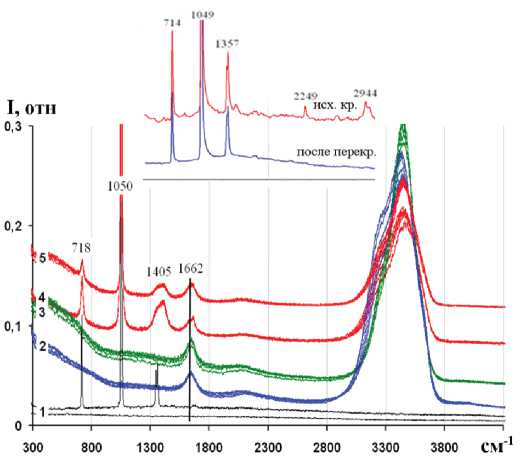
Рис. 2. КР спектры исходных веществ. 1 — кристаллические NaCl, KNO 3 ; 2 — H2O, 3 — раствор NaCl, 4 — раствор KNO3, 5 — смесь 1:1 растворов NaCl и KNO3. Температура растворов: T ~ 23, 30, 40, 50, 61 °C. На врезке спектры KNO3 до и после перекристаллизации.
Fig. 2. Raman spectra of initial substances. 1 — NaCl, KNO3 crystals; 2 — H2O, 3 — NaCl solution, 4 — KNO3 solution, 5 — 1:1 proportion mix of NaCl and KNO3 solutions. Solutions temperature: T ~ 23, 30, 40, 50, 61 °C. Picture insert is KNO3 spectra before and after recrystallization.
ления исследуемого раствора использовалась именно перекристаллизованная соль. На КР спектре кристаллического NaCl вообще отсутствуют пики в исследуемом интервале длин волн. Изменение температуры от ~ 24 до ~ 61 °C не влияет на КР спектры дистиллированной воды, кроме незначительного сдвига и изменения формы валентной полосы OH-групп в районе 3420 см-1. Спектры растворов NaCl и KNO3, точка насыщения которых соответствовала 20 °C, также практически не меняются с ростом температуры. При смешивании основного раствора KNO 3 с точкой насыщения 40 °C и дополнительного раствора NaCl в пропорции 1:1, произошел сдвиг точки насыщения основного раствора и процесс кристаллизации не был достигнут даже при температуре ниже 30 °C. В итоге, изменение температуры и присутствие простых примесных ионов NaCl никак не отразилось на наиболее интересной области спектра 500 ^ 1500 см-1 основного раствора.
После получения спектров исходных веществ и оценки температурного вклада был подготовлен следующий раствор KNO3 с точкой насыщения 40 °C. Измерения проводились при его охлаждении в интервале температур 56.7 ^ 18.5 °C с шагом ~ 5 °C до появления кристаллов внутри кюветы, что свидетельствовало о фазовом переходе, который привел к существенному изменению формы и сдвигу полос КР спектра. Была снята серия спектров для следующих температур (°C): 56.7 50.5, 45.6, 40, 35.1, 30.8, 21.8, 18.5; при этом спектры разделились на два основных массива (рис. 3). Cначала раствор находился в недосыщенном, а потом в пересыщенном состоянии до температуры 30.8 °C. Фазовый переход жидкость-кристалл происходил при дальнейшем понижении температуры и сопровождался сдвигами в область высоких частот и сужением основных пиков.
На спектрах имеют место незначительные внутри-массивные сдвиги OH полос, связанные с изменением температуры. Пик 1662 см-1 не меняет свое положение, т.к. он не относится к аниону NO 3 -. Основной пик аниона NO 3- (1050 см-1) имеет ярко выраженную асимметрию, что говорит о наличии нескольких компонент в его составе, которые могут характеризоваться присутствием разупорядоченных (ионы) и упорядоченных (кластеры) ассоциаций [5]. Пик 1405 см-1 претерпевает значительные изменения в процессе фазового перехода. При температуре 30.8 °C его форма представляет собой слияние «кристаллической» и «некристаллической» компонент, что свидетельствует о наличии кластерных образований в растворе (рис. 4). Валентная полоса OH-групп воды значительно сдвигается при переходе к точке насыщения, что связанно с их освобождением из-за агрегации вещества (рис. 5).
Особый интерес представляет основной пик 1050 см-1, который был снят отдельно в высоком разрешении, т. к. на его положение не влияет изменение температуры раствора. При температуре 50 и 60 °C пик обладает хорошей симметрией. Cнижение темпера-
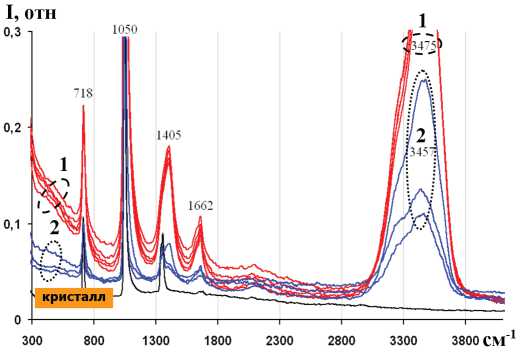
Рис. 3. КР спектры водного раствора KNO3 (насыщение при T = 40 °C). Температура: 1 — T = 56.7 ^ 35.1 °C, 2 — T = 30.8 ^ 18.5 °C
Fig. 3. Raman spectra of KNO3 water solution (saturation at T = = 40 °C). Temperature: 1 — T = 56.7 ^ 35.1 °C, 2 — T = 30.8 ^ 18.5 °C
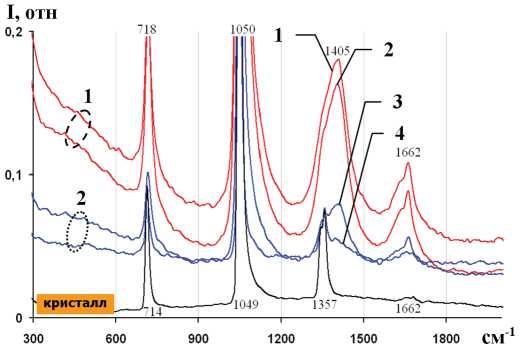
Рис. 4. КР спектры водного раствора KNO3 (область колебаний аниона NO3). Температура: 1 — T = 56.7 °C, 2 — T = 35.1 °C, 3 — T = 30.8 °C, 4 — T = 21.8 °C.
Fig. 4. Raman spectra of KNO3 water solution (NO3- anion fluctuation area). Temperature: 1 — T = 56.7 °C, 2 — T = 35.1 °C, 3 — T = 30.8 °C, 4 — T = 21.8 °C.
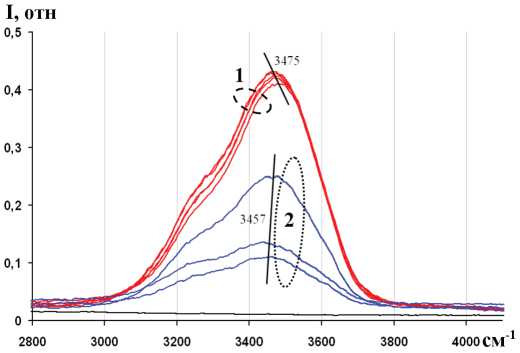
Рис. 5. КР спектры водного раствора KNO 3 (область колебаний OH-групп воды). Температура: 1 — T = 56.7 + 35.1 °C, 2 — T = 30.8 * 18.5 °C
Fig. 5. Raman spectra of KNO3 water solution (OH-groups fluctuation area). Temperature: 1 — T = 56.7 + 35.1 °C, 2 — T = 30.8 + 18.5 °C туры увеличивает асимметрию в сторону высоких частот, которая максимально проявляется в точке насыщения T = 40 °C (рис. 6). В каждом случае дополнительно контролировался источник возбуждающего излучения для соблюдения чистоты эксперимента.
Анализ показал наличие трех компонент в составе пика, которые относятся к колебаниям свободных, гидратированных и объединенных в кластеры ионов NO3-. При температуре превышающей точку насыщения раствора, симметрия пиков и их смещение в сторону низких частот OH-групп говорят о преобладании гидратированных и свободных ионов. При достижении точки насыщения увеличивается вклад высокочастотной компоненты, что свидетельствует об агрегации вещества в предкристаллизационные кластеры и, судя по скачку между массивами спектров, увеличении их количества. В метастабильной области, при дальнейшем понижении температуры наращивание кластеров идет незначительными темпами и увеличивается их размер, т. к. освобождаются OH-группы. После фазового перехода спектр представляет собой свертку спектров кристаллического вещества и насыщенного раствора, в котором так же есть кластеры.
Выводы
Таким образом, в исследуемом интервале температур происходят незначительные изменения деформационной, валентной и остальных полос воды, использовавшейся в качестве растворителя. Исследования также показали слабое влияние данного интервала температур на форму областей спектра как валентных колебаний аниона NO3-, так и OH-групп основного раствора KNO 3 , не испытывающего фазовый переход. Отсутствие уширений и сдвигов полос в спектрах одно- и двухкомпонентного растворов с минимальной точкой насыщения дает право утверждать, что наличие таких изменений в спектрах раствора, испытывающего фазовый переход, связаны не с влиянием температуры, а с наличием кластерных ассоциаций при фазовом переходе жидкость—кристалл. Полученные результаты показывают существование довольно широкой метастабильной области раствора KNO3, составляющей ~ 10 °C в диапазоне выбранных температур. В этой области будут проводиться дальнейшие исследования для определения не только наличия предкристаллизацион-ных кластеров, но и их физических параметров. Анализ основного пика раствора в высоком разрешении показал присутствие нескольких частотных компонент в его составе. Появление компоненты с более высокой частотой при увеличении насыщения раствора (за счет снижения температуры) можно объяснить нарастающей агрегацией вещества в предкристаллизационные кластеры.
Работа выполнена при использовании оборудования ЦКП «Геонаука» и финансовой поддержке программы РАН № 18-5-5-44.
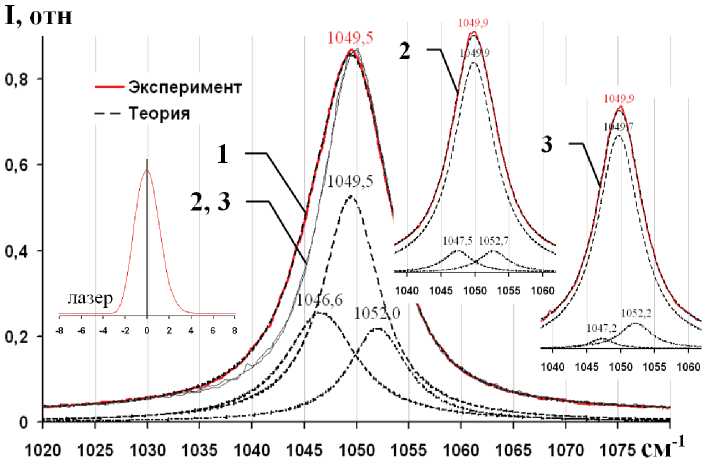
Рис. 6. КР спектры основного пика водного раствора KNO3 с раскладкой на три Лоренцевых компоненты (насыщение при T = 40 °C). На врезке симметричный основной пик возбуждающего лазера 532 нм. Температура: 1 — T = 40 °C, 2 — T = 50 °C, 3 — T = 60 °C.
Fig. 6. Main peak Raman spectra of KNO3 water solution with peak fitting by three Lorentz components (saturation at T = 40 °C). Picture insert is symmetric main laser peak 532 nm. Temperature: 1 — T = 40 °C, 2 — T = 50 °C, 3 — T = 60 °C.
Список литературы Исследование фазового перехода жидкость-кристалл в растворе KNO3 с использованием рамановской спектроскопии
- Асхабов A. M., Рязанов М. А. Кластеры «скрытой» фазы - кватароны и зародышеобразование // Докл. РАН, 1998. Т. 362. № 5. С. 630-633.
- Эйзенберг Д., Кауцман В. Структура и свойства воды. Л.: Гидрометеоиздат, 1975. 279 с.
- Буриков С. А., Доленко Т. А., Карпов Д. М. Вклад резонанса Ферми в формирование валентной полосы спектра комбинационного рассеяния воды // Оптика и спектроскопия, 2010. Т. 109. № 2. С. 306-312.
- Буриков С. А., Доленко Т. А., Пацаева С. В., Южаков В. И. Диагностика водно-этанольных растворов методом спектроскопии комбинационного рассеяния света // Оптика атмосферы и океана, 2009. № 11. С. 1082-1088.
- Rusli I. T., Schrader G. L., Larson M. A. Raman spectroscopic study of NaNO3 solution system - solute clustering in supersaturated solutions // Journal of Crystal Growth, 1989. V. 97. P. 345-351.


