Исследование и получение соединений карбоновых кислот из смол узгенских углей
Автор: Осекова Гулбара Арыновна, Ташполотов Ысламидин Ташполотович
Журнал: Бюллетень науки и практики @bulletennauki
Рубрика: Технические науки
Статья в выпуске: 1 т.7, 2021 года.
Бесплатный доступ
Получен ацетат натрия из карбоновых кислот угольной смолы бурого угля методом нейтрализации. Получен уксусноэтиловый эфир из карбоновых кислот смолы узгенского бурого угля, этерификационным способом и низкотемпературным перегонным методом. Исследованы избытки карбоновых кислот и азиотропных веществ, сделана повторная очистка и получен чистый уксусноэтиловый эфир при температуре 77-78 °С.
Карбоксил, карбонил, эфиры, вытяжка, кристаллизация, смола, бурый уголь
Короткий адрес: https://sciup.org/14117938
IDR: 14117938 | УДК: 662.668 | DOI: 10.33619/2414-2948/62/32
Research and obtaining compounds of carbonic acids from resins of Uzgen coals
In the article, sodium acetate was studied and obtained from carboxylic acids from coal tar of brown coal by the method of neutralization and drying and crystallization were made. Investigated and obtained ethyl acetate from carboxylic acids from the resin of Uzgen brown coal, by the esterification method and by the low-temperature distillation method. Excess carboxylic acids and azeotropic substances were checked, repeated purification was done, and pure ethyl acetate was obtained at a temperature of 77-78 °C.
Текст научной статьи Исследование и получение соединений карбоновых кислот из смол узгенских углей
Бюллетень науки и практики / Bulletin of Science and Practice
Известно, что из угля Сергеевского месторождения выделены две представительные группы органических кислот [1]. Первая — это карбоновые кислоты, содержащиеся в растворимой фракции угля (битумах). Вторая группа включает гуминовые кислоты, извлекаемые из остатка угольного вещества, нерастворимого в органических экстрагентах. Анализ группового состава свободных кислот свидетельствует о преимущественном значении насыщенных соединений нормального строения, более 50% которые приходится на карбоновые структуры С 8 –С 18 . Среди них преобладают кислоты, содержащие четное число углеродных атомов, однако доминирующую роль играет нечетный гомолог С 9 . В малых количествах присутствуют дикарбоновые кислоты изо-строения, ароматические соединения данной фракции представлены кислотами.
Выделение карбоновых кислот и других совместно полученных соединений проводим по методикам, описанным в работе [2]. Выделенную смесь карбоновых кислот растворяли в диэтиловом эфире (0,5–1,0 мл эфира на 1–2 мг смеси кислот) добавляем несколько капель метилового спирта и затем по каплям раствор диазометана, пока смесь не окрашивалось в желтый цвет. Смесь выдерживаем в течение 30 мин при комнатной температуре, после чего растворитель удаляем, пропуская через раствор окисления [3].
Смола узгенского угля отличается высоким содержанием воды. В смоле также содержится механические примеси. Определение содержание карбоновых кислот из смолы проводили по методике Стадникова.
Для определения карбоновых кислот эфирный раствор смолы переливали в делительную воронку емкостью 500 мл и туда же приливали 40–50 см3 NaHCO 3 . После чего смесь 3–4 раза не слишком энергично встряхивали и давали отстоять в течение 5 мин. Оставшихся нижний водный раствор натриевых солей органических кислот, сливали в колбу Эрленмейера емкостью 500 мл. Операцию извлечение карбоновых кислот повторяли 2 раза подобным же образом. Собранный от всех трех промывок содовой раствор экстрагировали серной кислотой. Эфирный слой возвращали в делительную воронку, а сам раствор осторожно обрабатывали 10% раствором серной кислоты. Промывали серным эфиром, отгоняли эфир на водяной бане.
Органические соединение, содержание в качестве функциональной группы карбоксил ♦ О с +
) носит название карбоновых кислот. В зависимости от характера радикала, с которым связана карбоксильная группа, различают кислоты предельные, непредельные, ароматические и др. По числу имеющихся в молекуле карбоновых групп их подразделяют на односновные, двухосновные и т. д.
Как в случае других функции, природа радикала, число и взаимное положение карбоксильных групп оказывают определенное влияние на свойства кислот, но все же они в первую очередь определяются функциональной группой [4].
о
—с
Рассматривая строение карбоксильной группы он можно увидеть, что формально оно является комбинацией двух уже рассмотренных функциональных групп-карбонильной и карбоксильной. Однако карбоксил не простая сумма двух упомянутых групп, это новая функция, со своими характерными свойствами, в которых ими отдаленно отражаются особенности «составных частей». Находясь в близком соседстве, группировки С=О и ОН друг на друга сильное взаимное влияние, общий характер которого можно предвидеть на основании того, что нам уже известно о группах С=О и О-Н.
Так становится понятной важнейшая химическая особенность соединений, содержащих карбоксильную функцию — проявление ими свойств кислот [5].
Экспериментальная часть
Для получения соединений карбоновых кислот, полученных из смол Узгенского угольного месторождения [2], предварительно сделали качественный и количественный анализ карбоновых кислот (уксусная кислота).
-
1. Качественный анализ
-
а) Взаимодействие растворимых карбоновых кислот с гидрокарбонатом натрия
приводит к выделению углекислого газа. Для этого берем 5 мл карбоновой кислоты, туда добавляем 0,5 г Na 2 CO 3 , бурно выделяется узгенский газ, на газовую трубку опускаем водный раствор гашенной извести, образуется мутный белый раствор.
-
1) Na 2 Co 3 +2HCOOH=2HCOONa+CO 2 ↑+H 2 O
-
2) Ca(OH) 2 +CO 2 =CaCO 3 + H 2 O
-
б) На карбоновые кислоты опускаем универсальный индикатор, который дает розовый цвет, лакмусовая бумага красный цвет, карбоновые кислоты обладают кислотными свойствами.
-
в) Карбоновые кислоты также можно определить путем идентификации по
-
2. Количественный анализ.
температуре. Для этого берем термостойкий стакан туда наливаем 50 мл карбоновой кислоты, ставим на плитку, который соединен терморегулятором ТКП-160-СЧ-М1, тогда увлажненный термометр показывает t пл — 16,75 °С, а температура кипения — t кип = 118 °С.
Для определения содержания карбоновых кислот титрование в неводных средах проводили с потенциометрическим методом с использованием в качестве индикаторного стеклянного электрода. В качестве электрода (для сравнения) применяли хлор серебряный электрод, и как электролитический мост, заполненный насыщенный раствор калия хлорида (это предотвращает попадание воды в титруемый раствор и возрастание электрического сопротивления моста в процессе титрования). Для эксперимента использовали универсальный pН метр ЭВ-74. Для проведения эксперимента сначала универсальный pН метр калибровали стандартными буферными раствором pН 1,65 и pН 9,18 при 20 °С температуре [6–7].
Для анализа берем 25 мл исследуемой пробы и титрируем раствором NaOH до значения pН 8,1, и записываем объем раствора, прошедший на титрование.
Обработка результатов
Сделаем расчет по следующей формуле:
V1 • C • M x=^
где V 1 — объем раствора гидроксида натрия прошедший на титрование, см3; С — точная концентрация раствора гидроксид натрия (NaOH) моль/дм3; V 0 — объем пробы образца взятый на титрование (как правило 25 см3) см3; М — Молярная масса г/моль равная для уксусной кислоты (М1/2 СН 3 СООН) = 60,50;
^ 1
V1 • C • M
V o
96^1,0^60,50
232,32 г\л
^ 2
98 • 1,0 • 60,50
= 237,16 г\л
^ 3
95^1,0^60,50
= 229,9 г\л
Хср = 233,11 г\л
1-й эксперимент. Получение ацетата натрия из карбоновых кислот.
В пробирку наливаем 0,5 мл из полученных карбоновых кислот [2] и добавляем 0,5 мл 10% раствора гидроксида натрия (NaOH), тогда происходит реакция нейтрализации с легким образованием солей, т. е. замена кислотного водорода на металл.
СНз-С^ +NaOH= СНз-С^ + Н2О ОН ONa
Полученный раствор сушили в водяной бане после этого сушили в сушильном шкафе при температуре 110 °С [8–9].
Карбоновая кислота и их соли применяются в медицине для консервирования продукт, и краски для текстильных изделий.
2-й эксперимент. Получение уксусно-этиловый эфир из карбоновых кислот из бурого угля Узгенского месторождения.
На колбу Вюрса с емкостью 100 мл наливаем 2,5 мл этиловый спирт. Добавляем 2,5 мл концентрированной серной кислоты (Н 2 SO 4 ) Хорошо перемешивают, колбу отпускают на водяную баню, закрепляют капельную воронку и соединяют водяной холодильник для перегонки низко кипящих жидкостей, и аллонжи и коническая колба для получения жидкостей. Водяная баня нагревают до 140 °С, через капельную воронку медленно капает 20 мл раствор этилового спирта и полученная карбоновая кислота [2] (1:1). Полученный жидкость (этиловый эфир) поступают на коническую колбу. Проверяем излишки карбоновой кислоты лакмусовой бумагой, добавляем раствор соды, чтобы получить чистый этиловый эфир, в водяной бане нагреваются при температуре 77–78 °С. Сделанный химический процесс называют реакцией этерификация.
СН3—сГ +СгН5ОН--2—^ СНзСГ +НгО он О—с2Н5
Уксусно-этиловый эфир применяются для получения мыла — синтетические моющие средства [9].
Для получения уксусно-этиловый эфир сделана следующая установка, представленная на Рисунке 1 и схема эксперимента — на Рисунке 2.
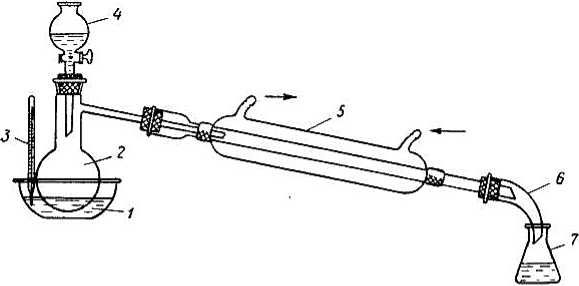
Рисунок 1. Лабораторная установка для получения уксусноэтилового эфира из карбоновых кислот: 1 — водяная баня, (электроплитка), 2 — колба Вюрца, водяная баня, 3 — термометр, 4 — капельная воронка, 5 — холодильник, 6 — аллонж, 7 — коническая колба.
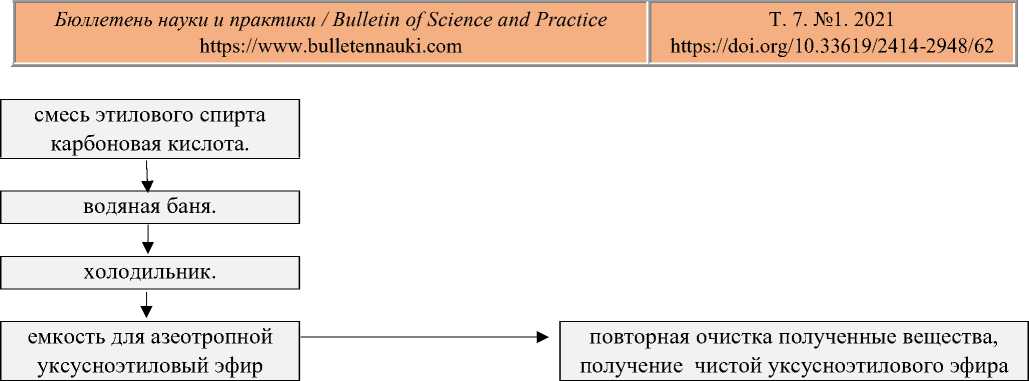
Рисунок 2. Технологическая схема получения уксусноэтилового эфира из карбоновых кислот.
Выводы:
-
1. Исследован и получен ацетат натрия из карбоновых кислот из угольной смолы Узгенского бурого угля, методом нейтрализации, сушили и получили кристаллы.
-
2. Выполнен качественный и количественный анализ по определению уксусной кислоты.
-
3. Получен уксусно-этиловый эфир из карбоновых кислот из смолы Узгенского бурого угля низкокипящим перегонным методом и экспериментально проверен избыток карбоновых кислот и азеотропных веществ. Выполнена повторная очистка полученных веществ и получен уксусноэтиловый эфир при температурном режиме 77–78 °С.
Список литературы Исследование и получение соединений карбоновых кислот из смол узгенских углей
- Носкова Л. П. Групповой состав кислот низкокалорийного угля // Фундаментальные исследования. 2015. №9-3. С. 497-501.
- Осекова Г. А., Ташполотов Ы. Т., Ысманов Э. М. Исследование содержания карбоновых кислот в смоле узгенского угля // Бюллетень науки и практики. 2019. Т. 5. №12. С. 242-245. DOI: 10.33619/2414-2948/49/28
- Рокосов Н. Н., Рокосов Ю. В. Карбонове кислоты в битумоидах сапропелитов // Химия твердого топлива. 2012. №4. С. 15-22.
- Ерыгев М. А. Кожевникова И. В. Особенности физико-химического исследования карбоновых кислот // Современные тенденции в науке и образовании. 2017. №4. С. 47-51.
- Смит М. Органическая химия. М., 2020. 458 с.
- Васильев В. П. Аналитическая химия. М.: Дрофа, 2002. 384 с.
- Цитович И. К. Аналитическая химия. М.: Высшая школа, 1985. 319 с.
- Понамарев С. В., Золотарев А. С., Сачинова Л. Г., Теренин В. И. Практикум по органической химии. М., 1999.
- Исраилов И., Хакимов Ю. Р. Практикум по органической химии для товароведов, Ташкент, 1983. 208 с.


