Исследование изотопного состава углерода 13С/12С засоленных почв Селенгинского среднегорья
Автор: Дамбаев В.Б., Давыдова Т.В.
Журнал: Природа Внутренней Азии @nature-inner-asia
Рубрика: Биология
Статья в выпуске: 2 (28), 2024 года.
Бесплатный доступ
С использованием методов изотопной масс-спектрометрии изучено влияние глюкозы на микробную деструкцию органического вещества засоленных почв Селенгинского среднегорья. Различия в изотопном составе глюкозы (513С -10,57 %о) и органического вещества (513С -26,55 %о) позволили рассчитать потоки диоксида углерода (СО2), образовавшиеся при их микробной деструкции в почве. Наибольшее количество выделившегося СО2 при внесении глюкозы в почву наблюдалось в первые 4 часа опыта, что в 12 раз больше, чем скорость деструкции органического вещества до внесения глюкозы. Наибольшее количество выделившейся углекислоты было отмечено в первые 4 часа опыта после внесения глюкозы в почву, а скорость минерализации органического вещества увеличилась 12 раз. Изотопный состав СО2 со значением -11,08 %о был отмечен при 8-часовой инкубации. 513С СО2 в проведенном опыте наследует 513С органических продуктов, используемых микроорганизмами в качестве субстратов. Различие в изотопном составе вносимой 513С экзогенной глюкозы и органического вещества может быть использовано как изотопная метка для определения происхождения СО2, образующейся при минерализации растительных остатков.
Органическое вещество, карбонаты, микробная деструкция, стабильные изотопы углерода (513с), со2
Короткий адрес: https://sciup.org/148330207
IDR: 148330207 | УДК: 579.26 | DOI: 10.18101/2542-0623-2024-2-6-12
Study of 13C/12C carbon isotopic composition in saline soils of the Selenga mid-mountain region
Using isotope mass spectrometry methods, we have studied the effect of glucose on microbial degradation of organic matter in saline soils of the Selenga mid-mountain region. Differences in the isotopic composition of glucose (513C -10,57%o) and organic matter (513C -26,55%) allowed us to calculate the fluxes of carbon dioxide (CO2) formed during their microbial degradation in soil. The highest amount of CO2 released was observed in the first 4 hours after application of glucose to the soil, which was 12 times higher than the rate of organic matter degradation before glucose application. The isotopic composition of CO2 with a value of -11.08% was observed at 8-hour incubation. In the experiment 513C CO2 inherits 513C of organic products used by microorganisms as substrates. The difference in the isotopic composition of exogenous glucose and organic matter contributed 513C can be used as an isotopic marker to determine the origin of CO2 produced during mineralization of plant residues.
Текст научной статьи Исследование изотопного состава углерода 13С/12С засоленных почв Селенгинского среднегорья
Почвенное плодородие является неотъемлемой частью цикла углерода, обеспечивающееся трансформацией органического вещества, так как органические соединения являются хранилищем энергии в наземных биомах [Song et al., 2017].
Важное значение для характеристики циклов углерода в биосфере имеет оценка потоков СО2 из почв. По активности СО2 в почвах можно судить о трансформации органического вещества [Шилова, 2014]. Оценка потоков углерода в почвенных системах проводится с использованием глюкозы как легко минерализуемого органического соединения, которое в природных условиях поступает в почву в составе корневых выделений [Yanardağ et al., 2017]. Внесение органических и минеральных веществ в почву оказывает определенное воздействие на микробиологические процессы [Зякун, Дилли, 2011]. Главное значение имеет почвенное органическое вещество, которое определяет состав и структуру микробных сообществ [Subedi et al., 2016; Wang et al., 2016].
В результате минерализации растительных остатков гетеротрофными микроорганизмами образуются углекислота, органические метаболиты и микробная биомасса с изотопным составом углерода δ13С использованных продуктов. Количество δ13С СО2, выделившейся из почвы в результате деструкции растительных остатков, было использовано для того, чтобы проследить минерализацию и других веществ, попадающих в почву.
Цель работы — влияние глюкозы на микробную деструкцию органических веществ и оценка продуцирования δ13С СО2 в засоленных почвах Селенгинского среднегорья.
Объекты и методы
Объектами исследования являлись прибрежные засоленные почвы озера Белое (51°32'86" с. ш. 107°02'53" в. д., высота 538 м над ур. м.).
Почвенные образцы были отобраны с верхнего слоя (0–20 см) почвы на участках Р1, Р2, Р3 на расстоянии 10 м друг от друга вверх по террасе на северовосточной оконечности озера Белое.
Содержание органического вещества в почве определяли методом мокрого сжигания [Воробьева, 1998]. Содержание карбонатов определяли по методу Хитрова [Хитров, 1984]. Продуцирование СО2 почвой определяли абсорбционным методом [Шарков, 1984].
Соотношение 13С/12С определяли на масс-спектрометре FINNIGAN Breath MAT Plus (ИБФМ РАН, г. Пущино).
Характеристики изотопного состава углерода анализируемых образцов представляли в виде величин δ13С (‰), которые рассчитывали согласно общепринятому выражению:
δ13С обр =((R обр /R ст )-1) × 1000 (‰)
где Rобр и Rст — отношения распространенности изотопов углерода [13С]/[12С] в образце и стандарте PDB [Slater, Preston, Weaver, 2001]. Знак «+» означает, что образец более обогащен тяжелым изотопом, чем стандарт, знак «-» — обеднен. Стандартная ошибка измерений изотопных характеристик ±0,2 ‰.
Материально-изотопный баланс для органического вещества (ОВ) и внесенной глюкозы (глю) в почву проводили, используя уравнение:
δ 13 СовQов+δ 13 СглюQглю
δ 13 С
(ов+глю)
(Q глю + Q ов ), (1)
где δ13Сов и δ13С(ов+глю) — содержание изотопа 13С в органическом веществе почвы до и после внесения глюкозы в почву;
δ13Сглю — изотопный состав углерода глюкозы; Qглю и Qов — количество органического вещества и глюкозы в почвенных образцах соответственно.
Используя (1), долю СО2 (F), которая образовалась при минерализации органического вещества после внесения глюкозы в почву, рассчитывали с помощью формулы (2):
F=(δ13С (ов+глю) -δ13С глю )/(δ13С глю -δ13С ов ), (2)
где δ13Сов и δ13С(ов+глю) отражают количество изотопа 13С в СО2, продуцируемое в почве до и после внесения глюкозы; δ13Сглю — изотопный состав углерода глюкозы.
Таким образом, разницу между количеством углерода СО2, продуцируемым при минерализации органического вещества в образцах почвы с глюкозой и в контроле, отнесенную к количеству СО2 в контроле (в процентах), использовали для оценки ПЭ глюкозы (3):
ПЭ=[ FС (ов+глю) -С ов )/С ов ]100 %, (3)
где С(глю+ов) — суммарное количество углерода СО2, образующееся при минерализации глюкозы и органического вещества в почве с глюкозой; FС(глю+ов) — количество углерода СО2, образующееся при минерализации органического вещества в почве с добавкой глюкозы и рассчитанное с учетом (2).
Результаты и их обсуждение
Содержание органического вещества в прибрежных засоленных почвах озера Белое невелико. В верхних 0–20 см изученных почв она варьировала в пределах 1,05–1,54 % воздушно-сухой навески. Значение рН водной вытяжки колебалось от 7,9 до 8,4 (табл. 1).
Таблица 1
Физико-химическая характеристика засоленных почв Селенгинского среднегорья
|
Ключевой участок |
Влажность, % |
рН |
Содержание карбонатов, % |
Содержание C орг , % |
|
Р1 |
6,5 |
8,4 |
0,17 |
1,13 |
|
Р2 |
6,3 |
7,9 |
1,2 |
1,05 |
|
Р3 |
12,5 |
8,2 |
12,4 |
1,54 |
Среднее значение δ13С органического вещества на участках Р1, Р2, Р3 составляло -26,55 ‰, что характерно для С3-растительности. Наименьшее количество карбонатов отмечено на участке Р1. Вверх по минитрансекту содержание карбонатов увеличивается. Наиболее обогащена карбонатами почва участка Р3, расположенная на вершине прибрежной террасы. С увеличением содержания карбонатов в почвах происходит утяжеление изотопного состава δ13Скарб — от -16,70 до -11,74 ‰ (табл. 2). р
Таблица 2
Изотопный состав углерода (δ13С) органического вещества и карбонатов
|
Ключевой участок |
Глубина, см |
δ 13С карб , ‰ |
δ 13С ОВ, ‰ |
Увлажнение почвы 60 %, δ 13С, ‰ |
|
Р1 |
0–20 |
-16,70 |
-26,19 |
-24,66 |
|
Р2 |
0–20 |
-13,76 |
-26,8 |
-22,97 |
|
Р3 |
0–20 |
-11,74 |
-26,66 |
-22,80 |
Изотопный состав δ13С почвенного СО2 составлял -23,47‰ и наследовал изотопный состав органического вещества почв -26,55‰. Фракционирование изотопов углерода при микробной деструкции органического вещества составляло 3,1 ‰. Вносимая в почву глюкоза 1,5 мг/г с изотопным составом δ13С -10,58 ‰ отличалась на 16 ‰ от углерода почвенного органического вещества. δ13С СО2 со значением -11,08 ‰ было отмечено при 8-часовой инкубации. Таким образом, δ13С СО2 в проведенном эксперименте наследует изотопный состав углерода δ13С органических продуктов, используемых почвенными микроорганизмами в качестве субстратов (рис. 1).
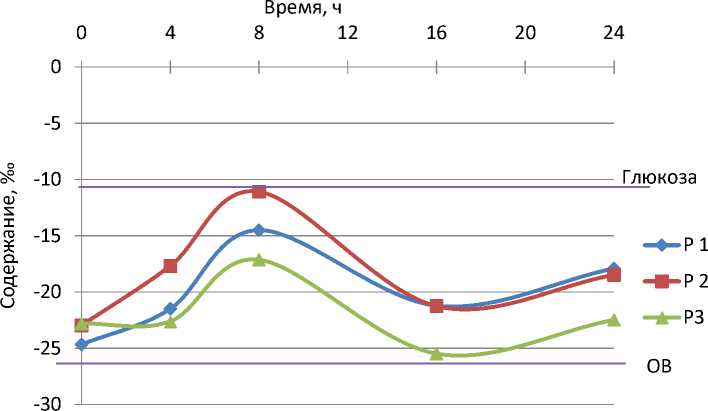
Рис. 1. Изотопный состав d13С выделившейся СО2 при внесении глюкозы в почву
Положительный прайминг-эффект составлял 264 % от исходной продукции СО2 почвы. Поэтому микробная деструкция органического вещества может быть активирована поступлением органических продуктов в почву и достигать значимых размеров.
Процесс потребления глюкозы микроорганизмами характеризовался двумя периодами и разной степенью минерализации. Высокие концентрации солей в почвах влияют на создание специфических микробных сообществ засоленных местообитаний [Сыренжапова, 2022].
Первичный период потребления глюкозы фиксировался в течение 4 часов с максимальным значением 1,68 мг СО2/100 г почвы. Во второй период после 8 часов инкубации происходило замедление скорости минерализации. Количество выделившегося СО2 из верхних слоев почвенных участков было в 12 раз больше и превышало скорость минерализации органического вещества до внесения глюкозы (табл. 3).
Таблица 3
Продуцирование СО2 на ключевых участках, мг/ч на 100 г почвы
|
Ключевой участок |
Глубина, см |
Увлажнение почвы, 60 % |
Добавление глюкозы 1,5 мг на 1 г почвы |
||||
|
сут |
1 ч |
4 ч |
8 ч |
16 ч |
24 ч |
||
|
Р1 |
0–20 |
3,36 |
0,14 |
1,68 |
0,78 |
0,33 |
0,20 |
|
Р2 |
0–20 |
2,13 |
0,08 |
1,62 |
0,70 |
0,24 |
0,15 |
|
Р3 |
0–20 |
3,06 |
0,12 |
1,68 |
0,83 |
0,42 |
0,28 |
Большое количество выделившегося СО2 из ключевого участка Р3 было связано с большим содержанием Сорг почвы. Судя по схожему характеру динамики продуцирования СО2, микроорганизмы поверхностных горизонтов одинаково откликались на внесение глюкозы.
Показано, что при внесении глюкозы в низких (до 47 мкг С/г) и высоких (4,87 мг С/г) концентрациях происходит увеличение выделения СО2. Эффект связан или с разложением внесенных соединений, или с окислением органического вещества почв [Blagodatskaya et al., 2011].
δ13С СО2, образующийся в процессе деструкции органического вещества и вносимого субстрата (глюкоза) в почву, является чувствительным параметром воздействия и продолжительности влияния этого субстрата на биогеохимические процессы, происходящие в почве.
Заключение
Изотопный состав углерода δ13С почвенных углеродсодержащих продуктов является важным показателем влияния условий среды, связанных с климатическими изменениями. Полученные данные показывают, что внесение глюкозы в почву приводит к увеличению потока СО2 в атмосферу и способствует деструкции органического вещества. Различие в изотопном составе δ13С органического вещества и глюкозы можно использовать для определения образующейся СО2
при минерализации растительных остатков в почве. Величины δ13С СО2, выделившейся из почвы в процессе разложения растительных остатков, могут быть также использованы для определения разложения растительных остатков и других веществ, попадающих в почву.
Список литературы Исследование изотопного состава углерода 13С/12С засоленных почв Селенгинского среднегорья
- Воробьева Л. А. Химический анализ почв. Москва: Изд-во МГУ, 1998. 272 с. Текст: непосредственный.
- Зякун А. М., Дилли О. Использование изотопной масс-спектрометрии для оценки метаболического потенциала почвенной микробиоты // Проблемы аналитической химии: изотопная масс-спектрометрия легких газообразующих элементов / под редакцией В. С. Севастьянова. Москва, 2011. Т. 15. С. 141–167. Текст: непосредственный.
- Сыренжапова А. С., Норовсурен Ж., Абидуева Е. Ю. Актиномицеты в прибрежных засоленных почвах озера Борзинское (Забайкальский край, Россия) // Экологические проблемы бассейна озера Байкал: материалы всероссийской научной конференции с международным участием (Улан-Удэ. 28 августа — 1 сентября 2022 г.). Улан-Удэ, 2022. С. 107–110. Текст: непосредственный.
- Хитров Б. Н. Ионно-солевой состав почв в одной навеске // Почвоведение. 1984. № 5. С. 119–127. Текст: непосредственный.
- Шарков И. Н. Определение интенсивности продуцирования СО почвой абсорбционным методом // Почвоведение. 1984. № 7. С. 136–143. Текст: непосредственный.
- Шилова Н. А. Динамика выделения CO2 в посевах полевых культур на дерново- подзолистых и торфяных почвах // Почвоведение и агрохимия. 2014. № 1(52). С. 104–113. Текст: непосредственный.
- Blagodatskaya E., Yuyukina T., Blagodatsky S., Kuzyakov Y. Three-Source-Partitioning of Microbial Biomass and of CO Efflux From Soil to Evaluate Mechanisms of Priming Effects.
- Soil Biol. Biochem. 2011; 43(4): 778–786. DOI: 10.1016/j.soilbio.2010.12.011.
- Slater C., Preston T., Weaver T. Stable Isotopes and the International System of Units. Rapid Communications in Mass Spectrometry. 2001; 15: 501–519.
- Song Y., Zou Y., Wang G., Yu X. Altered Soil Carbon and Nitrogen Cycles Due to the Freezethaw Effect: A Meta-Analysis. Soil Biol. Biochem. 2017; 109: 35–49. DOI: 10.1016/j. soilbio.2017.01.020.
- Subedi R., Taupe N., Ikovi I. et al. Chemically and Biologically-Mediated Fertilizing Value of Manure-Derived Biochar. Sci. Total Environ. 2016; 550: 924–933.
- Wang J., Xiong Z., Yan X., Kuzyakov Y. Carbon Budget by Priming in a Biochar- Amended Soil. Eur. J. Soil Biol. 2016; 76: 26–34. DOI: 10.1016/j.ejsobi.2016.07.003.
- Yanardağ I. H., Zornoza R., Bastida F. et al. Native Soil Organic Matter Conditions the Response of Microbial Communities to Organic Inputs with Different Stability. Geoderma. 2017; 295: 1–9. DOI: 10.1016/j.geoderma. 2017.02.008.


