Исследование кинетических закономерностей растворения сульфата свинца в растворах хлорида и гидроксида натрия
Автор: Рюмин А.И., Миронкина Н.В.
Журнал: Журнал Сибирского федерального университета. Серия: Техника и технологии @technologies-sfu
Статья в выпуске: 4 т.6, 2013 года.
Бесплатный доступ
Исследована кинетика выщелачивания свинца в растворах гидроксида и хлорида натрия при изменении их концентраций в интервале температур 20-80 °С. Рассчитана кажущаяся энергия активации данных процессов и определена область протекания реакций. В ходе исследований выявлены промежуточные соединения свинца, образующиеся в процессе выщелачивания сульфата.
Выщелачивание, сульфат свинца, пыль электрофильтров, хлорид натрия, гидроксид натрия
Короткий адрес: https://sciup.org/146114757
IDR: 146114757 | УДК: 669.43;
Study of dissolution kinetics of lead sulfate in solutions of sodium chloride and sodium hydrate
The kinetics of leaching of lead hydrate and sodium chloride concentrations change in the temperature range 20 – 80 o С. Calculated apparent activation energy of these processes and determined the area the reactions. The studies identified intermediate compounds of lead, formed during the leaching of sulfate.
Текст научной статьи Исследование кинетических закономерностей растворения сульфата свинца в растворах хлорида и гидроксида натрия
В технологии аффинажного производства платиновых металлов, в частности на ОАО «Красцветмет», на пирометаллургических операциях образуются пыли электрофильтров, содержащие такие примесные компоненты, как медь, свинец, сурьма, селен, теллур и др. Данный промпродукт требует дополнительной переработки, так как кроме перечисленных элементов содержит также до 1 % суммы металлов платиновой группы (∑МПГ) и до 10 % Ag.
Одним из самых проблемных компонентов, присутствующих в пылях, является свинец, содержание которого может достигать 30 %.
Из литературы известно, что выщелачивание свинца из промпродуктов металлургического производства возможно проводить такими реагентами, как хлориды натрия и кальция, ацетаты, щелочи, органические реагенты (алкиламины).
Методика исследований, результаты и обсуждения
При выборе продукта, в форме которого свинец выводится из цикла аффинажа БМ, предпочтение однозначно отдано PbSO4, так как это основная форма нахождения свинца в пылях электрофильтров аффинажного производства.
В данной статье приведены результаты исследований растворимости сульфата свинца в щелочных и солевых средах в условиях, имитирующих процессы аффинажного производства, определены кинетические закономерности процесса.
Методика экспериментов заключалось в следующем: навеску сульфата свинца определенной массой распульповывали в растворе изучаемого реагента, нагревали и перемешивали в термостатированной ячейке при заданной температуре. Опыты проводили в течение определенного времени. После завершения опыта отбирали пробу осветленного раствора и анализировали на содержание свинца методом атомно-эмиссионной спектрометрии с индукционносвязанной плазмой.
Первоначально была проверена щелочь (NaOH). В зависимости от концентрации щелочи свинец образует комплексы: Na2[Pb(OH)4], Na[Pb(OH)3].
Расчеты изменения энергии Гиббса (ΔGо 298 ) с использованием данных М.Х. Карапетянц и В. Латимера, проведенные авторами [1], свидетельствуют о том, что термодинамически наиболее вероятна реакция
PbSO 4 + 4NaOH ^ Na 2 [Pb(OH) 4 ] +
+ Na 2 SO 4 , A G °298 = - 28,7кДж/моль. (1)
Результаты серии опытов по растворению сульфата свинца при различной температуре (концентрации щелочи составляла 200 г/л) представлены на рис. 1.
Микроскопический анализ исходного сульфата свинца, проведенный с помощью электронного микроскопа, показал, что материал представлен в виде монодисперсных частиц изометрической формы (рис. 2). На основании этого для описания кинетики выщелачивания наиболее применимо уравнение Гинстлинга–Броунштейна [2]:
1-2/3α- (1-α) 2/3 = Кτ, (2)
где а - степень выщелачивания, К - константа скорости, мин1, т - продолжительность процесса, мин.
При обработке данных учитывали только начальную область кривых, так как при продолжительности более 15 мин наблюдается их выполаживание, обусловленное равновесными
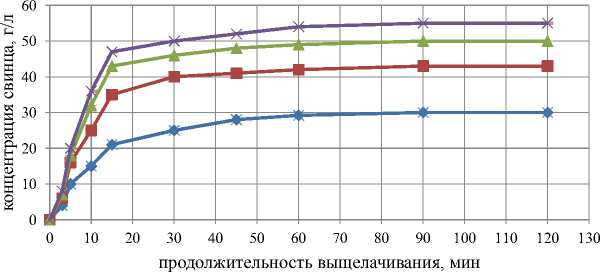
Рис. 1. Зависимость концентрации свинца в растворе от продолжительности процесса
20 С
40 С
60 С
80 С

Рис. 2. Результаты микроскопического анализа сульфата свинца
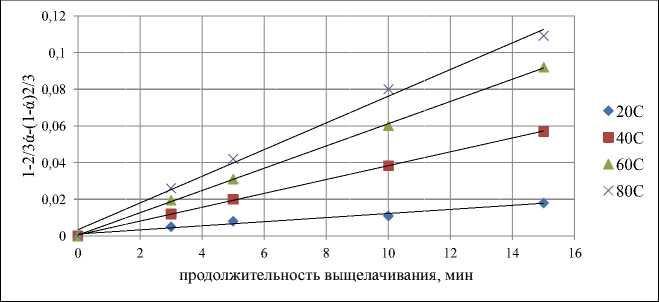
Рис. 3. Результаты обработки кинетических данных процессами растворения соли свинца и получения соединений, осаждаемых из пересыщенных растворов (рис. 3).
Полученные значения К составили 0,0015, 0,0035, 0,0049 и 0,0072 – при 20, 40, 60 и 80 °С соответственно.
Кажущаяся Еа (энергия активации) составила 42,6 кДж/моль, что соответствует переходной области протекания реакции выщелачивания сульфата свинца в растворе NaОН.
Проведен рентгенофазовый анализ твердой фазы, полученной по окончании опытов. При 20 °С образовался белый осадок, состоящий из PbSO 4 и Pb(SO 4 )∙PbO. При температуре 60-80 °С осадок желтого цвета β-PbO (массикот) и Pb3O4. Таким образом, формирование конечных растворимых соединений Na[Pb(OH) 3 ] или Na 2 [Pb(OH) 4 ] протекает через стадии образования промежуточных соединений оксисульфатов и оксидов, которые, вероятно, являются наиболее медленными стадиями процесса. Конечная твердая фаза представлена оксидами Pb(II) и Pb(II, IV).
В нашей работе была подробно изучена растворимость сульфата свинца в системе PbSO 4 –NaСl –H 2 O.
Растворение сульфата свинца протекает по реакции
PbSO4 + 4NaCl ^ Na2[PbCl4] + Na2SO4,
ΔGо 298 = – 32 кДж/моль. (3)
Предварительными опытами была выявлена продолжительность установления равновесия между раствором и осадком при растворении сульфата свинца в солевом растворе с изменением температуры от 25 до 80 °С с постоянной концентрацией хлорида натрия 300 г/л. Результаты опытов представлены на рис. 4.
На этом рисунке видно, что концентрация свинца в растворе существенно изменяется в первые 3÷10 мин и достигает равновесного значения в течение 1 ч. Повышение температуры также способствует увеличению концентрации свинца в растворе.
Для описания кинетики выщелачивания применяли уравнение Г инстлинга - Броунштей-на. Результаты обработки полученных данных изображены на рис. 5.
Полученные значения К равны 0,00184, 0,00368, 0,0115 и 0,02208 при 20, 40, 60 и 80 °С соответственно. При этом учитывалась только начальная область кривых (0 – 10 мин).
Кажущаяся Е а составила 68 кДж/моль, что соответствует кинетической либо переходной области протекания реакции.
В ходе экспериментов была проанализирована твердая фаза, полученная после 5 мин от начала процесса и через 15 мин. Данные РФА показали, что твердый продукт, полученный после 5 мин выщелачивания, состоит из трех фаз: 53 % - PbSO4, 32 % - PbCl2, 15 % - Na3Pb2(SO4)3Cl (караколит). Осадок, полученный через 15 мин, состоит только из двух фаз: 98 % - PbCl2, 2 % -
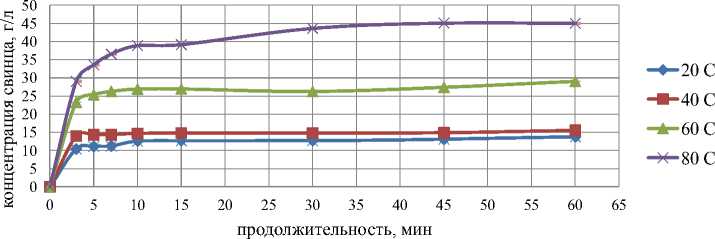
Рис. 4. Зависимость концентрации свинца от продолжительности выщелачивания
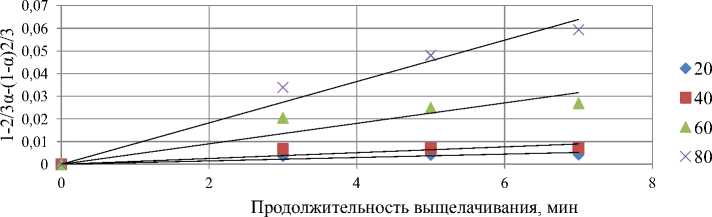
Рис. 5. Результаты обработки кинетических данных
PbSO4. Можно предположить, что переход свинца из сульфата в раствор и в твердый PbCl2 протекает через образование промежуточного сульфатно-хлоридного соединения свинца и натрия, а именно караколита. В ходе опытов была проанализирована твердая фаза, полученная после 5 мин от начала процесса и через 15 мин. Выщелачивание проводили при температуре 25 °С, концентрация хлорида натрия составляла 300 г/л. Данные РФА показали, что твердый продукт, полученный после 5 мин выщелачивания, состоит из трех фаз: 53 % - PbSO4, 32 % - PbCl2, 15 % - Na3Pb2(SO4)3Cl (караколит). Осадок, полученный через 15 мин, состоит только из двух фаз: 98 % - PbCl2, 2 % - PbSO4 . Можно предположить, что переход свинца из сульфата в раствор и в твердый PbCl2 протекает через образование промежуточного сульфатно-хлоридного соединения свинца и натрия.
Заключение
Из полученных данных можно сделать вывод, что солевое выщелачивание в растворах NaCl – более эффективный способ извлечения свинца, позволяющий перевести в раствор более 90 % данного элемента. Солевое выщелачивание может стать основной операцией технологии переработки промпродуктов аффинажного производства с высоким (до 30 %) содержанием свинца. Также данный реагент нетоксичен и является промпродуктом ОАО «Красцветмет», что выступает существенным плюсом данного метода. Технология и ее основные операции без проблем встраиваются в общую технологию аффинажного производства.


