Исследование модифицированного вермикулита
Автор: Баюрова Юлия Леонидовна, Губкина Татьяна Геннадиевна
Журнал: Горные науки и технологии @gornye-nauki-tekhnologii
Статья в выпуске: 2, 2014 года.
Бесплатный доступ
В этой статье вы можете увидеть методы получения гидрофобных сорбентов нефти путем термической и химической модификации поверхности вермикулита органическими силоксанами и электронные микроскопические исследования минеральной поверхности с иммобилизованными нефтеокисляющими бактериальными клетками.
Термоактивация вермикулита, химическая модификация вермикулита, иммобилизация бактериальных клеток, адсорбент, очищение воды от нефтепродуктов
Короткий адрес: https://sciup.org/140215840
IDR: 140215840 | УДК: 541(542.06)
Текст научной статьи Исследование модифицированного вермикулита
Вермикулит – минерал из группы гидрослюд, имеющих слоистую структуру с добавочной молекулярной межслоевой водой. Образуется в результате выветривания магнезиально-железистых слюд. Одно из крупнейших месторождений вермикулита находиться на Кольском полуострове и представлено Ковдорским месторождением [2].
Модификация вермикулита позволяет получить новый сорбционный материал с заданными адсорбционными свойствами. При термоактивации вермикулита вода, кристаллизованная между чешуйками слюды, испаряется, что приводит к образованию макро- и микропор в частице вермикулита и увеличению удельной поверхности. Сам по себе вспученный вермикулит гидрофилен. Для того чтобы вермикулит стал идеальным сорбентом для сбора нефтепродуктов, его подвергают химической модификации и создают на поверхности частиц углеродосодержащий слой. Химическая модификация вермикулита кремнийорганическими соединениями, позволяет получить новые адсорбционные материалы способные адсорбировать полярные и неполярные молекулы углеводородов. Такие материалы являются эффективными сорбентами нефтепродуктов, как с твердой, так и с водной поверхности [3].
Для термической модификации использовался вермикулит Ковдорского месторождения (КФК-1, КФК-4, КФК-8), модификацию проводили в наклонной печи при температуре 650ºС.
Исследовали вермикулит сырой, термоактивированный в статических и динамических условиях при 650ºС на изменение значения уровня pH и смыв ионов кальция и магния в зависимости от длительности взаимодействия с водной средой. Минерал взаимодействовал при постоянном перемешивании, измерение pH проводились через каждые 10 минут в течение первого часа (одно дополнительное измерение через 5 минут после начала эксперимента), и одно измерение через 3, 6, 24 часа. Затем раствор фильтровали и проводили химический анализ жидкой фазы.
Переход ионов кальция и магния в воду увеличивается закономерно с увеличением времени взаимодействия вермикулита (табл. 1-5). Концентрация ионов кальция при взаимодействии термоактивированного в статических условиях вермикулита с дистиллированной водой через сутки несколько меньше по сравнению с другими образцами. Концентрация ионов магния наименьшая при взаимодействии сырого вермикулита, при взаимодействии термоактивированного в динамических условиях вермикулита возрастает с уменьшением фракции. Жесткость воды увеличивается и меняется от очень мягкой через один и три часа, до мягкой через сутки.
Таблица 1.
Зависимость концентрации ионов кальция и магния в дистиллированной воде от времени взаимодействия с вермикулитом (сырец).
|
Время взаимодействия, мин |
С Cа , мг/л |
С Mg , мг/л |
Жесткость воды, мэкв/л |
|
|
60 |
8,62 |
7,50 |
1,05 |
очень мягкая |
|
60 |
8,60 |
8,06 |
1,09 |
очень мягкая |
|
180 |
11,55 |
6,82 |
1,14 |
очень мягкая |
|
180 |
10,98 |
7,45 |
1,16 |
очень мягкая |
|
1440 |
17,48 |
8,37 |
1,56 |
мягкая |
|
1440 |
17,19 |
8,55 |
1,56 |
мягкая |
|
1440 |
16,93 |
8,26 |
1,52 |
мягкая |
|
1440 |
16,32 |
8,57 |
1,52 |
мягкая |
Таблица 2.
Зависимость концентрации ионов кальция и магния в дистиллированной воде от времени взаимодействия с термоактивированным вермикулитом в статических условиях.
|
Время взаимодействия, мин |
С Cа , мг/л |
С Mg , мг/л |
Жесткость воды, мэкв/л |
|
|
60 |
9,60 |
6,40 |
1,01 |
очень мягкая |
|
60 |
8,90 |
6,00 |
0,94 |
очень мягкая |
|
180 |
10,20 |
10,90 |
1,41 |
очень мягкая |
|
180 |
9,50 |
12,40 |
1,49 |
очень мягкая |
|
1440 |
13,70 |
25,70 |
2,80 |
мягкая |
|
1440 |
13,40 |
24,50 |
2,68 |
мягкая |
|
1440 |
12,50 |
21,30 |
2,38 |
мягкая |
|
1440 |
12,70 |
24,40 |
2,64 |
мягкая |
Таблица 3.
Зависимость концентрации ионов кальция и магния в дистиллированной воде от времени взаимодействия с термоактивированным вермикулитом в динамических условиях КФК - 1.
|
Время взаимодействия, мин |
С , мг/л |
С , мг/л |
Жесткость воды, мэкв/л |
|
|
60 |
11,00 |
13,80 |
1,68 |
мягкая |
|
60 |
10,80 |
14,60 |
1,74 |
мягкая |
|
180 |
11,60 |
16,00 |
1,89 |
мягкая |
|
180 |
11,80 |
17,00 |
1,99 |
мягкая |
|
1440 |
15,80 |
25,20 |
2,86 |
мягкая |
|
1440 |
16,80 |
30,00 |
3,31 |
мягкая |
|
1440 |
15,00 |
24,40 |
2,76 |
мягкая |
|
1440 |
19,80 |
28,60 |
2,76 |
мягкая |
Таблица 4.
Зависимость концентрации ионов кальция и магния в дистиллированной воде от времени взаимодействия с термоактивированным вермикулитом в динамических условиях КФК - 4.
|
Время взаимодействия, мин |
С , мг/л |
С , мг/л |
Жесткость воды, мэкв/л |
|
|
60 |
7,08 |
7,91 |
1,00 |
очень мягкая |
|
60 |
7,50 |
7,80 |
1,02 |
очень мягкая |
|
180 |
13,36 |
15,71 |
1,96 |
мягкая |
|
180 |
11,99 |
15,18 |
1,85 |
мягкая |
|
1440 |
15,37 |
16,54 |
2,13 |
мягкая |
|
1440 |
13,31 |
19,08 |
2,23 |
мягкая |
|
1440 |
14,99 |
20,38 |
2,42 |
мягкая |
|
1440 |
14,71 |
18,30 |
2,42 |
мягкая |
Таблица 5.
Зависимость концентрации ионов кальция и магния в дистиллированной воде от времени взаимодействия с термоактивированным вермикулитом в динамических условиях КФК - 8.
|
Время взаимодействия, мин |
С , мг/л |
С , мг/л |
Жесткость воды, мэкв/л |
|
|
60 |
6,80 |
6,40 |
0,87 |
очень мягкая |
|
60 |
6,20 |
6,60 |
0,85 |
очень мягкая |
|
180 |
8,80 |
12,40 |
1,46 |
очень мягкая |
|
180 |
7,40 |
10,00 |
1,19 |
очень мягкая |
|
1440 |
16,20 |
20,40 |
2,49 |
мягкая |
|
1440 |
28,20 |
23,20 |
3,32 |
мягкая |
|
1440 |
14,40 |
16,80 |
2,10 |
мягкая |
|
1440 |
15,40 |
22,80 |
2,10 |
мягкая |
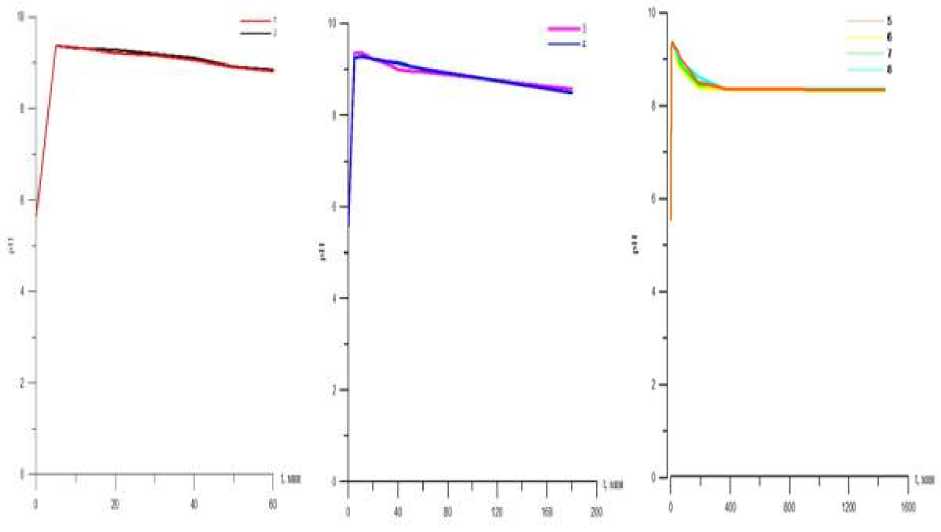
Рис. 1. Зависимость величины pH дистиллированной воды от времени взаимодействия с вермикулитом (сырец).
-
1, 2 два параллельных опыта по взаимодействию вермикулита с дистиллированной водой в течение часа; 3, 4 два параллельных опыта по взаимодействию вермикулита с дистиллированной водой в течение 3 часов; 5, 6, 7, 8 – четыре параллельных опыта по взаимодействию т вермикулита с дистиллированной водой в течение суток.
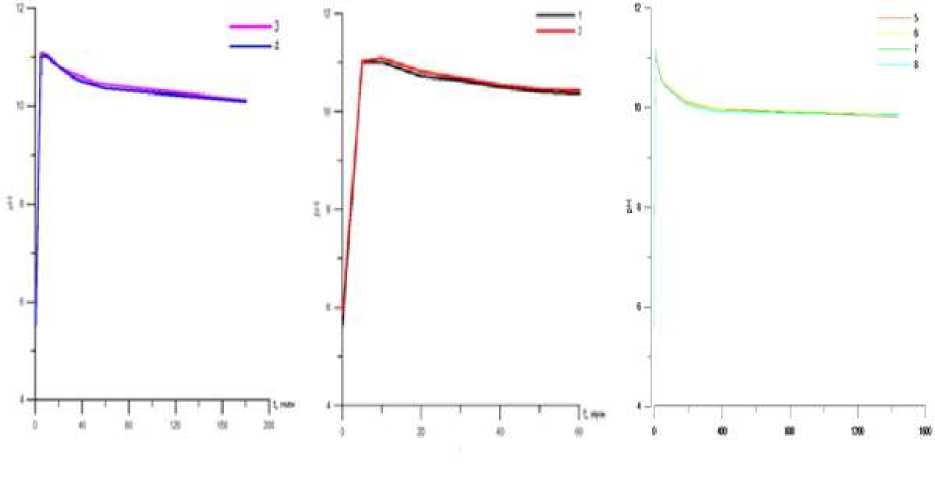
Рис. 2. Зависимость величины pH дистиллированной воды от времени взаимодействия с термоактивированным в статических условиях вермикулитом.
-
1, 2 два параллельных опыта по взаимодействию термоактивированного вермикулита с дистиллированной водой в течение часа; 3, 4 два параллельных опыта по взаимодействию термоактивированного вермикулита с дистиллированной водой в течение 3 часов; 5, 6, 7, 8 – четыре параллельных опыта по взаимодействию термоактивированного вермикулита с дистиллированной водой в течение суток.
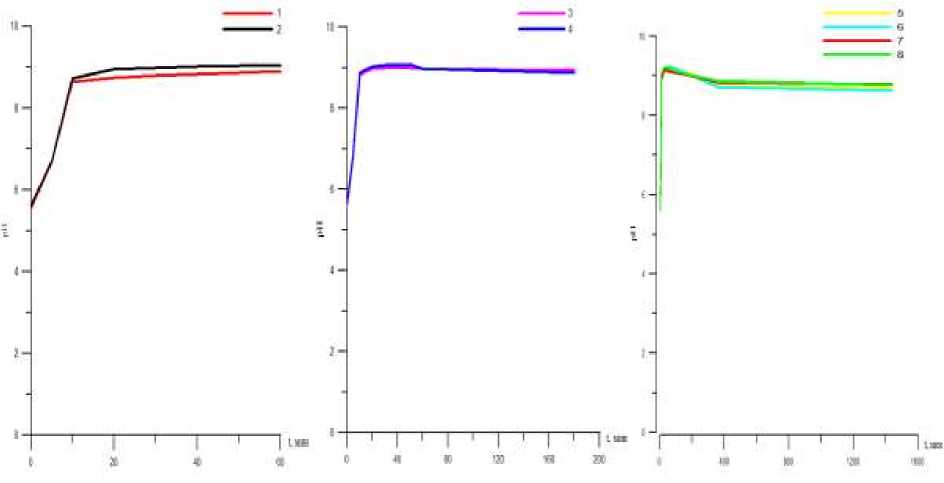
Рис. 3. Зависимость величины pH дистиллированной воды от времени взаимодействия с термоактивированным в динамических условиях вермикулитом КФК-1.
-
1, 2 два параллельных опыта по взаимодействию термоактивированного вермикулита (КФК-1) с дистиллированной водой в течение часа; 3, 4 два параллельных опыта по взаимодействию термоактивированного вермикулита (КФК-1) с дистиллированной водой в течение 3 часов; 5, 6, 7, 8 – четыре параллельных опыта по взаимодействию термоактивированного вермикулита (КФК-1) с дистиллированной водой в течение суток.
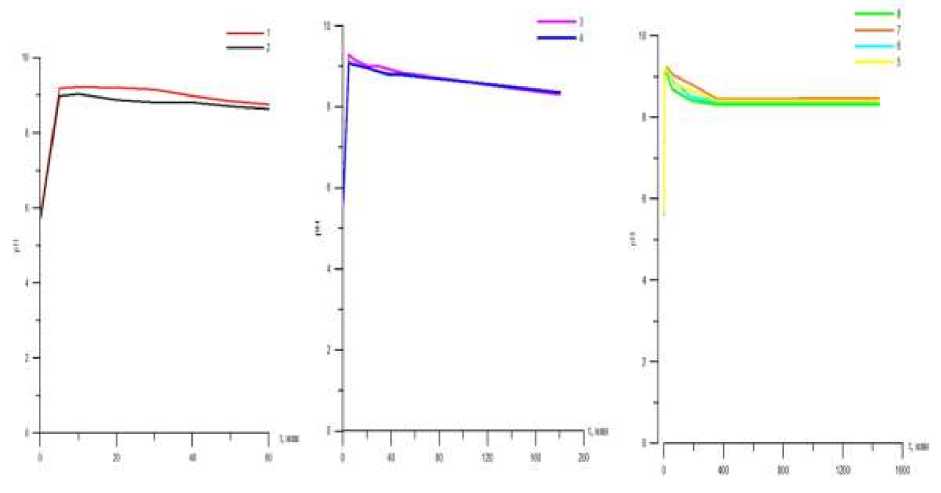
Рис. 4. Зависимость величины pH дистиллированной воды от времени взаимодействия с термоактивированным в динамических условиях вермикулитом КФК-4.
-
1, 2 два параллельных опыта по взаимодействию термоактивированного вермикулита (КФК-4) с дистиллированной водой в течение часа; 3, 4 два параллельных опыта по взаимодействию термоактивированного вермикулита (КФК-4) с дистиллированной водой в течение 3 часов; 5, 6, 7, 8 – четыре параллельных опыта по взаимодействию термоактивированного вермикулита (КФК-4) с дистиллированной водой в течение суток.
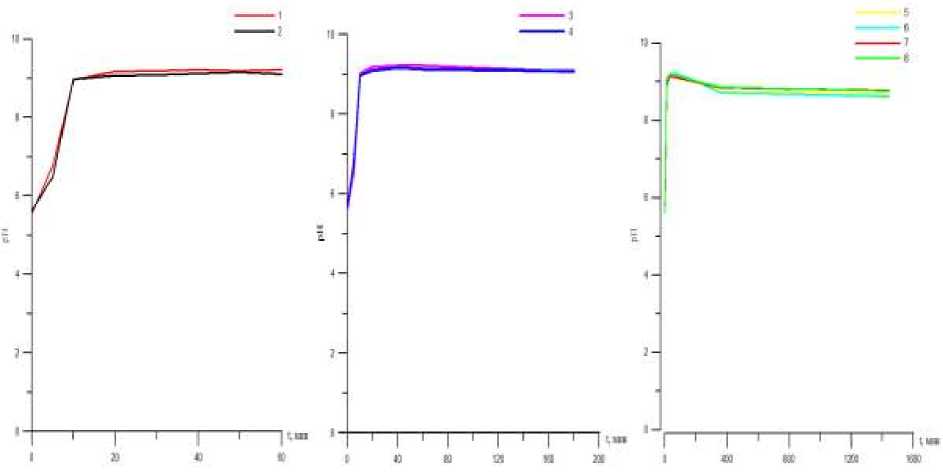
Рис. 5. Зависимость величины pH дистиллированной воды от времени взаимодействия с термоактивированным в динамических условиях вермикулитом КФК-8.
-
1, 2 два параллельных опыта по взаимодействию термоактивированного вермикулита (КФК-8) с дистиллированной водой в течение часа; 3, 4 два параллельных опыта по взаимодействию термоактивированного вермикулита (КФК-8) с дистиллированной водой в течение 3 часов; 5, 6, 7, 8 - четыре параллельных опыта по взаимодействию термоактивированного вермикулита (КФК-8) с дистиллированной водой в течение суток.
Наблюдается резкий рост pH в первые пять-десять минут, а затем происходит снижение (рис. 1-5). Наибольший рост pH характерен для вермикулита термоактивированного в статических условиях (pH=11) и даже через сутки в среднем составляет 9,84. Значение pH через сутки взаимодействия термоактивированного в динамических условиях вермикулита КФК-1, КФК-4, КФК-8 примерно одинаково.
Для придания гидрофобных свойств, вермикулит обрабатывали метилсиликонатом натрия (ГКЖ-11П) и олигометилгидридсилоксаном (Пента-804) [1].
Для ковалентной иммобилизации бактериальных клеток и прививки на поверхность вермикулита алифатических первичных аминогрупп, минерал обрабатывали спиртовым раствором 3-аминопропилтриэтоксисилана (АГМ-9) и инкубировали в течение 36 часов при температуре 45°С. Затем сорбент промывали дистиллированной водой и глутаровым альдегидом (2,2%), сушили в течение 24 часов при Т=50-60°С. В результате чего минерал приобретает красную окраску за счет образования оснований Шиффа между аминогруппами Si-АГМ-9 и карбонильными группами глутарового альдегида.
Наличие прочной ковалентной связи бактериальных клеток с носителем препятствует их отсоединению при жестких условиях применении в промышленных процессах.
Для иммобилизации использовали суспензию с бактериальными клетками рода Pseudomonas spp, которую культивировали на мясопептонном бульоне. Нефтеокисляющие бактериальные клетки, были выделенные из почв Кольского полуострова, загрязненных нефтепродуктами.
Для всех сорбентов был выбран метод иммобилизации бактериальных клеток с перемешиванием, где в течение трёх часов сорбенты взаимодействовали с суспензией бактериальных клеток.
После иммобилизации сорбенты сушили и исследовали на сканирующем электронном микроскопе SEM LEO-420 с программным обеспечением.

Рис. 6. Поверхность вермикулита: исходный термоактивированный (а); с иммобилизованными бактериальными клетками (б); обработанный метилсиликонатом натрия с иммобилизованными бактериальными клетками (в); обработанный олигометилгидридсилоксаном с иммобилизованными бактериальными клетками (г); с ковалентной сшивкой бактериальных клеток (д) под сканирующим электронным микроскопом SEM LEO-420.
В первом образце поверхность вермикулита представлена крупными пластинчатыми частицами вытянутой формы, на их внешней поверхности 19
наблюдаются более мелкие частицы с чёткими скольными контурами, а также участки выпуклой формы без чёткой огранки контура (рис. 6а). Термическая обработка зёрен увеличивает расстояние между параллельно идущими пластинами.
Во втором образце на всей поверхности сорбента после иммобилизации обнаружено наличие питательной среды, характер покрытия не равномерный. Бактериальные клетки сосредоточены в сгустках питательной среды и на участках вермикулита с развитой поверхностью. Обнаружены участки питательной среды с углублениями по форме и размеру похожие на следы от присутствующих там ранее бактериальных клеток. Из чего следует, что бактерии с питательной средой на поверхности вермикулита могут быть слабо связаны и при незначительном механическом воздействии (например, после вакуума) могут открепляться во внешнюю среду (рис. 6б). Адгезия клеток на не модифицированном вермикулите в основном определяется гидратационными эффектами и капиллярными силами, связанными с гидрофильностью поверхности вермикулита.
В третьем образце на поверхности сорбента, обработанного метилсиликонатом натрия, наблюдается неравномерное покрытие питательной средой, в которой встречаются лишь единичные бактериальные клетки (рис. 6в). Иммобилизация бактериальных клеток на данном сорбенте не произошла из-за высокой щелочности гидрофобизатора (pH=13).
В четвертом образце поверхность вермикулита, обработанного олигометилгидридсилоксаном, полностью покрыта бактериальными клетками (рис. 6г). Из этого следует, что реактив не оказывает токсичного действия на бактерии, а напротив, способствует их адгезии за счёт гидрофобных взаимодействий.
В пятом образце бактерии расположены практически на всей поверхности вермикулита, сосредоточены, как на гладкой поверхности, так и в активных зонах разлома минеральных пластин (рис. 6д).
Исследование количества адсорбированных клеток методом посева показало, что на вермикулите до иммобилизации были обнаружены бактериальные клетки численность, которых составила 5×103 клеток/г (из окружающей среды). Численность бактериальных клеток на вермикулите после иммобилизации составила 2×109 клеток/г, а на вермикулите, обработанном олигометилгидридсилоксаном, составил 2×108 клеток/г, тогда как количество бактериальных клеток в суспензии составило 2×1010 клеток/г.
Таким образом, иммобилизация бактериальных клеток на термоактивированном вермикулите и на сорбенте, модифицированном олигометилгидридсилоксаном, прошла успешно. Количество иммобилизированных клеток на гидрофильной и гидрофобной поверхности отличается не значительно.
В результате эксперимента по очистке воды от нефтепродуктов через трое суток, наибольшей степью очистки воды обладает гидрофобный сорбент (99,8%), обработанный олигометилгидридсилоксаном с нефтеокисляющими бактериальными клетками, при этом сорбент вместе с нефтепродуктами локализуется на поверхности воды, что обеспечивает благоприятные условия для деструкции нефтепродуктов бактериями клетками. Наименьшей степенью очистки воды от дизельного топлива, обладает термоактивированный вермикулит без модификатора (рис. 7).
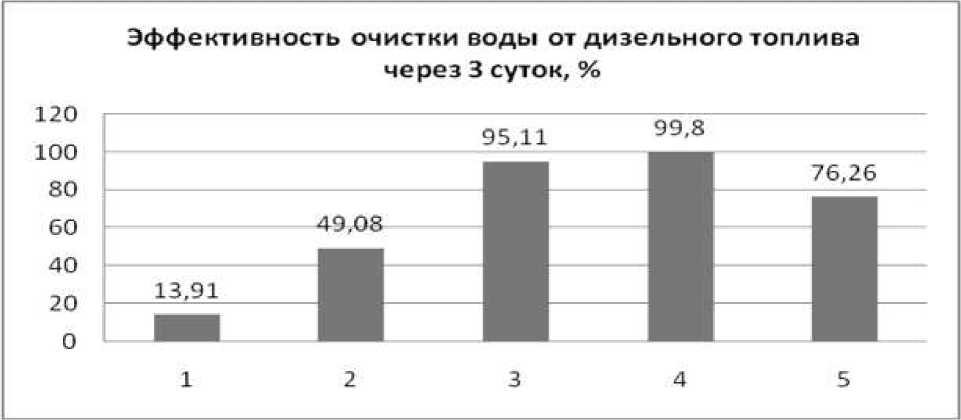
Рис. 7. Эффективность очистки воды от нефтепродуктов через трое суток: 1 - исходный термоактивированный вермикулит; 2 - вермикулит с иммобилизованными бактериальными клетками; 3 - вермикулит, обработанный метилсиликонатом натрия с иммобилизованными бактериальными клетками; 4 – вермикулит, обработанный олигометилгидридсилоксаном с иммобилизованными бактериальными клетками; 5 - вермикулит с ковалентной сшивкой бактериальных клеток.
Заключение.
Переход ионов кальция и магния в воду увеличивается закономерно с увеличением времени взаимодействия вермикулита. Концентрация ионов кальция при взаимодействии термоактивированного вермикулита в статических условиях с дистиллированной водой через сутки несколько меньше по сравнению с другими образцами. Концентрация ионов магния наименьшая при взаимодействии сырого вермикулита, при взаимодействии термоактивированного вермикулита в динамических условиях возрастает с уменьшением фракции.
В качестве основного механизма взаимодействия вермикулита с бактериальными клетками выступают анионный обмен: анионы карбоксильных групп замещают OH-группы на поверхности минерала. Также возможно участие OH-групп в лигандном обмене. Однако адсорбция бактериальных клеток по данному механизму является легко обратимой, а образующиеся соединения могут легко разрушатся при взаимодействии минерала с водой.
Иммобилизация бактериальных клеток на вермикулите, обработанном кремнийорганическими гидрофобизаторами, зависит от химической природы модификатора и pH. Так, бактериальные клетки на вермикулите, обработанном метилсиликонатом натрия, практически не иммобилизовались, из-за щелочной реакции реактива, тогда как на вермикулите, обработанном олигометилгидридсилоксаном с pH=7, иммобилизация прошла успешно. Бактерии удерживаются на поверхности минерала за чёт сочетания биоспецифической адсорбции и гидрофобных взаимодействий.
Олигометилгидридсилоксан является универсальным модификатором поверхности вермикулита, благодаря которому, минерал приобретает не только исключительные гидрофобные и олиофильные свойства, но и способствует адгезии нефтеокисляющих бактериальных клеток.
Ковалентная иммобилизация бактериальных клеток на вермикулите также прошла успешно. Однако, при таком способе модификации реактив склеивает мелкие частицы вермикулита, что способствует снижению адсорбционных свойств.
Способ очистки воды от нефтепродуктов с применением гидрофобных сорбционных материалов с иммобилизованными нефтеокисляющими бактериальными клетками наиболее эффективен, так как происходит уменьшение концентрации дизельного топлива в воде за счет физико-химической адсорбции и деструкции адсорбированных нефтепродуктов бактериальными клетками.
Список литературы Исследование модифицированного вермикулита
- Губкина Т.Г., Беляевский А.Т., Маслобоев В.А. Способы получения гидрофобных сорбентов нефти модификацией поверхности вермикулита органосилоксанами.//Вестник МГТУ, 2011. -Т. 14. -№ 4. -С. 767-773.
- Крашенинников О.Н., Быстрыгин С.В. Перспективы использования вермикулита Ковдорского месторождения в Мурманской области.//Север промышленный, 2012. -№ 3. -С. 1-4.
- Интернет-источник: http://spbsluda.ru/vermiculit_ecology.html
- Интернет-источник: http://www.romanlapshov.ru/labrabor/water.pdf


