Исследование неферментативного взаимодействия селена и серебра с цистеином и глутатионом с помощью приборного комплекса МХ-5310
Автор: Новиков А.В., Кошелева Г.Н., Бубляев Р.А., Манойлов А.В., Козьмин Ю.П., Краснов Н.В., Миргородская О.А.
Журнал: Научное приборостроение @nauchnoe-priborostroenie
Рубрика: Масс-спектрометрия для биотехнологии. Интерпретация данных, методология, применение
Статья в выпуске: 4 т.18, 2008 года.
Бесплатный доступ
С помощью разработанного в Институте аналитического приборостроения РАН приборного комплекса, включающего времяпролетный масс-спектрометр с электрораспылением МХ-5310 и жидкостной хроматограф Милихром А-02, было проведено исследование взаимодействия селена (Se) с элементами биологических систем на примере цистеина (Cys) и глутатиона (GSH). Выявлено образование двух типов продуктов - дисульфидов и Se-дисульфидов и определены условия, позволяющие изменять соотношения концентраций между этими типами продуктов при взаимодействии Se c GSH. Проведено сравнение процессов взаимодействия Se с GSH, Cys, и смеси GSH с Cys, которое выявило конкуренцию за Se у таких сульфгидрильных соединений. Определено также, что в конкурентных условиях не происходит образование Se-дисульфида Cys, но в значительной степени образуется смешанный дисульфид без Se и с Se. Показано, что образование смешанного Se-дисульфида может протекать через замещение GSH на Cys в симметричном Se-дисульфиде GSH. Можно полагать, что именно селективность замещения лежит в основе регуляции физиологических процессов с участием Se и различных тиолов в биологических средах.
Короткий адрес: https://sciup.org/14264577
IDR: 14264577 | УДК: [577.1:
Study of nonenzymatic selenium and silver interaction with cysteine and glutathione using MX-5310 complex
A study of the interaction of selenium (Se) with elements of biological systems cysteine (Cys) and glutathione (GSH) as an example was performed. The study was carried out using complex which includes the liquid chromatograph Milichrom А02 and time-of-flight mass spectrometer with electrospray ionization МХ-5310, developed in the Institute for Analytical Instrumentations RAS. Result of this study was a new scheme of chemical reactions. Besides a possibility of the analytical complex to perform a research of a competitive interaction of selenium and silver with sulfhydryl groups GSH was demonstrated.
Текст научной статьи Исследование неферментативного взаимодействия селена и серебра с цистеином и глутатионом с помощью приборного комплекса МХ-5310
ВВЕДЕНИЕ сутствующего в сопоставимых с GSH количествах
Антиоксидантная роль селена (Se) впервые была выявлена английским биохимиком А. Диплоком в 1970 г. [1]. В основе этого процесса лежит взаимодействие Se с глутатионом (GSH) [2].
GSH присутствует в клетке в восстановленном состоянии (SH) в концентрации около 5 мМ. Фактически такая высокая концентрация GSH в клетке приводит к тому, что он может восстанавливать любую дисульфидную связь (S–S), образующуюся между цистеинами цитозольных белков. При этом восстановленная форма GSH превращается в окисленную форму GSH — дисульфид глутатиона (GSSG). GSSG может быть восстановлен под действием фермента глутатионредуктазы, который постоянно находится в клетке в активном состоянии и индуцируется при оксидативном стрессе [1]. Важную роль в этих процессах выполняет Se, участвуя главным образом в функционировании Se-зависимых глутатионпероксидаз. Было показано, что процесс окисления GSH в безфер-ментативной среде ускоряется в присутствии Se (обычно в виде SeO 2 ). При этом зарегистрировано образование двух типов продуктов — окисленной формы GSH (GS-SG) и Se-дисульфида глутатиона (GS-Se-SG) [2]. Представляло интерес в рамках настоящей работы изучить особенности этого неферментативного взаимодействия Se с GSH, а также влияние на этот процесс другого сульфгидрильного соединения — цистеина (Cys), при-
во многих биологических средах [1–2].
В связи с тем что постулируется участие GSH в дезинтоксикации тяжелых металлов [3], представлялось целесообразным проверить возможное конкурентное участие в этом процессе Se на примере изучения воздействия на этот процесс ионов серебра, относящегося также к классу тяжелых металлов.
Для изучения особенностей неферментативного взаимодействия GSH и Cys с Se (в виде SeO 2 ) и в том числе в присутствии ионов серебра использовались два инструментальных метода: масс-спектрометрия с электрораспылением (ESI-o-TOF-MS) — для качественной и высокоэффективная жидкостная хроматография (ВЭЖХ) — для количественной оценок.
ЭКСПЕРИМЕНТАЛЬНЫЕ РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Независимое взаимодействие SeIV с GSH и SeIV с Cys
Для исследования взаимодействия SeIV с GSH и SeIV с Cys использовались смеси этих соединений в различных концентрациях. На рис. 1 представлены масс-спектры реакционных смесей, полученных при взаимодействии SeIV с GSH (а) и SeIV с Cys (б) в молярном соотношении 1:1 в водной среде.
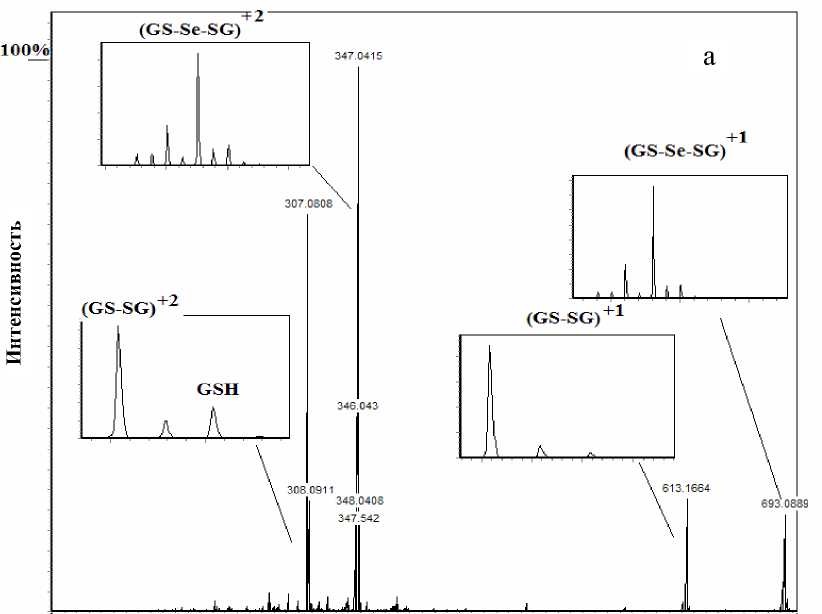
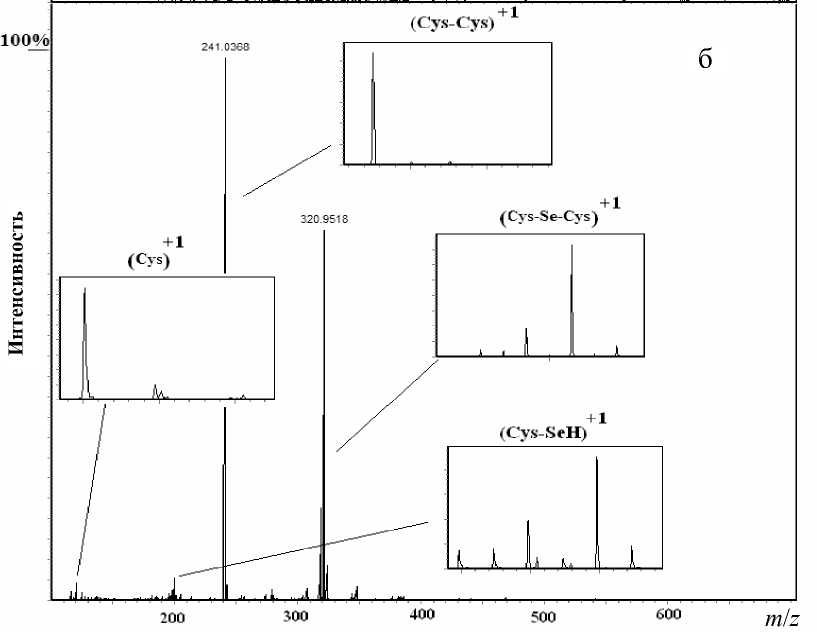
Рис. 1. ESI-масс-спектры реакционных смесей, полученных при взаимодействии SeIV с GSH (а) и SeIV с Cys (б)
Из рис. 1 следует, что в реакционных смесях образовались продукты окисления, а именно дисульфид глутатиона (GS-SG), представленный в масс-спектре двухзарядным ионом с m / z = 307.08 и однозарядным ионом с m / z = 613.16 (рис. 1, а), и дисульфид Cys (Cys-Cys) в виде только однозарядного иона с m / z = 241.04 (рис. 1, б).
Кроме того, наблюдается образование Se-содержащих продуктов для GSH (GS-Se-SG), представленных в масс-спектре двухзарядным ионом с m / z = 307.3 и однозарядным ионом с m / z = 693.16 (рис. 1, а), а для Cys-содержащих продуктов — Se-дисульфида (Cys-Se-Cys) (рис. 1, б). Все Se-содержащие продукты имеют изотопное распределение, характерное для Se.
В настоящей работе проведен количественный анализ образующихся продуктов в смеси SeIV с GSH с помощью ВЭЖХ. Результаты обработки полученных данных при различных количествах SeIV и GSH в водной среде представлены в табл. 1. Там же представлены данные по спонтанному окислению GSH без SeIV. Концентрации всех продуктов выражены в процентах, рассчитанных из площадей соответствующих хроматографических пиков, что отражает распределение в них глутатиона.
Из табл. 1 видно, что уже через 5 мин наблюдается значительная убыль GSH и появление продуктов окисления, основным из которых при соотношениях с Se и GSH 1:1 и 1:2 является GS-Se-SG. Отметим, что контрольный эксперимент показал, что в тех же условиях, но без Se окисление GSH не наблюдается по крайней мере в течение часа. Отметим, что доминирование образования GS-Se-SG, возникающее на первых 5 минутах, сохраняется в течение длительного времени (~20 ч).
Как показывают результаты представленные в табл. 2, в присутствии бикарбоната аммония (рН 7.4) ускоряется как реакция GSH с Se, так и скорость спонтанного окисления. В 1 %-й уксусной кислоте скорость взаимодействия с Se замедляется. При этом как в водной среде, так и в присутствии уксусной кислоты, спонтанное окисление GSH в отсутствие Se не наблюдается. Из анализа полученных результатов может быть сделан вывод о том, что увеличение в продуктах реакции доли окисленной формы (GS-SG) при переходе от кислой к щелочной среде связано с изменением концентрации непротонированных сульфгидрильных групп GSH, необходимых для образования этой формы, в то время как образование GS-Se-SG не зависит от рН. В конечном итоге это приводит к перераспределению конечных продуктов реакции и значительному изменению соотношения GS-SG и GS-Se-SG.
Табл. 1. Количественные характеристики реакционных смесей и продуктов реакции
|
№ п/п |
Исходные реагенты |
Время реакции, мин |
Состав продуктов, содержащих глутатион, % |
|||
|
SeIV, мМ |
GSH, мМ |
GSH |
GS-SG |
GS-Se-SG |
||
|
1 |
0.33 |
0.33 |
5 |
9 |
27 |
64 |
|
2 |
0.165 |
0.33 |
5 |
31 |
21 |
48 |
|
3 |
0.165 |
0.33 |
60 |
5 |
25 |
70 |
|
4 |
0.165 |
0.33 |
1140 |
0 |
26 |
74 |
|
5 |
0 |
0.33 |
60 |
100 |
0 |
0 |
Табл. 2. Состав реакционной смеси окиси селена и глутатиона при соотношении 1: 1 в разных средах
|
№ п/п |
Реакционная среда |
Время реакции, мин |
Состав продуктов, содержащих глутатион, % |
||
|
GSH |
GS-SG |
GS-Se-SG |
|||
|
1 |
Вода |
5 |
9 |
27 |
64 |
|
2* |
— ” — |
60 |
100 |
0 |
0 |
|
3 |
20 мМ NH 4 HCO 3 |
5 |
0 |
69 |
31 |
|
4* |
20 мМ NH 4 HCO 3 |
5 |
96 |
4 |
0 |
|
5 |
1 % CH 3 COOH |
14 |
16 |
20 |
64 |
|
6 |
1 % CH 3 COOH |
90 |
0 |
21 |
79 |
|
7* |
1 % CH 3 COOH |
60 |
100 |
0 |
0 |
Примечание. * — контроль без селена.
Bit
1800 000
GS-Cys 427.24
а
1600 000
1400 000
1200 000
1000 000
800 000
600 000
400 000
200 000
50 000
Cys-Cys
241.11
+2 (GS-Se-SG) 347.16
GSH 308.19
GS-Se-Cys
50719 GS-Se-SG
GS-SG 693.33
613.38 I
100 150 200 250 300 350 400 450 500 550 600 650 700 750 800
m / z
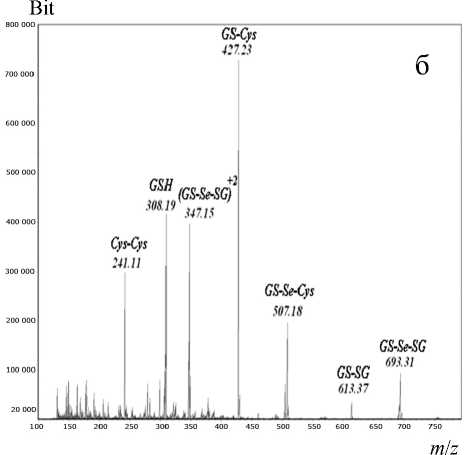
Рис. 3. ESI-масс-спектры реакционных смесей, полученных при взаимодействии SeIV с GSH и Cys при эквимолярном соотношении концентраций SeIV и сульфгидрильных соединений 1:1:1 (а) и при концентрации Se, в 2 раза уменьшенной — 1: 2 : 2 (б)
Конкурентное взаимодействие сульфгидрильных групп цистеина и глутатиона с селеном
Свободный цистеин, являющийся предшественником глутатиона, присутствует в биологических жидкостях одновременно с глутатионом. Оба соединения являются компонентами антиоксидантной защиты организма человека. Наличие в каждом из них свободной сульфгидрильной группы позволяет обоим соединениям конкурировать друг с другом при взаимодействии с селеном.
В настоящей работе были проведены масс-спектрометрические и хроматографические иссле- дования взаимодействия SeIV с GSH и Cys при различных концентрациях SeIV и сульфгидрильных соединений.
На рис. 3 представлены результаты масс-спектрометрической детекции смесей Cys и GSH с Se в различных концентрациях. Из рис. 3 видно, что в обоих случаях наиболее интенсивным из дисульфидов является ион с m/z 427.24, соответствующий смешанному дисульфиду SG-Cys. Кроме того, на масс-спектрах присутствуют ионы, соответствующие Cys-Cys и GS-SG. В обоих спектрах также регистрируется Se-дисульфиды GS-Se-SG и GS-Se-Cys в виде одно- и двухзарядных ионов и "следы" иона Se-дисульфид-цистеина (Cys-Se-Cys) даже в смеси с наибольшей концентрацией Se.
При хроматографии смесей SeIV с GSH и Cys (рис. 4) регистрируются только продукты, содержащие глутатион, поскольку как сам цистеин, так и его окисленная форма спектрофотометрически не детектируются. Наличие продуктов в хроматографических пиках, указаных на этих рисунках, подтверждено масс-спектрометрически. Отметим, что в пиках, подходящих для количественного анализа, не зарегистрирован продукт SG-Cys, однако его концентрация может быть рассчитана из баланса по GSH.
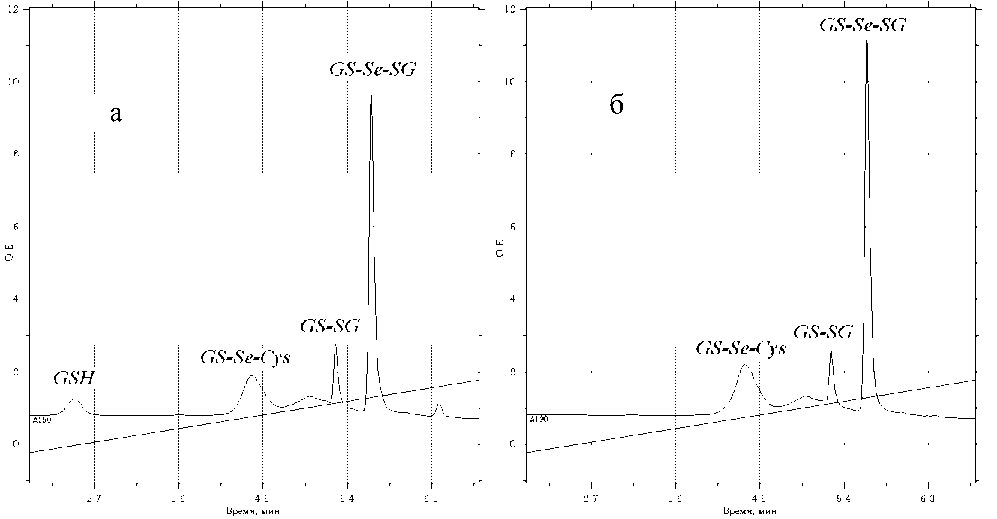
Рис. 4. Хроматограммы реакционных смесей, полученных при взаимодействии SeIV с GSH и Cys при эквимолярном соотношении концентраций SeIV и сульфгидрильных соединений 1:1:1 (а) и при концентрации Se, в 2 раза уменьшенной — 1: 2 : 2 (б)
Табл. 3. Распределение продуктов реакции Cys, GSH и Se в водных смесях при различных соотношениях реагентов
|
№ п/п |
Исходные реагенты, мM |
Состав продуктов, содержащих глутатион, % |
|||||
|
Se |
GSH |
Cys |
GSSG |
GS-Cys |
GSSeSG |
GS-Se-Cys |
|
|
1 |
3.33 |
3.33 |
3.33 |
2.0 |
14.3 |
37.9 |
45.8 |
|
2 |
1.66 |
3.33 |
3.33 |
2.5 |
31.4 |
31.8 |
34.3 |
|
3 |
0.83 |
3.33 |
3.33 |
32.0 |
28.5 |
16.4 |
23.1 |
|
4 |
0.33 |
3.33 |
3.33 |
5.1 |
68.6 |
16.6 |
9.8 |
С учетом вышеупомянутого из хроматографических данных было рассчитано содержание продуктов, содержащих GSH (табл. 3). Из представленных в таблице данных следует:
-
• содержание Se-дисульфидов с GSH (GS-Se-SG и GS-Se-Cys) сопоставимо между собой, но выше, чем соответствующих дисульфидов (GS-SG и GS-Cys);
-
• концентрация GS-Cys существенно превышает концентрацию GS-SG;
-
• соотношение концентраций обоих типов дисульфидов и Se-дисульфидов выравнивается при уменьшении концентрации в среде.
Для интерпретации полученного набора несимметричных продуктов, образующихся при одновременном взаимодействии с Se, были проведены специальные эксперименты для оценки возможности последующих превращений симметричных продуктов реакции с участием исходных сульфгидрильных соединений. Для этого первоначально была осуществлена реакция GSH c SeIV до полного превращения GSH в смесь окисленного глутатиона и его Se-дисульфида (рис. 5, а). Далее к реакционной среде, содержащей только продукты GS-SG и GS-Se-SG добавлялись в эквимолярных количествах либо GSH, либо Cys, либо их смесь в равных соотношениях. Хроматографический анализ полученных реакционных смесей после 2.5 ч инкубации представлен на рис. 5 (концентрации исходных реагентов и концентрации дополнительно вносимых в реакционную смесь сульфгидрильных соединений приведены в разделе "Материалы и методы").
Анализируя полученные результаты, представленные на рис. 5, можно отметить, что введение дополнительной порции GSH привело к дополнительному образованию GS-SG и GS-Se-SG (б), что указывает на достаточное количество SeO 2 в реакционной среде. Аналогичным образом продолжается реакция и при дополнительном введении смеси GSH и Cys (в). Однако при внесении одного Cys в реакционную среду в отсутствие GSH наблюдается исчезновение GS-Se-SG (10.1 мМ), и при этом образуется эквивалентное количество смешанного Se-дисульфида — GS-Se-Cys (9.5 мМ).
Таким образом, представленные выше эксперименты подтверждают наличие обменных процессов с участием Se-дисульфидов при наличии соединений со свободными сульфгидрильными группами со скоростями, сопоставимыми с образованием основных продуктов. При этом в процессе замещения
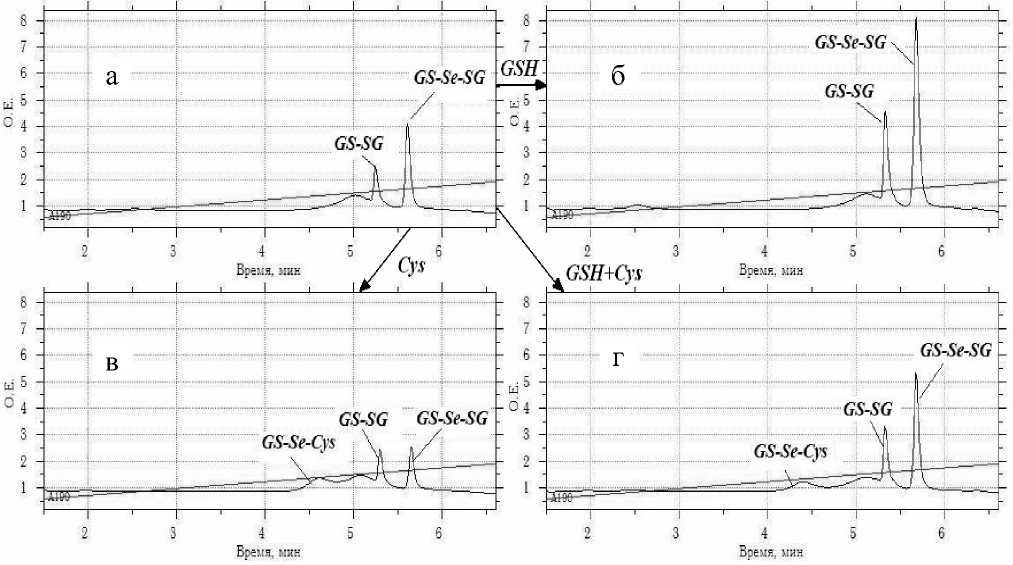
Рис. 5. Хроматограммы реакционных смесей до (а) и после дополнительного введения в реакционную среду GSH (б), Cys (в) и их смеси (г)
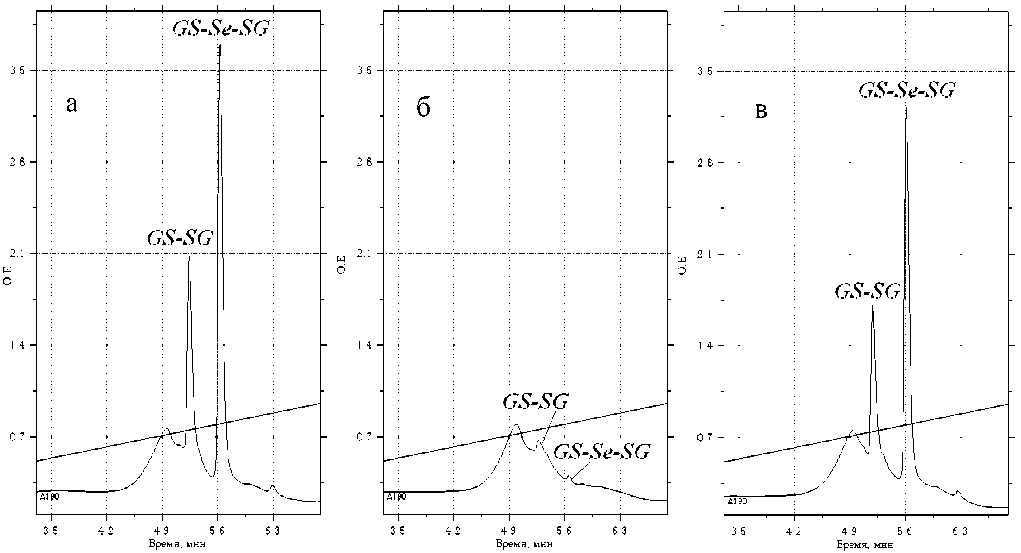
Рис. 6. Хроматограммы реакционных смесей при одновременном добавлении AgNO3 и Se к GSH (а) и при добавлении AgNO3 после взаимодействия GSH с Se
в симметричном Se-дисульфиде GS на Cys свободный GSH не регистрируется, поскольку он вступал бы в реакцию с SeO 2 с образованием тех же самых продуктов, которые имелись в реакционной среде до внесения Cys. В конечном итоге система через 2.5 ч приходит к некоторому равновесию, которое представлено набором продуктов, обозначенных на рис. 5, г.
Конкурентное взаимодействие сульфгидрильных групп глутатиона с селеном и ионами серебра
Как уже отмечалось выше, ряд биологически активных соединений и в том числе глутатион принимают активное участие в дезинтоксикациии, вызванной присутствием ионов тяжелых металлов. Такое действие может быть обусловлено взаимодействием с металлами сульфгидрильных групп GSH. Можно предположить, что и другие компоненты биологических сред, в том числе и селен, могут корректировать этот процесс. В связи с этим нами были проведены эксперименты по выяснению влияния ионов металлов на взаимодействие глутатиона с селеном на примере ионов серебра.
Эксперименты проводились следующим образом: в раствор со смесью селена и азотнокислого серебра добавлялся GSH. Далее реакционная смесь анализировалась с помощью ВЭЖХ по методике, описанной в предыдущем разделе. На рис. 6 представлены результаты хроматографии исследованных смесей; анализа хроматограмм — в табл. 4.
В экспериментах контролировалось образование двух продуктов: GS-SG и GS-Se-SG. Отметим, что ни хроматографически, ни масс-спектрометрически продукты GSH с ионами серебра не регистрируются, поскольку образование данного продукта приводит к потере растворимости GS-Ag.
Вместе с тем, как следует из результатов, представленных в табл. 4, при одновременном введении ионов серебра с продуктами реакции пропорционально уменьшается количество двух продуктов GS-SG и GS-Se-SG.
Введение ионов серебра после взаимодействия GSH с селеном не изменяет концентрации продуктов GS-SG и GS-Se-SG. Также было обнаружено, что ионы серебра не взаимодействуют с Se-дисульфидами.
ЗАКЛЮЧЕНИЕ
Таким образом, проделанные эксперименты свидетельствуют о том, что даже неферментативные реакции селена с глутатионом и цистеином представляют собой совокупность сложных процессов, приводящих к образованию набора продуктов, которые продолжают претерпевать изменения при изменении состава реакционной среды. Этим и обусловливается регуляция различных процессов, протекающих с участием GSH и Se
Табл. 4. Состав реакционных смесей после дополнительного введения азотнокислого серебра в концентрациях от 0 до 33 мM в реакционную среду, состоящую из 33 мM глутатиона и 33 мM селена
|
№ п/п |
AgNO3, мM |
GS-SG и GS-Se-SG |
GS-Ag, мМ |
|
|
мМ |
% |
|||
|
1 |
0 |
0.333 |
100 |
0 |
|
2 |
0.0165 |
0.32 |
96 |
0.013 |
|
3 |
0.0494 |
0.28 |
84 |
0.053 |
|
4 |
0.0825 |
0.25 |
76 |
0.083 |
|
5 |
0.165 |
0.08 |
23 |
0.253 |
|
6 |
0.333 |
0 |
0 |
0.333 |
|
7 |
0.333* |
0.333 |
100 |
0 |
Примечание. * — в течение 30 мин проведена прединкубация GSH c Se перед добавлением азотнокислого серебра.
в биологических средах, в которых активно участвует и ряд ферментов [4–6]. Отметим, что реальные биологические среды являются более многокомпонентными по набору соединений с сульфгидрильными группами. Они представлены как в белках и пептидах, так и в виде низкомолекулярных соединений, таких как гомоцистин, концентрация которого при ряде патологий существенно превосходит концентрацию GSH [7].
МАТЕРИАЛЫ И МЕТОДЫ
В работе были использованы вещества: глутатион восстановленный; глутатион окисленный; L-цистеин 99 % (Sigma); диоксид селена (ООО Вектон); муравьиная кислота (Merck); ацетонитрил (НПК Криохром).
Экспериментальные работы по разработке методики исследования влияния ионов тяжелых металлов и селена на биологические объекты проводились на приборе МХ-5310, оборудованном электрораспылительным источникам ионов (electrospray ionization, ESI) и времяпролетным масс-анализатором (TOF) с ортогональным вводом ионов, разработанным в Лаборатории биомедицинской масс-спектрометрии ИАнП РАН. Все спектры получены в режиме детектирования положительных ионов.
Хроматографию проводили на микроколоноч-ном жидкостном хроматографе Милихром А02 (Эконова, Новосибирск). Хроматографическая колонка размером 2 × 75 мм заполнена сорбентом Prontosil 120-5С18AQ (Bischoff, Германия). Элюцию осуществляли градиентом концентрации аце- тонитрила от 2 до 90 % (по объему) в растворе 0.25 % муравьиной кислоты со скоростью 100– 150 мкл/мин. При проведении анализа объем анализируемой пробы составлял 10 мкл, скорость подачи раствора образца — 2 мкл/мин. Площади пиков вычисляли, учитывая, что коэффициент молярной экстинкции глутатиона равен 1.5∙107.


