Исследование особенностей интеграции различных биоматериалов в мягких и костной тканях организма
Автор: Чернов Александр Владимирович, Ирьянов Юрий Михайлович, Радченко Степан Александрович, Чернов Владимир Федорович, Ирьянова Татьяна Юрьевна
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 1, 2012 года.
Бесплатный доступ
Проанализированы результаты клинического и экспериментально-морфологического исследования регенератов, формирующихся при замещении крупных дефектов брюшной стенки и большеберцовой кости в условиях применения имплантатов из различных биоматериалов. Показана хорошая перспектива использования сетчатых конструкций из никелида титана для успешного хирургического лечения данных заболеваний.
Биоматериалы, интеграция, имплантация, никелид титана, пролен, дефекты костей и брюшной стенки, хирургия
Короткий адрес: https://sciup.org/142121531
IDR: 142121531
Studying the integration features of different biomaterials in organism soft and bone tissues
The results of clinical and experimental-and-morphological studies of regenerated tissues being formed in filling large defects of abdominal wall and those of tibia under using implants of different biomaterials have been analyzed. Good perspectives have been demonstrated concerning the use of titanium nickelide grid constructions for successive surgical treatment of such diseases.
Текст научной статьи Исследование особенностей интеграции различных биоматериалов в мягких и костной тканях организма
Разработка и экспериментально-клиническое обоснование имплантационных технологий с целью восстановления ткани в области дефекта с использованием разнообразных биоматериалов — одно из наиболее актуальных направлений современной медицины [9, 11, 14]. Различные авторы определяют биоматериалы как «нежизнеспособные материалы, используемые для взаимодействия с биологической системой в медицинских целях» [5] или как фармацевтически инертные материалы, предназначенные для объединения с живыми системами организма, которые не обладают токсичными, иммуногенными и канцерогенными свойствами и не отторгаются как инородное тело [2, 13]. Биоматериалы значительно отличаются по своим механическим и физико-химическим свойствам, а также биоактивностью, биосовместимостью и биорезистентностью и используются с различной целью в зависимости от стоящей экспериментальной и клинической задачи [1, 4, 5, 6]. Эффективность применения различных имплантируемых в организм материалов и конструкций из них в значительной степени зависит от конкретных условий имплантации, морфо- функциональных особенностей живой ткани и механических характеристик используемого материала [8, 10, 12]. В настоящее время интенсивно развиваются медицинские технологии, связанные с применением имплантатов из никелида титана [3, 7, 8, 10]. В частности, авторами настоящей работы показано, что при имплантации тонких сетчатых конструкций из отечественного никелида титана формируется полноценная плотная соединительная ткань, замещающая дефект мышечно-апоневротического слоя брюшной стенки [3]. Отмечена хорошая приживаемость такого имплантата даже в условиях гнойной инфекции. Рядом авторов установлено, что механические свойства сплавов на основе никеля и титана приближаются к механическим характеристикам костной ткани и являются био-совместимыми [2, 4, 7, 8].
Цель настоящей работы — изучение особенностей формирования интегративного соединения при имплантации различных биоматериалов, используемых при замещении дефектов мягких и костной тканей, и анализ значения интеграции для разработки более совершенных имплантационных технологий.
МАТЕРИАЛ И МЕТОДЫ ИССЛЕДОВАНИЯ
В экспериментальных и клинических условиях исследовались имплантационные свойства ряда современных имплантационных материалов, биосовместимость которых доказана: политетрафторэтилен (PTFE) в форме пленки (24 опыта), реперен в виде часто перфорированной пленки (9 опытов), сетчатые импланта ты — пролен (24 опыта), тонкие проволочные имплантаты — титан ВТ-1.00 (12 опытов) и никелид титана ТН-10 (57 опытов). Данные имлантационные материалы и конструкции были отобраны как материалы с минимальными размерами по толщине пленки и калибру нити — от 60 до 200 мкм, но отличающиеся физико- техническими поверхностными характеристиками шероховатости, которые в случае титана и никелида титана приближаются к наноструктурированным.
Апробацию методики пластики дефектов мягких тканей проводили у экспериментальных животных: собак (32), кошек (9), кроликов (8), у которых с соблюдением правил асептики острым путем формировали дефекты в мышечно-апоневротическом слое брюшной стенки. В сформированные дефекты устанавливались указанные имплантаты. Имплантацию выполняли с фиксацией сеток одноименным шовным материалом. В 49 экспериментах имплантация дублировалась в однотипные участки брюшной стенки с соблюдением единой технологии эксперимента. У 25 крыс линии Вистар создавали дефекты в средней трети большеберцовой кости.
Биопсийный материал армированных имплантационных сегментов новообразованной соединительной ткани и большеберцовые кости изучали при помощи световой и сканирующей электронной микроскопии в ближайшем и отдаленном послеоперационном пе- риоде. Минеральный компонент костной ткани, формирующейся вокруг имплантата в дефекте кости, визуализировали при помощи электронно-зондового микроанализатора. Морфологические исследования у пациентов дополняли ультразвуковым сканированием (УЗИ) зоны имплантации. При этом изучалось смещение имплантата в ткани, изменение его формы, топографические взаимоотношения имплантата и окружающих тканей. Последовательные сроки наблюдения составили 1, 2, 3, 4 недели, 1, 3, 6 мес. и 1 год. Максимальные сроки наблюдения при имплантации титана ВТ–1.00, никелида титана (TiNi), пролена составили от 1,5 до 5 лет.
Исследования в гуманитарной клинике базируются на 412 клинических наблюдениях имплантации сетчатых конструкций из никелида титана ТН-10 и других материалов при крупных и гигантских дефектах брюшной стенки, в том числе 53 — в усло -виях тяжелого гнойного инфицирования брюшной стенки (эвентрации, перитониты, кишечные свищи, опухоли и др.).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Клинические наблюдения в раннем послеоперационном периоде отражают универсальную неспецифическую общую и местную тканевую реакцию организма на имплантацию биосовместимого инородного тела. В последующие сроки наблюдения результаты все больше зависят от свойств материала и конструктивных особенностей имплантата (рис. 1, 2).
Установлено, что в мягких тканях вокруг пленочных имплантатов формируется соединительнотканная капсула, в которой имплантат находится в свободном нефиксированном состоянии. Пленка из PTFE в любые сроки имплантации легко удаляется из капсулы, в которую она заключена.
Полимерные сетчатые имплантаты, образованные нитями с гладкой поверхностью, визуально неподвижны в рубце и фиксируются в новообразованной соединительной ткани за счет прорастания ее через ячейки конструкции, при этом, однако, остаются микрощели, заполненные экссудатом, в рубцовой ткани вокруг гладкой поверхности нити (рис. 3, а). Наблюдаются случаи скручивания имплантатов, что подтверждает их неполную фиксацию в живой ткани.
Значительно более плотная фиксация в мягких тканях отмечена при сетчатых имплантатах титана ВТ-1.00 и практически полное врастание сетки из нике-лида титана ТН-10 (рис. 3, б). Удаление всей конструкции и отдельных нитей этих материалов невозможно без разрыва ткани в зоне имплантации.
Морфологическое исследование при помощи методов УЗИ, световой и электронной микроскопии показало принципиальную разницу микроархитектоники новообразованной соединительной ткани при имплантации конструкций из материалов, обладающих различными характеристиками поверхности (рис. 1, 2, 3).
При использовании полимеров с поверхностью в виде сплошной пленки (PTFE) капсула вокруг имплантата всегда выражена, как и полость между им- плантатом и капсулой, и фиксация непосредственно на материале отсутствует.
При сетчатых конструкциях из имплантационного материала с полированной поверхностью (перфорированная пленка — реперен, сеть из полированных нитей — пролен) фиксирование элементов соединительной ткани наблюдается по типу обрастания конструкции в узлах переплетений (частичная интеграция). Однако на гладких участках материала рост соединительной ткани происходит по типу формирования капсулы с остаточной полостью в виде щели, содержащей экссудат, между имплантатом и живой тканью (рис. 4). Знакопеременная контракция армированной новообразованной соединительной ткани и «сморщивание» сетчатой полимерной конструкции могут привести к формированию общей сплошной капсулы вокруг всей конструкции или отдельных крупных сегментов имплантата.
При сетчатых проволочных имплантатах из титана ВТ-1.00 и никелида титана ТН-10, обладающих принципиально другой характеристикой поверхности (шероховатость, наноструктурированность) (рис. 5), рост соединительной ткани происходит с прочной фиксацией ее элементов на неровной поверхности, как отдельных фрагментов проволочного материала, так и всей конструкции (полная интеграция) (рис. 1, 2, 3).
Следует отметить полную интеграцию нике-лида титана в условиях инфицирования, независимо от степени контаминации и инфицирования раневого дефекта, тогда как другие полимерные имплантаты неизменно отторгались. При этом ни в одном случае не возникало необходимости удаления имплантата TiNi из инфицированной раны. Морфологические исследования показали, что присутствие данного имплантационного материала принципиально не осложняет процесс роста грануляционной ткани и формирование соединительнотканного рубца (см. рис. 1, 2).
Выполненными исследованиями показано, что при имплантации тонких сетчатых конструкций из никелида титана с наноструктурированной поверхностью в дефект большеберцовой кости в необычно ранние сроки (на 7-е сутки после операции) вокруг конструкций импланта- та формируются трабекулы новообразованной костной ткани, и замещение дефекта осуществляется по типу первичного заживления костных ран. При этом образуется плотное остеоинтегративное соединение материала имплантата с костной тканью регенерата (рис. 6).
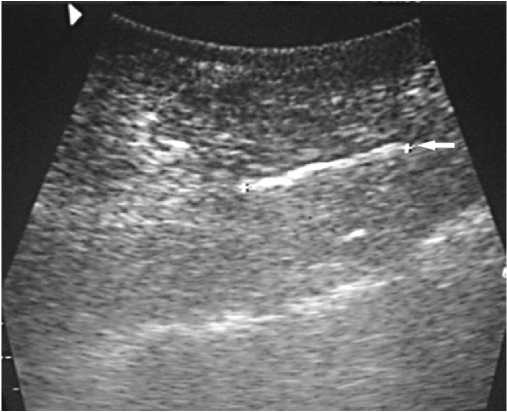
Рис. 1. Сонограмма брюшной стенки пациента А. через 3 месяца после закрытия дефекта путем имплантации сетчатой конструкции из никелида титана подтверждает неосложненный характер поведения имплантата. Отсутствие отека, скоплений тканевой жидкости в слоях брюшной стенки свидетельствует о полной интеграции имплантата (стрелка). Инкапсуляция имплантата не визуализируется
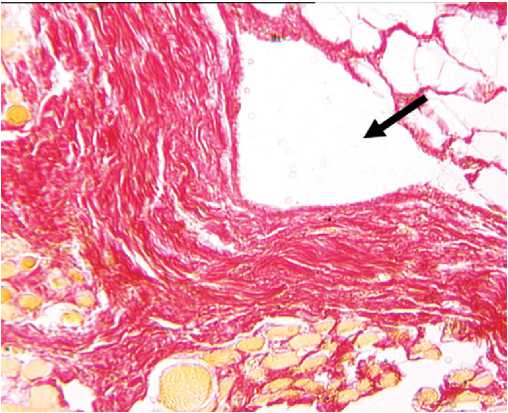
Рис. 2. Парафиновый срез брюшной стенки пациента А. через 3 месяца после имплантации сетчатой конструкции из никелида титана. Имплантат перед заливкой в парафин удален, вследствие чего на месте локализации элемента конструкции имплантата образовался округлый дефект неправильной формы (стрелка). Волокна новообразованной соединительной ткани имеют циркулярноконцентрическую ориентацию, огибают структуры имплантата и плотно фиксируются к его поверхности без формирования выраженной капсулы и признаков воспалительно-клеточной инфильтрации. Окраска пикрофуксином по Ван-Гизону. Увеличение 6,3×10
100МКГП
а

Рис. 3. Стереоультраструктурные особенности структур новообразованной соединительной ткани, армированной сетчатым имплантатом из пролена (а) и никелида титана (б), у пациента А. через 1 месяц после операции закрытия дефекта брюшной стенки. Вокруг конструкций имплантатов формируются муфтообразные пласты циркулярно ориентированных пучков коллагеновых волокон различной толщины с плотной фиксацией к поверхности материала, изготовленного из никелида титана (б), и частичной фиксацией, с образованием капсулы, заполненной экссудатом (стрелка), в случае использования конструкций из пролена (а). Сканирующая электронная микроскопия
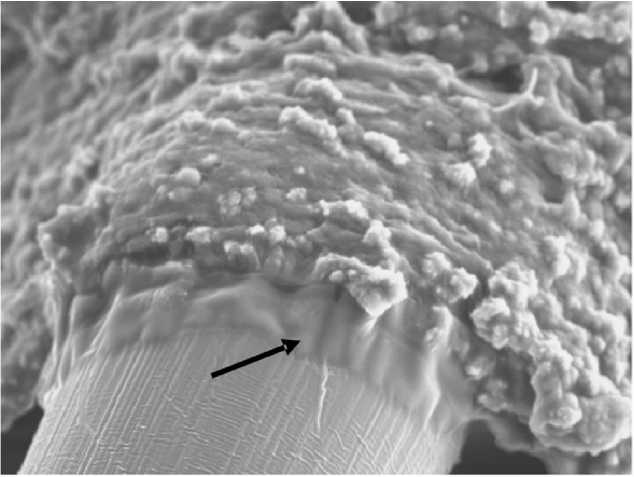
Рис. 4. Формирование капсулы с остаточной полостью, содержащей аморфное вещество экссудата (стрелка) вокруг поверхности элемента имплантата из нитей пролена, у пациента А. через 1 месяц после операции закрытия дефекта брюшной стенки. Сканирующая электронная микроскопия

ЮОмкт

Рис. 5. Микрорельеф поверхности конструкций (нитей) имплантата из никелида титана (а) и пролена (б) через 1 месяц после операции замещения дефекта брюшной стенки. Сканирующая электронная микроскопия

70мкт
Рис. 6. Крупные функционально активные остеобласты (белые стрелки), формирующие костную ткань остеоинтегративного соединения (черные стрелки) на поверхности имплантата из никелида титана в зоне дефекта большеберцовой кости крысы через 7 суток после операции. Сканирующая электронная микроскопия коррозионного препарата
Установлено, что полимерные имплантаты оказались неспособными к интеграции в условиях открытой раны, инфицирования, гнойного воспаления, и, кроме того, из-за неизбежного повреждения полимеров при использовании антисептиков, содержащих активный кислород, хлор или йод.
Безусловно, характер и интенсивность интеграционных процессов, неизбежно возникающих при имплантации, в конечном итоге являются результатом взаимодействия пластического материала и живой ткани, активность которой проявляется в росте соединительной ткани в ответ на имплантацию. Таким образом, «приживление» имплантата – это результат не только биохимической и биомеханической совместимости, но и интеграции всей имплантационной конструкции в живую ткань.
В свете полученных нами данных следует определить понятие «биосовместимость поверхности имплантационного материала» как адекватность и ее соразмерность элементам растущей и сформированной живой ткани. Являясь своеобразной армирующей основой для вновь образованной живой ткани, имплантационный материал должен создавать благоприятные условия для фиксации и роста элементов новообразованной соединительной ткани. От того, насколько прочно фиксированы элементы конструкции к живой ткани, зависит надежность интеграции и судьба всей имплантации. В свою очередь, прочность фиксации имплантированной конструкции прямо связана с поверхностью материала.
В целом считаем необходимым выделить следующие факторы, связанные с конструкцией имплантата, которые определяют его интегративную способность:
-
1. Общий объем имплантационного материала.
-
2. Общая площадь поверхности имплантационной конструкции.
-
3. Биосовместимость поверхности имплантационного материала.
-
4. Биомеханическая совместимость имплантационной конструкции и ее элементов.
-
5. Трехмерность конструкции.
Интеграция имплантационной конструкции может быть полной или частичной, в зависимости от прочности фиксации элементов имплантата в ткани.
При сплошной пленочной структуре интеграция имплантата отсутствует, наблюдается инкапсуляция всего биосовместимого материала как инородного тела. При сетчатой конструкции имплантата степень интеграции (от частичной до полной интеграции) зависит от биосовместимости поверхности имплантационного материала.
Подтверждением значения интеграционной способности имплантационной конструкции служит использование сетчатой конструкции из никелида титана ТН-10 в условиях гнойного воспаления. Данный материал и плетеная трехмерная конструкция обеспечивают надежное приживление и замещение крупных дефектов мягких и костной тканей, осложненных гнойной инфекцией, за счет прорастания имплантата новообразованной соединительной тканью без признаков отторжения при одновременном устранении гнойного процесса. Максимально полная интеграция при высокой физико-химической устойчивости материала имплантата в агрессивной среде является ключевым фактором заживления инфицированной раны, армированной имплантатом.
ВЫВОДЫ
-
1. Интегративная способность имплантата, т.е. способность имплантационного материала и конструкции формировать комплекс «живая ткань–имплантат» как единый армированный участок соединительной ткани, является важнейшим фактором, условием и индикатором качества «приживления» имплантата в живой ткани.
-
2. Степень интеграция имплантата в живую ткань зависит от биосовместимости поверхности
-
3. Свойством приживления в инфицированной ране обладают только имплантационные материалы, способные к полной интеграции в живую ткань.
имплантационного материала, которая должна быть адаптирована к росту и прочной фиксации новообразованной ткани на всех стадиях ее формирования.


