Исследование острой токсичности кормовой добавки «Комплисорбин» на белых крысах
Автор: Мишина Н.Н., Семенов Э.И., Алеев Д.В., Галяутдинова Г.Г., Валиев А.Р., Ганиев И.М., Ерохондина М.А.
Журнал: Вестник Омского государственного аграрного университета @vestnik-omgau
Рубрика: Ветеринария и зоотехния
Статья в выпуске: 1 (53), 2024 года.
Бесплатный доступ
Цель исследования - изучение острой токсичности кормовой добавки «Комплисорбин» (смесь шунгита, цеолита, лигнина и глюкана) на белых крысах. Для оценки острой токсичности изучено действие данной добавки при внутрижелудочном введении, поскольку пероральный путь введения является терапевтическим применением препарата и планируется в клинических исследованиях. Введение осуществляли однократно животным, лишенным корма (на промежуток времени не менее 8 ч), но со свободным доступом к воде. Объем введения, навески препарата взвешивали отдельно и рассчитывали индивидуально для каждого животного, основываясь на массе тела, зарегистрированной непосредственно перед введением вещества. Доступ к корму возобновляли через час после введения. Определение параметров острой токсичности проводилось с использованием метода Кербера. Были использованы крысы с массой тела 190-210 г, которые были разделены на 5 групп по 12 особей в каждой (6 самок и 6 самцов). Диапазон исследуемых доз кормовой добавки «Комплисорбин» составлял 2000, 3000, 4000 и 5000 мг/кг массы тела. Ввиду особенностей препарата (низкая растворимость в воде, низкая насыпная плотность, объемность) введение порошка в виде болюса более чем 5000 мг/кг массы тела не представлялось возможным. Контрольной группе крыс внутрижелудочно вводили однократно растворитель - дистиллированную воду в объеме 5 мл. В ходе проведенных исследований доказано, что однократное внутрижелудочное введение кормовой добавки «Комплисорбин» в дозах 2000, 3000, 4000, 5000 мг/кг массы тела не оказывало отрицательного воздействия на клинический статус, массу тела и гематологические показатели крови животных. В результате морфометрического анализа, макро- и микроскопического исследования внутренних органов животных летальная доза не установлена. Максимальная доза введения кормовой добавки составила 5000 мг/кг, что позволяет отнести кормовую добавку «Комплисорбин» к веществам 4 класса опасности - малоопасные вещества согласно ГОСТ 12.1.007-76.
Кормовая добавка «Комплисорбин», шунгит, цеолит, глюкан, лигнин, белые крысы, острая токсичность
Короткий адрес: https://sciup.org/142240552
IDR: 142240552 | УДК: 619:615.9:636.5
The study of acute toxicity of the feed additive “Complisorbin on white rats
The aim of the study was to investigate the acute toxicity of the Complisorbin feed additive (a mixture of shungite, zeolite, lignin and glucan) on white rats. To assess acute toxicity, the effect of this drug when administered intragastrically was studied, since the oral route of administration is the therapeutic use of the drug and is planned in clinical trials. The introduction was carried out once, animals deprived of food (for a period of time not less than 8 hours) with free access to water. The volume of administration, the preparation portions were weighed separately and calculated individually for each animal, based on the body weight recorded immediately before the administration of the substance. Access to food was resumed one hour after administration. Acute toxicity parameters were determined using the Kerber method. In the present study, we used rats weighing 190-210 g divided into 5 groups of 12 animals (6 females and 6 males). The range of studied doses of the Complisorbin feed additive was 2000, 3000, 4000 and 5000 mg/kg of body weight. Due to the characteristics of the drug (low solubility in water, low bulk density, volume), the administration of the powder in the form of a bolus of more than 5000 mg/kg body weight in rats was not possible. The control group of rats was injected intragastrically once with a solvent - distilled water in a volume of 5 ml. In the course of the studies, it was proved that a single intragastric administration of the Complisorbin feed additive at doses of 2000, 3000, 4000, 5000 mg/kg did not adversely affect the clinical status, body weight and hematological blood parameters of animals. As a result of morphometric analysis, macro- and microscopic examination of the internal organs of animals, the lethal dose has not been established. The maximum dose of the feed additive was 5000 mg/kg, which makes it possible to classify the feed additive “Complisorbinˮ to substances of hazard class 4 - low-hazard substances according to GOST 12.1.007-76.
Текст научной статьи Исследование острой токсичности кормовой добавки «Комплисорбин» на белых крысах
Микотоксины представляют собой вторичные метаболиты мицелиальных грибов и оказывают политоксическое действие на здоровье человека и животных, в том числе через продукцию животного происхождения, такую как мясо, молоко и яйца [1; 2]. Зерновые культуры в сельскохозяйственной практике могут быть заражены микотоксинами во время сбора урожая, транспортировки, переработки и хранения [3; 4]. Уже известно около 200 видов мицелиальных грибов, продуцирующих микотоксины, среди которых наиболее распространенными и токсическими являются афлатоксин В1, фумонизин B1, Т-2 токсин, ДОН и зеараленон [5–7]. Для снижения действия микотоксинов применяют множество способов, но метод энтеросорбции остается наиболее экономичным, не ухудшающим питательного качества корма, безвредным для организма животных и птицы [8–12].
Ранее нами было доказано, что использование поликомпонентного сорбента «Ком-плисорбин» при полимикотоксикозе белых крыс снижает токсическое действие токсинов на печень и другие внутренние органы-мишени [13].
Обязательной процедурой при разработке новых кормовых добавок является проведение доклинических испытаний для объективной оценки безвредности, наличия и обратимости токсических действий на органы и ткани, установления безопасной дозы применения [14].
Цель исследования – изучение острой токсичности кормовой добавки «Комплисор-бин» на белых крысах.
Объекты и методы
Работа проведена в условиях вивария ФГБНУ «ФЦТРБ-ВНИВИ». Объект исследования – кормовая добавка «Комплисорбин» на основе шунгита, цеолита, лигнина и глюкана, представляющая собой порошок темно-серого цвета. Кормовую добавку вводили однократно внутрижелудочно в виде водной взвеси белым крысам после 8-часового голодания. Каждому животному дозу введения рассчитывали индивидуально в зависимости от массы тела. Диапазон исследуемых доз составлял 2000, 3000, 4000 и 5000 мг/кг массы тела. Через час после введения животные получали свободный доступ к воде и корму. Определение параметров острой токсичности проводилось с использованием
Vestnik of Omsk SAU, 2024, no.1 53)
VETERINARY AND ZOOTECHNY метода Кербера. Для проведения эксперимента сформировали 5 групп крыс по 12 животных в каждой, внутри группы было равное количество самцов и самок. Контрольным животным в эквивалентном объеме вводили растворитель препарата – дистиллированную воду.
Схема эксперимента представлена в табл. 1.
Таблица 1
Схема эксперимента
|
Группа |
2 1 |
3 1 |
4 |
5 |
|
|
Рацион |
Кормовая добавка «Комплисорбин» |
Дистиллированная вода |
|||
|
доза 2000 мг/кг |
доза 3000 мг/кг |
доза 4000 мг/кг |
доза 5000 мг/кг |
||
|
Количество животных, голов |
2 |
2 |
2 |
2 |
2 |
Наблюдение за животными для выявления отклонений в состоянии здоровья и летальных исходов проводили один раз в день непосредственно перед введением препарата. При осмотре отмечали внешний вид животных, поведение каждой особи, состояние экскрементов и др. При обнаружении отклонений проводили подробный клинический осмотр.
Крыс взвешивали перед введением препаратов и в соответствии с запланированными исследованиями на весах «Ньютон» для лабораторных животных. Масса тела регистрировалась непосредственно перед введением препарата для расчета объема введения, далее на 14-е сут.
Ректальная температура регистрировалась непосредственно перед первым введением препарата, далее 1 раз в 3 дня с помощью медицинского термометра «Little Doctor».
На 14-е сут проводили эвтаназию животных и забор крови для изучения гематологических показателей (лейкоциты, лимфоциты, моноциты, гранулоциты, эритроциты, гемоглобин, средний объем эритроцита, среднее содержание гемоглобина в эритроците, средняя концентрация гемоглобина в одном эритроците, тромбоциты, тромбокрит) с помощью гематологического анализатора Mythic 18 Vet.
Патоморфологическое исследование включало некропсию, макроскопическое исследование, взвешивание внутренних органов. Парные органы взвешивали вместе, однако если присутствовали аномалии в массе или размерах, парные органы взвешивали отдельно. Массовые коэффициенты внутренних органов рассчитывали как отношение массы органа к массе тела (г/кг).
Обработку данных проводили с вычислением среднего арифметического (М) и ошибки среднего значения (m) с использованием критерия t-Стъюдента. Различия считали достоверными при уровне значимости р < 0,05.
Результаты исследований
В течение 30 мин после введения кормовой добавки «Комплисорбин» в дозах от 2000 до 5000 мг/кг при выполнении клинического осмотра у всех подопытных крыс отмечали незначительное понижение поведенческой активности, сохранение мышечного тонуса и двигательной активности, адекватную реакцию на звук и свет, взъерошен-ность шерсти, отсутствие функциональных нарушений в пищеварительной и мочевыделительной системе. Изменение психоэмоциональной возбудимости, вероятно, было связано с проведением манипуляций и объемом принудительно вводимых веществ. В последующие два часа происходило улучшение общей клинической картины и возвращение к показателям референтных значений, которые не имели отличий от биологического контроля.
По результатам наблюдения установлена 100%-ная выживаемость исследуемых крыс, живая масса всех крыс прибавилась синхронно и находилась в пределах нижней
Vestnik of Omsk SAU, 2024, no.1 53)
VETERINARY AND ZOOTECHNY границы и средних значений норм веса крыс данного возраста (рис. 1). Исходя из этого, можно заключить, что ни одна доза «Комплисорбина» не привела к гибели крыс, явным признакам интоксикации и снижению живой массы.
Грамм
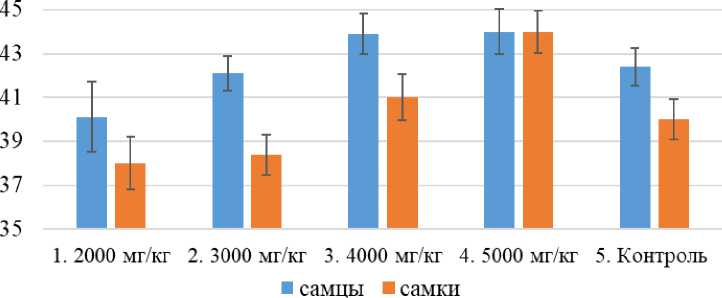
Рис. 1. Данные прироста живой массы белых крыс на 4сут эксперимента, г (М ± m) (n = 2)
При 95%-ном уровне вероятности не было достоверных отличий между опытом и контролем.
Не было зарегистрировано достоверного изменения ректальной температуры белых крыс, которым вводили различные дозы кормовой добавки, в сравнении с показателями контрольных животных.
Данные гематологических исследований представлены в табл. 2.
Таблица 2
Гематологические показатели крыс при внутрижелудочном введении кормовой добавки «Комплисорбин» на 14-й день исследования, (M ± m)
|
Пол |
Лейкоциты, × 03/мкл |
Эритроциты, × 06 /мкл |
Гемоглобин, г/л |
Тромбоциты, × 03/мкл |
Лимфоциты, % |
Моноциты, % |
|
1 группа |
||||||
|
Самцы |
3,0 ± 0,4 |
8,9 ± 0, |
30,0 ± 0,9 |
59 ,3 ± 6 ,7 |
60,4 ± 2,4 |
,7 ± 0, |
|
Самки |
3,2 ± 0,3 |
8,9 ± 0, |
34,7 ± ,5 |
523, ± 87,4 |
6 ,8 ± 2,7 |
, ± 0, |
|
2 группа |
||||||
|
Самцы |
3,2 ± 0,4 |
8,8 ± 0,3 |
35,8 ± 2,4* |
584,5 ± 79, |
63,0 ± 3,0 |
,8 ± 0, |
|
Самки |
3,6 ± 0,3 |
9, ± 0,3 |
36,2 ± 2,6 |
593,2 ± 78, |
63,5 ± 3,0 |
0,9 ± 0, |
|
3 группа |
||||||
|
Самцы |
2,6 ± 0,3 |
9,7 ± 0,2 |
27,6 ± 3, |
420,0 ± 82,7 |
59,7 ± 2,4 |
,6 ± 0, |
|
Самки |
2,7 ± 0,4 |
9,4 ± 0,2* |
35,6 ± 3,2 |
482,5 ± 54,4 |
6 , ± 2,4 |
, ± 0, |
|
4 группа |
||||||
|
Самцы |
2,8 ± 0,3 |
9, ± 0,2 |
34, ± 2,7 |
570,7 ± 67,6 |
60, ± 2,3 |
,3 ± 0, * |
|
Самки |
3, ± 0,4 |
9,2 ± 0, * |
33,8 ± 2,6 |
620,4 ± 68,0 |
6 ,3 ± 2,5 |
,4 ± 0,2 |
|
5 группа |
||||||
|
Самцы |
2,9 ± 0,5 |
9,0 ± 0, |
32,2 ± ,2 |
636,3 ± 66,3 |
60,7 ± 2,8 |
,4 ± 0, * |
|
Самки |
3,0 ± 0,6 |
8,9 ± 0, |
33,0 ± 2,2 |
596,4 ± 66, |
6 ,3 ± 2,6 |
,5 ± 0,2 |
*р < 0,05 по сравнению с контролем (группа 5)
Vestnik of Omsk SAU, 2024, no.1 53)
VETERINARY AND ZOOTECHNY
При анализе результатов морфологических исследований крови зарегистрировали повышение гемоглобина на 4% у самок крыс из 1 группы, эритроцитов на 6% и 4% у самок из 3 и 4 групп.
В результате вскрытия не было зафиксировано макроскопических изменений органов животных из всех групп.
Влияние введения различных доз кормовой добавки «Комплисорбин» на массовые коэффициенты органов представлено на рис. 2 и 3.
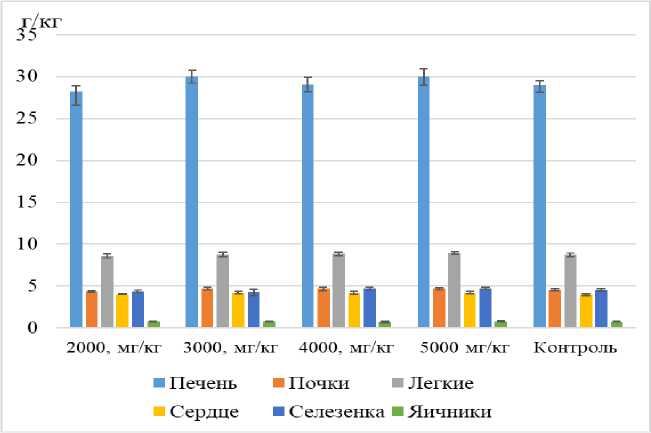
Рис. 2. Массовые коэффициенты органов самок крыс на 4-й день эксперимента (г/кг) (М ± m) (n = 2)
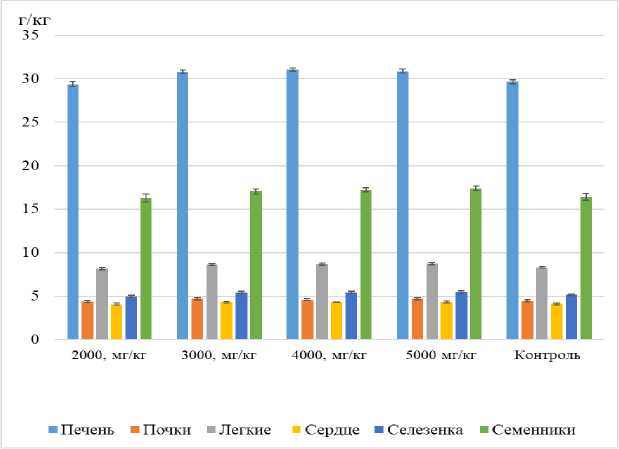
Рис. 3. Массовые коэффициенты органов самцов крыс на 4-й день эксперимента (г/кг) (М ± m) (n = 2)
Исходя из данных рис. 2 и 3, у самцов и самок белых крыс при введении различных доз кормовой добавки «Комплисорбин» не было достоверных различий показателей массовых коэффициентов внутренних органов по сравнению с данными контроля.
Vestnik of Omsk SAU, 2024, no. 1 53) VETERINARY AND ZOOTECHNY
Таким образом, при однократном внутрижелудочном введении в дозах от 2000 до 5000 мг/кг живой массы кормовая добавка «Комплисорбин» не вызывала гибели животных и не оказывала отрицательного влияния на клинико-гематологические показатели, массу тела, макроскопическую картину вскрытия. Вследствие того, что исследуемые дозы не вызывали гибели крыс, среднесмертельная доза средства не была определена.
Заключение
Таким образом, при однократном внутрижелудочном введении крысам кормовой добавки «Комплисорбин» в дозах от 2000 до 5000 мг/кг массы тела не наблюдалось отрицательного воздействия на общее состояние животных, массу тела, гематологические показатели и массовые коэффициенты внутренних органов. В результате морфометрического анализа и макроскопического исследования внутренних органов животных летальная доза не установлена. Максимальная доза введения кормовой добавки – 5000 мг/кг. Выявленные факты позволяют отнести средство «Комплисорбин» к веществам 4 класса опасности – малоопасные вещества согласно ГОСТу 12.1.007–76.
Список литературы Исследование острой токсичности кормовой добавки «Комплисорбин» на белых крысах
- Семенов Э.И. Фармако-токсикологические аспекты применения энтеросорбентов при сочетанных микотоксикозах: дис. … канд. биол. наук: 06.02.02 / Семенов Эдуард Ильясович. Казань, 2019. 342 с.
- Мишина Н.Н. Профилактическая эффективность лигнин- и полисахаридсодержащих энтеросорбентов при сочетанном Т-2 токсикозе: авто-реф. дис. … канд. биол. наук: 16.00.04 / Мишина Наиля Наримановна. Казань, 2009. 24 с.
- Микологическая статистика загрязненности кормов по отдельным районам Поволжья / Р.М. Потехина [и др.] // Вестник Марийского государственного университета. Серия: Сельскохозяйственные науки. Экономические науки. 2019. Т. 5, № 2(18). С. 197–203. DOI 10.30914/2411-9687-2019-5-2-197-203.
- Comparative Toxicity Assessment of Soil Fungi Isolated from Black Sea Coasts / R.M. Potekhina [et al.] // BioNanoScience. 2020. Vol. 10, No 3. P. 799-806. DOI 10. 1007/s12668-020-00745-x.
- Секвестранты микотоксинов: избирательность действия и побочные эффекты / Т.В. Герунов [и др.] // Вестник Омского государственного аграрного университета. 2022. № 2(46). С. 79–84.
- Jones F.T. Understanding and Coping with Effects of Mycotoxins in Livestock Feed And Forage / F.T. Jones [et al.] // North Carolina Cooperative Extension Service: Raleigh, NC, USA. 2007.
- Влияние Т-2 токсина и зеараленона на содержание белков теплового шока в первичных культурах клеток печени / А.И. Самсонов, А.Р. Макаева, Р.С. Мухаммадиев [и др.] // Ветеринарный врач. 2023. № 3. С. 22–29. DOI 10.33632/1998-698X_2023_3_22.
- Герунова Л.К. Углеродные сорбенты как секвестранты микотоксинов и инфекционных агентов // Каталог научных и инновационных разработок ФГБОУ ВО Омский ГАУ: сборник статей. Омск: Омский государственный аграрный университет имени П.А. Столыпина, 2022. С. 340–341.
- Галяутдинова Г.Г., Маланьев А.В., Егоров В.И. Диагностика, поиск средств лечения и профилактика сочетанного отравления крупного рогатого скота пестицидами и микотоксином // Вопросы нормативно-правового регулирования в ветеринарии. 2020. № 1. С. 218–219.
- Алеев Д.В. Изыскание методов обезвреживания кормов, контаминированных сочетанно микотоксинами – афлатоксином В1, охратоксином А и Т-2 токсином: дис. … канд. биол. наук: 16.00.04 / Алеев Дамир Вазыхович. Казань, 2003. 136 с.
- Zeolite, hepatoprotector and probiotic for aflatoxicosis in pigs international / L. Matrosova [et al.] // International Journal of Mechanical and Production Engeneering Research and Development (IJNPERD). 2020. Vol. 10. P. 7053-7060.
- Перфилова К.В., Мишина Н.Н., Семенов Э.И. Обоснование компонентного состава комплексного средства «Цеапитокс» в отношении Т-2 токсина в опытах in vitro // Ученые записки Казанской государственной академии ветеринарной медицины им. Н.Э. Баумана. 2021. Т. 247, № 3. С. 208–212.
- Экспериментальное обоснование использования поликомпонентного сорбента для детоксикации печени от микотоксинов / Н.Н. Мишина [и др.] // Вестник Омского государственного аграрного университета. 2023. № 1(49). С. 114–121. DOI 10.48136/2222-0364_2023_1_114.
- Руководство по проведению доклинических исследований лекарственных средств. Часть первая / под ред. А.Н. Миронова. М.: Гриф и К, 2012. 944 с.


