Исследование поведения моногидрата пероксипентафторотанталата калия при нагревании
Автор: Маслобоева С.М., Макаров Д.В., Нестеров Д.П., Тихомирова Е.Л.
Журнал: Вестник Мурманского государственного технического университета @vestnik-mstu
Статья в выпуске: 1 т.12, 2009 года.
Бесплатный доступ
Исследовано поведение моногидрата пероксипентафторотанталата калия при нагревании в атмосфере воздуха. Рассчитаны тепловые эффекты процессов обезвоживания и разложения. Изучена кинетика обезвоживания моногидрата пероксипентафторотанталата калия. Показано, что процесс протекает в диффузионно-кинетической области. В интервале температур 140-170°С рассчитаны кажущиеся константы скорости.
Короткий адрес: https://sciup.org/14294012
IDR: 14294012 | УДК: 546.883.05
Research of behaviour of the potassium peroxypentofluorotantalate monohydrate at heating
The behaviour of the К2ТаО2F5 H2O potassium peroxypentofluorotantalate monohydrate heated in air has been considered. Thermal effects of dehydration and decomposition processes have been calculated. The kinetics of potassium peroxypentofluorotantalate monohydrate dehydration has been studied. The process has been shown to occur in the diffusion-kinetic area. The apparent rate constants have been calculated for the temperature range of 140-170°С.
Текст научной статьи Исследование поведения моногидрата пероксипентафторотанталата калия при нагревании
Тантал и его соединения, благодаря своим уникальным свойствам, находят применение в различных областях – электронике, твердых сплавах и суперсплавах, химическом оборудовании и др. Танталовые порошки широко используются для изготовления конденсаторов небольших размеров с большой емкостью ( Колосов и др ., 2003).
Одним из распространенных способов получения металлического тантала является его натриетермическое восстановление из гептафторотанталата калия К 2 TaF 7 ( Колосов и др. , 2003). Вместе с тем, остается актуальной задача получения конденсаторных порошков со стабильными параметрами из других высокочистых соединений тантала, например, из моногидрата пероксипентафторотанталата калия К 2 ТаO 2 F 5 ⋅ H 2 O.
Целью настоящей работы являлось исследование термических свойств К 2 ТаO 2 F 5 ⋅ H 2 O.
Синтез К 2 ТаO 2 F 5 ⋅ H 2 O осуществляли из высокочистых фторидных танталсодержащих растворов (реэкстрактов), полученных при экстракционной переработке танталового сырья. Растворы содержали, г/л: Ta 2 O 5 – 119, HF – 110. При проведении укрупненных опытов брали 5 л исходного раствора, который нагревали до 70ºС и вводили 500 мл 30 %-ного Н2О2. Отдельно нагревали до 70ºС раствор KCl (300 г/л) и добавляли его в исходный раствор в количестве, соответствующем 120 % от стехиометрии. Охлаждение вели со скоростью 10-15 град/ч. Полученную смесь отфильтровывали. Осадок К 2 ТаO 2 F 5 ⋅ H 2 O сушили на воздухе в течение 6-8 часов.
Дифференциально-термические (ДТА) и термогравиметрические исследования (ТГА) выполнены на дериватографе Q-1500D (Венгрия) в воздушной атмосфере. Применяли динамический и квазиизотермический режимы.
Рентгенофазовый анализ (РФА) продуктов реакции проводили на дифрактометре ДРОН-2, излучение Cuk α .
ИК спектроскопические исследования выполнены на спектрометре Specord M 80.
Микрографический анализ продуктов синтеза проведен с помощью цифровой сканирующей электронной микроскопии (СЭМ) на микроскопе SEM LEO-420 (Германия).
3. Результаты и их обсуждение
Микрографическое представление кристаллов К2ТаO2F5 ⋅ H2O показано на рис. 1. Кристаллы крупные, имеют пластинчатый облик. По данным кристаллооптических исследований, продукт однофазен, анизотропен, характеризуется показателем преломления N ср = 1.450.
Маслобоева С.М. и др. Исследование поведения моногидрата…

Рис. 1. Пластинчатые кристаллы К 2 ТаO 2 F 5 ⋅ H 2 O. Снимок на СЭМ
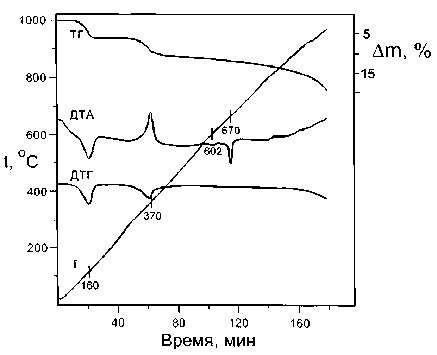
Рис. 2. Дериватограмма соединения К2ТаO2F5 ⋅ H2O. Динамический режим, воздушная атмосфера, скорость нагрева 5 град. ⋅ мин 1
Проведен комплексный термический анализ К2ТаO2F5 ⋅ H2O. На рис. 2 представлена типичная дериватограмма соединения. На кривой ДТА зафиксированы три эндотермических эффекта при температурах 160, 602 и 670ºС и один экзотермический эффект при 370ºС.
Съемка в квазиизотермическом режиме позволила уточнить температуры эффектов, сопровождающиеся потерей массы образца. Установлено, что в интервале 140-200ºС происходит удаление воды с образованием безводного соединения K2TaO2F5, которое остается устойчивым до ~370ºС. Это подтверждено данными РФА, а также ИК спектроскопии.
Потеря воды К2ТаO2F5 ⋅ H2O происходит по схеме:
К 2 ТаO 2 F 5 ⋅ H 2 O = K 2 TaO 2 F 5 + H 2 O.
При 370ºС наблюдается экзотермический эффект (рис. 2), сопровождаемый разложением K 2 TaO 2 F 5 с образованием двух фаз: K 3 TaOF 6 и K 2 Ta 2 O 3 F 6 , последнее из которых – соль Мариньяка. ИК спектр образцов (рис. 3), выдержанных при температурах 370-650ºС, свидетельствует об образовании соли Мариньяка. Фаза K 3 TaOF 6 диагностируется неуверенно из-за наложения полос.
Аналогичные фазы получены при прокаливании исходного соединения при 450ºС в вакууме.
Кристаллооптические исследования подтвердили наличие двух фаз, при этом облик исходных кристаллов сохранен, но кристаллы теряют прозрачность и становятся матовыми.
Можно предположить, что разложение K2TaO2F5 происходит по реакции:
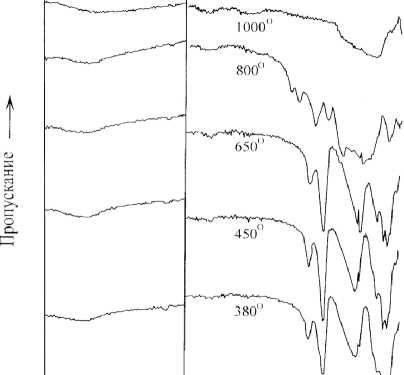
3600 3200 1600 1200 800 400
V, см"1
Рис. 3. ИК спектры продуктов нагревания К 2 ТаO 2 F 5 ⋅ H 2 O
4K 2 TaО 2 F 5 = 2K 3 TaOF 6 + K 2 Ta 2 O 3 F 6 + F 2 O + O 2 . (2)
По данным РФА выдержка образца К 2 ТаO 2 F 5 ⋅ H 2 O при температуре 800ºС в течение двух часов в воздушной атмосфере приводит к образованию смеси фаз K 3 TaO 2 F 4 , K 6 Ta 6,5 O 14,5 F 9,5 и KTaO 3 , а при температуре 1000ºС формируется фаза KTaO 3 (рис. 3). Последняя диагностируется по ИК спектру (широкая полоса поглощения в области 600 см-1).
Наблюдаемые по данным ТГА экспериментальные потери массы близки к расчетным (для процессов (1) и (2) 4.5 и 5.6 % соответственно).
По кривым ДТА были рассчитаны тепловые эффекты процессов потери воды (1) и разложения К 2 ТаO 2 F 5 (2). В качестве реперного вещества для построения калибровочной кривой использовали КСl квалификации о.с.ч. Тепловые эффекты составили для процесса (1) 12.8 кДж/моль, для процесса (2) – 16.2 кДж/моль.
Нами также проведено изучение кинетики обезвоживания моногидрата пероксипентафторотанталата калия, как наиболее важной с прикладной точки зрения стадии.
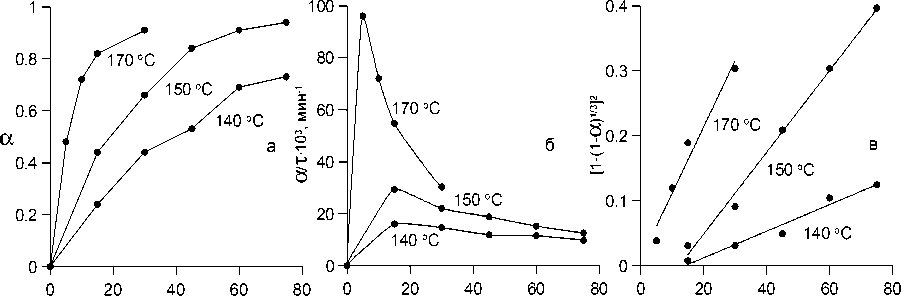
τ , мин. τ , мин τ , мин
Рис. 4. Зависимость степени (а) и скорости (б) потери воды К 2 ТаO 2 F 5 ⋅ H 2 O от времени и кинетические кривые процесса в координатах [1 – (1 – α )1/3]2 – τ (в)
Рис. 4а иллюстрирует степень потери воды К 2 ТаO 2 F 5 ⋅ H 2 O α от времени в интервале температур 140-170ºС. Вид кривых свидетельствует о том, что продолжительность автокаталитического периода исчезающе мала для всех исследованных температур. При 140ºС за 60 мин образец потерял 69 % воды. При повышении температуры на 30ºС за 30 мин степень обезвоживания составила 91 %.
На рис. 4б представлены зависимости α / τ от времени изотермической выдержки τ для исследованных температур. При 140ºС процесс идет практически с постоянной скоростью. При 170ºС кривая скорости обезвоживания проходит максимум через 5 мин взаимодействия (рис. 4б), что свидетельствует о протекании реакции по всей поверхности вещества. Процесс протекает в диффузионно-кинетической области.
Для расчета кажущейся энергии активации Е акт процесса потери воды К 2 ТаO 2 F 5 ⋅ H 2 O нами выбрано параболическое уравнение сжимающейся сферы [1 – (1 – α )1/3]2 = k . τ , используемое в кинетике для описания топохимических реакций, протекающих одновременно по всей поверхности ( Раков, Тесленко , 1982). По тангенсу угла наклона находили значения кажущихся констант скорости k (рис. 4в), расчет Е акт выполнен по уравнению Аррениуса.
Рассчитанные кинетические параметры процесса обезвоживания К 2 ТаO 2 F 5 ⋅ H 2 O:
-
t, ºC 140 150 170
-
k, мин-1 0.0020 0.0063 0.0102
4. Заключение
Е акт = 77 кДж/моль.
Исследовано поведение моногидрата пероксипентафторотанталата калия К 2 ТаO 2 F 5 ⋅ H 2 O при нагревании в атмосфере воздуха. Показано, что на первой стадии в интервале температур происходит удаление воды с образованием безводного соединения K2TaO2F5, которое при нагреве выше 370ºС разлагается с образованием двух фаз: K3TaOF6 и K2Ta2O3F6.
Рассчитаны тепловые эффекты процессов обезвоживания и разложения К 2 ТаO 2 F 5 , составившие 12.8 и 16.2 кДж/моль соответственно.
Изучена кинетика обезвоживания моногидрата пероксипентафторотанталата калия. Показано, что процесс протекает в диффузионно-кинетической области. В интервале температур 140-170ºС рассчитаны кажущиеся константы скорости. Величина кажущейся энергии активации Е акт процесса потери воды составила 77 кДж/моль.
Авторы признательны В.Я. Кузнецову за рентгенографические, О.А. Залкинду за ИК спектроскопические исследования и А.Т. Беляевскому за СЭМ диагностику синтезированного соединения.


