Исследование способности аполипопротеина А-I в комплексе с актиномицином Д оказывать кардиотоксическое действие на изолированное сердце крысы
Автор: Князев Роман Александрович, Трифонова Н.В., Колпаков А.Р., Поляков Л.М.
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Экспериментальные статьи
Статья в выпуске: 4 т.20, 2016 года.
Бесплатный доступ
Введение Химиотерапия - один из основных способов терапии злокачественных новообразований. Однако этот способ лечения связан с целым рядом побочных эффектов, среди прочих можно выделить осложнения, связанные с кардиотоксичностью. Разработка новых противоопухолевых препаратов напрямую связана с уменьшением общего токсического эффекта на организм и сердечно-сосудистую систему в частности. Цель Изучение способности аполипопротеина A-I с противоопухолевым препаратом актиномицином Д вызывать функциональные нарушения в работе изолированного сердца крысы в сравнении с чистым актиномицином Д. Методы Провели эксперименты на крысах-самцах Вистар массой 220-250 г. В качестве перфузата использовали модифицированный буфер Кребса - Хензеляйта при насыщении карбогеном (95% O2 и 5% CO2, температура раствора 37,5 °С). Изолированные сердца крыс перфузировали ретроградно по стандартной методике с регистрацией изоволюмического давления в левом желудочке. Аполипопротеин А-I выделяли из липопротеинов высокой плотности человека методом делипидирования с последующим разделением смеси белков методом колоночной хроматографии. В работе использовали аполипопротеин А-I с актиномицином Д в концентрации 0,1 мкг/мл перфузионного раствора. Результаты Актиномицин Д в концентрации 1 мкг/мл ухудшает функциональные показатели работоспособности сердца с увеличением энергетической нагрузки на миокард. Уменьшение концентрации цитостатика до 0,1 мкг/мл перфузата приводит показатели (с незначительными изменениями) на уровень контрольных. При аполипопротеине А-I с актиномицином Д в концентрации 0,1 мкг/мл нивелируются изменения, которые вносил цитостатик без переносчика. При этом аполипопротеин А-I с актиномицином Д улучшают показатели гемодинамики, что можно объяснить присутствием белкового компонента. Выводы На модели изолированного сердца крысы показано, что аполипопротеин А-I с актиномицином Д в концентрации 0,1 мкг/мл не обладают кардиотоксическим действием, а, напротив, способствуют улучшению функциональных показателей работоспособности миокарда за счет белкового компонента в качестве переносчика цитостатика.
Изолированное сердце крысы, аполипопротеин а-i, актиномицин д, кардиотоксичность
Короткий адрес: https://sciup.org/142140773
IDR: 142140773 | DOI: 10.21688-1681
Investigation of cardiotoxic effect of A-1 apo + D actinomycin complex on isolated rat heart
Aim. Chemotherapy is one of the main methods of treating malformations. However, this technique causes a great deal of side effects, among which are complications related to cardiac toxicity. Development of new anticancer drugs is directly related to a decrease in the general toxic effect on the organism and the cardiovascular system in particular. The aim of the study was to investigate the capability of apolipoprotein A-1 together with an anticancer drug, actinomycin D, to induce functional disturbances in the performance of an isolated rat heart and to compare the effect with that of pure actinomycin D. Methods. For experiments use was made of Wistar male rats weighing 220-250 g. A modified Krebbs-Henseleit buffer saturated with carbogene (95 % O2 and 5 % CO2, solution temperature 37.5 °C) was used as perfusate. Experiments were conducted on isolated rat hearts. The isolated rat hearts were perfused retrogradely by a standard procedure, with isovolumic pressure registered in the left ventricle. Apolipoprotein A-I was isolated of human high-density lipoprotein by delipidating followed by separation of the proteins mix by means of column chromatography. In the experiment, apolipoprotein A-I- was mixed with actinomycin D, with concentration of the anticancer drug in the complex being 0.1 μg/ml. Results. Actinomycin D with concentration 1 μg/ml aggravates the functional indicators of the heart and enhances energy load on the myocardium. Decreasing the concentration of cytostatic down to 0.1 μg/ml of perfusate brings the indicators to the baseline values. Apolipoprotein A-I combined with actinomycin D offsets the changes introduced by the cytostatic without a carrier. The complex improves hemodynamics, which can be interpreted by the presence of a protein component. Conclusion. An isolated rat heart model shows that apolipoprotein A-I in combination with 0.1 μg/ml actinomycin D does not cause cardio toxicity. The complex improves myocardial efficiency through the use of the protein component as a carrier of the anticancer drug.
Текст научной статьи Исследование способности аполипопротеина А-I в комплексе с актиномицином Д оказывать кардиотоксическое действие на изолированное сердце крысы
На сегодняшний день зарегистрировано большое количество препаратов, обладающих противоопухолевой активностью. Эффективность их применения доказана клинически. Главная проблема при их использовании в терапии рака — низкая избирательность действия и высокая системная токсичность. Разработка новых транспортных систем

Статья доступна по лицензии Creative Commons Attribution 4.0.
Patologiya krovoobrashcheniya i kardiokhirurgiya . 2016;20(4):88-95
доставки лекарственных препаратов имеет принципиальное значение для повышения эффективности химиотерапии [1].
Потенциальными переносчиками противоопухолевых препаратов могут выступать липопротеины низкой плотности, липопротеины высокой плотности (ЛПВП), а также их главный белковый компонент — аполипопротеин А-I (апоА-I) [2]. Специалисты Научно-исследовательского института биохимии (Новосибирск, Россия) обнаружили принципиальную возможность апоА-I образовывать устойчивые комплексы и проникать в цитоплазму и ядра клеток асцитной карциномы Эрлиха с такими противоопухолевыми препаратами, как винбластин и актиномицин Д [3]. На культуре клеток асцитной карциномы Эрлиха показано, что при использовании апоА-I с актиномицином Д в концентрации цитостатика 0,1 мкг/мл инкубационной среды снижается пролиферация опухолевых клеток, в то время как препарат без переносчика в этой же концентрации противоопухолевой активностью не обладает. Кроме того, на культуре гепатоцитов крыс показано, что апоА-I с актиномицином Д не оказывают цитостатического эффекта на нормальные (здоровые) клетки [4].
Среди побочных эффектов противоопухолевых препаратов следует выделить кардиотоксичность, которая может выражаться бессимптомными изменениями на электрокардиографии, инфарктом миокарда, вплоть до токсической кардиомиопатии с явлениями тяжелой сердечной недостаточности [5]. Разработка новых противоопухолевых препаратов напрямую связана с оценкой их влияния на сердечно-сосудистую систему. Следует отметить, что данные о влиянии актиномицина Д на работу миокарда противоречивы, а также трудно сопоставимы из-за немногочисленности.
Цель исследования: изучить способность аполипопротеина A-I с противоопухолевым препаратом актиномицином Д вызывать функциональные нарушения в работе изолированного сердца крысы в сравнении с чистым актиномицином Д.
Методы
Эксперименты на лабораторных животных проводили в соответствии с «Правилами работ с использованием экспериментальных животных» (приказ Министерства здравоохранения СССР от 12.08.1977 №755 и приложение к приказу № 565 от 04.10.1977), принципами Хельсинкской декларации Всемирной медицинской ассоциации. Животные содержались на стандартной диете и имели свободный доступ к воде. Работа одобрена комитетом по биоэтике НИИ биохимии.
Провели эксперименты на крысах-самцах Вистар массой 200–300 г. За 1 ч до опыта животным внутрибрюшинно вво- дили гепарин (500 ед. на крысу). После декапитации сердце быстро извлекали и помещали в стаканчик с охлажденным перфузионным раствором. В аорту вводили канюлю, которую подсоединяли к перфузионной системе. Перфузию проводили через коронарные сосуды под постоянным давлением 60 мм ртутного столба. В качестве перфузата использовали модифицированный буфер Кребса – Хензеляйта, содержащий NaCl — 118 mM, KCl — 4,7 mM, CaCl2 — 3 mM, MgSO4 — 1,2 mM, KH2PO4 — 1,2 mM, NaHCO3 — 25 mM, ЭД-ТА-Na2 — 0,5 mM, глюкозу — 5 mM при насыщении карбогеном (95% O2 и 5% CO2) и постоянном контроле рН (7,4); температура раствора — 37,5 °С. Для регистрации давления в левом желудочке в левом предсердии за ушком делали разрез, через него вводили с перфузионным раствором латексный баллончик, соединенный с цифровым датчиком. Баллончик вводили сначала в полость предсердия, затем через митральный клапан в полость левого желудочка. Объемную скорость коронарного потока определяли по объему оттекающей от сердца жидкости (мл/мин). Содержание кислорода устанавливали полярографическим методом с использованием электрода Кларка. Регистрировали частоту и скорость сокращения. Работоспособность (Р) определяли как произведение прироста давления на частоту сокращений в минуту. Показателем эффективности работы было отношение выполненной работы (работоспособности) к величине коронарного потока (Р/КП). В качестве показателя энергетической нагрузки на миокард определяли отношение произведения (АО2 х КП) на единицу выполненной работы [6].
Перфузию сердца проводили в режиме рециркуляции перфузионного раствора, что позволяло значительно уменьшать количество перфузата по сравнению с незамкнутой системой. Объем перфузируемой жидкости в системе не превышал 30 мл.
Каждое выделенное сердце работало не менее 15 мин без рециркуляции перфузионного раствора до установления постоянных показателей амплитуды и частоты сокращений. Затем в перфузионный раствор вносили исследуемый компонент, и сердце работало в режиме рециркуляции в течение 30 мин.
Исходные (фоновые) показатели работы сердца крысы различались между собой, поэтому изменения в работе миокарда под влиянием изучаемых компонентов оценивали в процентах по отношению к исходным показателям.
Аполипопротеин А-I выделяли из фракции ЛПВП. Де-липидирование проводили охлажденной смесью хлороформа и метанола (1 : 1): 20 мл смеси на 1 мл ЛПВП с последующей многократной отмывкой эфиром. Для получения апоА-I суммарные белки ЛПВП в растворе
3% Ds-Na и 0,1% меркаптоэтанола наносили на колонку (1,6 х 100 см) с Сефарозой 6B-CL (Pharmacia, Швеция) и элюировали 5 мМ Трис-НСl буфером, рН 8,6, содержащим 6 М мочевины, 0,01% азида натрия и 1 мМ фенилметансуль-фонилфторида. Проверка чистоты апоА-I осуществлялась с помощью электрофореза в 10% ПААГ с Ds-Na. Белковые полосы визуализировали 0,1% Кумасси G-250 в смеси метанола и 10% уксусной кислоты (1 : 1) [7].
Обессоливание апоА-I проводили методом гель-фильтрации (колонка: 40 х 0,8 см, Сефадекс G-25 (Pharmacia, Швеция), элюент: 5 мМ трис-НСl буфер, рН 7,4, содержащий 0,15 М NaCl). Профиль элюции регистрировали на детекторе ультрафиолета при длине волны 280 нм. Концентрация обессоленного белка составляла 0,2 мг/мл. Полученный белок стерилизовали фильтрами BIOFIL 45 µм и использовали в течение 3–5 дней. В работе использовали 1 мМ маточный раствор актиномицина Д (Applichem, Германия).
Комплекс аполипопротеина А-I с актиномицином Д получали, выдерживая их смесь в 0,05 М калий-фосфатном буфере, рН 7,4 в течение 15 мин при комнатной температуре. Актиномицин Д в перфузате исследовали в двух концентрациях — 1 и 0,1 мкг/мл. Образование комплексов апоА-I с актиномицином Д подтверждали методом тушения триптофановой флуоресценции [3].
Дизайн исследования
Проводили эксперименты в трех группах: 1-я — актиномицин Д в концентрации 1 мкг/мл перфузата; 2-я — ак- тиномицин Д в концентрации 0,1 мкг/мл перфузата; 3-я — аполипопротеин А-I c актиномицином Д в концентрации 0,1 мкг/1 мл перфузата. В каждой группе было пять особей. Каждое выделенное сердце работало не менее 15 мин без рециркуляции перфузионного раствора до установления постоянных показателей амплитуды и частоты сокращений. После этого измеряли исходные (КП, Р, Р/КП) и (АО2 и (АО2 х КП)/Р) контрольные показатели. Затем в перфузионный раствор вносили исследуемый компонент, и сердце работало в режиме рециркуляции в течение 30 мин. В работе представлены данные, полученные на 20-й мин перфузии в присутствии исследуемых компонентов, поскольку в это время установили максимальные показатели работоспособности (КП, Р, Р/КП) и энергетической нагрузки на миокард (АО2 и (АО2х КП)/Р).
Исходные (фоновые) показатели работы сердца крысы различались между собой, поэтому изменения в работе миокарда под влиянием изучаемых компонентов оценивали в процентах по отношению к исходным контрольным показателям.
Статистический анализ
Данные подвергали статистическому анализу с использованием программы StatPlus 2009 Professional 5.8.4 (США). Статистическую значимость результатов оценивали с помощью t-критерия Стьюдента для связанных выборок (до и после введения исследуемого компонента) при p<0,05.
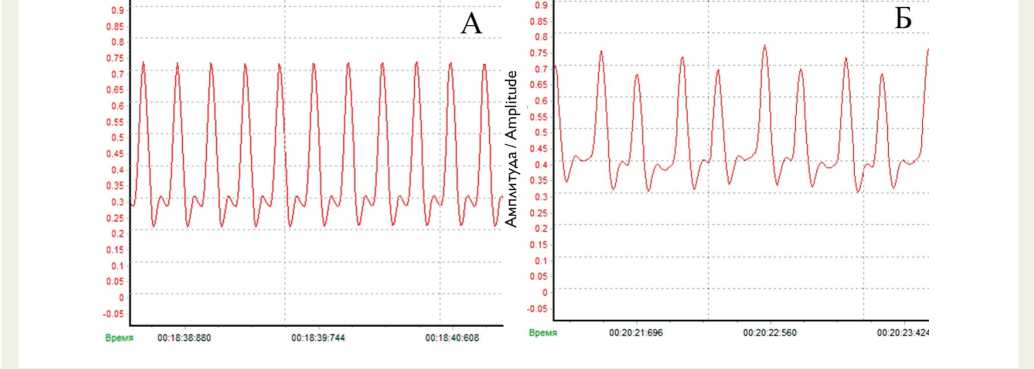
Рис. 1. Запись работы изолированного сердца крысы: A — в контроле (исходное состояние); B — при добавлении в перфузат 1 мкг/мл актиномицина Д. Время перфузии 20 мин
Fig. 1. Isolated rat heart performance: ( A ) the control (baseline); ( B ) when adding 1 µg/ml of actinomycin D into perfusate. Perfusion time 20 min
Контроль / Control Актиномицин Д /
Actinomycin D
КП
ЧСС Давление ΔО в ЛЖ 2
P/КП О 2 /ед. вып.
работы
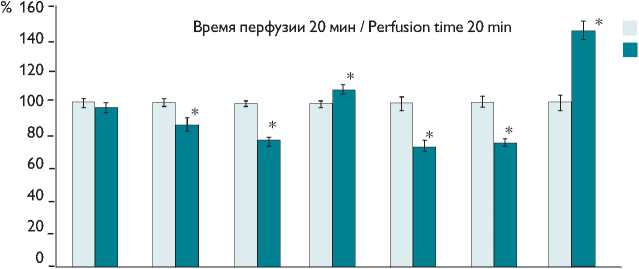
Рис. 2. Показатели работоспособности и энергетической нагрузки изолированного сердца в присутствии актиномицина Д в концентрации 1 мкг/мл (M±m)
Примечание. КП — коронарный поток, ЧСС — частота сердечных сокращений, ЛЖ — левый желудочек, Р — работоспособность сердца, * — p<0,05 по отношению к контролю
Fig. 2. Isolated heart efficiency and energy load, with actinomycin D administered in concentration of 1 µg/ml (M+m). КП — coronary flow; ЧСС — heart rate; ЛЖ — left ventricle; P — heart efficiency; * — p<0.05 against the control
Результаты
В перфузионном растворе актиномицин Д в концентрации 1 мкг/мл приводил к снижению систолического давления в левом желудочке на 22% (рис. 1). При этом отмечено увеличение давления в левом желудочке в фазу диастолы на 50% относительно исходных показателей, что говорит об уменьшении способности миокарда к расслаблению.
Как следует из рис. 2, актиномицин Д снижал частоту сердечных сокращений на 13% и работоспособность сердца на 26%. Коронарный поток в свою очередь оставался на контрольных значениях, что уменьшало эффективность выполненной работы (Р/КП) на 25%. В присутствии актиномицина Д повышалось поглощение кислорода на 8%, при этом показатель потребления кислорода на единицу выполненной работы увеличивался на 44%, что свидетельствует о существенном росте энергетической нагрузки на ткань миокарда (рис. 2).
Десятикратное снижение концентрации актиномицина Д в перфузате до 0,1 мкг/мл приводило практически к исходным показателям гемодинамики. Можно отметить даже снижение давления в левом желудочке в фазу диастолы на 16% относительно исходных показателей, что говорит об увеличении способности миокарда к расслаблению.
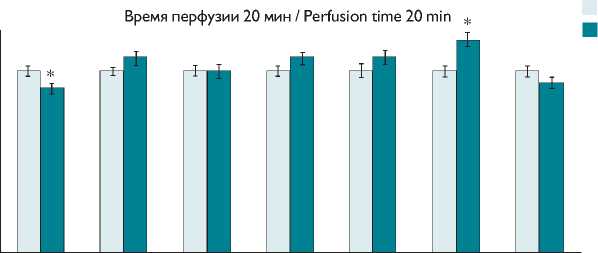
Из данных на рис. 3 следует, что происходило достоверное снижение коронарного потока на 9% и увеличение эффективности работы сердца на 16% (Р/КП). Другие показатели не имели достоверных отличий по отношению к исходным величинам.
Присутствие в перфузате актиномицина Д в концентрации 0,1 мкг/мл с апоА-I (рис. 5) приводило к росту давления в левом желудочке в фазу систолы на 10%, а также частоты сердечных сокращений на 15% относительно исходных значений, что говорит об увеличении сократительной способности миокарда. При этом способность сердечной мышцы к расслаблению снижалась на 16% относительно исходных показателей (рис. 4).
Присутствие в перфузате актиномицина Д в концентрации 0,1 мкг/мл с апоА-I повышало работоспособность сердца на 26%, однако увеличение коронарного потока на 30% приводило работоспособность на уровень контроля (рис. 5). Потребление кислорода снижалось на 11%, в то время как потребление кислорода на единицу работы уменьшилось на 8%, что указывает на снижение общей энергетической нагрузки на миокард.
Обсуждение
Актиномицин Д (дактиномицин) — цитостатический препарат из группы противоопухолевых антибиотиков, подгруппы актиномицинов, продуцируемый.
Противоопухолевое действие связано с тем, что он ин-теркалирует между парами азотистых оснований гуанин —
% 140
Контроль / Control Актиномицин Д /
Actinomycin D
КП
P
ЧСС Давление ΔО в ЛЖ2
P / КП О /ед. вып. работы
Рис. 3. Показатели работоспособности и энергетической нагрузки изолированного сердца в присутствии актиномицина Д в концентрации 0,1 мкг/мл (M±m)
Примечание . КП — коронарный поток, ЧСС — частота сердечных сокращений, ЛЖ — левый желудочек, Р — работоспособность сердца, * — p<0,05 по отношению к контролю
Fig. 3. Indicators of isolated heart efficiency and energy load, when adding 0.1 µg/ml of actinomycin D (M+m)
КП — coronary flow, ЧСС — heart rate, ЛЖ — left ventricle, P — heart efficiency * — p<0.05 against the control цитозин дезоксирибонуклеиновой кислоты и препятствует движению полимеразы рибонуклеиновой кислоты, нарушая таким образом транскрипцию антиапоптозных генов [8]. В основном актиномицин Д используют в качестве средства для лечения различных опухолей у детей, в том числе опухоли Вильмса, рабдомиосаркомы и саркомы Юинга [9]. История препарата насчитывает уже более 70 лет, исследо- ваны механизм, дозировки, различные побочные эффекты, среди которых, как правило, гепатотоксичность, гематологические и дерматологические нарушения [10]. Показано, что актиномицин Д без существенных побочных проявлений в комбинации с кортикостероидами позволял практически вдвое снижать курсовую дозу последних у больных с пересаженным сердцем [11]. Однако исследования на изо-
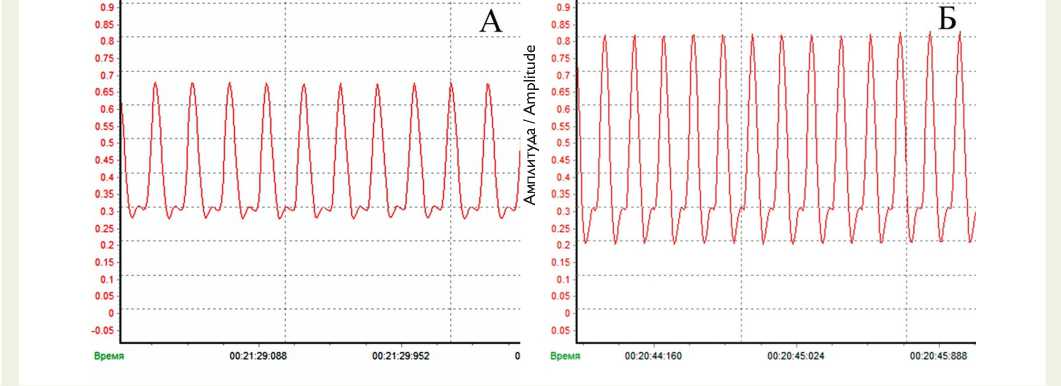
Рис. 4. Запись работы изолированного сердца крысы: A — в контроле (исходное состояние); B — при добавлении в перфузат апоА-I и актиномицина Д. Концентрация цитостатика в комплексе 0,1 мкг/мл. Время перфузии 20 мин
Fig. 4. Isolated rat heart performance: A — the control (baseline); B — when adding apoA-1 and actinomycin D. Cytostatic concentration is 0.1 µg/ml. Perfusion time 20 min
Время перфузии 20 мин / Perfusion time 20 min
Контроль / Control ■ Актиномицин Д /
Actinomycin D
КП ЧСС Давление ΔО P в ЛЖ 2
P / КП О 2 /ед. вып. работы
Рис. 5. Показатели работоспособности и энергетической нагрузки изолированного сердца в присутствии апоА-I и актиномицина Д. Концентрация цитостатика в комплексе 0,1 мкг/мл (M±m)
Примечание. КП — коронарный поток; ЧСС — частота сердечных сокращений; ЛЖ — левый желудочек; Р — работоспособность сердца; * — p<0,05 по отношению к контролю
Fig. 5. Indicators of isolated rat heart performance and energy load when adding apoA-1 and actinomycin D. Cytostatic concentration in the complex is 0.1 µg/ml (M+m). КП — coronary flow; ЧСС — heart rate; ЛЖ — left ventricle; P — heart efficiency; * p <0.05 against the control лированном сокращающемся сердце крысы показали, что актиномицин Д устраняет кардиопротекторное действие дексаметазона при ишемии/реперфузии [12]. Таким образом, данные о влиянии дактиномицина на работу миокарда противоречивы, а также трудно сопоставимы из-за их немногочисленности. Тем не менее в литературе отсутствуют данные о кардиотоксических свойствах препарата [6], поэтому на первом этапе мы изучили влияние актиномицина Д на функциональные показатели гемодинамики и энергетический статус миокарда. Мы использовали концентрации, при которых актиномицин Д ингибировал пролиферацию клеток остеосаркомы человека MG63 [13]. В концентрации 1 мкг/мл актиномицин Д оказывал выраженное кардиоток-сическое действие, снижал показатели работоспособности сердца при одновременном увеличении энергетической нагрузки на миокард. При этой концентрации (1 мкг/мл актиномицина Д) показатели достигали максимальных негативных значений уже на 20 мин перфузии. Вопрос о механизме такого эффекта остается открытым и требует дальнейших исследований. Однако полученные данные указывают на необходимость оценки особенностей и функционального состояния сердечно-сосудистой системы при назначении актиномицина Д как противоопухолевого препарата.
Использование актиномицина Д в концентрации 0,1 мкг/мл не приводит к нарушениям в работе сердца, что предсказуемо, поскольку при такой концентрации актиномицин Д оказывал слабый противоопухолевый эффект [13].
Следует отметить, что ранее мы получили данные об эффективности апоА-I с актиномицином Д в концентрации 0,1 мкг/мл в отношении культуры клеток асцитной карциномы Эрлиха [4]. Логично было предположить, что комплекс также способен вызывать нарушения в работе миокарда, однако апоА-I с актиномицином Д показал неожиданный результат. Комплекс усиливает функциональные показатели работоспособности сердца при снижении потребления кислорода на единицу выполненной работы. Такой эффект можно объяснить использованием в качестве переносчика апоА-I. Действительно, на изолированном сердце крысы показано, что апоА-I в физиологической концентрации вызывал стабильное увеличение давления внутри левого желудочка, повышал скорость сокращения и расслабления мускулатуры при незначительном изменении частоты сердечных сокращений [7]. Отличие эффекта апоА-I с актиномицином Д от воздействия апоА-I без цитостатика заключается в увеличении скорости коронарного потока, что также может благоприятно влиять на показатели гемодинамики пациентов, получающих химиотерапию.
Заключение
В условиях эксперимента на модели изолированного сердца крысы показано, что аполипопротеин А-I с актиномицином Д в концентрации 0,1 мг/мл не вызывают кардиотоксического действия, а, напротив, способствуют улучшению функциональных показателей работоспособности миокарда за счет белкового компонента в качестве переносчика цитостатика. Учитывая способность комплекса обладать кардиотоническим действием на фоне вазодилатации, можно рекомендовать его для исследований эффективности противоопухолевого действия при моделировании функциональных нарушений сердечно-сосудистой системы.
Финансирование
Работа поддержана бюджетным проектом федерального государственного бюджетного научного учреждения «Научно-исследовательский институт биохимии» по теме НИР – 085.
Список литературы Исследование способности аполипопротеина А-I в комплексе с актиномицином Д оказывать кардиотоксическое действие на изолированное сердце крысы
- Jeffrey S., David P., Pietrusko R., Rolfe M., Gerald P., Stec J., Nancy E., Geoffrey S., Symmans F., Pusztai L., Gabriel N. Targeted therapies for cancer 2004//American journal of clinical pathology. 2004. Vol. 122. No 4. P. 598-609. http://dx.doi.o DOI: rg/10.1309/5CWP-U41A-FR1V-YM3F
- Glickson J.D., Lund-Katz S., Zhou R., Choi H., Chen I.W., Li H., Corbin I., Popov A.V., Cao W., Song L., Qi C., Marotta D., Nelson D.S., Chen J., Chance B., Zheng G. Lipoprotein nanoplatform for targeted delivery of diagnostic and therapeutic agents//Molecular imaging. 2008. Vol. 7. No. 2. P. 101-110.
- Князев Р.А., Трифонова Н.В., Поляков Л.М. Изучение способности липопротеинов высокой плотности и аполипопротеина А-I связывать и транспортировать противоопухолевые препараты в клетки асцитной карциномы Эрлиха//Международный журнал прикладных и фундаментальных исследований. 2015. № 11 (часть 4). С. 538-542.
- Твердохлеб Н.В., Князев Р.А., Поляков Л.М. Влияние аполипопротеина A-I в комплексе с актиномицином Д на биосинтез ДНК в культуре клеток асцитной карциномы Эрлиха//Современная биология: актуальные вопросы. 2014. С. 52-55.
- Фандеев О.А., Васечкин С.С., Алехин М.Н., Одинцов С.В., Каллистов В.Е., Сидоренко Б.А. Клиническое значение кардиотоксичности антрациклинов: современные подходы к диагностике, профилактике и лечению//Кардиология. 2011. № 7. С. 40-46.
- Колпаков А.Р., Князев Р.А., Трифонова Н.В., Поляков Л.М. Кардиотонические свойства аполипопротеина А-I человека//Атеросклероз. 2015. Т. 11. № 4. С. 20-24.
- Polyakov L.M., Sumenkova D.V., Knyazev R.A., Panin L.E. The analysis of interaction lipoproteins and steroid hormones//Biochemistry (Moscow). Supplement Series B: Biomedical Chemistry. 2010. Vol. 4. No. 4. P. 362-365. http://dx.doi.o DOI: rg/10.1134/S1990750810040062
- Siboni R.B., Nakamori M., Wagner S.D., Struck A.J., Coonrod L.A., Harriott S.A., Cass D.M., Tanner M.K., Berglund J.A. Actinomycin D Specifically Reduces Expanded CUG Repeat RNA in Myotonic Dystrophy Models//Cell reports. 2015. Vol. 13. No. 11. P. 2386-2394. http://dx.doi.o DOI: rg/10.1016/j.celrep.2015.11.028
- Cortes C.L., Veiga S.R., Almacellas E., Hernandez-Losa J., Ferreres J.C., Kozma S.C., Ambrosio S., Thomas G., Taule A. Effect of low doses of actinomycin D on neuroblastoma cell lines//Molecular cancer. 2016. Vol. 15. P. 1. http://dx.doi.o DOI: rg/10.1186/s12943-015-0489-8
- Горбунова Т.В., Березовская И.В., Постникова Т.В. Сравнительная характеристика токсичности противоопухолевых антибиотиков группы актиномицинов при лечении солидных опухолей у детей//Онкопедиатрия. 2014. № 1. C. 20-24.
- DiSalvo T.G., Narula J., Cosimi A.B., Keck S., Dec G.W., Semigran M.J. Actinomycin D is an effective adjunctive immunosuppressive agent in recurrent cardiac allograft rejection//J. Heart Lung Transplant. 1995. Vol. 14. No. 5. P. 955-962.
- Varga E., Nagy N., Lazar J., Czifra G., Bak I., Biro T., Tosaki A. Inhibition of ischemia/reperfusion-induced damage by dexamethasone in isolated working rat hearts: the role of cytochrome c release//Life Sci. 2004. Vol. 75. No. 20. P. 2411-2423. http://dx.doi.o DOI: rg/10.1016/j.lfs.2004.04.031
- Lu D., Wang Y., Li Ch., Wei G., Chen R., Dong D., Yao M. Actinomycin D inhibits cell proliferations and promotes apoptosis in osteosarcoma cells//Int. J. Clin. Exp. Med. 2015. Vol. 8. No. 2. P. 1904-1911.


