Исследование стойкости лекарственного покрытия на медицинских стентах
Автор: Ермакова Т.А., Мордвинкин Д.В., Акатьев В.В., Камышанова Л.В.
Журнал: НБИ технологии @nbi-technologies
Рубрика: Нанотехнологии и наноматериалы
Статья в выпуске: 3 т.17, 2023 года.
Бесплатный доступ
Проведены исследования по разработке лекарственного покрытия на основе поливинилпирролидона с добавлением ацетилсалициловой кислоты (АСК). Данное покрытие нанесено на поверхность аналога медицинского стента электрохимическим осаждением. Дана оценка полученного лекарственного покрытия. Проведены коррозионные испытания исследуемых образцов с нанесенным покрытием методом поляризационного сопротивления. Выявлена зависимость коррозионной стойкости материала от концентрации ацетилсалициловой кислоты в составе лекарственного покрытия.
Коррозия, поливинилпирролидон, ацетилсалициловая кислота, стентирование, рестеноз
Короткий адрес: https://sciup.org/149144873
IDR: 149144873 | УДК: 544.77:678.746.532 | DOI: 10.15688/NBIT.jvolsu.2023.3.2
Study of drug coating durability on medical stents
One of the effective methods of treatment of cardiovascular diseases is a minimally invasive method of surgical intervention called stenting. The structure of the stent in the form of a cylindrical metal mesh makes it possible to deliver the implant to the place of installation in a compressed state and, on site, to expand it to the size required by the vessel. To reduce the risk of restenosis, drug-coated stents are used in drug therapy. Despite this, to date, it has not been possible to completely prevent the development of restenosis. In this regard, the works on the development of drug coating composition and methods of their application on the metal surfaces of the medical stent are relevant. Studies on the development of a drug coating based on polyvinylpyrrolidone with the addition of acetylsalicylic acid have been carried out. This coating was applied to the surface of the medical stent analog by electrochemical deposition. The obtained drug coating was evaluated. Corrosion tests of the investigated samples with the applied coating were carried out by polarization resistance method. The dependence of corrosion resistance of the material on the concentration of acetylsalicylic acid in the composition of the drug coating was revealed.
Текст научной статьи Исследование стойкости лекарственного покрытия на медицинских стентах
DOI:
Сердечно-сосудистые заболевания, обусловленные атеросклерозом, остаются наиболее актуальной проблемой здравоохранения, несмотря на существенный прогресс последних десятилетий в сфере диагностики и лечения кардиоваскулярной патологии. Одним из эффективных методов лечения сердечно-сосудистых заболеваний является малоинвазивный метод хирургического вмешательства – стентирование. Структура стента в виде металлической сетки цилиндрической формы дает возможность доставлять имплант к месту установки в сжатом состоянии, а на месте – расширять до необходимого сосуду размера. Для снижения риска развития рестеноза в медикаментозной терапии используются стенты с лекарственным покрытием [4–9]. Несмотря на то, что стенты снижают риск повторной закупорки сосуда, до настоящего времени не удается полностью предотвратить развитие рестеноза. В связи с этим, работы по разработке состава лекарственных покрытий и методов их нанесения на металлические поверхности медицинского стента, являются актуальными.
Для изготовления коронарных стентов одним из доступных, а потому и распространенным сплавом является нержавеющая аустенитная сталь 316L (импортное производство) или 03Х17Н14М3 (отечественный аналог), в состав которого входят железо (60–65 %), хром (17–18 %), никель (12–14 %) и молибден (2– 3 %). Несмотря на слабую рентгеноконтраст-ность, данный материал имеет высокие антикоррозионные свойства, радиальную прочность, достаточную пластичность и высокую биосовместимость с клетками крови [3].
В работах [1; 2] представлены результаты по разработке лекарственного покрытия на основе поливинилпирролидона с добавлением ацетилсалициловой кислоты (АСК) электрохимическим осаждением. Покрытие на основе по-ливинилпирролидона является перспективным для транспортировки и высвобождения лекарственного средства, поскольку данный полимер обладает отличной биосовместимостью с тканями организма, способствует выведению токсинов из организма и увеличивает действие лекарственных препаратов. Ацетилсалициловая кислота является антиагрегантом и потому предотвращает возникновение тромбов, тем самым повышая реологию (текучесть) крови.
Универсальным методом получения неметаллических покрытий для медицинских стентов является электрофоретическое осаждение, поскольку процесс не повреждает структуру и свойства биологически активных материалов. И в отличие от других процессов осаждения, используемых в настоящее время, его можно использовать при стандартной температуре и давлении окружающей среды на сложных формах без дорогостоящего оборудования. Ранее были выявлены оптимальные параметры нанесения лекарственного покрытия: сила тока I = 5 мА, время осаждения – 20 минут [1; 2].
Исследование покрытий оптическими методом показало границу между нанесенной и ненанесенной поверхностью исследуемой стали, что свидетельствует о том, что атомы пленки сильнее взаимодействуют с атомами подложки, чем друг с другом, провоцируя механизм послойного роста Франка – Ван-дер-Мерве. При таком механизме рост покрытия происходит равномерно. Результаты приведены на рисунке 1.
Толщина лекарственного покрытия на основе поливинилпирролидона с ацетилсалициловой кислотой, нанесенного электрохимическим осаждением на подложку из хромоникельмолибденового сплава, была определена с помощью сканирующего электронного микроскопа Phenom XL, обеспечивающего увеличение до х 100000. Источником электронов является электронная пушка с катодом из гексаборида церия. Микроскоп имеет полупроводниковый детектор обратно-рассеянных электронов и детектор вторичных электронов, обеспечивающий получение изображений в режиме SE.
Из рисунка 2, б видно, что лекарственное покрытие наносится в основном квазиравномерно. Толщина покрытия варьируется от 360 до 600 нм.
При выборе лекарственного покрытия необходимо учитывать и коррозионную стойкость материала с нанесенным лекарственным покрытием.
Коррозионные испытания образцов проводились посредством метода поляризационного сопротивления. Метод, основанный на измерении поляризационного сопротивления, является одним из эффективных методов оценки коррозионной стойкости металла.

а б
Рис. 1. Поверхность исследуемой стали при х 100: а – без покрытия; б – с покрытием

Рис. 2. Вид лекарственного покрытия: а - при х 16; б - при х 2500
Для определения коррозионной стойкости исследуемых образцов и регистрирования вольтамперограмм использовали установку, состоящую из электрохимической ячейки, термопары, потенциостата-гальваностата Р-40Х, предназначенного для исследования электрохимических процессов на границе раздела электрод-электролит. Принцип работы установки основан на электролизе по трехэлектродной схеме. В качестве индикаторного (рабочего) электрода использовался образец из хромоникельмолибденовой стали, в качестве электрода сравнения – хлорсеребряный электрод, а платиновый электрод – в качестве вспомогательного электрода. В электрохимической ячейке с помощью термопары поддерживалась постоянная температура.
Образцы, на которых было нанесено лекарственное покрытие с разной концентрацией ацетилсалициловой кислоты (от 0,002М до 0,01М), поочередно подвергались взаимодействию с модельной жидкостью (раствор Рингера-Локка), имитирующий состав плазмы крови. Подбор потенциала выдержки подбирался экспериментально – до стабилизации тока в течении 0,5 ÷ 1 часа. Вольтамперограммы фиксировались в режиме циклической вольтамперометрии (ЦВА) при скорости развертки потенциала 0,4 ÷ 0,6 мВ/сек.
Характер вольтамперограммы образца из хромоникельмолибденовой стали без покрытия, взятого для сравнительного анализа, представлен на рисунке 3.
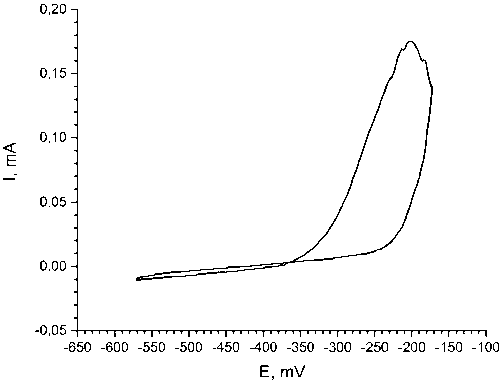
Рис. 3. Вольтамперограмма образца без покрытия в растворе Рингера – Локка
В интервале значений потенциалов от –570 до –250 мВ растворение исследуемого образца практически не наблюдается. В диапазоне потенциалов от –250 до –190 мВ наблюдается активное растворение стали, что сопровождается резким ростом плотности тока. Увеличение поляризационного сопротивления свидетельствует о замедлении (торможении) коррозионного процесса.
Вольтамперограммы образцов с нанесенными полимерными покрытиями с различным содержанием ацетилсалициловой кислоты представлены на рисунках 4 и 5 (общий вид вольтамперограмм). У образца с полимерным покрытием, но без добавления ацетилсалициловой кислоты (см. рис. 4, а ) активное анодное растворение происходит на отметке –350 мВ, тогда как с добавлением максимально допустимой концентрации ацетилсалициловой кислоты (см. рис. 4, д ) на отметке –180 мВ. Следовательно, время до наступления фазы активного растворения стали увеличивается в 1,2 раза.
В таблице 1 представлены результаты коррозионных исследований для всех экспериментальных образцов, скорость коррозии рассчитана по формуле vcorr = jcorr * 0,011655, где vcorr – скорость коррозии; jcorr – плотность тока коррозии, мкА/см2.
Из таблицы 1 видно, что наилучшим показателем плотности тока коррозии и максимальным поляризационным сопротивлением обладает лекарственное покрытие, в состав которого входит поливинилпирролидон и максимально концентрация ацетилсалициловой кислоты (образец № 6).
Полученные экспериментальные данные показывают (см. рис. 6), что зависимость коррозионной стойкости лекарственного покрытия увеличивается с увеличением концентрации ацетилсалициловой кислоты.
Для количественной и качественной оценки коррозионной стойкости металлов применяется десятибалльная шкала коррозионной стойкости по ГОСТ 9.908-85 [2]. Результаты сравнительной оценки коррозионной стойкости представлены в таблице 2.
Результаты, представленные в таблице 2, показывают, что коррозионная стойкость металла снижается при нанесении полимерного покрытия с низким содержанием ацетилсалициловой кислоты относительно металла без полимерного покрытия (образцы № 3 и № 4) в 1,5 и 1,25 раза соответственно, а полимерное покрытие, не обладающее в своем составе ацетилсалициловой кислоты, снижает коррозионную стойкость в 2,5 раза (образец № 2). Вероятно, причиной таких результатов являются частицы соли хлорида натрия, привнесенные при синтезе покрытий, поскольку раствор хлорида натрия обладает высокой электропроводностью. Однако увеличение концентрации ацетилсалициловой кислоты в составе лекарственного покрытия до 0,01М коррозионно-защитные свойства хромоникельмолибденовой стали повышаются в 4 раза (образец № 6).
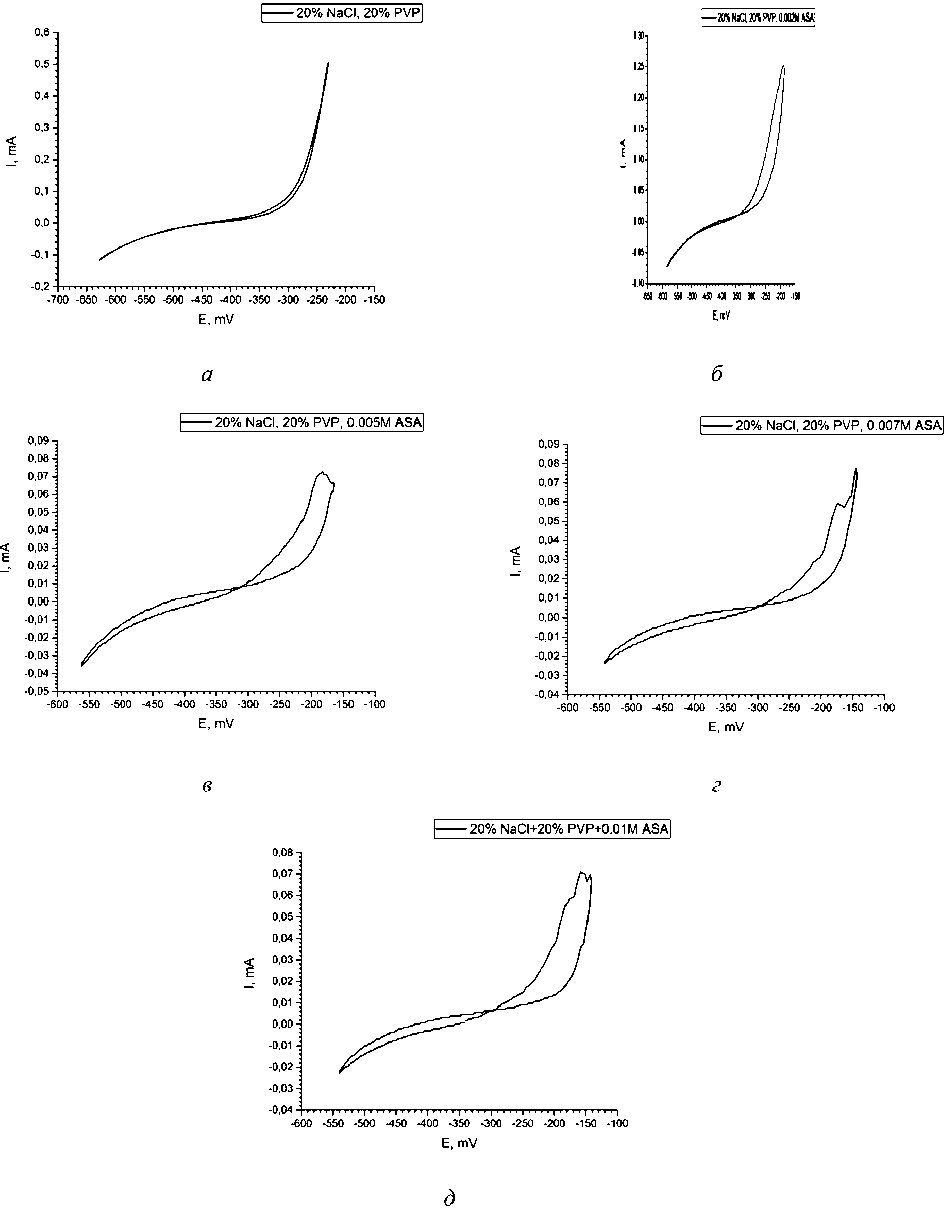
Рис. 4. Вольтамперограммы образцов с полимерным покрытием в растворе Рингера – Локка, полученные методом циклической вольтамперометрии:
а – без добавления АСК; б – с добавлением 0,002М АСК; в – с добавлением 0,005М АСК;
г – с добавлением 0,007М АСК; д – с добавлением 0,01М АСК
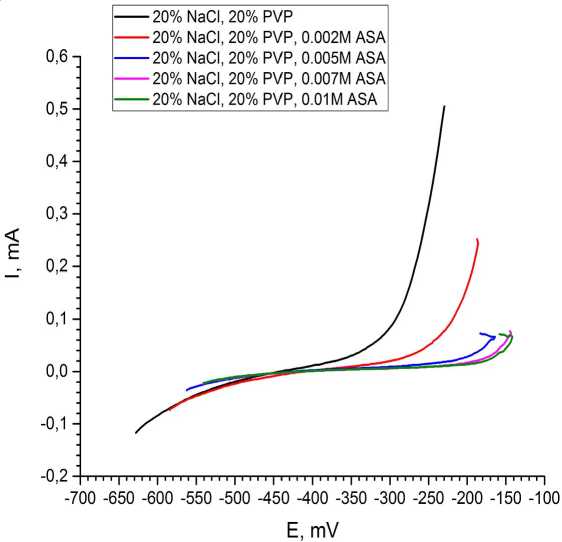
Рис. 5. Общий вид вольтамперограмм образцов
Результаты коррозионных исследований
|
№ |
Образец |
j corr , мкА/см2 |
v corr , мм/год |
|
1 |
Без покрытия |
3,37 |
0,04 |
|
2 |
ПВП 20%+NaCl 20% |
8,54 |
0,1 |
|
3 |
ПВП 20%+NaCl 20%+АСК 0,002М |
5,43 |
0,06 |
|
4 |
ПВП 20%+NaCl 20%+АСК 0,005М |
4,35 |
0,05 |
|
5 |
ПВП 20%+NaCl 20%+АСК 0,007М |
3,12 |
0,04 |
|
6 |
ПВП 20%+NaCl 20%+АСК 0,01М |
1,07 |
0,01 |
Скорость коррозии, мм/год
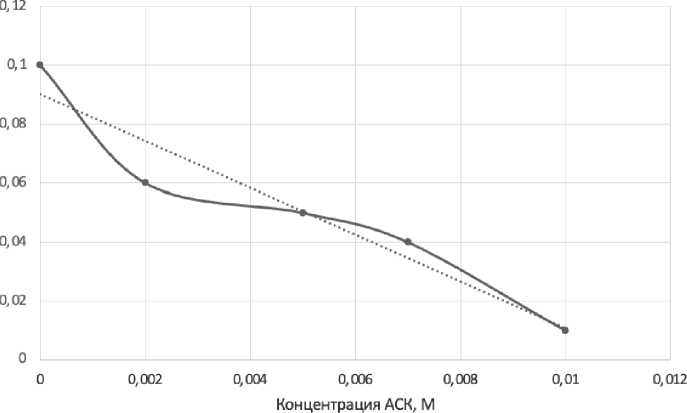
Рис. 6. Зависимости скорости коррозии полученного покрытия от концентрации ацетилсалициловой кислоты
Таблица 1
Таблица 2
Сравнительная оценка коррозионной стойкости
|
№ |
Образец |
Скорость коррозии, мм/год |
Коррозионная стойкость |
|
|
Баллы стойкости |
Группа стойкости |
|||
|
1 |
Без покрытия |
0,04 |
4 |
Стойкие |
|
2 |
ПВП 20%+NaCl 20% |
0,1 |
5 |
Стойкие |
|
3 |
ПВП 20%+NaCl 20%+АСК 0,002М |
0,06 |
5 |
Стойкие |
|
4 |
ПВП 20%+NaCl 20%+АСК 0,005М |
0,05 |
4 |
Стойкие |
|
5 |
ПВП 20%+NaCl 20%+АСК 0,007М |
0,04 |
4 |
Стойкие |
|
6 |
ПВП 20%+NaCl 20%+АСК 0,01М |
0,01 |
3 |
Весьма стойкие |
Таким образом, коррозионные испытания методом поляризационного сопротивления показали, что нанесение лекарственного покрытия на основе поливинилпирролидона с 0,01М ацетилсалициловой кислотой увеличивает коррозионную стойкость хромоникельмолибденовых сплавов медицинских стентов.
Список литературы Исследование стойкости лекарственного покрытия на медицинских стентах
- Акользин, А. П. Контроль коррозии металла котлов / А. П. Акользин. - М.: Энергоатомиздат, 1994. - 240 с.
- ГОСТ 9.908-85 Единая система защиты от коррозии и старения (ЕСЗКС). Металлы и сплавы. Методы определения показателей коррозии и коррозионной стойкости (с Изменением № 1) // Электронный фонд правовой и нормативно-технической информации. - Электрон. текстовые дан. - Режим доступа: https://docs.cntd.ru/document/1200007383. - Загл с экрана.
- Ермакова, Т. А. Создание лекарственных покрытий медицинских артериальных стентов электрохимическим методом / Т. А. Ермакова, В. Т. Фомичев, Д. В. Мордвинкин // НБИ технологии. - 2022. - Т. 16, № 1. - С. 27-32. -. DOI: 10.15688/NBIT.jvolsu.2022.1.5 EDN: NGKQEW
- Лупанов, В. П. Лечение больных ишемической болезнью сердца после коронарного шунтирования и чрескожных коронарных вмешательств / В. П. Лупанов// Атмосфера. Новости кардиологии. - 2007. - №3. - С. 18-24.
- Миронов, В. Н. Имплантация биорастворимого сосудистого стента Absorb / В. Н. Миронов, А. Н. Самко, Е. В. Меркулов // Современные стенты. - Электрон. текстовые дан. - Режим доступа: https://noatero.ru/ru/peredovye-tehnologii/sovremennye-stenty. - Загл. с экрана.
- Создание лекарственных покрытий на металлических медицинских стентах электрохимическими методами / Д. В. Мордвинкин [и др.] // ХХI Менделеевский съезд по общей и прикладной химии: сб. тез. В 6 т. T. 5 (Санкт-Петербург, 9-13 сент. 2019 г.). - СПб., 2019. - C. 211. EDN: IQMVBT
- Стентирование коронарных артерий, ангиопластика. - Электрон. текстовые дан. - Режим доступа: http://www.medmanager.ru/operacii_stentirovanie_koronarnyh_sosydov. - Загл. с экрана.
- High On-Treatment Platelet Reactivity to Both Aspirin and Clopidogrel is Associated with the Highest Risk of Adverse Events Following Percutaneous Coronary Intervention / N. J. Breet [et al.] // Heart. - 2011. - № 12 (97). - P. 983-990.
- Mazaev, V. P. Clinical Condition and Cardiovascular Risk Factors Displaying Neoatherosclerosis in Stented Coronary Arteries with Developing Restenosis / V. P. Mazaev, A. A. Komkov, S. V. Ryazanova // Cardiovascular Therapy and Prevention. - 2016. - № 5 (15). - P. 64-69. EDN: WYJSID


