Исследование влияния минерального субстрата на процесс гумификации растений
Автор: Курочкина Галина Николаевна
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Землепользование
Статья в выпуске: 3-3 т.15, 2013 года.
Бесплатный доступ
Установлена взаимосвязь между природой поверхности почвенных минералов и свойствами гуминовых кислот, выделенных из гумусовых веществ, сформировавшихся в процессе гумификации растительных веществ различного вида (клевер, пшеница) на поверхности кварцевого песка и бентонита, а также бескарбонатного суглинка при определенных термовлажностных условиях. По данным ИК-спектроскопии и элементному составу выявлено, что изученные образцы можно отнести к гуминовым кислотам различной степени созревания.
Поверхность, минералы, гумификация, гуминовые кислоты, ик-спектроскопия, растения
Короткий адрес: https://sciup.org/148201953
IDR: 148201953 | УДК: 631.445.41:661.185.22
Research the influence of mineral substratum on process of plants humification
The interrelation between the nature of soil minerals surface and properties of humic acids, emitted from humic substances, created in the process of humification of vegetable substances of a various type (clover, wheat) on surface of quartz sand and bentonite, and also noncarbonated loam under certain thermomoist conditions is established. According to IR-spectroscopy and to element structure it is revealed that the studied samples can be carried to humic acids of various extent of ripening.
Текст научной статьи Исследование влияния минерального субстрата на процесс гумификации растений
представляет возможность регулирования почвенных процессов, определяющих плодородие и устойчивость почв к антропогенным воздействиям [7]. Добровольским В.В [8] установлено, что в процессе почвообразования на поверхности высокодисперсных минеральных частиц почвы формируются полимолекулярные пленки гуминовых кислот (ГК). Исследования поверхностных свойств на примере сформировавшихся природных почвенных минералах или илистых фракциях почв показано, что механизмы устойчивости проявляются в буферных, прочностных, адсорбционных, лиофильно-лиофобных и других свойствах почв [9-14]. Следовательно, изучение влияния природы поверхности почвенных минералов и почв на процессы минерализации и гумификации растительных остатков является актуальной проблемой.
Цель работы : исследование в модельном эксперименте влияния природы минерального субстрата на гумификацию растительных остатков и анализ продуктов гумификации по элементному анализу и ИК-спектроскопическим методом.
Объекты и методы исследования. В данной работе использованы препараты ГК, любезно предоставленные Малыгиной Т.П. и Золотаревой Б.Н. Препараты ГК получены в лабораторных моделях, где в качестве минеральных сред использовался чистый кварцевый песок, отмытый от примесей и пленок железа соляной кислотой и промытый дистиллированной водой, бентонит в смеси с кварцевым песком в соотношении 1: 6 и бескарбонатный суглинок. Состав суглинка: гидрослюда – 32,6%; смектит + хлорит – 1,2%; каолинит – 20,7%; кварц – 38,3%; микроклин – 7,0%; ОВ – 1,81%. Измельченную наземную растительную массу (РМ) клевера и озимой пшеницы смешивали с минеральной средой (МС) в соотношении РМ: МС 1:10. Разложение растительных остатков проводили инкубированием при влажности 60% ПВ и температуре 190С в термостатированных условиях с инокуляцией почвенными микроорганизмами, добавляя в среду почвенной болтушки [7]. ГВ, образовавшиеся при разложении РМ, экстрагировали последовательно водными растворами нейтрального пирофосфата натрия (0,1 М Na4P2O7, рН 7,0) и гидроксида натрия (0,1 М NaOH) (эксперимент с клевером) или однократной обработкой водным раствором щелочного пирофосфата натрия (0,1М Na4P2O7 + 0,1 М NaOH; рН 10) (эксперимент с озимой пшеницей). ГК выделяли путем подкисления экстрактов ГВ до рН=1-2. Определение C, H, N выполнено методом автоматического микроанализа на автоматическом HCNS-анализаторе “Vario EL III” (“Elementur”, Германия). ИК-спектры препаратов ГК, выделенных после 30, 180, 360 суток инкубирования, снимали на модернизированном (компьютеризированном) спектрофотометре «Specord М-80». Образцы ОВ сушили при 400С в течение 2-х суток. Затем навеску образца 1 мг растирали со 199 мг КВr в агатовой ступке и формовали таблетку в пресс-форме при давлении 10 атм. и одновременном откачивании воздуха форвакуумным насосом. В качестве образца сравнения использовали ГК промышленную – немецкий препарат фирмы «Aldrich-Chemie D 7924 Stein heim» Hummussaeure Natriumsalt в натриевой форме, выделенный из торфа. Элементный состав ГК (GK2): вода – 11,96%; COOH – 4,8%; C – 41,9%; H – 4,1%; O – 50,4%; N – 0,55%; S – 1,84%.
Результаты исследований. Продукты гумификации растительных веще-ств, полученные на субстратах различной природы, были проанализированы на элементный состав (табл. 1). Во все сроки инкубации отношения Н/С для большинства образцов ГК примерно одинаковое, колеблется в пределах 1,03-1,22 и только для системы клевер-суглинок выявлено повышенное отношение Н/С 1,78-1,85. По данным Д.С. Орлова [15] отношение Н/С в препаратах ГК более 2 указывает на преимущественное содержание в молекуле насыщенных углеводородов – парафинов. Для циклопарафинов эти отношения составляют от 1,5 до 1,8-2,0, а для ароматических углеводородов – менее 1,0. Следовательно, повышенное отношение Н/С для системы клевер-суглинок при длительности компостирования 210 и 360 суток свидетельствует о преобладании в продуктах гумификации алифатических цепочек, то есть ГК данного продукта по составу ближе к циклопарафинам. Для более точного определения типа углеводорода по элементному составу, найденные при анализе величины Н/С, нами исправлены на содержание кислорода. Полученные значения Н/Сисп. показывают число замещенных водородных атомов с учетом кислородных функций. Так, приведенные в таблице значения Н/Сисп. указывают на возможность образования в некоторых продуктах гумификации ароматических углеводородов, например, в системах «клевер-песок» и «озимая пшеница-песок». Однако следует отметить преобладание в молекулах ГК алифатических углеводородов, что особенно характерно для системы «клевер-суглинок» и «озимая пшеница-суглинок». Различие продуктов гумификации на изученных субстратах подтверждено ИК-спектроскопичес-кими исследованиями.
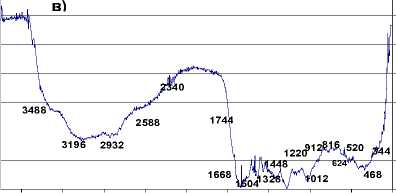
На рис. 1 а, б, в, г, д, е, ж приведены ИК-спектры выделенных продуктов гумификации. Как известно, ИК-спектры специфических гумусовых веществ имеют характерный облик и постоянный набор полос поглощения, позволяющий отличить ГК от соединений других классов [15]. Так, исследование ИК-спектра ГК промышленной показало (рис. 1а), что она имеет широкую полосу поглощения в области 36002200 см-1. Она состоит из полосы поглощения валентных колебаний свободной гидроксильной группы (3600 см-1) и гидроксильных групп, связанных межмолекулярными водородными связями 3448-3192 см-1. Слабые полосы поглощения в высокочастотной области 2908, 2848, 2628 и 2328 см-1 идентифицируются в области валентных колебаний -С- Н, как полосы метильных и метиленовых группировок. Кроме того, указанные полосы обнаруживаются и в области деформационных колебаний в интервале 13121372 см-1 (несколько мелких полос). Полосы поглощения в диапазоне 1200-1216 см-1 обусловлены, по-видимому, гидроксильной группой и группой =С-О- . Четко выделяются полосы деформационных колебаний гидроксильных групп спирта и полосы поглощения полисахаридов при 1056 см-1. Карбоксильная группа СООН проявляется по полосе с максимумом 1744 см-1. Часть карбоксильных групп находится в ионизированной форме, то есть свободная карбоксильная группа преобразуется в карбоксилатную с образованием солей ГК-ООNa, которая интенсивно поглощает колебания при 1692, 1590, 1400-1390 см-1. Кроме того, в спектре GK 2 в интервале 1604-1508 см-1 проявляются С=С связи алифатических и ароматических систем, а также азотсодержащие группировки [16]. Однако в спектре GK 2 они совпадают с ароматическими группировками (1604 и 1550 см-1). Слабые ароматические группы проявляются также при 748 и 848 см-1.
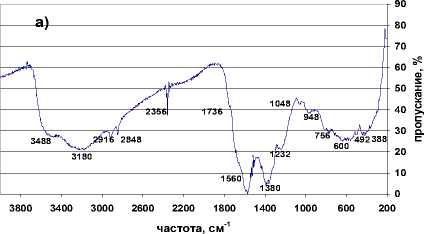
а)
о частота, см-1
3800 3400 3000 2600 2200 1800 1400 1000 600 200
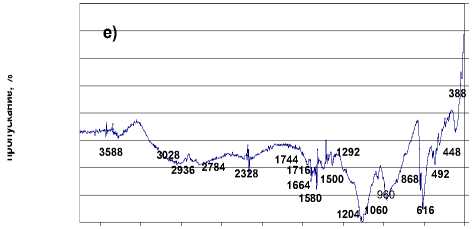
е)
частота,см
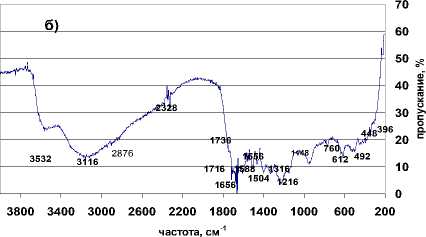
б)
3800 3400 3000 2600 2200 1800 1400 1000 600 200
частота, см-
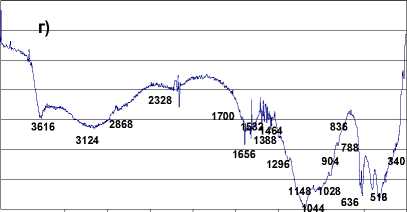
в)
3800 3400 3000 2600 2200 1800 1400 1000 600 200
частота, см-1
г)
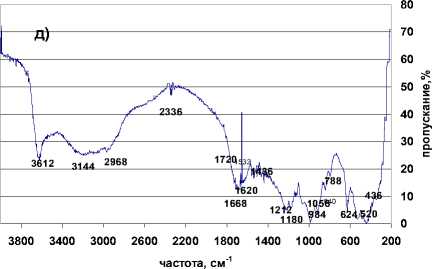
д)
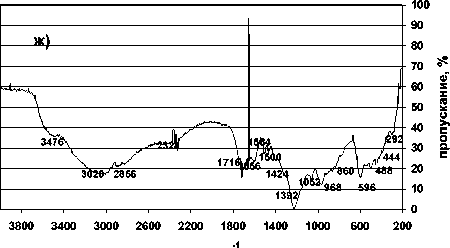
ж)
Рис. 1. ИК-спектры гуминовых кислот (ГК), образующихся в процессе гумификации растений на минеральных субстратах:
а) ГК промышленная (Humic acid, sodium salt, Aldrich – Chemie, Fp. >300); б) ГК 180 модельной системы «клевер – песок» экстрагирована 0.1M Na4P2O7, pH 7; в) ГК180 модельной системы «клевер-песок» экстрагирована последовательно водным раствором 0,1 M Na4P2O7 и 0,1 M NaOH; г) ГК 210 модельной системы «клевер – суглинок» экстрагирована водным раствором 0,1 M Na 4 P 2 O 7 , pH 7; д) ГК210 модельной системы «клевер-суглинок» экстрагирована 0,1 M Na 4 P 2 O 7 + 0,1 M NaOH, pH 10; е) ГК 180 модельной системы «пшеница – песок» экстрагирована 0,1 M Na 4 P 2 O 7 + 0,1 M NaOH, pH 10; ж) ГК 6 месяцев модельной системы «пшеница – суглинок» экстрагирована 0,1 M Na 4 P 2 O 7 , + NaOH
ИК-спектры для продуктов гумификации зависят как от времени инкубации, так и от вида субстрата и растения. В частности, для системы клевер-песок инкубирование 180 суток, вытяжка пирофосфат натрия (рис. 1б), можно отметить появление валентных колебаний свободных 3520 см-1 и связанных 3072 см-1 гидроксильных групп, а также небольшой полосы поглощения при 1744 см-1 карбоксильной группы и при 1656 см-1 переменной полосы поглощения «амид 1», при 1558 и 1400-1390 см-1 переменной группы – СОО-, зависящей от степени замещения водорода карбоксильных групп. Следует отметить слабую полосу поглощения ароматической группы (1600-1598 см-1) и небольшие спиртовые группы (1224, 1000-924 см-1).
Таблица 1. Элементный состав гуминовых кислот, атомные проценты
|
Минеральная среда |
Время инкубации, сутки |
С |
Н |
N |
О |
Н/С |
О/С |
С/N |
Н/С исп |
|
озимая пшеница |
|||||||||
|
песок |
90* |
34 |
40 |
2 |
25 |
1,18 |
0,73 |
17 |
2,14 |
|
360 |
38 |
41 |
3 |
18 |
1,08 |
0,47 |
13 |
1,71 |
|
|
суглинок |
90 |
34 |
40 |
3 |
24 |
1,18 |
0,7 |
11 |
2,10 |
|
360 |
33 |
34 |
3 |
29 |
1,03 |
0,88 |
10 |
2,25 |
|
|
клевер |
|||||||||
|
песок |
90** |
37 |
43 |
3 |
16 |
1,16 |
0,43 |
12 |
1,78 |
|
180 |
36 |
41 |
3 |
20 |
1,14 |
0,55 |
12 |
1,88 |
|
|
360 |
36 |
40 |
2 |
22 |
1,11 |
0,61 |
18 |
1,93 |
|
|
90*** |
39 |
43 |
3 |
15 |
1,1 |
0,38 |
13 |
1,61 |
|
|
180 |
36 |
44 |
3 |
17 |
1,22 |
0,47 |
12 |
1,85 |
|
|
360 |
36 |
42 |
2 |
19 |
1,17 |
0,53 |
18 |
1,92 |
|
|
песок: бентонит 6:1 |
180 |
27 |
50 |
3 |
21 |
1,85 |
0,78 |
9 |
2,84 |
|
360 |
27 |
48 |
3 |
23 |
1,78 |
0,8 |
9 |
2,88 |
|
Примечание: * - ГК, экстрагируемые водным раствором щелочного пирофосфата натрия (рН 10); ** - ГК, экстрагируемые водным раствором нейтрального пирофосфата натрия (рН 7); *** - ГК, экстрагируемые водным раствором гидроксида натрия после нейтрального пирофосфата натрия
Список литературы Исследование влияния минерального субстрата на процесс гумификации растений
- Зубкова, Т.А. Матричная организация почв/Т.А. Зубкова, Л.О. Карпачевский. -М.: Русаки, 2001. 207 с.
- Заварзина, А.Г. Образование почвенных гуминовых веществ путем окислительной полимеризации на поверхностях минералов/А.Г. Заварзина, Т.А. Семенова, А.М. Кузнецова, Е.Ю. Погожев//Труды IV Всероссийской конференции «Гуминовые вещества в биосфере». -СПб., 2007. С. 139-145.
- Курочкина, Г.Н. Адсорбция полиэлектролитов на синтетических алюмосиликатах заданного состава/Г.Н. Курочкина, Д.Л. Пинский//Журнал физической химии. 2002. Вып. 76, № 6. С. 1113-1118.
- Курочкина, Г.Н. Кинетика и термодинамика адсорбции полиэлектролитов на синтетических алюмосиликатных гелях/Г.Н. Курочкина, Д.Л. Пинский//Почвоведение. 2003. № 2. С. 164-172.
- Курочкина, Г.Н. Формирование минералорганической матрицы при адсорбции полиэлектролитов на почвенных минералах и почвах/Г.Н. Курочкина, Д.Л. Пинский//Почвоведение. 2012. № 11. С. 1199-1210.
- Золотарева, Б.Н. Гидрофильные коллоиды и почвообразование. Монография. -М.: Наука, 1982. 289 с.
- Демкина, Т.С. Активность микробоценоза и трансформация растительных остатков в модельных условиях/Т.С. Демкина, А. Горник, Т.П. Малыгина, Л.М. Мироненко//Динамика продукции биомассы растений и гумуса почв. -М.: Наука, 1992. 169 с.
- Добровольский, В.В. Роль гуминовых кислот в формировании миграционных массопотоков тяжелых металлов//Почвоведение. 2004. № 1. С. 32-39.
- Милановский, У.Ю. Лиофильно-лиофобные свойства органического вещества и структура почвы/У.Ю. Милановский, Е.В. Шеин, А.А. Степанов//Почвоведение. 1993. № 6. С. 122-126.
- Перминова, И.В. Анализ, классификация и прогноз свойств гумусовых кислот. Автореф…дисс. д-ра хим. наук. -М., 2000. 50 с.
- Murphy, EM.M. The sorption of humic acids to mineral surfaces and theirrole in contaminant binding/EM.M. Murphy, J.M. Zachara, S.C. Smith, J.L. Phillips//Sci.Total Environ. 1992. 117/118. P. 413-423.
- Murphy, EM.M. Inter action of hydrophobic organic compounds with mineral-bound humic sub stances/EM.M. Murphy, J.M. Zachara, S.C. Smith et al.//Environ. Sci. and Technol. 1994. V. 28. P. 1291-1299.
- Theng, B.K.G. The adsorption of 14C-labelled humic acid by montmorillonite/B.K.G. Theng, H.W. Sharpenseel//Proc. Int. Clay Conf. 1975. P. 643-653.
- Varadachari, C. The influence of crystal edges on clay-humus complexation/C. Varadachari, A.H. Mondal, K. Ghosh//Soil Science. 1995. V. 159, No. 3. P. 185-190.
- Орлов, Д.С. Гуминовые вещества в биосфере. Монография. -М.: Наука, 1993. С. 16-26.
- Литтл, Л. Инфракрасные спектры адсорбированных молекул. -М.: Мир, 1969. 514 с.


