Исследование влияния вспомогательных веществ на технологические параметры сырья и стабильность действующего вещества в процессе изготовления твердой лекарственной формы
Автор: Кравцова М.В., Бежеская Е.В., Гукина О.А., Мешайкина А.В.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Химическая технология
Статья в выпуске: 1 (95) т.85, 2023 года.
Бесплатный доступ
Проведено теоретическое исследование подходов к решению проблем, связанных с однородностью смеси для таблетирования и стабильностью действующего вещества. Проведено исследование данных по влиянию вспомогательных веществ на свойства смеси для гранулирования. В результате обращения к литературным источникам найдены работы, рассматривающие взаимосвязь состава, текучести смеси и времени перемешивания. Кроме того, рассмотрены работы в области стабильности субстанций, которая связана с используемыми вспомогательными веществами. В результате проведенного обзора показаны различные варианты влияния на технологические характеристики смеси такие, как растворение, сыпучесть, сегрегация. Наблюдение за взаимосвязями между технологическими параметрами помогает понять зависимость параметров контроля качества от них. Так, например, однородность дозирования сильно зависит от сегрегации и, соответственно, от текучести смеси. Вспомогательные вещества оказывают так же влияние и на стабильность действующего вещества. Они должны быть инертны к нему, но с помощью вспомогательных веществ возможно регулировать необходимый уровень pH, процент влажности. В некоторых случаях вспомогательные вещества обратимо связываются с действующим веществом для снижения деградации. В заключении сделан вывод о том, что в ходе разработки технологического состава твердой лекарственной формы необходимо учитывать влияние вспомогательных веществ. При разработке состава возможен подбор оптимальной комбинации вспомогательных веществ, которая улучшит технологические параметры смеси, качество и срок годности лекарственного препарата. Для производства препаратов-дженериков данный вопрос наиболее актуален, поскольку при разработке состава препарата требуется повтор характеристик оригинального препарата. При этом возможно использовать альтернативный состав плацебо, что позволяет увеличить экономическую эффективность производства.
Технология, вспомогательные вещества, таблетки, стабильность, субстанция, сырье, производство, дженерик
Короткий адрес: https://sciup.org/140301810
IDR: 140301810 | УДК: 615.014.21 | DOI: 10.20914/2310-1202-2023-1-212-220
Study of the influence of excipients on the technological parameters of raw materials and the stability of the active substance in the process of manufacturing a solid dosage form
A theoretical study of approaches to solving problems related to the uniformity of the mixture for tableting and the stability of the active substance was carried out. A study of data on the influence of excipients on the properties of the mixture for granulation was carried out. As a result of reference to literary sources, works were found that consider the relationship between the composition, fluidity of the mixture, and mixing time. In addition, work in the field of stability of substances, which is associated with the excipients used, is considered. As a result of the review, various options for influencing the technological characteristics of the mixture, such as dissolution, flowability, segregation, are shown. Observing the relationship between process parameters helps to understand the dependence of quality control parameters on them. Thus, for example, the homogeneity of dosing is highly dependent on segregation and, accordingly, on the fluidity of the mixture. Excipients also have an effect on the stability of the active substance. They should be inert to it, but with the help of excipients it is possible to regulate the required pH level, the percentage of moisture. In some cases, excipients reversibly bind to the active substance to reduce degradation. In conclusion, it was concluded that in the course of developing the technological composition of a solid dosage form, it is necessary to take into account the influence of excipients. When developing the composition, it is possible to select the optimal combination of excipients, which will improve the technological parameters of the mixture, the quality and shelf life of the medicinal product. For the production of generic drugs, this issue is most relevant, since the development of the composition of the drug requires the repetition of the characteristics of the original drug. In this case, it is possible to use an alternative placebo composition, which allows to increase the economic efficiency of production.
Текст обзорной статьи Исследование влияния вспомогательных веществ на технологические параметры сырья и стабильность действующего вещества в процессе изготовления твердой лекарственной формы
Для процесса таблетирования учитывают параметры всех компонентов прессуемой смеси. Вещества должны быть достаточно однородными по размеру частиц и иметь приемлемую остаточную влажность. Комбинация веществ должна обладать достаточной текучестью для обеспечения однородности продукта. Различие в размере частиц сказывается на ходе процесса производства ввиду подверженности разделению из-за разности в плотности. Данный фактор сказывается на показателе «Однородность дозирования» для твердых готовых форм по содержанию активной фармацевтической субстанции (АФС) [1–4].
Некоторые АФС могут быть таблетированы в виде чистых веществ, но это бывает достаточно редко; большинство составов включают эксципиенты. Обычно добавляют фармакологически неактивный ингредиент (наполнитель), называемый связующим, чтобы помочь скрепить таблетку и придать ей прочность. Часто также необходим ингредиент, который действует как дезинтегрант или разрыхлитель, чтобы способствовать диспергированию таблетки после проглатывания, высвобождая АФС. Связующие вещества так же могут выступать в роли разрыхлителей, к таким вспомогательным веществам относятся крахмал и целлюлоза [5].
При разработке оптимального состава для лекарственного средства возникает необходимость учитывать свойства вспомогательных веществ одновременно с разных позиций. Таким образом учитывают их взаимодействие с действующим веществом с физической точки зрения, их свойства для таблетирования и свойства для выполнения функции таблеток [8, 13]. Кроме того, вспомогательные вещества и технологические параметры процесса могут влиять на стабильность АФС, что должно контролироваться в соответствии с регламентами технологического процесса.
Материалы и методы
Объекты исследования: научные статьи, содержащие исследования и обзоры по теме влияния вспомогательных веществ на технологические параметры смеси для таблетирования и на стабильность действующего вещества.
В ходе проведения теоретического исследования использовались: анализ научной литературы, систематизация данных, описание систематизированной информации.
Сбор научной литературы осуществлен через поисковые системы: Google Scholar, Researchgate, Google Patents.
Предметом исследования выбрано влияние на технологический процесс производства твердой лекарственной формы вспомогательных веществ.
post@vestnik-vsuet.ru Результаты
Проведен анализ научной литературы, описывающей влияние вспомогательных веществ на процесс производства таблеток.
В ходе систематизации полученной информации выявлены два основных направления возможного влияния плацебо:
влияние плацебо на технологические параметры смеси для таблетирования (растворение, текучесть, сегрегация);
стабильность активной фармацевтической субстанции в ходе процесса производства и при хранении готового препарата.
Влияние на физические технологические параметры
Основной задачей является подбор комбинации вспомогательных веществ для получения оптимальных физических свойств таблетки. От вспомогательных веществ зависят технологические параметры продукта и дальнейшее его соответствие по показателям качества, таким как: растворение, однородность дозирования, примеси и количественное определение. Таким образом, например в работе Щиковского, Крут-ских и Датхаева рассмотрено влияние вспомогательных веществ на критические показатели качества препарата «Боризол». По результатам исследования сделан вывод о влиянии содержания кальция гидрофосфата безводного и микрокристаллической целлюлозы на кинетику растворения in vitro таблеток. При увеличении количества кальция гидрофосфата безводного наблюдалось уменьшение растворения труднорастворимой субстанции и, соответственно, при увеличении количества микрокристаллической целлюлозы растворение увеличивалось [6].
На примере таблеток S-Амлодипина никотината авторы статьи привели зависимость однородности дозирования от состава и времени перемешивания [7]. По проведенному обзору авторы выяснили, что порошок S-амлодипина никотината имеет низкую сыпучесть и частицы разного размера и формы. Препарат имеет низкую дозировку, в результате возникает проблема с однородностью дозирования. В работе представлены результаты по исследованию влияния состава смеси на сыпучесть и времени перемешивания на однородность с использование 12 модельных смесей с лактозой и без нее [7]. По полученным в ходе эксперимента данным авторы сделали вывод о том, что АФС не влияет на изменение сыпучести смеси в то время, как лактоза оказывает большее влияние на данный показатель, чем микрокристаллическая целлюлоза. Измерения для эксперимента проводили в четырех временных точках и по полученным данным видно, что для составов 1–6 без лактозы время перемешивания с оптимальной однородностью дозирования составляет 15 минут, а в присутствии лактозы (составы 7–12) в это же время обладают меньшей однородностью, что приводит к необходимости увеличивать время перемешивания [7].
В результате можно сделать вывод о прямой зависимости однородности дозирования от высокой сыпучести смеси и времени перемешивания, что дает фактор, который необходимо учитывать в составе препарата и выбранной технологии [7].
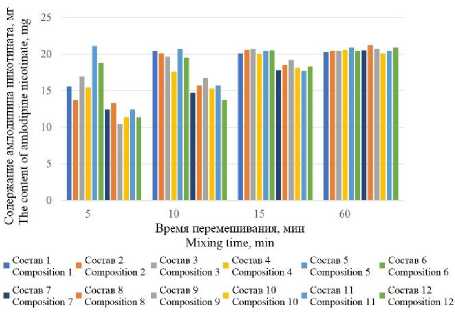
Рисунок 1. Однородность дозирования массы для таблетирования [14]
Figure 1. Uniformity of mass dosing for tableting [14]
На однородность смеси оказывает большое влияние разность размеров частиц. В случае эффективно перемешанных смесей имеет место явление сегрегации. Данное расслоение может происходит в соответствии с механизмами просеивания, псевдоожижения, а также влияние оказывает используемое оборудование. В обзоре Jakubowska и Ciepluch подробно описаны механизмы данного явления. По результату проведенного обзора авторами сделан вывод о непредсказуемости корреляции факторов на способность смесей к расслоению [8].
Данное явление зависит от множества факторов, кроме размера частиц: процентного содержания АФС в смеси, соотношения плотности частиц, когезивности смеси, условий смешивания, времени прибывания смеси в определенных этапах технологического процесса. Процесс расслоения не должен рассматриваться на одном конкретном этапе, поскольку возможно противодействие на другом этапе, вследствие чего наиболее корректно рассматривать процесс в целом.
Кроме рабочих параметров процесса необходимо уделить внимание рецептуре препарата и процессам получения лекарственной формы. Наиболее приемлемым способом улучшить однородность смеси является использование грануляции, поскольку при прямом прессовании смеси добиться хорошей однородности сложнее. Во втором случае следует прибегнуть к предварительным исследованиям свойств смеси с оптимизацией пропорций для соответствия нормам однородности [8].
Во время влажной грануляции может наблюдаться неравномерное распределение частиц. Пример такого случая по работе Koide и коллег представлен в обзоре Jakubowska и Ciepluch. Процесс обеспечивал оптимальное перемешивание для однородности распределения компонентов в смеси, но в данном случае с помощью ИК в ближней области наблюдалась агломерация лактозы из-за чрезмерной грануляции при этом гидрофобные АФС отделялись. В результате сделан вывод об отсутствии влияния сегрегации внутри гранул на распределение частиц АФС. Соответственно, в процессе влажной грануляции необходимо уделять внимание распределению вспомогательных веществ в полученном грануляте [8].
На расслоение смеси оказывает влияние содержание АФС. Так в работе Ока и коллег приведено, что при более высокой скорости импеллера и при загрузке ацетаминофена 7 % (по сравнению с 3 %) потенциал расслоения был ниже. В работе исследовано неоднородное распределение компонентов между фракциями, в которых крупные гранулы были субактивными, когда более мелкие гранулы содержали избыток ацетаминофена. [9].
Выдвинуто три гипотезы:
-
1. Причиной неравномерности состава является преимущественное смачивание одного компонента рецептуры связующим на стадии смачивания и зародышеобразования из-за различных свойств поверхности (смачиваемости) частиц.
-
2. Причиной неравномерности состава является сегрегация частиц на стадии сухого смешивания, что приводит к обогащению поверхности порошкового слоя одним из компонентов и, следовательно, его предпочтительному контакту со связующим.
-
3. Причина неравномерности содержания – различная кинетика элементарных скоростных процессов (агломерация, расслоение, истирание, ломкость), которые зависят от состава таким образом, что приводят к систематическому обогащению определенных классов крупности одним из рецептурных составных частей.
Первая гипотеза проверена экспериментально по проникновению капель, в ходе которых анализировался состав зародыша, образованного из одиночной капли, осажденной на хорошо перемешанный слой порошка, и сравнивался с номинальным составом слоя. Вторая гипотеза была проверена путем изменения продолжительности фазы сухого смешивания в эксперименте по грануляции и оценки взаимосвязи между временем сухого смешивания и неоднородностью содержания в конечных гранулах. Третья гипотеза была проверена путем изменения продолжительности фазы влажного гранулирования и начала фазы влажного гранулирования как в хорошо перемешанных, так и в максимально разделенных начальных условиях. По результату работы сделан вывод, что избирательное смачивание не являлось основной причиной неоднородности состава, а большие агломераты образовывались на ранних стадиях добавления связующего. Кроме того, при растворении АФС в связующем наблюдали отсутствие влияния его на однородность и в результате этого выдвинуто предположение о влиянии процесса сушки в этом случае [4].
Влияние на стабильность АФС
Вспомогательные вещества должны подбираться исходя из инертности по отношению к действующему веществу и физических характеристик. Однако стоит учитывать их влияние на стабильность субстанции, поскольку в течение технологического процесса возможна деградация АФС, что приведет к возрастанию примесей и дефектам продукции. Подбор вспомогательных веществ основывается на необходимые свойства для дальнейшего процесса. Так, например, в патенте на препарат, содержащий бетагистин, при разработке введена лимонная кислота в качестве стабилизирующего вещества [12–14].
Стабильность субстанции может зависеть от количества влаги, особенно если используется гигроскопичная субстанция. В этом случае используемые вспомогательные вещества подбираются таким образом, чтобы они обладали: хорошей прессуемостью, низкой сорбцией влаги из воздуха, устойчивостью при хранении [15].
Аналогичным образом производят анализ сродства действующих веществ в комбинированных препаратах для снижения вероятности деградации или взаимодействия на отдельных этапах производства [16].
Таким образом провели исследование стабильности при разработке препарата с комбинированным составом рамиприл + лерканидипин. Для проведения эксперимента на стабильность были заложены 28 бинарных модельных смесей, как в сухом, так и в увлажненном виде. Анализ смесей показал, что совмещение данных субстанций возможно, но при условии отсутствия увлажнения рамиприла, а в особенности в присутствии лерканидипина, поскольку в таком случае образуется большее количество примесей. Кроме того, проведено исследование совместимости АФС в таблетке, покрытой пленочной оболочкой. В этом случае изучали все полупродукты. По результату стабильности такого варианта таблеток сделан вывод о необходимости варианта двухслойных таблеток, по причине отсутствия стабильности рамиприла. Уменьшения количества
Вспомогательные вещества могут иметь большое влияние на защиту от влаги действующего вещества. Снижение нестабильности лекарственного средства по причине взаимодействия с влагой охарактеризована несколькими механизмами:
-
• действие в качестве физического барьера;
-
• снижение подвижности влаги;
-
• снижение доступности влаги.
Подробный обзор влияния вспомогательных веществ на защиту от влаги написан Nаtаliа Veronica, Paul Wan Sia Heng и Celine Valeria Liew. В работе описаны ключевые моменты при выборе вспомогательных веществ для препаратов, чувствительных к влаге. Примеры вспомогательных веществ с предлагаемыми влагозащитными механизмами представлены в таблице 1 [18–20].
В ходе обзора авторами выделено несколько вспомогательных веществ, которые улучшают стабильность лекарственных средств, в числе которых: крахмал и поливинилпирролидон. Кроме того, рассмотрено влияние аморфных и низкокристаллических вспомогательных веществ по отношению к деградации активной фармацевтической субстанции [19].
Вспомогательные вещества, оказавшиеся способными снижать реакционную способность влаги, обладают такими свойствами, как: низкая активность воды, хорошее сродство к влаге, способность связывать влагу и снижать подвижность влаги. Напротив, эксципиенты с высокой степенью кристалличности играют ограниченную роль в уменьшении деградации лекарственного средства, вызванной влагой.
Этот обзор также включал краткое изложение аналитических методов для оценки активности воды, сорбции влаги, молекулярной подвижности молекул воды и энергии связывания влаги, чтобы обеспечить понимание взаимодействия влаги и вспомогательных веществ. Кроме того, были рассмотрены различные состояния влаги (связанные или несвязанные) и их отношение к стабильности лекарственного средства. В совокупности этот обзор показал, что несвязанная влага или влага с более высокой подвижностью увеличивает деградацию лекарственного средства. Соответственно, аналитические инструменты для оценки подвижности влаги могут быть полезны при определении гидролитической стабильности лекарственных средств в составах [19].
Таблица 1.
Примеры вспомогательных веществ с предлагаемыми влагозащитными механизмами [19].
Table 1.
Examples of excipients with proposed moistur e barrier mechanisms [1 9].
|
Возможный механизм |
Влагочувствительный препарат |
Вспомогательные вещества исследованы |
Лекарственная форма или состояние |
Наблюдения |
|
1 |
2 |
3 |
4 |
5 |
|
Действует как физический барьер |
Ацетилсалициловая кислота |
Твердый жир (жировой солидус тип 36) Глицерилбегенат Глицерил дистеарат Октадеканол Стеариновая кислота |
Пеллеты |
Низкий уровень деградации ацетилсалициловой кислоты в липидной матрице, содержащей твердый жир и бегенат глицерина |
|
Моногидрохлорид [S]-1-[2-(5-ци-ано-2-пиридиниламино)эти-ламино]ацетил-2-пиролидинкар-бонитрила (запатентованный ингибитор дипептидилпептидазы IV) |
Гидрогенизированное касторовое масло лактоза Стеариновая кислота |
Таблетки |
Грануляция из расплава с липофильными материалами (гидрогенизированное касторовое масло или стеариновая кислота) повышает стабильность ингибитора дипептидилпептидазы IV в присутствии влаги по сравнению с сухой грануляцией с лактозой. |
|
|
Снижение подвижности влаги |
Цефалотин |
Кукурузный крахмал Микрокристаллическая целлюлоза |
Лиофилизированный порошок |
Препараты цефалотина, содержащие кукурузный крахмал, имели меньшую деградацию, чем микрокристаллическая целлюлоза. |
|
Нифедипин |
Кукурузный крахмал Метилцеллюлоза Микрокристаллическая целлюлоза Поливиниловый спирт Поливинилпирролидон |
Порошок |
Скорость кристаллизации нифедипина варьировалась в зависимости от наполнителя. При одинаковом количестве влаги (0,04 г/г влажности) скорость кристаллизации нифедипина в препаратах, содержащих кукурузный крахмал, была ниже, чем в микрокристаллической целлюлозе. |
|
|
Оланзапин |
Полиэтиленгликоль Поливинилпирролидон Гидроксипропилцеллюлоза |
Порошок, суспензия, таблетки |
Снижение превращения безводного оланзапина в его гидратные формы в препаратах, содержащих поливи-нилпирролидон. Эффект был более заметным в физических смесях и суспензиях, чем в таблетках. |
|
|
ТАК-457 (запатентованный препарат) |
Инозитол Маннитол |
Лиофилизированный порошок |
При содержании влаги 2% составы, содержащие инозитол, имели лучшую стабильность, чем составы, содержащие маннит. Однако при содержании влаги 8% составы, изготовленные с маннитом, имели лучшую или аналогичную стабильность, чем инозит. |
|
|
Теофиллин |
Маннитол Микрокристаллическая целлюлоза Поливинилпирролидон |
Порошок |
Поливинилпирролидон снижает превращение ангидрида теофиллина в его гидратные формы. |
|
|
γ-гобулин |
Натриевая соль карбоксиметилцеллюлозы Декстран Метилцеллюлоза Поливинилпирролидон Гидроксипропилметилцеллюлоза α,β-поли(N-гидроксиэтил)-лазпартамид |
Лиофилизированный порошок |
Хотя составы, содержащие поливинилпирролидон, имели большее количество подвижной влаги, влага имела более низкую подвижность, чем составы, содержащие декстран или метилцеллюлозу, что приводило к меньшему снижению стеклования составов на основе поливинилпирролидона. |
Kravtsova M.V. et al. Proceedings of VSUET, 2023, vol. 85, no. 1, pp. 212-220 post@vestnik- vsuet.ru
Продолжение таблицы 1 | Continuation of table 1
|
1 |
2 |
3 |
4 |
5 |
|
Снижение доступности влаги |
Ацетилсалициловая кислота |
Целлюлозы различной степени кристалличности |
Порошок |
Препараты с целлюлозой меньшей степени кристалличности обладали лучшей устойчивостью к ацетилсалициловой кислоте. |
|
Дигидрат дикальцийфосфата лактоза Микрокристаллическая целлюлоза Прежелатинизированный крахмал |
Таблетка |
Ацетилсалициловая кислота обладала лучшей стабильностью в препаратах, содержащих прежелатини-зированный крахмал, чем в лактозе, микрокристаллической целлюлозе или дигидрате дикальцийфосфата. |
||
|
Дигидрат дикальцийфосфата Кукурузный крахмал Микрокристаллическая целлюлоза |
Таблетка |
Таблетки, приготовленные из кукурузного крахмала, имели более низкую деградацию ацетилсалициловой кислоты, чем таблетки, содержащие микрокристаллическую целлюлозу или дигидрат дикальцийфосфата. |
||
|
Цилазаприл |
Гидроксипропилметилцеллюлоза лактоза Кукурузный крахмал Тальк |
Таблетка |
Деградация цилазаприла была наименьшей в таблетках, изготовленных из кукурузного крахмала. |
|
|
Лимапрост-альфадекс |
Декстран40 Декстрин Гидроксипропилметилцеллюлоза Гидроксипропилцеллюлоза Пуллулан |
Лиофилизированный порошок |
Лимапрост-альфадекс обладал большей стабильностью, если в его состав входили декстран40, декстрин или пуллулан. |
|
|
Нитрофуранторин |
Лактоза Гидроксипропилцеллюлоза Частично прежелатинизированный Крахмал Силикатизированная микрокристаллическая целлюлоза |
Порошок |
Частично прежелатинизированный крахмал и гидрок-сипропилцеллюлоза лучше замедляли превращение безводного нитрофуранторина в моногидрат нитрофурантоина, чем силикатизированная микрокристаллическая целлюлоза и моногидрат лактозы. |
Кравцова М.В. и др. Вестник ВГУИТ, 2023, Т. 85, №. 1, С. 212-220 post@vestnik-vsuet.ru
Во время технологического процесса стабилизация субстанции может обеспечиваться наличием вспомогательных веществ, которые способны обратимо связываться с действующим веществом. Использование лимонной кислоты для субстанций обосновано образованием обратимых соединений для снижения доли процесса деградации как во время процесса производства лекарственного средства, так и в течение заявленного срока годности. В этом случае молекула действующего вещества связывается и предотвращаются в основном процессы окисления.
Использование в качестве кислотного стабилизатора лимонной кислоты отдельно или в смеси с аскорбиновой кислотой предусмотрено, например, в составе препарата на основе бетагистина дигидрохлорида. Патент RU 2 308 941 С1 содержит описание механизма стабилизации бетагистина кислотой, который заключается в связывании неподеленной электронной пары азота, входящего в состав молекулы бетагистина, что приводит к снижению его реакционной способности, и как следствие, придает большую устойчивость к воздействию компонентов воздуха в присутствии влаги [13].
Вспомогательные вещества могут сильно повлиять на фотостабильность активной фармацевтической субстанции. В исследовании по данному вопросу Thoma и Kübler сделали несколько основных заключений. Авторы обнаружили, что используемый растворитель для растворов лекарственных средств способен вызвать различия в кинетике деградации и в продуктах деградации действующего вещества. Вспомогательные вещества, которые обладают способностью поглощать УФ-излучение, выступают в роли фотостабилизаторов. Другие вспомогательные вещества могут значительно ускорять процесс фотодеградации. В результате сделан вывод о необходимости проведения испытаний на фотостабильность как чистой субстанции, так и модельных смесей, содержащих вспомогательные вещества [21].
Аналогичным образом авторам Sherif I. Farag Badawy, Reed C. Williams и Donna L. Gilbert с помощью кислотного агента удалось добиться стабильности разрабатываемого лекарственного средства в твердом виде в присутствии вспомогательных веществ. Цель исследования заключалась в определении возможность нормализации стабильности в условиях при 40⁰C и 75 % относительной влажности с содержанием безводной лактозы. Действующее вещество DMP 754 является новым препаратом, потенциально может быть пероральным антитромбоцитарным средством, которое может снизить вероятность и тяжесть образования тромбов в артериях, которые могут привести к сердечным приступам, или инсульты. Данное действующее вещество является стабильным в условиях ускоренного старения, однако при добавлении лактозы безводной происходит ускорение гидролиза как сложноэфирной, так и амидиновой групп. В данном случае на стабильность влияет рН раствора. Насыщенный раствор лактозы имеет рН около 6, а раствор действующего вещества с максимальной стабильностью обладает рН около 4. В соответствии с данным фактом авторы включили в смесь кислотный агент для увеличения кислотности среды с целью повысить стабильность. В результате добавление кислот снижало скорость гидролиза амидиновой группы, и этот эффект был более выражен в случае более сильных кислот. Однако более кислые ингредиенты приводили к более быстрому гидролизу сложноэфирной группы. Исследование проводили в присутствии различных кислотных агентов: лимонной кислоты, фумаровой кислоты, динатрия цитрата, натрия дигидрофосфата, натрия цитрата. По итогу сделан вывод о возможности стабилизировать DMP 754 в твердом состоянии за счет использования соответствующей кислоты, которая регулирует рН микросреды примерно до 4. Кроме того, экспериментально лучшие результаты получили при использовании лимонной кислоты [18, 22].
Заключение
В ходе обзора рассмотрено влияние вспомогательных веществ на технологические параметры смеси, в результате чего можно сделать вывод о прямой зависимости технологического процесса от выбранного состава вспомогательных веществ. Влияние вспомогательных веществ на каждую конкретную субстанцию индивидуально. От физических свойств смеси зависит качество получаемого продукта, а в особенности соответствие показателям качества данного лекарственного средства. Кроме того, с помощью подбора подходящей комбинации вспомогательных веществ удается добиться большей стабильности действующего вещества как в течение технологического процесса производства каждой лекарственной формы, так и во время всего периода заявленного срока годности. В этом случае большое влияние оказывает способность вспомогательных веществ уменьшить долю взаимодействия субстанции с влагой, а также стабилизировать рН среды и минимизировать влияние УФ-излучения для снижения деградации действующего вещества.
Список литературы Исследование влияния вспомогательных веществ на технологические параметры сырья и стабильность действующего вещества в процессе изготовления твердой лекарственной формы
- Зырянов С.К., Чистяков В.В. Фармакокинетика, безопасность и переносимость первого отечественного дженерика анагрелида в сравнении с референтным препаратом // Клиническая онкогематология. 2020. V. 13. № 3. P. 346-353.
- Монинец И. Производство твердых лекарственных форм // GMProject. 2005.
- Соколов А.В., Липатова И.С. Оригинальные препараты и дженерики: проблема выбора // Медицинские технологии. 2010. V. 2. P. 44-48.
- Стрилец О.П. Исследование влияния вспомогательных веществ // Человек и его здоровье. 2014. V. 7. № 2. P. 107-115.
- Емшанова С.В. Методологические подходы к выбору вспомогательных веществ для получения таблетированных препаратов методом прямого прессования // Химико-фармацевтический журнал. 2008. V. 42. № 2. P. 38-43.
- Щиковский А.Э., Крутских Т.В., Датхаев У.М. Изучение влияния вспомогательных веществ и параметров технологического процесса на критические показатели качества таблеток лекарственного препарата “Боризол” // Фармация Казахстана. 2018. V. 12. № 209. P. 25-31.
- Пчелинцев С.О., Краснюк И.И., Козлова Ж.М. Обоснование метода прямого прессования для таблеток S-амлодипина никотината // Медико-фармацевтический журнал «Пульс». 2020. Т. 22. №. 1. С. 75-79.
- Jakubowska E., Ciepluch N. Blend segregation in tablets manufacturing and its effect on drug content uniformity - a review // Pharmaceutics. 2021. V. 13. № 11.
- Oka S., Smrčka D., Kataria A., Emady H. et al. Analysis of the origins of content non-uniformity in high-shear wet granulation // International Journal of Pharmaceutics. 2017. V. 528. №. 1-2. P. 578-585. https://doi.org/10.1016/j.ijpharm.2017.06.034
- Garcia T.P., Prescott J.K. Blending and blend uniformity // Pharmaceutical Dosage Forms: Tablets. 2008. V. 1. P. 111-174.
- Zhong L., Gao L., Li L., Zang H. Trends-process analytical technology in solid oral dosage manufacturing // European Journal of Pharmaceutics and Biopharmaceutics. 2020. V. 153. P. 187-199. https://doi.org/10.1016/j.ejpb.2020.06.008
- Yonghuang L. Betahistine mesilate orally disintegrating tablet and preparation method thereof. 2010. P. 1-13.
- Кучугурин В.А. Твердая лекарственная форма, обладающая гистаминоподобным действием, и способ ее получения. 2006. № 19. P. 1-7.
- Gavi E., Reynolds G.K. System model of a tablet manufacturing process // Computers & chemical engineering. 2014. V. 71. P. 130-140. https://doi.org/10.1016/j.compchemeng.2014.07.026
- Badawy S.I.F. Wet Granulation and Chemical Stability of Drug Products // Handbook of Pharmaceutical Wet Granulation. Academic Press, 2019. P. 149-172. https://doi.org/10.1016/B978-0-12-810460-6.00013-0
- Łaszcz M., Trzcińska K., Filip K., Szyprowska A. et al. Stability studies of capecitabine //Journal of thermal analysis and calorimetry. 2011. V. 105. №. 3. P. 1015-1021. https://doi.org/10.1007/s10973-011-1351-x
- Шадрин А.А. Исследование химической совместимости двух субстанций в дной комбинированной лекарственной форме // Прикладная Биохимия И Микробиология. 2005. Т. 41. № 5. С. 662-668.
- Farag Badawy S.I., Williams R.C., Gilbert D.L. Effect of different acids on solid-state stability of an ester prodrug of a IIb/IIIa glycoprotein receptor antagonist // Pharm. Dev. Technol. 1999. V. 4. № 3. P. 325-331.
- Veronica N., Heng P.W.S., Liew C.V. Ensuring Product Stability-Choosing the Right Excipients // Journal of Pharmaceutical Sciences. 2022. V. 111. №. 8. P. 2158-2171. https://doi.org/10.1016/j.xphs.2022.05.001
- Ahlneck C., Zografi G. The molecular basis of moisture effects on the physical and chemical stability of drugs in the solid state // Int. J. Pharm. 1990. V. 62. № 2-3. P. 87-95.
- Thoma K., Kübler N. Influence of excipients on the photodegradation of drug substances // Pharmazie. 1997. V. 52. P. 122-129.
- Lambros M., Tran T. Citric Acid: A Multifunctional Pharmaceutical Excipient // Pharmaceutics. 2022. V. 14. № 5.


