Исследование возможности получения пигментов из отработанных электролитов цинкования
Автор: Чепрасова Виктория Игоревна, Залыгина Ольга Сергеевна, Марцуль Владимир Николаевич
Журнал: Вестник Витебского государственного технологического университета @vestnik-vstu
Рубрика: Химическая технология и экология
Статья в выпуске: 1 (30), 2016 года.
Бесплатный доступ
В работе исследовано осаждение ионов цинка из отработанных электролитов цинкования различных белорусских предприятий с целью получения пигментов. В качестве осадителей использовались карбонат, фосфат и гидрофосфат натрия. Изучен элементный и фазовый состав полученных осадков, а также влияние добавок, входящих в состав отработанных электролитов, на состав и свойства осадков. Подобраны температуры термообработки осадков в зависимости от используемого осадителя и получены оксид, орто- и пирофосфат цинка, которые могут использоваться в качестве пигментов. Исследовано их соответствие требованиям ГОСТ по таким показателям, как маслоемкость и укрывистость. Результаты полученных исследований позволят решить проблему утилизации отработанных растворов электролитов цинкования, а так же расширить сырьевую базу для производства пигментов.
Гальваническое производство, ортофосфат цинка, отработанный электролит цинкования, пигмент, пирофосфат цинка, укрывистость, маслоемкость
Короткий адрес: https://sciup.org/142184936
IDR: 142184936 | УДК: 504.064.47:621.357.7
Research of the possibility for pigments obtaining from spent zinc electrolytes
The work considers the investigation deposition of zinc ions from the spent zinc electrolyte various Belarusian enterprises to obtain pigments. As precipitants used sodium carbonate, sodium phosphate, sodium hydrophosphate. Studied elemental and phase composition obtained precipitations and the effect of additives, incoming in the spent electrolytes, on composition and properties of precipitations. Selected temperature heat treatment of precipitations depending on the precipitant and obtained zinc oxide, pyro- and ortho- zinc phosphate, which may be used as pigments. Investigate its compliance with GOST on such indicators as the oil absorption and spreading rate. Obtained results allow to solve the problem of utilization of spent zinc electrolyte solutions, as well as to expand the raw material base for the production of pigments.
Текст научной статьи Исследование возможности получения пигментов из отработанных электролитов цинкования
WASTE ELECTROLYTE OF GALVANISING, THE GALVANIC PRODUCTION, COLORANT, ZINC ORTHOPHOSPHATE, ZINC PYROPHOSPHATE, COVERING ABILITY, OIL-ABSORPTION POWER
The work considers the investigation deposition of zinc ions from the spent zinc electrolyte various Belarusian enterprises to obtain pigments. As precipitants used sodium carbonate, sodium phosphate, sodium hydrophosphate. Studied elemental and phase composition obtained precipitations and the effect of additives, incoming in the spent electrolytes, on composition and properties of precipitations. Selected temperature heat treatment of precipitations depending on the precipitant and obtained zinc oxide, pyro- and ortho- zinc phosphate, which may be used as pigments. Investigate its compliance with GOST on such indicators as the oil absorption and spreading rate.
Obtained results allow to solve the problem of utilization of spent zinc electrolyte solutions, as well as to expand the raw material base for the production of pigments.
В Республике Беларусь в настоящее время процессы нанесения металлических покрытий реализуются на более чем 140 предприятиях машино-, приборостроения, авиационной, электронной и радиотехнической промышленности [1]. Нанесение гальванических покрытий является не только хорошим способом защиты металлов от коррозии, но и возможностью значительно повысить их износостойкость, электропроводность и ряд других свойств. Вместе с тем, гальваническое производство является одним из наиболее опасных источников загрязнения окружающей среды, прежде всего тяжелыми металлами.
Процесс нанесения гальванических покрытий сопровождается образованием отработанных технологических растворов (электролиты нанесения покрытий, щелочные и кислые травильные растворы, растворы снятия покрытий и др.) и промывных вод, которые отводятся на очистные сооружения.
Отработанные растворы электролитов содержат значительное количество ионов тяжелых металлов (до 250 г/л) и характеризуются небольшим расходом (до 1,5 м3), определяемым объемом гальванических ванн. Периодичность замены растворов электролитов составляет от 1 до 4 раз в год и зависит от их состава и условий эксплуатации. Промывные сточные воды характеризуются невысокой концентрацией ионов металлов – до 1 г/л и значительными объемами. Образующиеся сточные воды чаще всего поступают на локальные очистные сооружения предприятий.
Анализ работы очистных сооружений гальванических производств Республики Беларусь показывает, что в большинстве случаев отработанные электролиты подаются в общую систему очистки совместно с промывными сточными водами. Это приводит к увеличению нагрузки на очистные сооружения и опасности нарушения установленных нормативов содержания загрязняющих веществ в очищенной воде. Исследования, проведенные на ряде предприятий Республики Беларусь, свидетельствуют о том, что в случае совместного отведения на станцию нейтрализации промывных вод и отработанных технологических растворов вклад последних в общее загрязнение сточных вод может составлять до 70 % [2]. Кроме этого, с отработанными растворами электролитов теряется значительное количество цветных металлов, являющихся ценным и дефицитным сырьем. Следовательно, обезвреживание отработанных растворов электролитов на локальных установках совместно с промывными водами может применяться лишь как временное или вынужденное решение при отсутствии других вариантов использования этих отходов.
Известны различные направления переработки отработанных растворов электролитов: регенерация, извлечение ценных металлов, получение катализаторов и пигментов [3—7].
Регенерация электролитов является достаточно трудоемким процессом и требует значительных затрат. Она может включать в себя целый ряд операций, таких как: глубокая очистка от взвешенных и коллоидных примесей, а также от высокомолекулярной органики методом ультрафильтрации, выпаривание, электродиализ с использованием ионоселективных мембран, электрохимическая и химическая обработка, фильтрование, корректировка состава [3]. Необходимо отметить, что электролит может выдерживать лишь определенное количество циклов регенерации, поскольку в нем накапливаются различные примеси, удаление которых стано- вится затруднительным.
Извлечение металлов из отработанных растворов электролитов можно осуществлять методами ионного обмена, обратного осмоса, ультрафильтрации, электродиализа и др., однако эти методы являются трудоемкими и энергоемкими, требуют специального дорогого оборудования, во многих случаях экономически не выгодны и поэтому не нашли широкого практического применения [4].
Сотрудниками РХТУ им. Д.И. Менделеева изучалась возможность использования отработанных электролитов для производства катализаторов, в частности переработка отработанных электролитов хромирования с получением железохромовых катализаторов для процессов среднетемпературной конверсии оксида углерода. Также исследовалось осаждение Ni2+ из отработанных электролитов никелирования с образованием осадка, который предлагается использовать в качестве сырья при приготовлении раствора Ni(NO3)2 в технологии катализаторов нанесенного типа и как основное сырье в технологии катализаторов смешанного типа [5]. Получение катализаторов из отработанных электролитов является перспективным направлением, однако затруднено вследствие высоких требований, предъявляемых к чистоте получаемых катализаторов.
В [6, 7] описываются исследования, свидетельствующие о возможности получения пигментов на основе отработанных электролитов гальванического производства. Предлагается получать пигменты из отработанных электролитов хромирования, цинкования, никелирования и меднения путем их осаждения в виде труднорастворимых соединений. Однако число таких работ ограничено, не установлены условия осаждения хромофорных соединений, не изучено влияние состава отработанного электролита на свойства пигментов, не выявлены закономерности формирования их структуры. Вместе с тем мировая потребность в пигментах постоянно увеличивается и составляет в 5,5—6 миллионов тонн ежегодно. Основными потребителями пигментов являются лакокрасочная промышленность и производство пластмасс, на которые приходится 43 и 27 % соответственно [8].
Белорусские предприятия, потребляющие пигменты, работают в основном на импортном сырье – до 80 % необходимого количества пигментов поставляется из Германии, Чехии, Китая, Испании и др. При производстве пигментов используется дорогое химически чистое сырье, также ввозимое из-за рубежа. В связи с этим, увеличение объема производства пигментов, особенно на основе отходов, является для Республики Беларусь чрезвычайно актуальным.
Поэтому целью работы является исследование возможности получения пигментов из отработанных электролитов гальванического производства.
Наиболее распространенными на предприятиях Республики Беларусь являются цинковые покрытия. Широкое применение цинкования в различных отраслях промышленности объясняется хорошими защитными свойствами цинкового покрытия вследствие его анодного характера и низкой стоимостью. Для осаждения цинковых покрытий применяют различные электролиты: кислые, цианистые, аммиакатные и др. Главным недостатком кислых электролитов является низкая рассеивающая способность. Цианистые цинковые электролиты отличаются высокой рассеивающей способностью и применяются для покрытия деталей сложной конфигурации, однако они обладают высокой токсичностью. Наиболее эффективными заменителями токсичных цианистых электролитов являются аммиакатные, в которых цинк находится в виде комплексных катионов типа [Zn(NH3)n(H2O)m]2+. Наиболее широкое распространение получили хлораммонийные электролиты. Они характеризуются высокой катодной поляризацией и хорошей электропроводностью, что оказывает благоприятное воздействие на рассеивающую способность, которая выше рассеивающей способности всех нецианидных электролитов.
В таблице 1 представлены составы хлораммонийных электролитов некоторых белорусских предприятий: ОАО «Минский завод автоматических линий» (МЗАЛ), ОАО «Амкодор» (г. Минск), ОАО «Минский тракторный завод» (МТЗ).
Как видно из таблицы 1, растворы хлораммонийных электролитов цинкования различных предприятий мало отличаются по составу и характеризуются высокой концентрацией ионов цинка.
В процессе эксплуатации технологических растворов их исходный состав меняется в связи с накоплением различных примесей, которые вносятся в ванну вместе с обрабатываемыми деталями, образуются в результате растворения анодов, при разложении блескообразователей, смачивателей и других добавок. Загрязнение электролитов также происходит за счет остающихся на поверхности деталей остатков полировальных паст и эмульсий при механической обработке изделий. Кроме этого в отработанных
Объектом исследования являлись отработанные электролиты цинкования вышеназванных белорусских предприятий.
Определение содержания ионов цинка в отработанных электролитах осуществлялось титриметрическим методом с эриохромом черным Т , ионов железа – фотоколориметрическим методом, хлорид-ионов и ионов аммония – методом прямой ионометрии. Элементный состав полученных осадков определялся методом электронной сканирующей микроскопии на электронном сканирующем микроскопе JSM-5610 LV с системой химического анализа EDXJED-2201 (JEOL, Япония). Для идентификации фазового состава использовался рентгенофазовый анализ, который проводился на рентгеновском дифрактометре D8 Advance Bruker (Германия). Дифференциально-термический анализ осуществлялся с помощью термоаналитической системы TGA/ DSC-1/1600 HF (METTLERTOLEDO Instruments, Швейцария).
Анализ отработанного раствора электролита цинкования ОАО «МЗАЛ» показал, что в нем содержится 65,37 г/л Zn2+ ; 128,39 г/л Cl– ; 47,1 г/л NH4 +; 0,227 г/л Fe3+ . Высокая концентрация в отработанных электролитах хромофорных ионов цинка позволяет предположить перспективность их переработки с получением пигмента.
В настоящее время среди цинксодержащих пигментов традиционно используемыми в различных отраслях промышленности являются цинковые белила ZnO , фосфат цинка Zn3(PO4)2 , и литопон ZnS•BaSO4 , характеризующиеся белым цветом. Кроме этого известны феррит цинка ZnFe2O4 бежевого цвета, цинковый крон (синтетический неорганический пигмент с различным содержанием оксида цинка, оксида калия и оксида хрома) желтого цвета и цинковая зелень (синтетический неорганический пигмент, получаемый смешением или соосаждением цинкового крона с синими пигментами) [10].
Исходя из состава наиболее распространенных пигментов, для осаждения Zn2+ из отработанного раствора цинкования были выбраны гидроксид, карбонат и фосфаты натрия. Использование в качестве осадителей растворов щелочей нецелесообразно, так как при этом происходит образование амфотерного гидроксида цинка, который растворяется при рН более 10,5. Использование дигидрофосфата натрия NaH2PO4 нецелесообразно, поскольку в результате его взаимодействия с хлоридом цинка ZnCl2 происходит образование кислой соли – дигидрофосфата цинка Zn(H2PO4)2:
ZnCl^ +2NaH:P0A = Zn^H.PO^.+lNaCl . (1)
Точных данных о растворимости Zn(H2PO4)2 нет, но она сопоставима с растворимостью сульфата цинка, который является хорошо растворимым соединением. Проведенный эксперимент подтверждает эти данные – осаждения цинка при использовании дигидрофосфата натрия не наблюдалось.
Осаждение ионов цинка производили насыщенными растворами карбоната натрия ( Na2CO3 ), фосфата натрия ( Na3PO4 ) и гидрофосфата натрия ( Na2HPO4 ). Полученный после стадии старения осадок подвергался пятикратной декантации с последующей промывкой на фильтре и высушивался при температуре 80 °С. Определялись выход осадка и остаточная концентрация ионов цинка в фильтрате. Результаты экспериментальных данных представлены в таблице 2.
Как видно из таблицы 2, максимальный выход осадка и минимальная остаточная концентрация Zn2 + в фильтрате наблюдались при стехиометрическом соотношении электролита и осаждающего раствора 1:2 (для карбоната натрия) и 1:1,34 (для фосфата натрия). Наибольший выход осадка составляет от 126 до 197 г на 1 л отработанного электролита. При этом остаточная концентрация ионов цинка в фильтрате не превышает 1,3 г/л, что сопоставимо с концентрацией Zn2+ в промывных сточных водах и позволяет сбрасывать их совместно на очистные сооружения. В случае использования гидрофосфата натрия целесообразно использовать соотношение 1:1,995, т.к. дальнейшее увеличение Na2HPO4 не приводит к существенному изменению выхода осадка и остаточной концентрации Zn2+ в фильтрате.
Аналогичные результаты были получены при использовании отработанных технологических растворов других предприятий Республики Бе-
|
Таблица 2 – Результаты осаждения ионов цинка из отработанного электролита цинкования ОАО «МЗАЛ» |
|||
|
Стехиометрическое соотношение электролита и раствора осадителя |
Выход осадка на 1 л электролита, г |
Остаточная концентрация ионов цинка в фильтрате, г/л |
рН фильтрата |
|
Осадитель – насыщенный раствор карбоната натрия Na2CO3 |
|||
|
1:1 |
60 |
4,2 |
5,8 |
|
1:1,5 |
106 |
3,6 |
6,4 |
|
1:2 |
126 |
1,3 |
7,6 |
|
1:2,5 |
120 |
2,8 |
8,1 |
|
Осадитель – насыщенный раствор фосфата натрия Na3PO4 |
|||
|
1:0,67 |
88 |
13,07 |
6,5 |
|
1:1 |
124 |
4,25 |
7,1 |
|
1:1,34 |
150 |
0,98 |
7,6 |
|
1:1,675 |
124 |
4,10 |
8,0 |
|
Осадитель – насыщенный раствор гидрофосфата натрия Na2HPO4 |
|||
|
1:1,33 |
128 |
5 |
3,2 |
|
1:1,995 |
182 |
0,325 |
4,0 |
|
1:2,66 |
188 |
0,11 |
5,9 |
|
1:3,325 |
197 |
0,065 |
6,2 |
Различный выход осадка связан с различной исходной концентрацией Zn2+ в электролитах цинкования ОАО «МЗАЛ», ОАО «Амкодор» и ОАО «МТЗ» (таблица 1); степень извлечения ионов цинка практически во всех случаях одинакова.
При использовании в качестве осадителя насыщенного раствора карбоната натрия возможно образование гидроксида цинка и (или) гид-роксокарбоната цинка по реакции совместного гидролиза хлорида цинка с карбонатом натрия возможно образование фосфата цинка белого цвета:
по следующей схеме: ----------------------------------------------------------------------------\
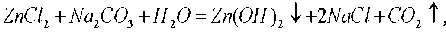
^ZnCl2+»1CO3+H1O = (ZnOH\CO^+4NaCUCO1 1
3ZnCL+2Na5PO4 = Zn;(PO4), +6XaCl . (3)
Согласно данным рентгенофазового анализа в состав осадка входят тетрагидрат ортофосфата
Данные рентгенофазового анализа получен- цинка Z n3(PO4)2 • 4H2O и пентагидрат пирофос-ного осадка свидетельствуют об образовании фата цинка Zn2P2O7 • 5H2O .
более сложных комплексов – на рентгенограмме Результаты дифференциально-термического наблюдаются характеристические пики основ- анализа этого осадка представлены на рисунке ного карбоната цинка Zn5(OH)6(CO3)2 (рисунок 4.
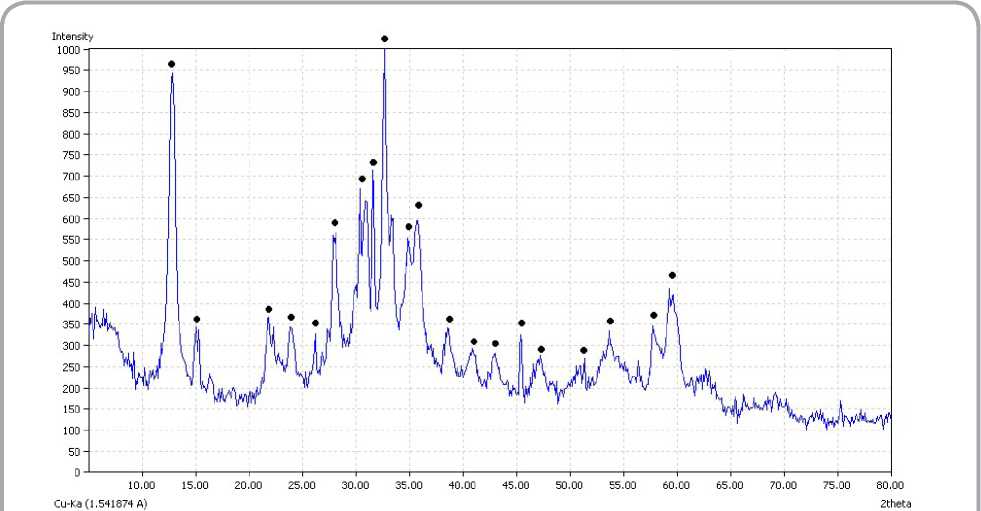
Рисунок 1 – Рентгенограмма осадка, полученного осаждением ионов цинка из отработанного электролита цинкования ОАО «МЗАЛ» раствором карбоната натрия (• - характеристические пики Zn5(OH)6(CO3)2)
На приведенной термограмме этого осадка (рисунок 2) наблюдается эндотермический минимум при температуре 230 °С, который, по-видимому, связан с разложением основных карбонатов и образованием оксида цинка, что подтверждается данными рентгенофазового анализа (рисунок 3).
Согласно данным электронной микроскопии содержание цинка в осадке составляет 81,15 %, кислорода – 18,85 %. Наличие каких-либо примесей не зафиксировано.
При использовании в качестве осадителя насыщенного раствора фосфата натрия Na3PO4
Согласно литературным данным [10] вопрос об образовании промежуточных продуктов при дегидратации тетрагидрата ортофосфата цинка и о температурных интервалах их устойчивости не имеет точного ответа. Имеются работы, в которых показано, что обезвоживание тетрагидрата фосфата цинка происходит в две стадии с образованием промежуточного дигидрата. При этом имеются сведения о возможности обезвоживания тетрагидрата в одну или три стадии. Дегидратация одной из модификаций Zn3(PO4)2•4H2O описывается следующим образом:
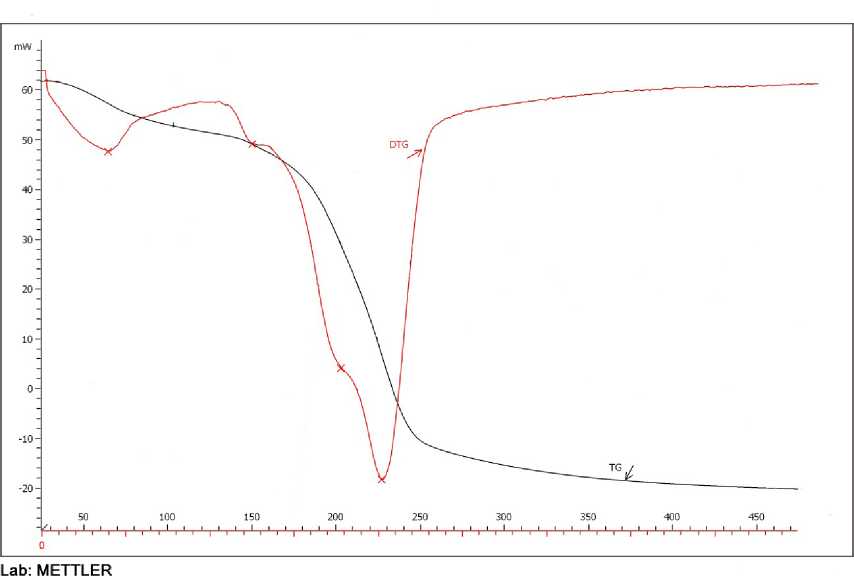
Рисунок 2 – Результаты дифференциально-термического анализа осадка, полученного осаждением ионов цинка из отработанного электролита цинкования ОАО «МЗАЛ» раствором карбоната натрия

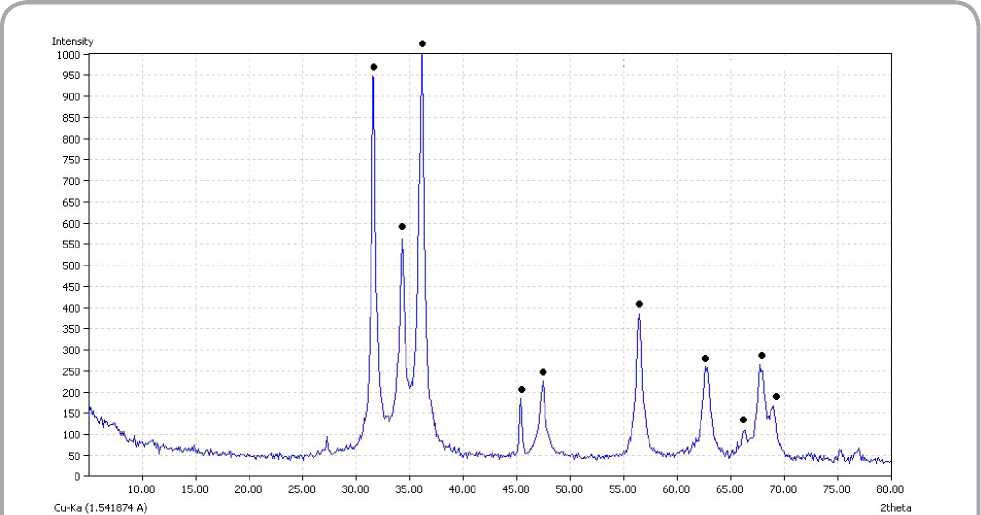
Рисунок 3 – Рентгенограмма осадка, полученного осаждением ионов цинка из отработанного электролита цинкования ОАО «МЗАЛ» раствором карбоната натрия, прокаленного при температуре 230 °С (• - характеристические пики ZnO )
Zn3(PO4\ ■ 4H2O^^Zn3(PO4\ .IHp^^Zn^POJ, »0,SH2O^^
.
Другая модификация Zn3(PO 4 )/4H 2 O обезвоживается в две стадии, в качестве побочных продуктов выступают дигидрат и безводный фосфат:
81, 110, 156, 197 и 384 °С происходит поэтапная дегидратация тетрагидрата ортофосфата цинка Zn3(PO4)2^4H 2 O и пентагидрата пиро-
. 5)
В [11] сообщается, что дегидратация Zn2P2O7•5H2O при температуре до 400 °С идет с образованием аморфного пирофосфата цинка через стадию образования моногидрата пирофосфата при температуре 65—100 °С. Переход аморфного Zn2P2O 7 в кристаллическое состояние происходит в интервале температур 400— 500 °С.
На приведенной термограмме (рисунок 4) наблюдается ряд эндотермических эффектов. Можно предположить, что при температурах
фосфата цинка Zn2P2O7•5H2O с образованием безводных ортофосфата и пирофосфата цинка ( Zn3(PO4)2 и Zn 2 P2O 7 ). Эндотермические эффекты при 464 и 483 °С могут соответствовать переходу аморфного Zn2P2O 7 в кристаллическое состояние. Это подтверждается данными рентгенофазового анализа - на рентгенограмме образцов, прокаленных при температуре 480 °С, присутствуют характеристические пики Zn3(PO4)2 и Zn2P2O7 .
Согласно данным электронной микроскопии
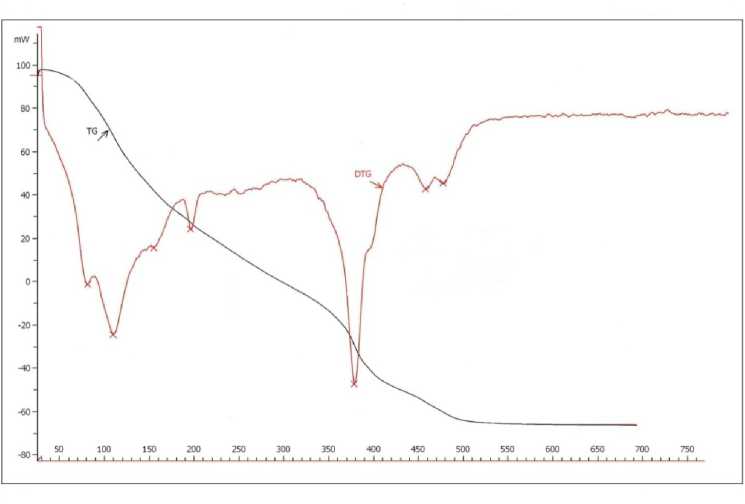
Рисунок 4 – Результаты дифференциально-термического анализа осадка, полученного осаждением ионов цинка из отработанного электролита цинкования ОАО «МЗАЛ» раствором фосфата натрия
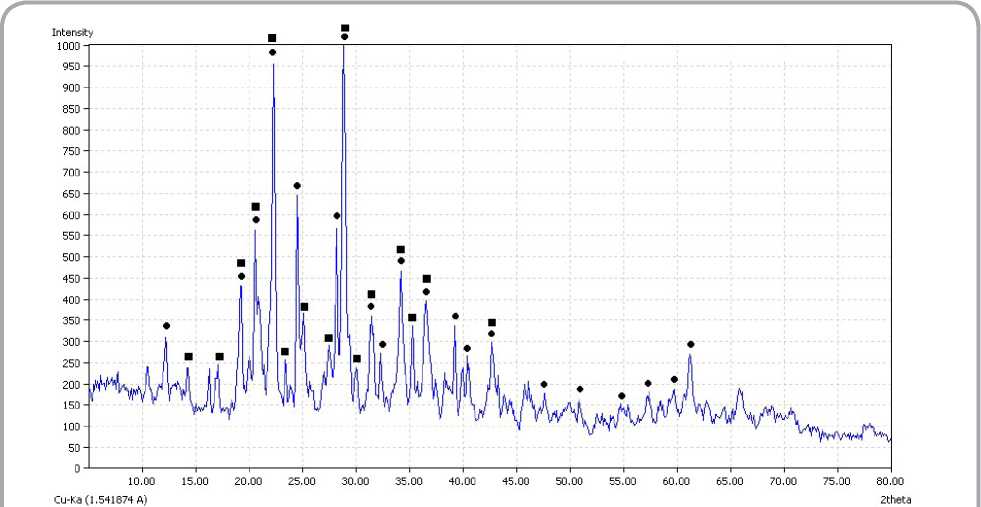
Рисунок 5 – Рентгенограмма осадка, полученного осаждением ионов цинка из отработанного электролита цинкования ОАО «МЗАЛ» раствором фосфата натрия, прокаленного при температуре 480 °с ( • — характеристические пики фосфата цинка, — пирофосфата цинка)
содержание цинка в полученном осадке составляет 66,54 мас. %, кислорода – 20,55 мас. %, фосфора – 12,91 мас. %. Наличие примесей не наблюдается.
Процесс осаждения ионов цинка раствором гидрофосфата натрия описывается уравнением:
лением аммиака и образованием пирофосфата цинка, что подтверждается данными рентгенофазового анализа (рисунок 7).
Согласно данным электронной микроскопии содержание цинка в полученном осадке составляет 43,86 мас. %, кислорода – 34,75 мас. %,
. (6)
Однако поскольку осаждение происходит из отработанного электролита цинкования, представляющего собой сложную многокомпонентную систему с высоким содержанием хлорида аммония, наблюдается образование цинк-аммо-ний фосфата (NH 4 )Zn(PO 4 ) , что подтверждается данными рентгенофазового анализа (рисунок 6). Образование цинк-аммонийфосфата при использовании в качестве осаждающего раствора гидрофосфата натрия обусловлено более высоким значением рН по сравнению с осаждением фосфатом натрия.
Наличие на термограмме полученного осадка эндотермического минимума при температуре 430 °С свидетельствует о разложении цинк-ам-моний фосфата, которое сопровождается выде-
фосфора – 21,39 мас. %. Наличие примесей не наблюдается.
Данные рентгенофазового анализа и электронной микроскопии осадков, полученных осаждением Zn2 + из отработанных электролитов цинкования других белорусских предприятий, подтверждают образование во всех случаях одинаковых по химическому и фазовому составу осадков, а также их схожее поведение при термообработке (таблица 4).
Полученные экспериментальные данные свидетельствуют о том, что примеси, присутствующие в отработанных электролитах (блескообразователи, смачиватели и др.), не влияют на осаждение ионов цинка, а полученные материалы могут использоваться в качестве пигментов
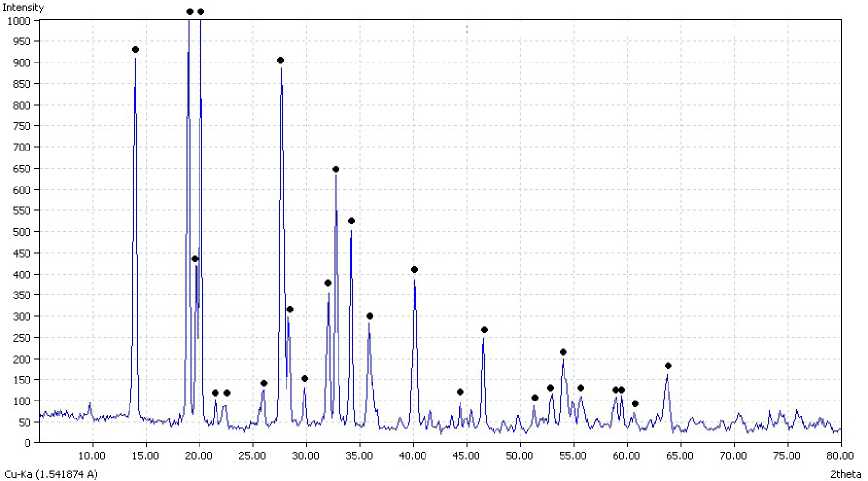
Рисунок 6 – Рентгенограмма осадка, полученного осаждением ионов цинка из отработанного электролита цинкования оао «мзал» раствором гидрофосфата натрия ( • - характеристические пики цинк-аммоний фосфата)

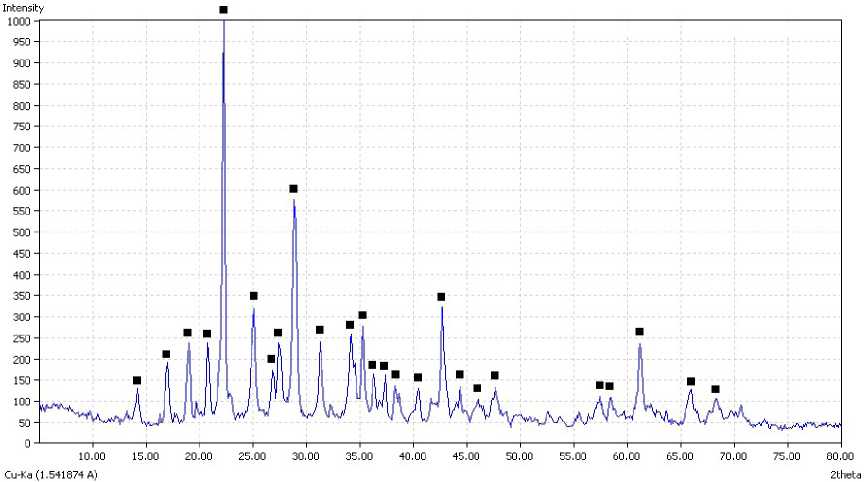
Рисунок 7 – Рентгенограмма осадка, полученного осаждением ионов цинка из отработанного электролита цинкования ОАО «МЗАЛ» раствором гидрофосфата натрия, прокаленного при температуре 430 °С ( -характеристические пики пирофосфата цинка)
Для подтверждения возможности использования полученных порошков в качестве пигментов после их измельчения были определены такие свойства, как маслоемкость и укрывистость. Укрывистость составила от 140 до 175 г/м2, мас-лоемкость – от 36 до 45 г/100 г. Оптимальное значение маслоемкости пигментов, применяе-
мых в лакокрасочной промышленности, составляет 30—50 г/100 г пигмента [12]. При высокой маслоемкости пигмента затрудняется его диспергирование в пленкообразующем веществе, при низкой маслоемкости, обусловленной гидрофильностью пигмента, получаемые краски нестойки при хранении и расслаиваются.
Результаты проведенных исследований позволят решить проблему утилизации отработанных растворов электролитов цинкования и расширить сырьевую базу для производства пигментов.
Список литературы Исследование возможности получения пигментов из отработанных электролитов цинкования
- Марцуль, В.Н., Залыгина, О.С. (2014), Экологические вопросы организации гальванического производства, Экология на предприятии, 2014, No 8 (38), С. 34-49.
- Марцуль, В.Н., Залыгина, О.С., Шибека, Л.А., Лихачева, А.В., Романовский, В.И., (2012), Некоторые направления использования отходов гальванического производства, Труды БГТУ, Химия и технология неорганических веществ, 2012, No 3, С. 70-75
- Пат. 2208067 Российская федерация, МПКC 25 D 21/18, C 22 B34/32. Способ регенерации хромовых электролитов, В.В. Трибунский, А.В. Николаева, В.А. Никулин, В.Л. Подберезный, В.И. Аксенов. Опубл. 10.07.03.
- Тураев, Д.Ю. (2006), Опыт применения метода мембранного электролиза в гальваническом производстве на участке цинкования и кадмирования, Гальванотехника и обработка поверхности, 2006, No 3, С. 28-33.
- Агафонова, Е.Ю. (2013), физико -химический состав продуктов осаждения никеля из отработанных никельсодержащих растворов, Технология -2013, Сборник тезисов докладов международной научно -технической конференции, Северодонецк, 2013, с. 69.
- Пат. 2069240 Российская федерация, МПКC 25 D 21/18. Способ утилизации кислого отработанного раствора гальванического производства, Н.К. Рослякова, Р.С. Росляков. Опубл. 20.11.1996, 2006.
- Горева, Т.В. (2007), Технология получения свинцового крона с использованием отходов гальванического производства, автореф. дис... канд. тех. наук, Москва, 2007, -140 с.
- Дринберг, А.С. (2007), Неорганические пигменты, производство и перспективы, Лакокрасочные материалы и их применение, 2007, No 12, С. 20-28.
- Беленький, Е.ф. (1960), Химия и технология пигментов, Ленинград, 756 с
- Щегров, Л.Н. (1987), Фосфаты двухвалентных металлов, Киев, 212 с.
- Горловский, И.А., Козулин, Н.А. (1980), Оборудование заводов лакокрасочной промышленности, Ленинград, 200 с


