Изменение показателей скелетного гомеостаза в динамике лечения пациентов с закрытыми переломами нижней конечности, сочетанными с черепно-мозговой травмой
Автор: Лунева Светлана Николаевна, Стогов Максим Валерьевич, Бойчук С.П., Лукин С.Ю., Ерофеева Т.Н.
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 1, 2005 года.
Бесплатный доступ
Изучены особенности скелетного гомеостаза, экскреции кальция, фосфора и оксипролина с мочой у больных с закрытыми переломами нижних конечностей сочетанными с черепно-мозговой травмой. Показано, что динамика экскреции кальция, фосфора и оксипролина у пациентов с закрытыми переломами конечностей, сочетанными с черепно-мозговой травмой, не отличалась от таковой при неосложненных переломах, однако глубина изменений более выражена при сочетанном переломе. Отсутствие межгрупповых различий в характере корреляционной зависимости между концентрацией изученных показателей в сыворотке крови и уровнем их экскреции с мочой говорило о том, что наличие сопутствующего повреждения, а именно ЧМТ, не влияло на тип экскреции кальция, фосфора и оксипролина с мочой.
Сочетанная черепно-мозговая травма, биохимия крови, суточная моча, скелетный гомеостаз
Короткий адрес: https://sciup.org/142120784
IDR: 142120784
The change of skeletal homeostasis measurements in the treatment dynamics of patients with lower limb closed fractures combined with craniocerebral injury
The characteristic features of skeletal homeostasis, urinary excretion of calcium, phosphorus and oxyproline in patients with lower limb closed fractures combined with craniocerebral injury were studied. It was demonstrated that the dynamics of urine excretion of calcium, phosphorus and oxyproline in patients with lower limb closed fractures combined with craniocerebral injury didn't differ from that for uncomplicated fractures; however, the intensity of changes was more marked in case of combined fractures. The absence of the differences between the groups in the character of correlation dependence of serum concentration of the measurements studied and their urine excretion degree indicated the fact that the presence of associated damage, it means craniocerebral injury, didn't influence the type of urine excretion of calcium, phosphorus and oxyproline.
Текст научной статьи Изменение показателей скелетного гомеостаза в динамике лечения пациентов с закрытыми переломами нижней конечности, сочетанными с черепно-мозговой травмой
Нейроэндокринная регуляция адаптационной функции организма, обеспечивающей и поддерживающей гомеостаз, существенно нарушается при травматической болезни головного мозга. Расстройства эндокринной регуляции функций организма развиваются в первые минуты после черепно-мозговой травмы (ЧМТ), они быстро прогрессируют и вызывают значительные изменения в активности многих физиологических систем [1, 2]. Изменения в функционировании центральной нервной системы и желез внутренней секреции, нарушение активности висцеральных органов и сдвиги в метаболизме неизбежно отражаются на состоянии крови [3]. Исследования последнего десятилетия внесли существенный вклад в раскрытие меха- низмов репаративных процессов при сочетанной ЧМТ. В то же время, несмотря на значительные успехи, достигнутые в изучении биохимических изменений, развивающихся при травматических репаративных процессах, в связи с большой сложностью проблемы остается множество неясных вопросов, и до сих пор не существует единых общепринятых представлений о закономерностях сдвигов показателей скелетного гомеостаза в сыворотке крови при переломах длинных костей, сочетанных с ЧМТ.
Целью настоящего исследования явилось изучение особенностей скелетного гомеостаза, экскреции кальция, фосфора и оксипролина с мочой у больных с закрытыми переломами нижних конечностей, сочетанными с черепно-мозговой травмой.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Была исследована сыворотка крови и суточная моча 14 человек с закрытыми переломами костей нижней конечности (1-я группа) в возрасте 18-51 года (средний возраст 33,6) и 22 пациента с закрытыми переломами костей нижней конечности, сочетанными с черепно-мозговой травмой (2-я группа) в возрасте от 18 до 55 лет (средний возраст 30,8). Все пациенты были пролечены методом чрескостного остеосинтеза аппаратом Г.А. Илизарова. Средний срок между травмой и наложением аппарата составлял 7 суток. В качестве нормы использовали значения показателей суточной мочи и сыворотки крови 19 практически здоровых людей обоего пола от 18 до 42 лет (средний возраст 32,9). Концентрацию общего кальция, неорганического фосфата в моче и сыворотке крови определяли на биохи- мическом анализаторе Stat Fax 1904 Plus, используя наборы реактивов фирмы «Vital Diag-nostic». Концентрацию оксипролина - по реакции с реактивом Эрлиха [4]. Количество гексуроновых кислот (ГУК) определяли по Bitter [5], сульфатной серы по Morgan [6, 7], сиаловых кислот (СК) по Warren [8], вычисляли также соотношение сульфат /гексуроновые кислоты.
Для нахождения достоверности различий с нормой использовали непараметрические критерии рандомизации (для выборок n<12) и Вил-коксона для независимых выборок (выборки умеренной численности n 12). Достоверность межгрупповых различий определяли с помощью непараметрического критерия Крускала-Уоллиса.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Проведенное нами изучение содержания гексуроновых кислот, сиаловых кислот и сульфатов в группе больных с ЧМТ выявило достоверные отличия значений этих показателей от аналогичных в сыворотке крови больных 1-й группы. Нами было обнаружено увеличение концентрации сульфатов у больных 2-й группы (рис. 1) до операции на 14 %, тогда как содержание ГУК в сыворотке крови больных возросло лишь на 6 % (рис. 2). Отношение сульфат/ГУК в сыворотке крови этих больных превышало нормальное в 2 раза. Вместе с этим было обнаружено достоверное уменьшение содержания СК в сыворотке крови больных с ЧМТ (рис. 3). Очевидно, протеогликаны соединительной ткани больных с ЧМТ включают структурно измененные молекулы гликозаминогликанов с высоким содержанием сульфатных групп, что подтверждается значительным возрастанием содержания сульфатов на фоне менее значительного увеличения концентрации ГУК. Наиболее выраженные изменения содержания сульфатных групп наблюдались нами через 14 дней и через 3 месяца после операции.
□ норма □ 1 группа ■ 2 группа
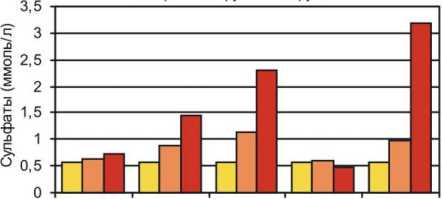
д/о 3 дн. 14 1 мес. 3 мес.
дни после операции
Рис. 1. Содержание сульфатов неорганических в сыворотке крови больных с переломами нижних конечностей (1 группа) и сочетанной ЧМТ (2 группа)
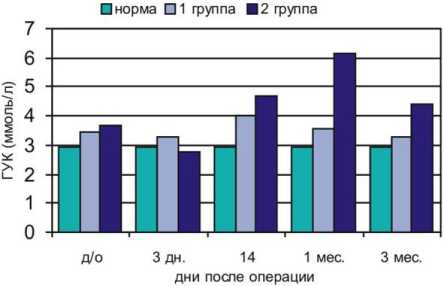
Рис. 2. Содержание гексуроновых кислот в сыворотке крови больных с переломами нижних конечностей (1 группа) и сочетанной ЧМТ (2 группа)
□ норма П1 группа П2 группа
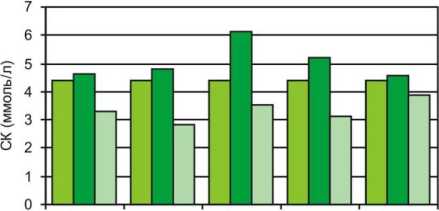
д/о 3 дн. 14 1 мес. Змее, дни после операции
Рис. 3. Содержание сиаловых кислот в сыворотке крови больных с переломами нижних конечностей (1 группа) и сочетанной ЧМТ (2 группа)
Известно, что сульфгидрильные группы помимо молекул протеогликанов входят в состав различных ферментов и гормонов, что обусловливает их функциональную активность в осуществлении процессов интрамедиарного обмена. У больных первой группы мы наблюдали схожую тенденцию изменения концентрации сульфатов
(рис. 1). В исследованиях, проведенных ранее С.С. Рабиновичем, наблюдалось снижение в крови как общих, так и белковых сульфгидрильных групп [9]. Вероятно, этот показатель зависит от тяжести ЧМТ и его значения уменьшаются при возникновении глубоких патологических сдвигов во внутренней среде организма. Разнонаправленными оказались изменения в содержании СК в сыворотке крови больных 1-й и 2-й групп. Так, у больных с сочетанной ЧМТ происходило достоверное снижение концентрации СК на протяжении всего срока лечения (рис. 3). Это косвенно может свидетельствовать об изменении синтеза белков в печени и снижении иммунитета у больных с ЧМТ и высокой вероятности развития у них вторичного иммунодефицита.
Ведущую роль в обеспечении скелетного гомеостаза организма играют электролиты, общее количество которых в биологических жидкостях должно быть относительно постоянным. Перестройка регуляторных механизмов скелетного гомеостаза происходит в первые трое суток после остеосинтеза, что подтверждают приведенные на рисунках 4-7 результаты исследования ряда показателей минерального обмена у больных с переломами длинных костей и больных с переломами костей нижней конечности, сочетанных с ЧМТ, а также здоровых людей той же возрастной группы.
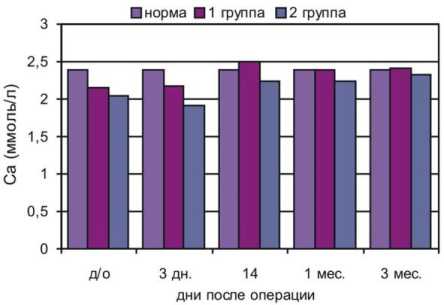
Рис. 4. Содержание кальция в сыворотке крови больных с переломами нижних конечностей (1 группа) и сочетанной ЧМТ (2 группа)
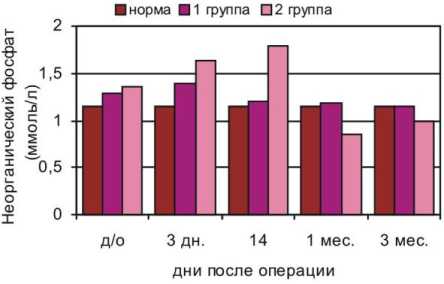
Рис. 5. Содержание фосфата неорганического в сыворотке крови больных с переломами нижних конечностей (1 группа) и сочетанной ЧМТ (2 группа)
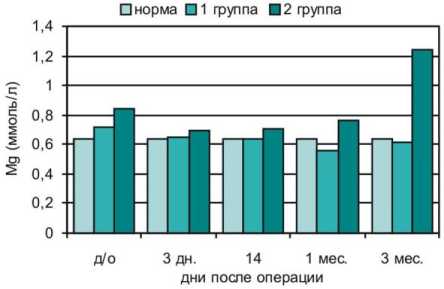
Рис. 6. Содержание магния в сыворотке крови больных с переломами нижних конечностей (1 группа) и сочетанной ЧМТ (2 группа)
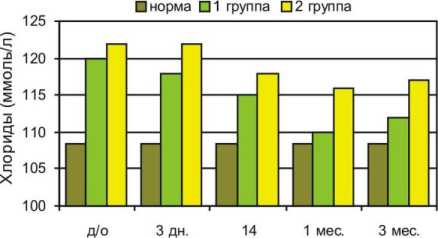
дни после операции
Рис. 7. Содержание хлоридов в сыворотке крови больных с переломами нижних конечностей (1 группа) и сочетанной ЧМТ (2 группа)
Представленные на рисунках данные позволяют заключить, что динамика содержания электролитов в сыворотке крови больных 1-й и 2-й групп была схожа, однако глубина изменений более выражена при сочетанной травме. Это побудило нас исследовать показатели суточной мочи у пациентов с закрытыми переломами конечностей, сочетанными с черепномозговой травмой, и больных с неосложненными переломами нижних конечностей.
Динамика экскреции с мочой кальция, фосфора и оксипролина в ходе лечения представлена на рисунках 8-10. Концентрация кальция в суточной моче в обеих группах имела тенденцию к росту, при этом статистически значимые отличия от нормы наблюдались лишь для первой группы через месяц после операции, на этом же сроке были отмечены и достоверные межгрупповые различия (рис. 8).
Уровень экскреции фосфата в обеих группах достоверно снижался на третьи сутки после операции (рис. 9). К данному сроку наблюдались и достоверные межгрупповые отличия: содержание фосфора в суточной моче пациентов 2-й группы было ниже, чем у пациентов 1-й группы. Сравнивая динамику экскреции фосфора и кальция в обеих группах в ходе лечения, можно отметить общую тенденцию снижение концентрации фосфора в суточной моче сопровождалось ростом в ней концентрации кальция.
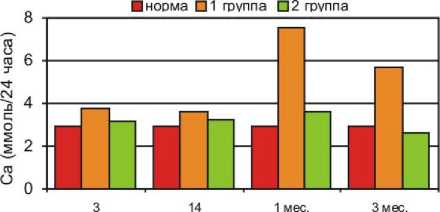
дни после операции
Рис. 8. Содержание кальция в суточной моче больных с переломами нижних конечностей (1 группа) и сочетанной ЧМТ (2 группа)
■ норма П1 группа D2 группа
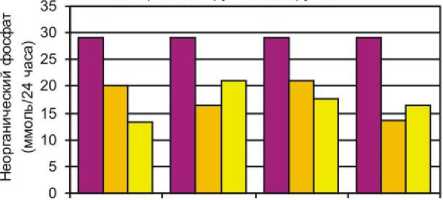
3 14 1 мес 3 мес.
дни после операции
Рис. 9. Содержание фосфата в суточной моче больных с переломами нижних конечностей (1 группа) и сочетанной ЧМТ (2 группа)
Концентрация оксипролина в суточной моче в обеих группах на всех этапах лечения значи- тельно превышала норму, причем максималь- ные значения приходились на третьи сутки после операции (рис. 10). Межгрупповые отличия наблюдались в первом месяце после операции, когда уровень оксипролина у пациентов 2-й группы был выше, чем у пациентов первой.
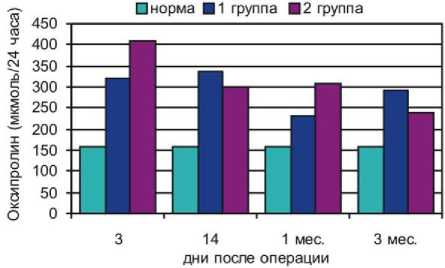
Рис. 10. Содержание оксипролина в суточной моче больных с переломами нижних конечностей
(1 группа) и сочетанной ЧМТ (2 группа)
В свою очередь, во 2-й группе экскреция оксипролина была повышенной, а экскреция фосфора сниженной в отличие от пациентов 1-й группы. Отмеченные закономерности экскреции кальция, фосфора и оксипролина соответствуют трем фазам репаративного костеобразования, выделенных А.М. Герасимовым (1986) [10]. Так, фаза резорбции при консолидации костных переломов начиналась одновременно в обеих группах на третий день после операции и со- провождалась резким снижением экскреции фосфора и увеличением экскреции кальция, при этом наиболее выражены эти изменения были во 2-й группе. Сглаживание межгрупповых различий на второй неделе после операции говорило о начале фазы регенерации в обеих группах. Этап кальцификации в обеих группах начинался через три месяца после операции, когда экскреция кальция и фосфора с мочой уменьшалась.
Для более полной оценки межгрупповых различий мы провели корреляционный анализ между уровнем кальция, фосфора и оксипролина в сыворотке крови и экскрецией их с мочой.
Анализ выявил, что между уровнем общего кальция, фосфора, свободного и белоксвязанно-го оксипролина в сыворотке крови и моче пациентов обеих групп отсутствовала линейная зависимость, значения коэффициента корреляции, характеризующего линейную зависимость, были недостоверны и не превышали 0,30 (табл. 1).
Поэтому для определения степени взаимосвязи признаков определяли корреляционное отношение (η), характеризующее любой тип связи. Оказалось, что корреляционное отношение для всех показателей было близко к единице, что характеризовало высокую степень нелинейной зависимости. Дальнейший анализ позволил выявить тип этой зависимости, которая выражалась через уравнение параболы второго порядка. Корреляционное отношение приближалось к линейному типу лишь для отношения оксипролина мочи к свободному оксипролину сыворотки в первой группе. Наличие нелинейной зависимости между концентрацией кальция и фосфора в сыворотке крови и их уровнем в суточной моче связано с регулирующим влиянием ЦНС и гормонов на процесс их экскреции. Увеличение экскреции одного из этих ионов сопровождалось снижением выделения другого. В том случае, когда один из них начинал выделяться в избыточном количестве, наступала перестройка типа гормонального регулирования, и уровень его экскреции с мочой уменьшался. Подобный тип регулирования, по-видимому, характерен и для экскреции оксипролина.
Представленные данные позволяют заключить, что динамика экскреции кальция, фосфора и оксипролина у пациентов с закрытыми переломами конечностей, сочетанных с черепномозговой травмой, не отличалась от таковой при неосложненных переломах, однако глубина изменений более выражена при сочетанном переломе. Отсутствие межгрупповых различий в характере корреляционной зависимости между концентрацией изученных показателей в сыворотке крови и уровнем их экскреции с мочой говорило о том, что наличие сопутствующего повреждения, а именно ЧМТ, не влияло на тип экскреции кальция, фосфора и оксипролина с мочой.
Таблица 1
Коэффициенты корреляции и корреляционное отношение между исследуемыми показателями в суточной моче и сыворотке крови
|
Ca мочи /Са крови |
P мочи /P крови |
ОП моча /ОПС кровь |
ОП моча /ОПБ кровь |
||||||
|
1 гр. |
2 гр. |
1 гр. |
2 гр. |
1 гр. |
2 гр. |
1 гр. |
2 гр. |
||
|
r р |
0,25 |
0,04 |
0,11 |
-0,04 |
r s |
0,30 |
-0,05 |
-0,14 |
0,08 |
|
n |
23 |
45 |
23 |
45 |
n |
10 |
28 |
10 |
28 |
|
p r |
0,12 |
0,39 |
0,30 |
0,59 |
p r |
0,20 |
0,60 |
0,64 |
0,35 |
|
η |
0,89 |
0,90 |
0,97 |
0,83 |
η |
0,65 |
0,70 |
0,98 |
0,95 |
|
p η |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
p η |
<0,05 |
<0,001 |
<0,01 |
<0,001 |
Сокращения: r р – коэффициент корреляции по Пирсону; r s коэффициент корреляции по Спирману; n – количество наблюдений;
р – уровень значимости; η – корреляционное отношение; ОПС – свободный оксипролин; ОПБ – белоксвязанный оксипролин.


