Изменения активности процессов липопброксидации под влиянием экстракта очитка большого (Sedum maximum (L.) Hoffm.)
Автор: Пластун В.О., Комарова Е.Э., Дурнова Н.А., Афанасьева Г.А., Курчатова М.Н., Андреева Н.В.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Медико-биологические науки
Статья в выпуске: 2, 2015 года.
Бесплатный доступ
Изучено изменение активности процессов липопероксидации (ПОЛ) в сыворотке крови белых крыс под влиянием водного раствора спиртового экстракта очитка большого (Sedum maximum (L.) Hoffm., Crassulaceae) в концентрациях 100, 200 и 300 мг/кг на модели индуцированного окислительного стресса. Интенсивность процессов ПОЛ оценивали по содержанию в сыворотке крови животных МДА и ГПЛ, интенсивность аутоинтоксикации - по содержанию МСМ. Установлено, что экстракт в концентрации 200 мг/кг и выше обладает способностью снижать содержание промежуточных продуктов ПОЛ в сыворотке крови крыс, подвергшихся прооксидантному действию диоксидина.
Пол, растительные экстракты
Короткий адрес: https://sciup.org/147204722
IDR: 147204722 | УДК: 577.164.39+352.38
Lipoperoxidation activity alteration influenced by big stonecrop (Sedum maximum (L.) Hoffm.) extract
Lipoperoxidation activity (LPO) alteration in white rat blood serum, influenced by big stonecrop (Sedum maximum (L.) Hoffm., Crassulaceae) dry extraction water solution in concentrations 100, 200 and 300 mg/kg on the model of induced oxidation stress was studied. Lipoperoxidation activity was evaluated, measuring lipid hydroperoxide and malondialdehyde in rat blood serum autointoxication activity - measuring molecules of average weight concentration. The ability of big stonecrop extraction to decrease lipoperoxidation products amount in DO prooxidant-effected rat blood serum in dose 200 mg/kg and more was ascertained.
Текст научной статьи Изменения активности процессов липопброксидации под влиянием экстракта очитка большого (Sedum maximum (L.) Hoffm.)
Проблема оксидативного стресса и состояния активности процессов липопероксидации в норме и при различных формах патологии привлекает внимание многих специалистов [Бобырев, 1989; Заггщуллина. 2005; Гнусина, 2007]. В настоящее время нс вызывает сомнения тот факт, что активация процессов перекисного окисления липидов (ПОЛ) является типовым патологическим процессом, сопровождающим развитие различных патологических состояний, в частности, в этиологии и клинических проявлениях бактериальных инфекций и интоксикаций, неоплазий, эндокринных, сердечно-сосудистых, желудочно-кишечных и др. заболеваний [Афанасьева, Чеснокова, 2009].
В большинстве случаев исход развития патологии определяется не только особенностями происхождения, механизмами воздействия этиологических факторов, но и интенсивностью вторичных неспсцифичсских функциональных и метаболических сдвигов, развивающихся, зачастую, по сте-
(С Пластун В. О., Комарова Е. Э Урнова Н А.. Афанасьева Г. А., Курчатова М. Н.; Андреева Н. В., 2015
реотипным механизмам и в значительной мере потенцирующих действие патогенного агента. Поэтому актуальное значение приобретает проблема фармакологической коррекции свободно-радикальных процессов с использованием препаратов, оказывающих антиоксидантное и антигипоксант-ное действие.
Одним из перспективных направлений поиска новых средств патогенетической и симптоматической терапии заболеваний и патологических процессов является исследование возможностей эффективной регуляции процессов ПОЛ с помощью биологически активных соединений растительного происхождения. Преимуществами этих веществ ЯВЛЯЮТСЯ отсутствие токсических, побочных эффектов. «мягкое» воздействие на организм, что позволяет использовать их не только для коррекции патологических СДВИГОВ, НО и в целях профилактики развития заболеваний и осложнений.
Очиток большой VSedum maximum (L.) НоЛпт. Crassuiaceae) широко применяется в народной медицине. в том числе как тонизирующее и адапто-генное средство [Шнякина. Краснов, 1974: Барна) лов и др., 2001]. однако спектр действия его БАВ пока мало изучен. Имеются сведения о способности отвара близкородственного вида о. пурпурного (S. lelephium L.) ингибировать окислительные процессы in vitro [Барнаулов и др., 2001]. До настоящего момента в отечественной и зарубежной литературе отсутствуют сведения о влиянии биологически активных компонентов травы о.
большого на состояние активности процессов ли-попероксидации в условиях нормы и патологии.
Целью работы явилось установление возможностей влияния водного раствора спиртового экстракта травы очитка большого на активность свободнорадикального окисления липидов в экспериментальных условиях.
Материалы и методы исследования
Материалом для исследований являлась трава о. большого, собранная на территории Саратовской области в августе 2013 г. Спиртовые извлечения были получены методом двукратной экстракции 95%-ным этанолом, после чего упарены насухо. Спиртовые экстракты упаривали насухо, после чего растворяли сухой остаток в воде.
Исследования проводили в экспериментах in vivo на 54 беспородных белых крысах-самцах массой 180.0 ± 20.0 г, которые содержались в одинаковых условиях на стандартном пищевом рационе. Оксидативный стресс моделировали путем внутрибрюшинного введения экспериментальным животным 1%-ного раствора диоксидина (ДО) в дозе 100 мг/мл. ДО часто используется в экспериментах в качестве прооксиданта, поскольку индуцирует образование в организме свободных форм кислорода (Н2О2. Он-радикалов) [Дурнев и др,, 1989; Абдуллин и др., 2002; Празднова. 2013].
В эксперименте были использованы 9 групп но 6 крыс в каждой (таблица). Все животные содержались в стандартных условиях вивария.
Группы животных» использованных в эксперименте
|
№ группы |
Название группы |
Вводимые вещества и их концентрации, мг/кг |
|
1 |
Интактная |
|
|
2 |
Контроль 1 (позитивный) |
ДО 100 |
|
3 |
Контроль 2 (негативный) |
Вода юо |
|
4 |
Опытная 1 |
ДО 100; экстракт 100 |
|
5 |
Опытная 2 |
Экстракт 100 |
|
6 |
Опытная 3 |
ДО 100; экстракт 200 |
|
7 |
Опытная 4 |
Экстракт 200 |
|
8 |
Опытная 5 |
ДО 100; экстракт 300 |
|
9 |
Опытная 6 |
Экстракт 300 |
Все препараты вводились внутрибрюшинно один раз в день на протяжении 4 сут. На четвертые сутки через 1 ч. после введения растворов животных дскапитировали и отбирали кровь для анализа. Состояние активности процессов свободнорадикального окисления липидов оценивали по содержанию в сыворотке крови экспериментальных крыс промежуточных продуктов ПОЛ - гидроперекисей липидов (ГПЛ) и малонового диальдегида (МДА). Уровень ГПЛ и МДА определяли общепринятыми епскрофотометрическими методами на спектрофотометре «Shimadzu» СФ-UV 1800. Уро вень аутоинтоксикации определяли по содержанию в сыворотке крови молекул средней массы (МСМ) [Медицинские .... 2002].
Статистическую обработку проводили при помощи пакета программного обеспечения StatSoft Статистика 10.0. Достоверность полученных результатов оценивалась с использованием критерия Манна - Уитни, различия групп считались достоверными при уровне значимости р<0.05.
Результаты и их обсуждение
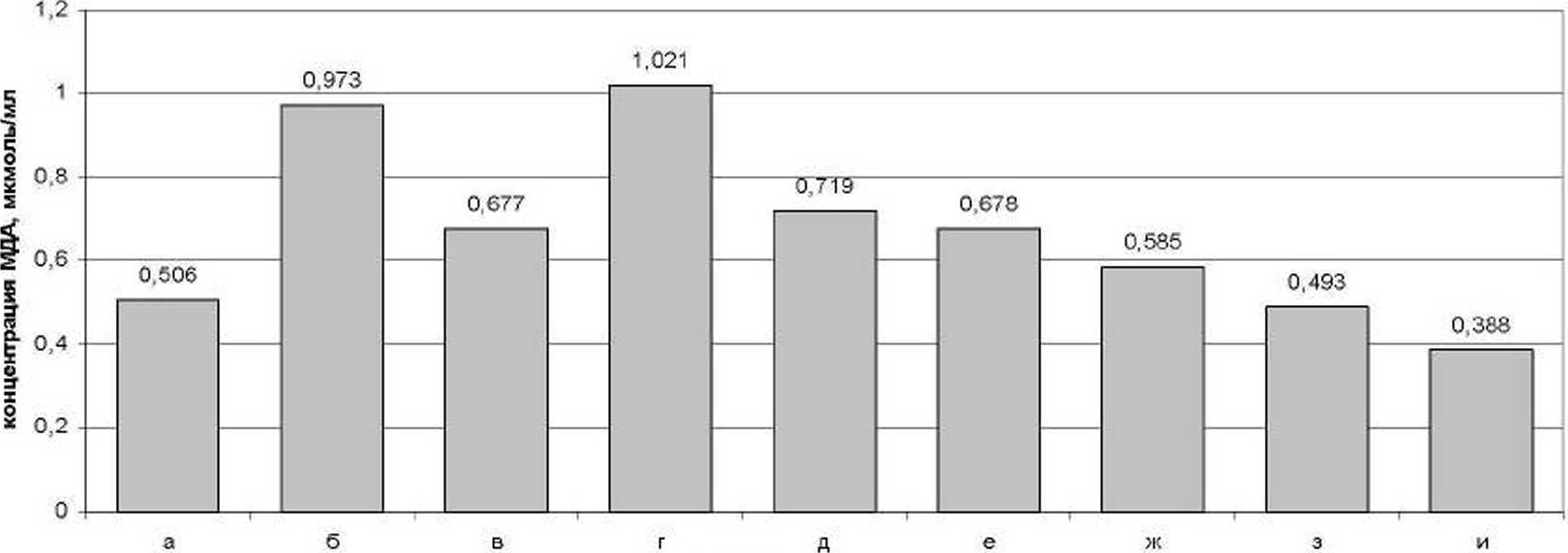
Как показали результаты проведенных иссле- дований, после внутрибрюшинного введения белым крысам 1%-ного раствора ДО на протяжении 4 сут. в дозе 100 мг/кг происходило повышение уровня МДА (рис. 1. б) в сыворотке крови на 90%.
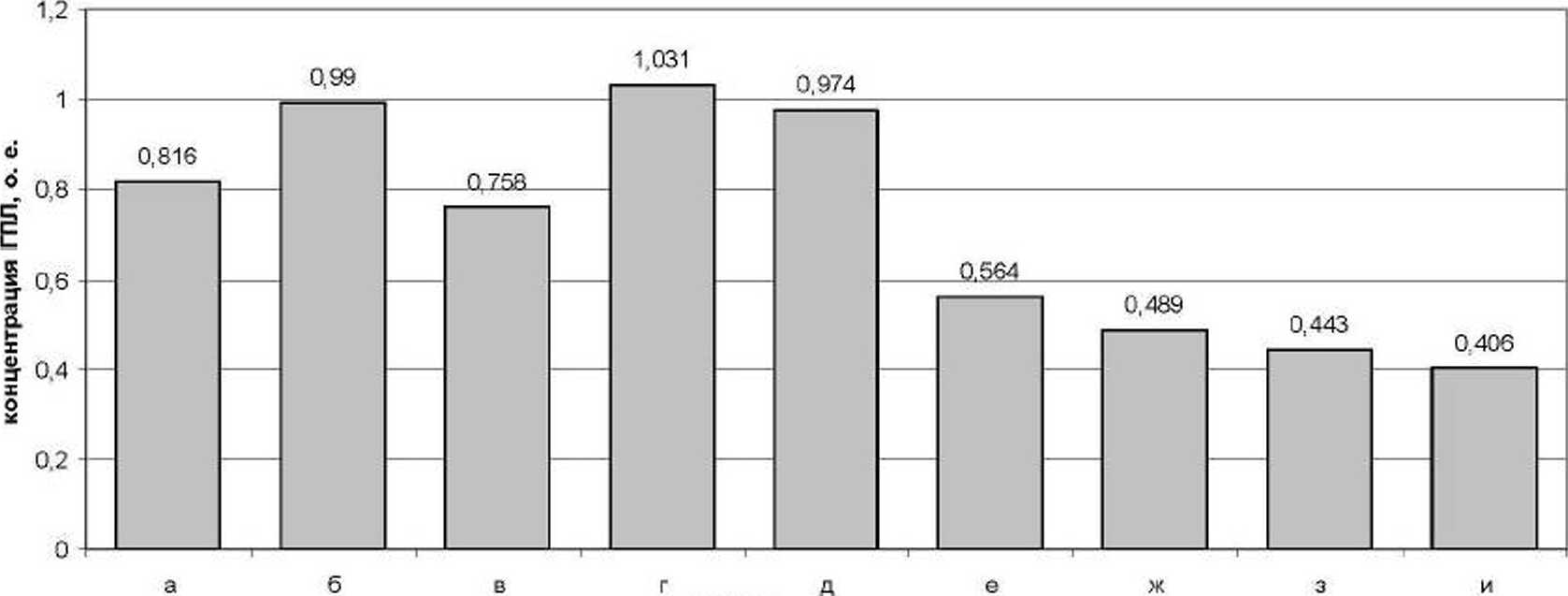
ГПЛ (рис. 2. б) на 20% раза (р<0.05) по сравнению с аналогичными показателями интактной группы животных (рис. 1. а: рис. 2. а) и группой негативного контроля (рис.1, в. рис.2, в).
группы
Рис. 1. Концентрация МДА в сыворотке крови экспериментальных белых крыс: а - интактная группа; б - контроль 1; в - контроль 2; г - опытная 1; д - опытная 2; е - опытная 3; ж -опытная 4; з - опытная 5; и - опытная 6
группы
Рис. 2. Концентрация ГПЛ в сыворотке крови экспериментальных белых крыс.
Обозначения такие же, как на рис. 1
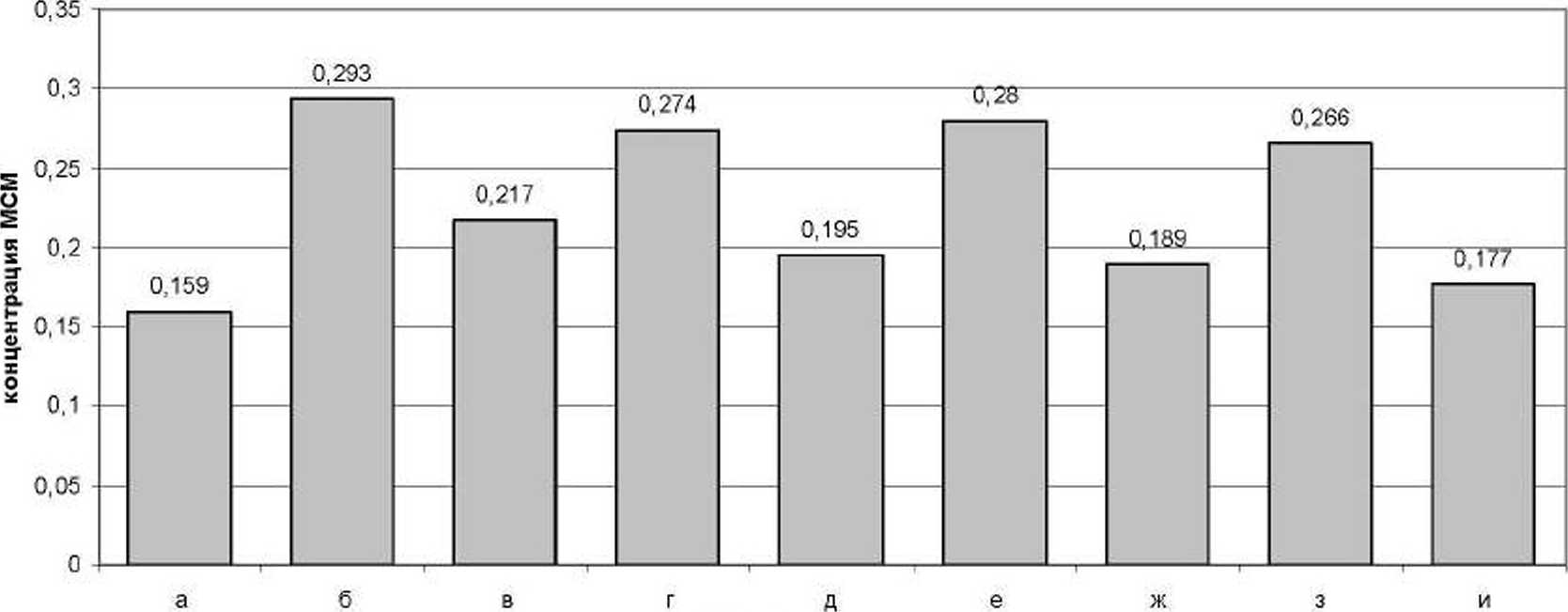
Накопление промежуточных продуктов липо-пероксидации на фоне введения диоксидина сочеталось с развитием выраженной эндогенной интоксикации белых крыс, что подтверждалось увеличением содержания в сыворотке крови МСМ (рис. 3. б) на 40% по сравнению с показателями животных, которым вводили эквивалентный объем воды (р<0.01) (рис. 3, в). Полученные результаты свидетельствовали об активации процессов липопсрок-сидации под влиянием ДО.
В последующих сериях экспериментов исследовали возможности биологически активных веществ водного раствора спиртового экстракта травы о. большого коррегировать прооксидантные эффекты ДО. Как оказалось, при сочетании введе ния на протяжении 4 сут. 1%-ного раствора ДО в дозе 100 мг/кг и последующего внутрибрюшинного введения водного раствора спиртового экстракта о. большого в дозе 200 мг/кг происходило значительное снижение уровня продуктов липоперок-сидации в сыворотке крови белых крыс: МДА на 40% (рис. 1, е). ГПЛ на 75% (р<0.01) (рис. 2, е). Фоновое введение экстракта о. большого в дозе 200 мг/кг вызывало незначительное повышение уровня этих веществ в сыворотке экспериментальных животных (рис. 1. ж; рис. 2, ж) в сравнении с интактной группой и было сопоставимо с их уровнем у группы негативного контроля.
Уровень эндогенной интоксикации у экспериментальных животных, оиенивемый по содержа- нию МСМ в сыворотке крови, при использовании этой концентрации экстракта о. большого сохранялся на том же уровне, что и у животных контрольных групп. Отличие количества МСМ как в о. большого в сочетании с ДО. от позитивного контроля. так и у группы животных, получавших только экстракт от негативного контроля, было не значимо (р>0.05: рис. 3, е. ж).
сыворотке крови животных, получавших экстракт
группы
Рис. 3. Концентрация МСМ в сыворотке крови экспериментальных белых крыс.
Обозначения такие же, как на рис. 1
Далее была изучена зависимость протекторных эффектов водного раствора спиртового экстракта травы о. большого от величины используемой дозы растительного препарата. Для этого провели сравнительную оценку содержания промежуточных продуктов липопероксидации (ГПЛ, МДА) и интегративного показателя аутоинтоксикации -МСМ в крови белых крыс при использовании экстракта о. большого в дозах 100 мг/кг и 300 мг/ кг.
Полученные результаты свидетельствовали об отсутствии протекторного эффекта препарата при использовании его в дозе 100 мг/кг. что подтверждалось сохранением высокого содержания МДА (рис. 1, г, д) и ГПЛ (рис.2, г, д) в сыворотке крови животных, сопоставимого с таковым в группе позитивного контроля.
В серии экспериментов с сочетанным введением ДО с экстрактом о. большого в дозе 300 мг/кг отмечалось снижение уровня обоих продуктов липопероксидации не только по сравнению с соответствующими показателями группы животных, которым вводился только ДО. но и с показателями белых крыс, получавших ДО в сочетании с экстрактом травы о. большого в дозе 200 мг/кг.
Уровень эндогенной интоксикации в сыворотке крови экспериментальных животных одинаков во всех группах, которым вводили ДО в сочетании с экстрактом, независимо от его концентрации, и значимо не отличается от группы позитивного контроля (р<0.05). В группах, получавших только экстракт о. большого в различных концентрациях, эндогенная интоксикация сохраняется на уровне негативного контроля дтя концентраций 100 и 200
мг/мл (р<0.05). При введении исследуемого экстракта в концентрации 300 мг/мл количество МСМ в сыворотке крови экспериментальных животных снижается относительно позитивного контроля на 20% (р<0.05) и становится сопоставимо с количеством МСМ у интактной группы. В целом, уровень эндогенной интоксикации, оцениваемый по концентрации МСМ в сыворотке крови экспериментальных животных, слабо коррелирует с концентрацией вводимых веществ и интенсивностью протекающих процессов ПОЛ.
Заключение
Установлено, что водный раствор спиртового экстракта о. большого обладает способностью снижать содержание промежуточных продуктов ПОЛ (МДА и ГПЛ) в сыворотке крови крыс, подвергшихся прооксидантному действию ДО. Способность компонентов экстракта подавлять интенсивность процессов липопероксидации в условиях патологии носит дозозависимый характер и проявляется при использовании экстракта о. большого в дозе 200 мг/кг и более. В связи с этим является перспективным более детальное изучение его антиоксидантных свойств по другим маркерам окси-дативного стресса.
Список литературы Изменения активности процессов липопброксидации под влиянием экстракта очитка большого (Sedum maximum (L.) Hoffm.)
- Абдуллин И.Ф. и др. Экспрессная оценка антиоксидантной активности растительного сырья//Тез. докл. II Всерос. конф. «Химия и технология растительных веществ». Казань, 2002. С. 77-78.
- Азнабаева Ю.Г., Каспранский Р.Р., Фархутдинов Р.Р. Антиоксидантные свойства чайных напитков фирмы «Травы Башкирии»//Эфферентная терапия. 2001. Т. 7, № 2. С. 52-56
- Афанасьева Г.А., Чеснокова Н.П. О патогенетической значимости активации процессов липопероксидации в механизмах нарушения реологических свойств крови при экспериментальной чумной интоксикации, индуцируемой фракцией FII вакцинного штамма EV Y.pestis//Вестник Российской академии медицинских наук. 2009. № 2. С. 14-18
- Барнаулов О.Д. и др. Сравнительная оценка антиоксидантной активности (АОА) водных извлечений из растений.//Материалы Х конф. «Нейроиммунология». СПб, 2001. Т. 2. С. 223297
- Бобырев В.Н. Антиоксиданты в клинической практике//Терапевтический архив. 1989. № 3. С. 122-125
- Гнусина С.В. Перекисное окисление липидов и антиоксидантная система у больных сахарным диабетом I типа разного возраста: автореф. дис.... канд. мед. наук. Иркутск, 2007. 21 с
- Дурнев А.Д. и др. Роль свободных радикалов кислорода в механизме мутагенного действия фотрина и диоксидина//Химико-фармацевтический журнал. 1989. Т. 23, № 11. С. 1289-1291
- Загидуллина А.И. Патогенетическое значение процессов перекисного окисления липидов, антиоксидантной защиты и системы гемостаза, коррекция их нарушений методом озонотерапии при роже: автореф. дис.... канд. мед. наук. СПб., 2005. 24 с
- Колесова В.Г. и др. Антиоксидантная терапия растениями//Эфферентная терапия. 1996. Т. 2, № 1. С. 67-70
- Медицинские лабораторные технологии: справочник/под ред проф. А.И. Карпищенко. СПб.: Интермедика, 2002. 600 с
- Празднова Е.В. Оценка биологической активности антиоксидантов на основе анализа экспрессии стресс-индуцибельных бактериальных оперонов: автореф. дис.. канд. биол. наук. Ростов н/Д, 2013. 24 с
- Шнякина Г.П., Краснов Е.А. О фитохимической и медико-биологической изученности видов рода Sedum L.//Растительные ресурсы. 1974. Т. 10, вып. 1. С. 130-135


