Изменения в гемодинамике сегмента конечности вследствие туннелизации при повышенном пульсирующем давлении в полости диафиза длинной кости
Автор: Шевцов В.И., Бунов В.С., Гордиевских Н.И.
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 2, 2005 года.
Бесплатный доступ
В эксперименте на 10 собаках изучены изменения гемодинамики в полости диафиза большеберцовой кости и мягких тканях голени при пульсирующем давлении (ВКД). Выявлено, что туннелизация диафиза приводит к усилению кровообращения в кости и увеличению притока крови к сегменту конечности. При этом в неповреждѐнных тканях вследствие включения механизмов ауторегуляции происходит ограничение кровообращения в пределах диапазона изменений «в норме», которое исчезает после заживления дефектов компактного вещества. Исследование обосновывает применение оперативного вмешательства для получения длительного увеличения притока крови к конечности.
Кость, мышцы, туннелизация, гемодинамика
Короткий адрес: https://sciup.org/142120804
IDR: 142120804
The changes in limb segment hemodynamics as a result of tunnelization with increased pulsing pressure in the cavity of long bone shaft
The changes of hemodynamics in the tibial shaft cavity and in the leg soft tissues have been studied experimentally at pulsing intraosseous pressure (IOP) using 10 dogs. It has been revealed that shaft tunnelization leads to increase of both blood circulation in bone and blood inflow to a limb segment. In addition, in intact tissues circulation is limited within "norma" changes due to turning on the mechanisms of autoregulation, and the limitation disappears after healing compact defects. The authors substantiate the use of surgical intervention to produce prolonged increase of blood inflow to a limb.
Текст научной статьи Изменения в гемодинамике сегмента конечности вследствие туннелизации при повышенном пульсирующем давлении в полости диафиза длинной кости
В РНЦ "ВТО" имени академика Г.А. Илизарова при ишемии для улучшения периферического кровообращения применяют туннелиза-цию костей конечности спицей [4].
Для изучения изменений в гемодинамике диафиза длинной кости после туннелизации были проведены эксперименты с применением медуллографии и электрофизиологических методов исследования. Результаты показали, что через создаваемые спицей дефекты компактного вещества интерстициальная жидкость из полости диафиза перемещается к окружающим кость тканям, вследствие чего внутрикостное давление (ВКД) снижается, что приводит к увеличению фильтрации жидкости из сосудистого русла. ВКД устанавливается на уровне, при котором количество жидкости, фильтрующейся в интерстициальное пространство и перемещаю- щейся за пределы полости диафиза, приходит в соответствие. Через 2-4 месяца происходит заживление дефектов компактного вещества органотипичной костью, перемещение интерстициальной жидкости за пределы кости прекращается и ВКД восстанавливается [5, 6].
Изменения «высокого» пульсирующего ВКД имеют следующие особенности: снижение происходит по мере увеличения дефекта компактного вещества, динамика соответствует таковой амплитуде пульсового кровенаполнения сосудов полости диафиза, восстановление идёт до минимальных величин диапазона значений в контроле [7].
Так как туннелизация костей нашла применение в клинике, для выявления взаимосвязи после её осуществления между изменениями в гемодинамике диафиза кости и кровообращени- ем в сегменте конечности были сопоставлены результаты электрофизиологических исследований в полости диафиза большеберцовой кости, задней группе мышц и артериях голени у животных, отличающихся наличием «высокого» пульсирующего ВКД.
МАТЕРИАЛ И МЕТОДЫ
Анализу подвергнуты архивные материалы исследований 10 взрослых собак, у которых изначально и в течение периода наблюдений регистрировали «высокое» пульсирующее ВКД в полости диафиза большеберцовой кости. Оперативные вмешательства и электрофизиологические исследования были выполнены на наркотизированных животных в условиях операционной при артериальном давлении 120-130 / 70–80 мм рт.ст.
Для исследований применяли канюли, изготовленные из игл для переливания крови И-65. Иглу укорачивали до 2 см, затачивали на 3 грани, и на прилежащую к павильону часть надевали обтягивающий синтетический катетер, обеспечивающий ограничение погружения конца иглы в полость диафиза до 3 мм и изоляцию от мягких тканей. Канюлю вставляли в наконечник, имеющий мандрен, и с помощью электродрели вводили на границе средней и нижней трети в полость диафиза большеберцовой кости. После заполнения изотоническим раствором хлорида натрия с добавлением гепарина (5000 единиц на 1 литр) канюлю соединяли ригидным синтетическим катетером с датчиком давления комплекса «Мингограф-2», расположенном на уровне сердца собаки.
Известно, что межэлектродное сопротивление обратно пропорционально количеству электролита и его регистрация в динамике позволяет судить об изменениях количества жидкости в изучаемом регионе. Регистрацию межэлектродного сопротивления и его пульсовых колебаний обеспечивает реография [5].
Для реографии в полости диафиза большеберцовой кости на 5 см выше первой вводили вторую канюлю, заполняли изотоническим раствором хлорида натрия с добавлением гепарина и закрывали заглушкой. Соответственно канюлям игольчатыми электродами снаружи поперечно пронизывали заднюю группу мышц голени. Канюли и игольчатые электроды попарно присоединяли к реографу РГ 4–01. Реография при силе зондирующего тока 1 мА и частоте 46 кГц. Калибровочный сигнал - 0,05 Ом. Амплитуду рео-грамм рассчитывали по формуле А = max к1 / К, где max – амплитуда реограмм, мм; к1 – амплитуда калибровки, Ом; К – амплитуда калибровки, мм. Минутный объём крови вычисляли по формуле Vq100 = 6000 maxd к1 Тизг / Тс R Кд, где maxd – мплитуда дифференцирующей реограммы, мм; к1 амплитуда калибровки, Ом,
Тизг– период изгнания, с; Кд амплитуда калибровки дифференцирующей реограммы, мм; Тс длительность сердечного цикла, с; R межэлек тродное сопротивление, Ом [2].
Из анатомии известно, что в нижней трети голени количество мягких тканей минимально, следовательно, объёмная сфигмография в этой области отражает в основном пульсовые изменения кровенаполнения магистральных сосудов. Для объёмной сфигмографии на нижнюю треть голени накладывали манжету шириной 3 см и создавали в ней давление воздуха равное 30 мм рт.ст. Запись ВКД, реограмм и сфигмограмм одновременно с помощью комплекса «Мингограф-82» при скорости движения ленты 100 мм/с.
Под туннелизацией кости понимали создание спицевого хода. Спицу с «перьевой» заточкой конца диаметром 1,8 мм проводили через диафиз кости поперечно на расстоянии 1 и 2 см выше и ниже канюли для измерений ВКД и сразу удаляли.
Для анализа были отобраны результаты исследований перед туннелизацией диафиза кости – контроль, через 1 и 2 месяца – следствие тун-нелизации, через 3-4 месяца – окончание периода восстановления ВКД, через 6-12 месяцев – отдалённый период. Из полученных данных составляли невзвешенные вариационные ряды. Анализ с помощью программы Excel 7,0: определяли средние, ошибку, достоверность средних и их различий по Стьюденту, коэффициент ранговой корреляции по Спирмену.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
В контроле ВКД составляло 45,4 6,4 мм рт.ст., минутный объём крови в полости диафиза большеберцовой кости ( Vq100пд ) 0,955 0,129 мл/мин/100см3, минутный объём крови в задней группе мышц голени ( Vq100м ) 1,115 0,139 мл/мин/100см3, амплитуда объёмных сфигмограмм ( Асф ) 0,311 0,015 Ом. Различия между Vq100пд и Vq100м недостоверны (табл. 1).
После туннелизации ВКД составляло 53-
45 % (p<0,05), Vq100пд – 102-123 %, Vq100м – 70-86 %, Асф – 108-109 %. При достоверном снижении ВКД увеличилась объёмная скорость кровотока в полости диафиза и уменьшилась в задней группе мышц голени; амплитуда пульсового кровенаполнения магистральных сосудов голени увеличилась. Изменения параметров кровообращения произошли в пределах диапазонов значений в контроле.
Таблица 1
Изменения давления в полости диафиза большеберцовой кости (ВКД), амплитуды объёмных сфигмограмм ( Асф ), объёмной скорости кровотока в полости диафиза большеберцовой кости ( Vq100пд ) и задней группе мышц голени ( Vq100м ), амплитуды реограмм в полости диафиза ( Апд ) и задней группе мышц ( Ам )
|
n |
ВКД, мм.рт.ст. |
% |
p< |
Асф, мм |
% |
p< |
||
|
Контроль |
17 |
45,4 6,4 |
100 |
0,311±0,015 |
100 |
|||
|
1 м |
10 |
24,2±5,7 |
53 |
0,05 |
0,339±0,036 |
109 |
- |
|
|
2 м |
9 |
20,5±3,8 |
45 |
0,01 |
0,337±0,024 |
108 |
- |
|
|
4 м |
8 |
40,0±5,8 |
88 |
- |
0,306±0,025 |
98 |
- |
|
|
6-12 м |
8 |
33,5±5,5 |
74 |
- |
0,461±0,049 |
148 |
0,05 |
|
|
Vq100пд, |
Vq100м, |
Vq100пд / |
||||||
|
мл/мин/100см3 |
мл/мин/100см3 |
Vq100м, p< |
||||||
|
Контроль |
17 |
0,955±0,129 |
100 |
1,115±0,139 |
100 |
- |
- |
|
|
1 м |
10 |
1,178±0,281 |
123 |
- |
0,785±0,138 |
70 |
- |
- |
|
2 м |
9 |
0,970±0,220 |
102 |
- |
0,963±0,128 |
86 |
- |
- |
|
4 м |
8 |
0,627±0,059 |
66 |
- |
0,971±0,152 |
87 |
- |
- |
|
6-12 м |
8 |
3,142±0,452 |
329 |
0,01 |
1,139±0,083 |
102 |
- |
0,01 |
|
Апд,Ом |
Ам,Ом |
Апд / Ам, p< |
||||||
|
Контроль |
17 |
0,124±0,007 |
100 |
0,050±0,002 |
100 |
0,001 |
||
|
1 м |
10 |
0,117±0,018 |
94 |
- |
0,053±0,008 |
106 |
- |
0,01 |
|
2 м |
9 |
0,093±0,016 |
75 |
- |
0,051±0,010 |
102 |
- |
0,05 |
|
4 м |
8 |
0,121±0,014 |
98 |
- |
0,049±0,013 |
98 |
- |
0,05 |
|
6-12 м |
8 |
0,119±0,013 |
96 |
- |
0,054±0,007 |
108 |
- |
0,001 |
При окончании периода восстановления ВКД составляло 88 %, Vq100пд – 66 %, Vq100м – 87 %, Асф – 98 %. При повышении ВКД до минимальных величин диапазона значений в контроле уменьшилась объёмная скорость кровотока в полости диафиза и осталась уменьшенной в задней группе мышц голени; амплитуда пульсаций магистральных сосудов голени уменьшилась.
В отдалённом периоде ВКД составляло 74 %, Vq100пд – 329 % (p<0,01), Vq100м –102 %, Асф – 148 % (p<0,05). При сохранении ВКД в области минимальных величин диапазона значений в контроле достоверно увеличились объёмная скорость кровотока в полости диафиза и восстановилась в задней группе мышц голени; амплитуда пульсаций магистральных сосудов голени достоверно увеличилась.
Сопоставления показали, что различия между Vq100пд и Vq100м в контроле, после тунне-лизации и по окончании периода восстановления были недостоверны и стали достоверными в отдалённом периоде (p<0,001). На основании корреляционного анализа изменения Vq100пд и Vq100м происходили не взаимосвязанно.
Корреляционный анализ подтвердил наличие уже выявленной ранее взаимосвязи между ВКД и Апд (p<0,05) и указал на наличие взаимосвязи между Vq100пд и Асф (p<0,05). На основании того, что первичны изменения, возникающие вследствие травмы, приходим к следующему заключению: изменения объёмной скорости кровотока в полости диафиза большеберцовой кости служили причиной адекватных изменений амплитуды пульсового кровенаполнения магистральных артерий голени.
Однако сопоставление параметров кровообращения не отразило причину изменений объ-
ёмной скорости кровотока в задней группе мышц голени, и было решено провести сопоставление показателей гемодинамики в изучаемых регионах.
В контроле амплитуда реограмм полости диафиза ( Апд ) составляла 0,124 0,007 Ом, участка задней группы мышц голени ( Ам ) 0,050 0,002 Ом. Различия достоверны (p<0,001).
После туннелизации Апд составляла 94-60 %, Ам – 102-106 %. Амплитуда реограмм уменьшилась в полости диафиза и увеличилась в задней группе мышц голени.
При окончании периода восстановления Апд и Ам составляли 98 %. Амплитуда реограмм незначительно увеличилась в полости диафиза и уменьшилась в задней группе мышц голени.
В отдалённом периоде Апд составляла 96 %, Ам – 108 %. Амплитуда реограмм в полости диафиза незначительно уменьшилась и увеличилась в задней группе мышц голени.
Сопоставления показали, что различия между Апд и Ам были во все сроки достоверны, изменения происходили в пределах диапазонов значений в контроле. Корреляция между изменениями не выявлена. На основании корреляционного анализа взаимосвязанно происходили изменения Асф и Ам (p<0,05).
В контроле продолжительность анакроты в полости диафиза ( а пд ) составляла
0,059 0,004 с, в задней группе мышц голени ( а м ) 0,061 0,003 с. Различия недостоверны.
Сопоставления показали (рис. 1), что через 1 и 2 месяца а пд и а м менялись с противоположной направленностью, различия между ними были достоверны (p<0,05). Затем, в периоде восстановления и отдалённом периоде, различия между показателями стали недостоверными. На основа- нии корреляционного анализа изменения а пд, а м, параметров кровообращения и показателей гемодинамики происходили не взаимосвязанно. Следовательно, изменения продолжительности анакроты не обеспечивали взаимосвязь между гемодинамикой в полости диафиза большеберцовой кости и задней группе мышц голени.
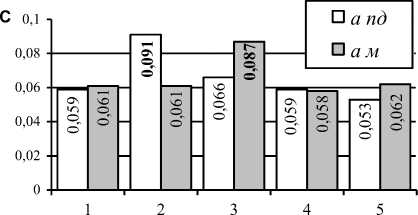
Рис. 1. Центральные тенденции изменений продолжительности анакроты в полости диафиза большеберцовой кости ( а пд ) и задней группе мышц голени ( а м ). Жирным шрифтом отмечены величины, достоверно отличающиеся от величины в контроле (р<0,05). Обозначение: 1 контроль; 2 туннелиза-ция 1 м; 3 туннелизация 2 м; 4 период восстановления; 5 отдаленный период
В контроле межэлектродное сопротивление участка полости диафиза ( Rпд ) составляло
840 47 Ом, задней группы мышц голени ( Rм ) 456 5 Ом. Различия достоверны (р<0,001).
Сопоставления показали (рис. 2), что различия между Rпд и Rм были всегда достоверны (р<0,01). На основании корреляционного анализа изменения Rпд, Rм, параметров кровообращения и гемодинамики происходили не взаимо- связанно. Следовательно, изменения количества жидкости не обеспечивали взаимосвязь между гемодинамикой в полости диафиза большеберцовой кости и задней группе мышц голени.
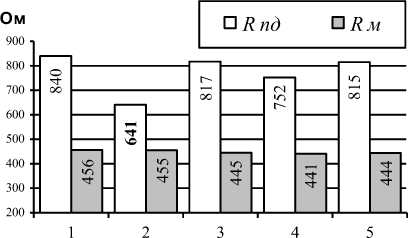
Рис. 2. Центральные тенденции изменений межэлектродного сопротивления в полости диафиза большеберцовой кости ( R пд ) и задней группе мышц голени ( R м ). Жирным шрифтом отмечены величины, достоверно отличающиеся от величины в контроле (р<0,05). Обозначение: 1 контроль; 2 тун-нелизация 1 м; 3 туннелизация 2 м; 4 период восстановления; 5 отдаленный период
Таким образом, взаимосвязь между изменениями показателей гемодинамики в полости диафиза большеберцовой кости и задней группе мышц голени не выявлена. На основании выявленной взаимосвязи между Асф и Ам изменения гемодинамики в задней группе мышц голени служили следствием изменений кровотока по магистральным артериям сегмента конечности.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
В проведенном исследовании вновь проявилась взаимосвязь между ВКД и амплитудой пульсовых изменений кровенаполнения сосудов полости диафиза кости. Следовательно, получило подтверждение заключение о том, что «высокое» пульсирующее ВКД было результатом поступления жидкости пульсирующим потоком из сосудов в интерстициальные пространства полости диафиза под влиянием пульсовых изменений кровенаполнения [7].
Сопоставление параметров кровообращения в полости диафиза большеберцовой кости, задней группе мышц голени и магистральных сосудах голени показало, что после туннелизации их изменения происходили в пределах диапазонов значений в контроле. Следовательно, тун-нелизация диафиза кости не приводила к нарушениям кровообращения и её применение в предлагаемом объёме возможно при ишемических изменениях тканей сегмента конечности.
Установлено, что изменения объёмной скорости кровотока в полости диафиза и амплитуды пульсаций магистральных сосудов голени происходили взаимосвязано: в течение двух месяцев показатели кровообращения были увеличены в пределах диапазона значений в контроле; при заживлении дефектов компактного вещества органотипичной костью – соответствовали средним значениям, в процессе приспособления структуры кости к функциональным нагрузкам, через 6-12 месяцев, – были резко увеличены. На основании того, что первично происходили изменения вследствие нанесения травмы, приходим к следующему заключению: изменения кровообращения в кости служили причиной однонаправленных изменений пульсового кровенаполнения магистральных сосудов голени.
При этом в задней группе мышц голени в течение четырех месяцев объёмная скорость кровотока была уменьшена до минимальных значений диапазона изменений в контроле. Так как взаимосвязь изменений объёмной скорости кровотока в задней группе мышц голени с изменениями гемодинамики в полости диафиза большеберцовой кости не была установлена и выявлена с изменениями амплитуды пульсаций магистральных сосудов голени, приходим к за- ключению о том, что причиной изменений кровообращения в неповреждённых мягких тканях служили эффекты ауторегуляции, порождаемые изменениями кровотока в магистральных артериях сегмента конечности [3].
При анализе изменений кровообращения в изучаемых регионах было также выявлено, что взаимосвязанно менялись только амплитудные параметры пульсового кровотока. Коррекция кровообращения осуществлялась без учёта изменений содержания жидкости (на основании изменений межэлектродного сопротивления) и продолжительности анакроты. Вероятно, изменения гидратации тканей и частотных параметров пульсового кровотока служили следствием изменений гемодинамики, не учитываемыми в качестве основных характеристик при регуляции кровообращения.
На основании полученных данных после туннелизации кости регуляция кровообращения в изучаемых регионах осуществлялась следующим образом. Вследствие нанесения травмы в сосудистой системе кости усиливалось кровообращение и для его обеспечения увеличивалось пульсовое кровенаполнение магистральных артерий сегмента конечности. Усиление кровотока по магистральным артериям активировало механизмы ауторегуляции в неповреждённых мягких тканях, и в них происходило ограничение кровообращения в пределах диапазона «изменений в норме».
На основании проведенных исследований с учётом результатов исследований в полости диафиза большеберцовой кости этих животных приходим к следующей версии изменений.
У данной группы животных ВКД было относительно высоким и пульсировало вследствие того, что под влиянием пульсовых изменений кровенаполнения жидкость пульсирующим потоком перемещалась из сосудов в интерстициальные пространства полости диафиза. Туннели-зация привела к появлению дефектов компактного вещества, через которые интерстициальная жидкость стала перемещаться к окружающим кость тканям, и ВКД снизилось. Снижение ВКД привело к увеличению фильтрации жидкости из сосудов обмена в интерстициальные пространства полости диафиза. При отсутствии патологии «нагнетание» жидкости в интерстициальные пространства полости диафиза привело бы к восстановлению ВКД, а при наличии дефектов компактного вещества оно обеспечило лишь стабилизацию ВКД на сниженном уровне, при котором количество фильтрующейся из сосудистого русла и перемещающейся за пределы кости жидкости приходило в соответствие.
Для обеспечения увеличения фильтрации жидкости в сосудистой системе кости усиливалось кровообращение. Усиление кровообращения в кости служило причиной увеличения при- тока крови к сегменту конечности. Из-за увеличения амплитуды пульсового кровенаполнения магистральных артерий конечности в неповреждённых мягких тканях срабатывали механизмы ауторегуляции, и кровообращение в них ограничивалось в пределах диапазона «изменений в норме». До заживления дефектов компактного вещества продолжалось перемещение интерстициальной жидкости из полости диафиза кости к окружающим мягким тканям, что поддерживало усиление кровообращения в сосудистой системе кости и увеличение артериального притока крови к конечности.
Постепенно вследствие репаративных процессов увеличивался объём сосудистого русла кости и шло заживление дефектов компактного вещества. Через 4 месяца перемещение жидкости за пределы полости диафиза полностью прекращалось, ВКД восстанавливалось до минимальных величин диапазона значений в контроле, вследствие этого уменьшалась объёмная скорость кровотока в полости диафиза и уменьшался до величины в контроле приток крови к конечности. Вследствие уменьшения амплитуды пульсового кровенаполнения магистральных артерий конечности в неповреждённых мягких тканях включались механизмы ауторегуляции и кровообращение в задней группе мышц усиливалось.
Известно, что регенерацию кости обеспечивают сосудистые системы полости диафиза и надкостницы, образование и усиление функции анастомозов между которыми приводит к «спонгизации» части компактного вещества [1, 8]. Участием сосудистой системы надкостницы мы объясняем то, что ВКД восстанавливалось до минимальных значений диапазона изменений в контроле в условиях ограничения объёмной скорости кровотока в сосудистой системе полости диафиза.
Основной особенностью отдалённого периода служила структурная перестройка кости, обеспечивающая структурное приспособление зон повреждений к функциональным нагрузкам [8]. Структурной перестройкой кости мы объясняем резкое усиление кровообращения в сосудистой системе кости и соответствующее увеличение притока крови по магистральным артериям конечности. Вероятно, к этому времени завершилось развитие коллатеральных сосудов, вследствие чего увеличение артериального притока обеспечило усиление кровообращения в кости без изменений кровообращения в неповреждённых мягких тканях.
Исследование показало, что туннелизация диафиза длинной кости в предлагаемом объёме способствует длительному усилению кровообращения в кости и увеличению притока крови к сегменту конечности. Одновременно в неповреждённых тканях происходит ограничение кровообращения в пределах диапазона изменений «в норме». Так как ухудшение кровообращения в сегменте конечности как в раннем послеоперационном периоде, так и в течение следующих 12 месяцев после оперативного вмешательства не выявлено, ишемические изменения, не относящиеся к критическим, не являются противопоказанием для применения туннелиза-ции костей конечности.
В связи с тем, что в течение четырех месяцев возможно ограничение кровообращения в непо- вреждённых тканях у пациентов с ишемическими изменениями конечности, в течение этого времени желательно применение местной стимулирующей кровообращение терапии, например, применение функциональных нагрузок. После шести месяцев происходящие в кости процессы служат причиной постоянно сохраняющегося увеличения притока крови к конечности, следовательно, в это время желательны нагрузки, стимулирующие развитие коллатерального кровообращения.
ВЫВОДЫ
-
1. Туннелизация диафиза длинной кости приводит к усилению кровообращения в кости и увеличению притока крови к конечности.
-
2. В послеоперационном периоде вследствие «включения» механизмов ауторегуляции кровообращение в неповреждённых тканях сегмента конечности ограничивается в пределах диапазо-
- на изменений «в норме». После заживления дефектов компактного вещества органотипичной костью кровообращение в этих тканях восстанавливается.
-
3. Туннелизация диафиза кости показана для получения длительного увеличения притока крови к сегменту конечности.


