Изолированная химиогипертермическая перфузия органов малого таза в эксперименте на животных
Автор: Садыкова Р.Ф., Ястребов И.П., Демко А.Е., Суров Д.А., Соловьев И.А., Беляев А.М., Сенчик К.Ю., Безмозгин Б.Г., Кандыба Д.В., Киреева Г.С., Петрова А.Н., Шевченко Е.А., Святненко А.В., Бабков О.В., Габриелян М.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.12, 2017 года.
Бесплатный доступ
Разработана экспериментальная модель открытой и закрытой ИХГПТ, и в условиях эксперимента произведена оценка безопасности данной методики. Эффективность сосудистой изоляции при отрытой и закрытой ИХГПТ оценивалась путем сравнительного анализа концентраций химиопрепарата в системном кровотоке и перфузионном контуре. Экспериментальная часть работы выполнена на 4 свиньях породы крупная белая массой 45-55 кг. В группе А (n = 2) ИХГПТ проводилась открытой методикой. Для этого посредством тотальной срединной лапаротомии осуществляли доступ к магистральным сосудам. В группе В (n = 2) ИХГПТ проводилась закрытой методикой под контролем рентгенодиагностической хирургической установки. ИХГПТ проводилась в следующем режиме: скорость перфузии 300 мл/мин., температура перфузата 42 ± 0,5о С, продолжительность перфузии 30 мин., давление в контуре 100 мм^. В качестве химиопрепарата был использован цисплатин, который вводился в перфузионный контур в дозе 200 мг в виде однократной болюсной инъекции. Созданная экспериментальная модель наглядно показала, что метод изолированной химиогипертермической перфузии органов малого таза является технически воспроизводимым и относительно безопасным. Эксперимент подтвердил, что показатели гемодинамических параметров животных оставались стабильными на протяжении всей процедуры. Сравнительный анализ концентрации цисплатина в системном кровотоке и малом тазу показал высокую эффективность сосудистой изоляции перфузируемого региона, минимальную утечку химиоперапарата, что обеспечивает снижение системной токсичности и связанных с нею осложнений, а также доказывает высокую эффективность ИХГПТ.
Опухоль малого таза, изолированная перфузия таза, ипт, экспериментальная модель
Короткий адрес: https://sciup.org/140188698
IDR: 140188698 | УДК: 618.13-006:615.28
Hyperthermic isolated pelvic chemoperfusion in test
The experimental model of the open and close IPP has been developed in the course of the study; the technique has been given the safety evaluation in the experiment. The efficiency of vascular isolation in open and close IPP was estimated by comparative analysis of chemotherapeutic drug concentration in systemic blood circulation and perfusion boundary. The experimental procedure was carried out on four pigs of large white breed with bulk of 45-55 kg. In the group A(n = 2) IPP was conducted by the open technique. For this purpose the access to the major vessels was gained via total midline laparotomy. In the group B(n = 2) IPP was conducted by the close technique under the control of X-ray surgical unit. The IPP was conducted in the following terms: perfusion speed -300 ml/min, perfusate temperature - 42 ± 0,5о С, perfusion duration - 30 min., circuit pressure- 100 mmHg. Cisplatin was used as a chemotherapeutic agent which was administered in the perfusion circuit at a dose of 200 mlg by means of a single bolus injection. This test model clearly demonstrated that hyperthermic isolated pelvic chemoperfusion technique is technically reproduced and relatively harmless. The experiment confirmed that hemodynamic parameters indices of the animals remained stabile during the whole manipulation. The comparative analysis of cisplatin concentration in the systemic blood circulation and small pelvis showed high efficiency of vascular isolation of the perfused region, minimal leakage of chemotherapeutic drug, that assured the reduction of systemic toxicity and connected complications as well as proved the highly effective technique of IPP.
Текст научной статьи Изолированная химиогипертермическая перфузия органов малого таза в эксперименте на животных
В структуре онкологической заболеваемости населения России злокачественные опухоли органов малого таза составляют в совокупности более 25%. [1] Одной из особенностей опухолей данной локализации является тенденция к местному распространению, различные варианты которого диагностируются у 20–40% больных [2, 3]. Приоритетное значение в лечении данной категории пациентов имеют методы комбинированной терапии, которые оказывают не только выраженный цитотоксический эффект по отношению к злокачественной опухоли, но и в ряде случаев существенно увеличивают частоту и тяжесть системных побочных реакций и осложнений [4]. В связи с этим одним из наиболее перспективных путей повышения эффективности лечения больных с местнораспространенными опухолями малого таза является усиление локальной противоопухолевой активности и минимизация системных эффектов комбинированной терапии. В настоящее время рентгенэндоваскулярные вмешательства и регионарная химиотерапия являются важными составляющими программ комбинированного лечения онкологических больных в адъювантном и неоадъювантном режиме, а также симптоматической терапии у пациентов с различными осложнениями (кровотечение, интенсивный болевой синдром и т.д.). Совершенствование методологии внутрисосудистых вмешательств у больных с опухолями малого таза и дальнейшее развитие идеологии создания высокой концентрации химиопрепарата в опухоли во многом определило появление новых методов локорегионарной терапии, одним из которых является изолированная химиогипертермическая перфузия органов малого таза (ИХГПТ).
В настоящее время концепция изолированной перфузии широко применяется у больных злокачественными опухолями конечностей и легких [5, 6, 7]. В тоже время, изолированная химиоперфузия при местнораспространенных злокачественных опухолях малого таза является

инновационной технологией, о результатах применения которой сообщается в ограниченном числе публикаций зарубежных авторов [7, 8, 9, 10, 11].
Систематический анализ зарубежной литературы позволяет выделить открытый и закрытый варианты проведения ИХГПТ, последний из которых представляется наиболее перспективным в связи с меньшей травматичностью, незначительной частотой послеоперационных осложнений и возможностью проведения повторных вмешательств [7, 8, 9, 10, 11, 12, 13, 14].
Основными составляющими данной технологии являются:
-
1 – сосудистая изоляция малого таза, которая достигается окклюзией аорты и нижней полой вены в их инфраре-нальном отделе, а также наложением пневматических турникетов в верхней трети обоих бедер и на уровне пупка.
-
2 – перфузия сосудистого бассейна таза раствором химиопрепарата посредством аппарата искусственного кровообращения.
-
3 – отмывка контура перфузии от химиопрепарата.
-
4 – возобновление системного кровотока [5, 6, 7, 10, 12].
В настоящее время режимы выполнения изолированной перфузии таза нестандартизированы, однако, принципиально возможно проведение вмешательства в нормотермическом или гипертермическом режимах, а также в условиях гипоксии, либо гипероксигенации [7, 8, 9, 10, 11, 12].
Цель исследования
Разработать экспериментальную модель открытой и закрытой ИХГПТ и оценить в условиях эксперимента безопасность данной методики. Путем сравнительного анализа концентраций химиопрепарата в системном кровотоке и перфузионном контуре оценить эффективность сосудистой изоляции при отрытой и закрытой ИХГПТ.
Материалы и методы
Животные. Экспериментальная часть работы выполнена на 4 свиньях породы крупная белая массой 45–55 кг в условиях операционной вивария НИИ онкологии им. Н.Н. Петрова. Проведение опытов осуществлялось в строгом соответствии с «Правилами проведения работ с использованием экспериментальных животных», введенными в действие приказом Министра высшего образования СССР № 724 от 1984 года и Хельсинской декларацией о гуманном отношении к опытным животным от 1983 года. Свиньи подвергались карантинизации в течение 14 дней. В эксперимент допускались животные без каких-либо заболеваний и травм. Режим кормления был всегда стандартным. За сутки до проведения эксперимента кормление животных прекращалось, однако сохранялся свободный доступ к воде.
Анестезиологическое пособие и мониторинг гемодинамических показателей. Все процедуры были выполнены в условиях сочетанной анестезии (общая + спинальная)
с инвазивной искусственной вентиляцией легких (ИВЛ). С целью обеспечения инфузионной поддержки катетеризировали периферическую вену (краевую вену уха). Для премедикации применялись внутривенные инъекции атропина сульфата 1,0 мл, пропофола 100 мг, дроперидола 5 мг. Под местной анестезией 0,5% раствором новокаина выполняли трахеостомию с целью проведения ИВЛ через трахеостомическую трубку. В условиях местной анестези-ии 0,5% раствором новокаина для обеспечения аналгезии производили катетеризацию эпидурального пространства с введением маркаинаспинал 15 мг. Поддержание анестезии – севоран в концентрации 2,0 объемных процента.
В течение всей процедуры выполняли мониторинг основных витальных функций: артериального давления (АД), частоты сердечных сокращений (ЧСС), частоты дыхания (ЧДД), - для чего был использован комплекс регистрации и анализа параметров витальных функций «Телец» (Центральный научно-исследовательский институт робототехники и технической кибернетики, Санкт-Петербург). Насыщение периферической артериальной крови кислородом в ходе эксперимента поддерживали на уровне 95% и выше, и контролировали с помощью пульсоксиметра, прикрепленного к уху свиньи.
Для забора крови и контроля центрального венозного давления (ЦВД) обеспечивали доступ к внутренней яремной вене. Помимо этого в ходе эксперимента проводили термометрию, рН-метрию с использованием устройства, разработанного в Центральном научно-исследовательском институте робототехники и технической кибернетики.
Элементы перфузионного контура
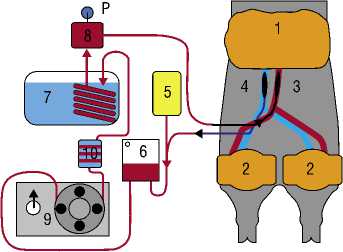
Рис. 1. Принципиальная схема изолированной перфузии таза на животном. Элементы перфузионного контура.
-
1 – пневматическая манжета, наложенная в околопупочной области (ЗАО «Медтехника», СПб, Россия); 2 – пневматические манжеты, наложенные в верхней трети обоих бедер (ЗАО «Медтехника», СПб, Россия); 3 – окклюзионный баллонный катетер, установленный в аорте ниже отхождения почечных артерий; 4 – окклюзионный баллонный катетер, установленный в нижней полой вене ниже отхождения почечных вен; 5 – система быстрого заполнения контура (ОАО «Курган Синтез», Курган, Россия); 6 – жидкостной резервуар;
-
7 – термостатическая водяная баня с теплообменником (LOIP, Санкт-Петербург); 8 – воздушный фильтр (MAQUET, Германия);
-
9 – центробежный насос (Центральный научно-исследовательский институт робототехники и технической кибернетики, Санкт-Петербург). 10 – устройство для контроля температуры и величины рН в перфузионном контуре
Экспериментальные группы и техника. ИХГПТ выполнялась открытым и закрытым способами.
В группе А (n = 2) ИХГПТ проводилась открытой методикой. Для этого посредством тотальной срединной лапаротомии осуществляли доступ к магистральным сосудам. Дистальнее почечных сосудов выделяли аорту и нижнюю полую вену до бифуркации. На сосуды накладывали турникеты. Ниже турникетов накладывали кисетные швы, выполняли аортотомию и каватомию и устанавливали канюли 10 и 6 Fr соответственно (рис. 2). Для полной изоляции малого таза на нижние конечности в проекции нижней трети бедер накладывали пневматические манжеты. После системной гепаринизации в дозе 100 ЕД/кг массы тела канюли подключали к перфузионной установке.
В группе В (n = 2) ИХГПТ проводилась закрытой методикой под контролем рентгенодиагностической хирургической установки РТС-612. С целью максимальной сосудистой изоляции области таза предварительно на уровне нижних третей обоих бедер и на живот по краю реберной дуги были наложены пневматические турникеты. Бедренные артерию и вену выделяли через короткий продольный разрез в паховой области. После системной гепаринизации (100 ЕД/кг массы тела) осуществляли канюляцию бедренных артерии и вены сосудистыми катетерами 11Fr (рис. 3).
Один трех-просветный баллонный катетер через бедренную вену устанавливали в нижнюю полую вену, а второй – через бедренную артерию в аорту. Позиционирование катетеров осуществляли под контролем рентгеноскопии в области ниже почечных сосудов и над бифуркацией аорты и вены. Для окклюзии аорты использовали баллонный катетер 5 Fr, для окклюзии полой вены – 6 Fr. Перед началом перфузии аортальный и венозный окклюзионные баллоны наполняли контрастным веществом (Ультравист), разведенным в физиологическом растворе (1:1). Данный процесс происходил под контролем рентгеноскопии, чтобы убедиться, что баллон плотно прилегает к стенке сосуда. Полноту окклюзии проверяли введением рентгеноконтрастного раствора через внутренний просвет аортального баллонного катетера для подтверждения остановки кровотока в дистальной части аорты. Полноту венозной окклюзии проверяли введением рентгеноконтрастного вещества через венозную канюлю, чтобы убедиться в отсутствии притока крови в нижнюю полую вену. Последовательно выполняли окклюзию аорты, раздували пневматические турникеты на нижних конечностях до 300 мм рт. ст. и до 150 мм рт. ст. на животе, окклюзию нижней полой вены (рис. 4).
Затем в обеих группах подключали канюли к перфузионной установке, предварительно заполненной раствором натрия хлорида (0,9%–500,0) и гепарином 5000 ЕД. ИХГПТ проводилась в следующем режиме: скорость перфузии 300 мл/мин., температура перфузата 42 ± 0,5о С, продолжительность перфузии 30 мин., давле-
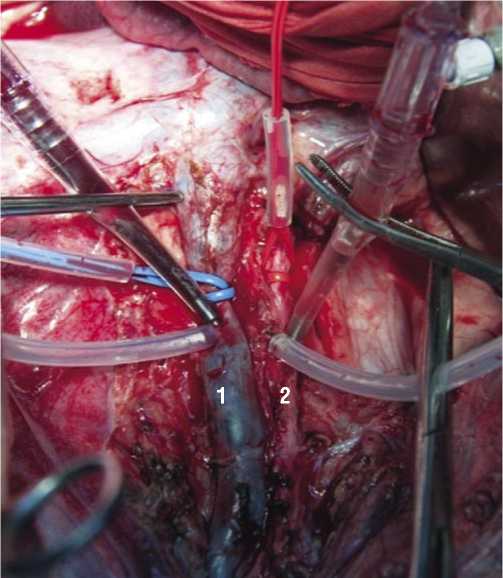
Рис. 2. Канюлированные нижняя полая вена (1) и аорта (2) во время открытой изолированной химиогипертермической перфузии органов малого таза у свиньи
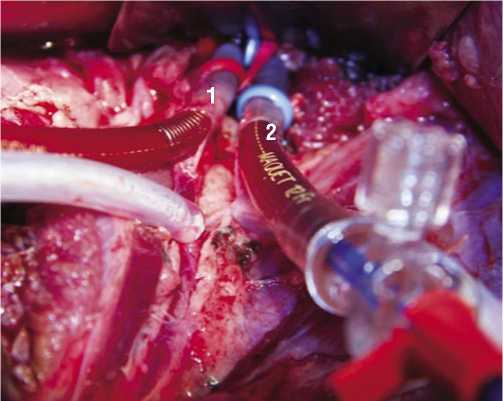
Рис. 3. Канюлированные бедренные артерия (1) и вена (2) во время закрытой изолированной химиогипертермической перфузии органов малого таза у свиньи ние в контуре 100 ммHg. В качестве химиопрепарата был использован цисплатин, который вводился в перфузионный контур в дозе 200 мг в виде однократной болюсной инъекции.
После окончания сеанса перфузии в течение 15 мин. было выполнено замещение крови из перфузионного контура физиологическим раствором в объеме 500 мл.
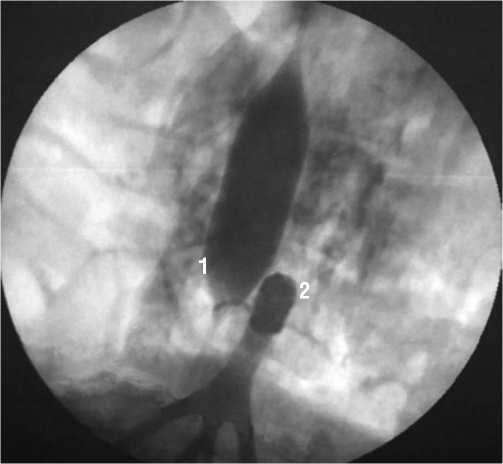
Рис. 4. Баллоны-окклюдеры, установленные в нижней полой вене (1) и в аорте (2)
На завершающем этапе в группе А извлекали канюли из нижней полой вены и аорты с ушиванием деффекта сосудов. Последовательно снимали турникет с нижней полой вены, пневматические турникеты с нижних конечностей и турникет с аорты. В группе В: запускали кровоток по нижней полой вене, снимали пневматические турникеты и восстанавливали кровоток по аорте, деканюлировали бедренные сосуды, удаляли баллонные катетеры из аорты и нижней полой вены и восстанавливали их целостность.
Нейтрализация гепарина осуществлялась инфузией 1% раствора протамин-сульфата из расчета 1 мг на 100 ЕД гепарина. Раны послойно ушивали.
Фармакокинетический анализ . Для оценки и сравнительного анализа концентрации цисплатина в системном кровотоке и малом тазу осуществляли забор крови из внутренний яремной вены и из артериальной канюли перфузионного контура до начала процедуры, на 1, 5, 10, 15, 20, 25, 30 мин.
По окончанию перфузии в группе А взята биопсия m. psoas major.
Измерение концентрации цисплатина в исследуемом материале проводилось путем масс-спектрометрии.
Результат
Все животные перенесли изолированную химио-гипертермическую перфузию органов малого таза удовлетворительно, без развития каких-либо осложнений, как во время, так и после эксперимента.
Влияние на гемодинамические показатели. Показатели ЧСС, AД, ЧД животных до, во время и после перфузии представлены в таблице 1. Во время изолированной перфузии колебания показателей были незначительны и не выходили за пределы нормы.
Табл. 1. Показатели витальных функций
|
Параметры |
До перфузии |
Во время перфузии |
После перфузии |
|
АД (мм рт. ст) |
120 ± 11,1 |
110 ± 16,3 |
110 ± 18,3 |
|
ЧСС (уд в мин.) |
79 ± 9,6 |
105 ± 15,7 |
98 ± 12,3 |
|
ЧДД (в мин.) |
22 ± 2 |
31 ± 5 |
24 ± 6 |
Результаты рН-метрии и термометрии совместно для групп А и В представлены на рисунках 5 и 6, соответственно. Резкий скачок в значении рН произошел в первые 5 мин. перфузии, когда кровь из изолированной области малого таза свиньи смешивалась с физиологическим раствором, которым предварительно был заполнен перфузионный контур. Далее на протяжении всей ИХГПТ значение рН оставалось практически неизменным и составило в среднем 7,02 ± 0,05 (в норме кровь свиней имеет слабощелочную среду с рН около 7,5).
Температура перфузата поддерживалась на уровне целевых значений. Контроль эффективности гипертермии изолированной области малого таза осуществлялся измерением ректальной температуры на протяжении всего времени перфузии (рис. 6).
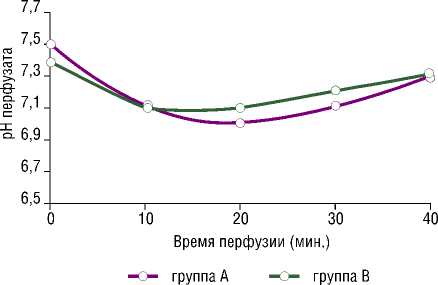
Рис. 5. Динамика изменения показателя рН перфузата во время изолированной химиогипертермической перфузии органов малого таза у животных в группах А и В
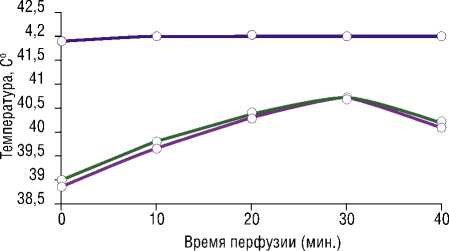
—:— температура перфузата
—с— ректальная температура группа А
—:— ректальная температура группа В
Рис. 6. Динамика изменения температуры перфузата во время изолированной химиогипертермической перфузии органов малого таза у животных в группах А и В

Табл. 2. Концентрация цисплатина в малом тазу и системном кровотоке. Группа А
|
Группа А (n=2) |
||||
|
№1 |
№2 |
|||
|
МТ |
СК |
МТ |
СК |
|
|
С-max (мг/л) |
64,1 |
6,2 |
62,7 |
6,0 |
|
AUC (мг*мин./л) |
1442,7 |
129,5 |
1471,3 |
144,2 |
Примечание : МТ – малый таз, СК – системный кровоток, n – количество животных в группе, № животного.
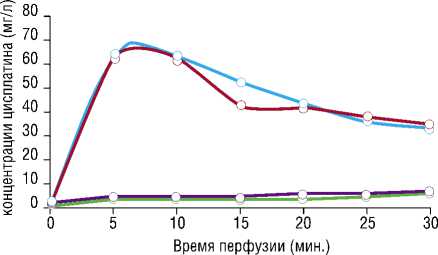
Концентрация цисплатина в кровеносном русле малого таза (МТ) и системном кровотоке (СК) в группе А (табл. 2, рис. 7). Среднее значение максимальной концентрации (С-max) цисплатина в кровенусном русле малого таза для группы А составило 63,4 мг/л, площадь под кривой (AUC) – 1457,0 мг*мин./л.
Среднее значение максимальной концентрации цисплатина (С-max) в системном кровотоке для группы А составила 6,1 мг/л, AUC – 136,9 мг*мин./л.
Концентрация цисплатина в кровеносном русле малого таза (МТ) и в системном кровотоке (СК) в группе В (табл. 3, рис. 8). Среднее значение максимальной концентрации (С-max) цисплатина в кровенусном русле малого таза для группы В составило 63,1 мг/л, AUC – 1250,7 мг*мин./л.
Среднее значение максимальной концентрации цисплатина (С-max) в системном кровотоке для группы В составило 8,9 мг/л, AUC – 167,4 мг*мин./л.
Концентрация цисплатина в биопсийном материале. Среднее значение концентрации цисплатина в биопсийном материале, полученом из m.psoas major животных группы А составило 2,15 мг/л (табл. 4).
Заключение
Созданная экспериментальная модель наглядно показала, что метод изолированной химиогипертерми-ческой перфузии органов малого таза является технически воспроизводимым и относительно безопасным. Эксперимент подтвердил, что показатели гемодинамических параметров животных оставались стабильными на протяжении всей процедуры. Сравнительный анализ концентрации цисплатина в системном кровотоке и малом тазу показал высокую эффективность сосудистой изоляции перфузируемого региона, минимальную утечку химиоперапарата, что обеспечивает снижение системной токсичности и связанных с нею осложнений, а также доказывает высокую эффективность ИХГПТ. Полученные результаты позволяют рассматривать ИХГПТ в качестве перспективной методики у больных с осложненными местнораспространенными опухолями малого таза и, в том числе, с неблагоприятным премор-бидным фоном. Очевидно, что практическая реализация концепции изолированной регионарной перфузии требует не только наличия высокотехнологичного оборудования, но и слаженного мультидисциплинарного
—2— концентрации цисплатина в малом тазу п1
—2— концентрации цисплатина в малом тазу п2
-2- концентрации цисплатина в системном кровотоке п1
— — концентрации цисплатина в системном кровотоке п2
Рис. 7. Динамика изменения концентрации цисплатина в малом тазу и системном кровотоке при ИХГПТ открытой методикой
Табл. 3. Концентрация цисплатина в малом тазу и системном кровотоке. Группа В
|
Группа В (n=2) |
||||
|
№1 |
№2 |
|||
|
МТ |
СК |
МТ |
СК |
|
|
С-max (мг/л) |
64,4 |
7,9 |
61,8 |
9,8 |
|
AUC (мг*мин./л) |
1272,5 |
158,7 |
1228,9 |
176,1 |
Примечание : МТ – малый таз, СК – системный кровоток, n – количество животных в группе, № животного.
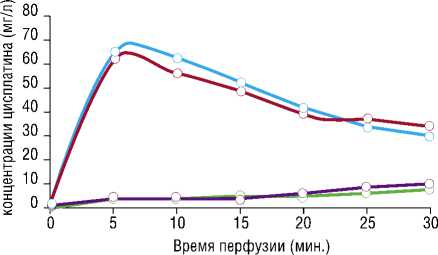
— — концентрации цисплатина в малом тазу п1
—:— концентрации цисплатина в малом тазу п2
концентрации цисплатина в системном кровотоке п1
— — концентрации цисплатина в системном кровотоке п2
Рис. 8. Динамика изменения концентрации цисплатина в малом тазу и системном кровотоке при ИХГПТ закрытой методикой
Табл. 4. Концентрация цисплатина в биопсийном материале

Список литературы Изолированная химиогипертермическая перфузия органов малого таза в эксперименте на животных
- Карпин А.Д. Злокачественные новообразования в России в 2013 (заболеваемость и смертность)/Карпин А.Д., Старинский В.В., Петрова Г.В.//М.:МНИОИ им. П.А. Герцена-филиал ФГБУ «ФМИЦ им. П.А. Герцена» Минздрава Росии 2015; 250 с.
- Майстренко Н.А. Экзентерация малого таза в лечении местно-распространённых опухолей./Майстренко Н.А., Хватов А.А., Учваткин Г.В., Сазонов А.А.//Вестник хирургии им. И.И. Грекова 2014; (6): 37-42.
- Бойко В.В. 10-летний опыт применения комбинированных операций при местнораспрастраненном раке прямой кишки./Бойко В.В., Криворотько И.В.//Международный медицинский журнал 2009; (1): 50-57.
- Гранов А.М. Интервенционная радиология в онкологии (пути развития и технологии.)/Гранов А.М., Давыдов М.И., Таразов П.Г.//СПб: Фолиант 2013; 560 с.
- Гафтон Г.И. Перспективные методы терапии больных саркомами мягких тканей конечностей (изолированная регионарная перфузия, локальная гипертермия)/Гафтон Г.И., Пхакадзе Н.Р., Сенчик К.Ю., Гельфольд В.М.//Практическая онкология 2004; (4): 276-284.
- Левченко Е.В. Изолированная химиоперфузия легкого по поводу метастазов солидных опухолей./Левченко Е.В., Сенчик К.Ю., Барчук А.С. и др.//Онкохирургия. 2012; (3): 46-53.
- Aigner KR Regionale Therapie maligner Tumoren./Aigner KR, Stephens FO, Vogl TJ, Padberg W.//Munich: Springer Science+Business, 2013; 427 p.
- Murata S. Negative-balance isolated pelvic perfusion in patients with incurable symptomatic rectal cancer: results and drug dose correlation to adverse events./Murata S, Onozawa S, Kim C et al.//Acta Radiol 2014; 55 (7): 793-801.
- Uzan C. Isolated pelvic perfusion in irradiated unresectable recurrence of pelvic tumor: preliminary outcome and ongoing study/Uzan C, Goere D, Dumont F et al.//J Visc Surg 2014; 151: 11-15.
- Bonvalot S. Hyperthermic pelvic perfusion with tumor necrosis factor-а for locally advanced cancers: encouraging results of a phase II study./Bonvalot S, de Baere T, Mendiboure J et al.//Ann Surg 2012; 255: 281-286.
- Wanebo H.J. Isolated chemotherapeutic perfusion of pelvis as neoadjuvant or palliative therapy for advanced cancer of the rectum./Wanebo HJ, DiSiena M, Begossi G et al.//Ann Surg Oncol. 2008; 15: 1107-1116.
- van IJken MGA Balloon catheter hypoxic pelvic perfusion with mitomycin C and melphalan for locally advanced tumours in the pelvic region: a phase I-II trial./van IJken MGA, van Etten B, Guetens G, et al.//Eur J Surg Oncol. 2005; 31: 897-904.
- Wile A. Hypertermic pelvic isolation-perfusion in the treatment of refractory pelvic cancer./Wile A, Smolin M.//Arch Surg 1987; 122: 1321-1325.
- Vaglini M. Isolated pelvic perfusion for the treatment of unresectable primary or recurrent rectal cancer./Vaglini M, Cascinelli F, Chiti A, et al.//Tumori 1996; 82: 459-462.


