Изучение физиолого-биохимических свойств новых штаммов микроорганизмов, выделенных из промышленных отходов
Автор: Утепешева Алия Алимгазиевна, Сопрунова Ольга Борисовна
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Биотехнология
Статья в выпуске: 5-3 т.13, 2011 года.
Бесплатный доступ
Дана характеристика новым штаммам микроорганизмов, выделенных из промышленных отходов, обладающих полезными свойствами.
Гетеротрофные микроорганизмы, свойства, деградация, поверхностно-активные вещества
Короткий адрес: https://sciup.org/148205559
IDR: 148205559 | УДК: [579/22:57.063.8]:661.185.002.68
The studying of fiziologo-biochemical properties of new strains of microorganisms allocated from industrial wastes
In this article is given the characteristic new штаммам the microorganisms allocated from industrial wastes, possessing useful properties.
Текст научной статьи Изучение физиолого-биохимических свойств новых штаммов микроорганизмов, выделенных из промышленных отходов
В настоящее время во всем мире, в том числе и в России, остро стоят проблемы загрязнения воздуха, почвы, воды различными поллютантами [2]. Такие соединения, как поверхностно-активные вещества (ПАВ), пестициды, различные органические соединения, содержащие нитрогруппу, галоидорга-нические соединения, фосфорорганические соединения, пластмассы, синтетические смолы и некоторые другие продукты промышленности органического синтеза разрушаются в природе медленно и отличаются высокой устойчивостью к действию микроорганизмов. Такие синтетические вещества кумулируются в водоемах и почве, загрязняют окружающую среду [7].
Целью исследований являлось выделение новых штаммов микроорганизмов из промышленных отходов и изучение их свойств. Задачи исследования: выделение микроорганизмов из сточных вод и почв прилегающей территории очистных сооружений; изучение культурально-морфологических и физиолого-биохимических свойств выделенных штаммов микроорганизмов; изучение способности микроорганизмов к деградации ПАВ (катионные и анионные).
Объектом исследований являются гетеротрофные микроорганизмы, выделенные из сточных вод и почв прилегающей территории завода «Стекловолокно».
Микроорганизмы выделяли методом Коха [1] с использованием поверхностного и глубинного культивирования на следующих питательных твердых средах: питательный агар и агаризованная среда М9 следующего состава (г/л): Na 2 HPO 4 – 6,0; KH 2 PO 4 – 3,0; NaCl – 0,5; NH 4 Cl – 1,0; pH 7,0–7,2. Для выделения специфичной микрофлоры использовали ПА и М9, в которые вносили ПАА в количестве 1 г/л. Посевы со средой ПА инкубировали при комнатной температуре в течение недели; со средой М9 – в течение 3-4 недель.
В результате микробиологических исследований установлено, что в сточных водах и почвах
присутствует гетеротрофная (1,7·106…1,4·107 КОЕ/мл; 6,0·104…1,4·105 КОЕ/г) и специфическая (3,0·104…1,7·107 КОЕ/мл; 0,2·102…0,4·102 КОЕ/г) микрофлора.
Доминирующие формы микроорганизмов представлены в основном бактериями кокковидной формы, Г+ спорообразующими и неспорообразующими палочками.
В результате периодических пересевов в чистые культуры выделено 12 штаммов бактерий, изучены их культурально-морфологические и физиологобиохимические свойства.
Для изучения физиолого-биохимических свойств исследовали особенности углеродного и азотного питания, амилолитические, протеолитические, эмульгирующие, фунгицидные свойства, а также способность выделенных штаммов усваивать поверхностно-активные вещества.
В качестве источников углерода использовали различные моно- и дисахариды, которые вносили (1%) в ПА [6]. Рост микроорганизмов оценивали визуально в баллах (шкала от 0 до 5) (рис. 1).
Для изучения способности использовать азот минеральных солей применяли среду следующего состава (г/л): глюкоза – 20,0; K 2 HPO 4 – 1,0; KH 2 PO 4 – 1,0; MgSO 4 ·7H 2 O – 0,5; NaCl – 0,5; агар-агар – 15,0; раствор микроэлементов – 1 мл (CuSO 4 ·5 H 2 O – 0,64 г; FeSO 4 ·7H 2 O – 0,11 г; MnCl 2 ·4H 2 O – 0,79 г; ZnSO 4 ·7H 2 O – 0,15 г; дистиллированная вода – 100 мл). Использование солей аммония определяли путем добавления к основной среде NH 4 Cl (1,0 г) и CaCO 3 (5,0 г), использование нитратов – KNO 3 (1,0 г). Среды стерилизовали при 0,5 атм.
Изучение роста бактерий на среде с различными источниками углерода показало, что наилучший рост всех штаммов наблюдается на среде с добавлением мальтозы и галактозы. На среде с добавление сахарозы штамм № 4 выделял пигмент красного цвета. Штаммы № 1, 3 и 5 растут на среде с добавлением NH 4 Cl, штаммы № 4 и 5 – с добавлением KNO 3 .
При изучении амилолитических свойств обнаружено, что выделенные штаммы микроорганизмов данной способностью не обладают.
Изучение протеолитических свойств показало, что этой способностью обладают штаммы № 4, 5,
10. Причем штамм № 4 при этом выделял пигмент цвета [6]. розового цвета, штамм № 10 – пигмент черного
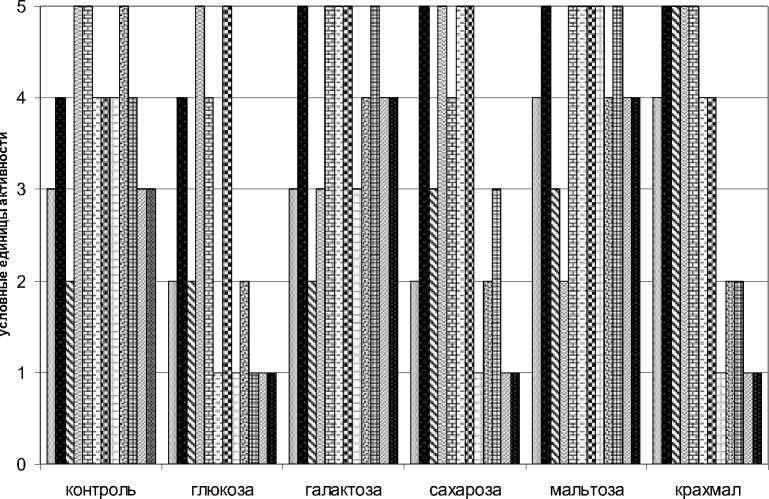
■1■2в3□4а5□6в7□8в9в 10 □ 11 0 12
Рис. 1. Рост бактериальных штаммов на среде с различными источниками углерода.
Для определения эмульгирующей активности культуры выращивали в течение 5 сут на скошенной агаризованной среде. Клетки смывали средой следующего состава (г/л): K2HPO4 – 7,0; KH2PO4 – 3,0; CaCl2 (1%, мл) – 1,0; MgSO4 ·7H2O – 0,1; (NH4)2SO4 – 1,0; FeSO4 7H2O – 0,5; ZnSO4 7H2O – 0,5; MnSO4 3H2O – 0,5; H2SO4 (0,1н, мл) – 10,0. Суспензию клеток оставляли на сутки, далее 4 мл суспензии центрифугировали при 6000 об/мин в течение 15 мин. Эмульгирующую активность определяли путем добавления к 4 мл исследуемого образца 4 мл бензина и дизельного топлива (ДТ) с последующим встряхиванием в течение 10 мин. Полученную эмульсию оставляли на 24 ч при комнатной температуре. Эмульгирующую активность определяли как отношение высоты эмульсионного слоя к общей высоте жидкости в измерительной пробирке и выражали в % [8].
При изучении эмульгирующей активности наблюдалась высокая активность эмульгирования с использованием бензина у штаммов № 1 (40%), 3 (60%), 8 и 11 (53%); с использованием ДТ эмульгирующая активность значительно ниже (0-7%) (рис. 2).
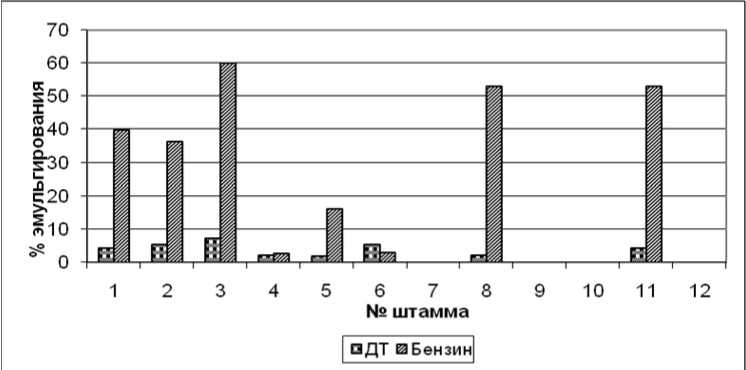
Рис. 2. Эмульгирующая активность бактериальных штаммов (%).
Изучение фунгицидной активности проводили в (КГА), содержащем картофельный экстракт – 230 чашках Петри на картофельно-декстрозном агаре мл, глюкозу – 20,0, водопроводную воду – 770 мл, 199
и глюкозо-пептонном агаре следующего состава (г/л): глюкоза – 5,0; пептон – 5,0; K 2 HPO 4 – 4,0; KH 2 PO 4 – 2,0; агар-агар – 15,0. Суспензию спор тест-гриба высевали на агаризованную среду, а исследуемую культуру вносили, делая посев уколом поверх газона гриба. Чашки инкубировали в термостате в течение 5-7 сут при температуре 25ºС. Антагонистов выявляли по наличию вокруг колонии бактерий зоны подавления роста тест-гриба [3].
В качестве тест-объектов для определения фунгицидной активности штаммов служили следующие мицелиальные грибы: Alternaria tennuissima , Fusarium culmorum , F. graminearum , Phytophtora ultum .
Изучение фунгицидной активности показало, что данным свойством обладают штаммы № 2, 6, 10, проявляя фунгицидную активность к Fusarium graminearum , F. culmorum, Phytophtora ultum .
Для определения способности штаммов микроорганизмов усваивать поверхностно-активные вещества (ПАВ) использовали ПА с добавлением катионных и анионных ПАВ. Микроорганизмы высевали радиальными штрихами. Контролем служили чашки с посевом без добавления ПАВ. Чашки помещали в термостат. Интенсивность развития культур бактерий по штриху оценивали в баллах визуально (шкала от 0 до 5) (рис. 3).
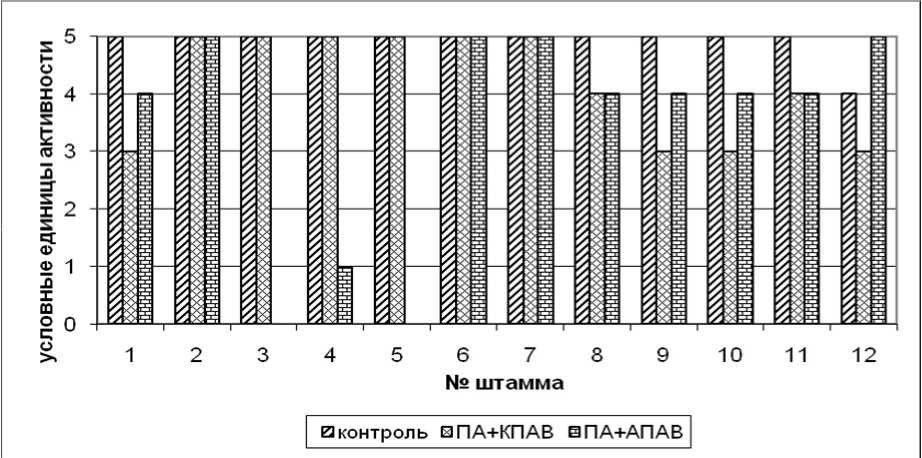
Рис. 3. Активность бактериальных культур по отношению к катионным и анионным ПАВ.
При изучении способности использовать КПАВ наблюдался рост всех штаммов микроорганизмов. На ПА с добавлением АПАВ активный рост наблюдался практически для всех культур, за исключением штаммов № 3, 4, 5.
Способность микроорганизмов деградировать ПАВ изучали флуориметрическим методом, который основан на экстракции хлороформом ионных пар АПАВ с красителем акридиновый желтый [5], деградации КПАВ – на экстракции хлороформом ионных пар КПАВ с красителем эозин [4] и измерении концентрации ПАВ в полученном экстракте с помощью анализатора жидкости «Флюорат-02».
Для эксперимента использовали растворы КПАВ с концентрацией 1, 5, 10 мг/л, растворы АПАВ – 1, 2, 10, 20 мг/л. В данные растворы вносили бактериальные штаммы, титр клеток, при внесении в растворы КПАВ составляет 2,5·103 КОЕ/мл, в растворы АПАВ – 1,47·106 КОЕ/мл. Убыль ПАВ и титр клеток в ходе эксперимента отмечали через каждые 24 ч в течение 4 сут.
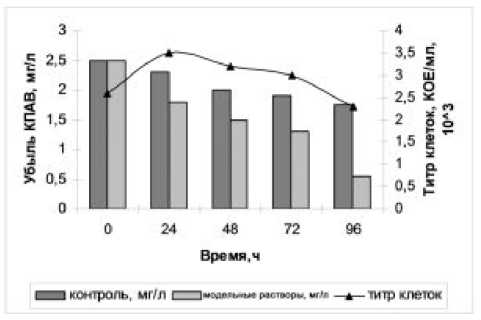
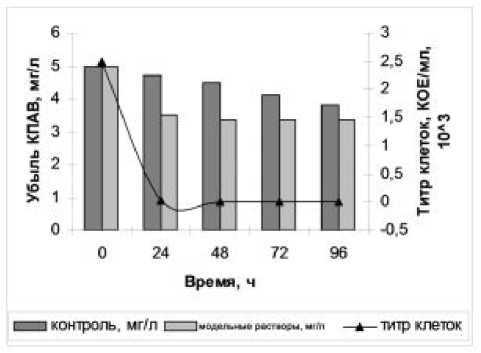
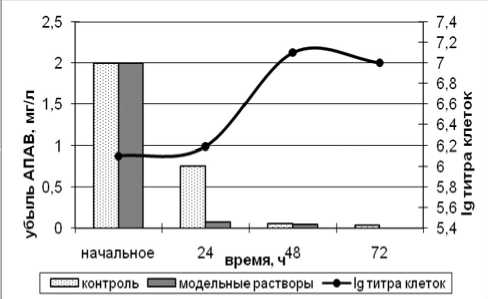
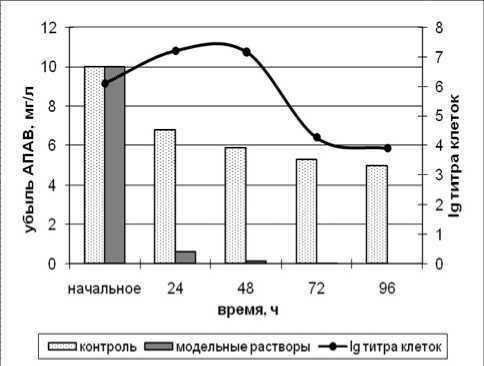
Установлено, что все исследуемые штаммы осуществляют деградацию КПАВ и АПАВ. Максимальной способностью деградировать ПАВ обладает штамм № 11. Деградация КПАВ с концен- трацией 1 мг/л в течение 96 ч достигла 60%, 5 мг/л – 65%, 10 мг/л – 62% (рис. 4). Деградация АПАВ в течение 96 ч достигла 100% во всех модельных растворах (рис. 5).
Убыль КПАВ с концентрацией 1 и 5 мг/л происходит постепенно в течение 96 ч. При этом численность микроорганизмов возрастает и убывает постепенно. В первом случае численность микроорганизмов имеет два пика: 24 ч и 72 ч, после чего резко уменьшается. При концентрации 5 мг/л титр клеток в первые 24 ч увеличивается, затем постепенно снижается в течение эксперимента. Деструкция КПАВ с концентрацией 10 мг/л происходит незначительно в первые 24 ч, затем никаких изменений не наблюдается. При этом численность микроорганизмов резко уменьшается также в течение 24 ч культивирования. Исходя из этого, можно предположить, что концентрация КПАВ 10 мг/л, является летальной для данного штамма.
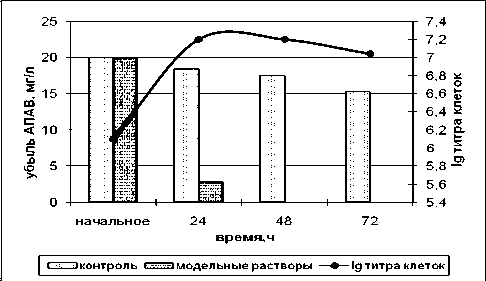
Во всех модельных растворах происходит резкое снижение концентрации АПАВ в первые 24 ч, в последствии к 72 ч происходит полная деградация АПАВ. При этом титр клеток увеличивается (до 107) в течение 48 ч, затем постепенно снижается (до 104).
Таким образом, в ходе исследований выделены новые штаммы микроорганизмов, способные использовать поверхностно-активные вещества в качестве источников питания, что позволяют сделать вывод о возможности применения бактериальных культур для разработки способов очистки от ПАВ.
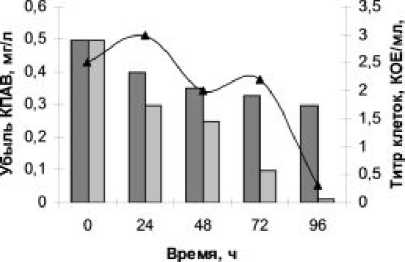
I I контроль, мг/л I J мс<мль»*»е соггвсои. w?p —д— TWip КЛОТОК
а
б
в
Рис. 4. Деградационная способность штамма № 11 по отношению к КПАВ: а) концентрация 1 мг/л; б) концентрация 5 мг/л; в) концентрация 10 мг/л.
б
В
Рис. 5. Деградационная способность штамма № 11 по отношению к АПАВ: а) концентрация 2 мг/л; б) концентрация 10 мг/л; в) концентрация 20 мг/л.
Список литературы Изучение физиолого-биохимических свойств новых штаммов микроорганизмов, выделенных из промышленных отходов
- Градова Н.Б., Бабусенко Е.С., Горнова И.Б. Лабораторный практикум по общей микробиологии. М., 2004. 144 с.
- Егорова Т.А., Клоунова С.М., Живухина Е.А. Основы биотехнологии. М.: Академия, 2005. 208 с.
- Логинов О.Н. Бактерии Pseudomonas и Azotobacter как объекты сельскохозяйственной биотехнологии. М.: Наука, 2005. 166 с.
- ПНД Ф 14.1:2:4.39-95. Методика выполнения измерений массовой концентрации катионных поверхностно-активных веществ (КПАВ) в пробах природной, питьевой и сточной воды флуориметрическим методом на анализаторе жидкости «Флюорат-02»: Утв. 1995-06-23. М., 1995. 21 с.
- ПНД Ф 14.1:2:4.158-2000 Методика выполнения измерений массовой концентрации анионных поверхностно-активных веществ (АПАВ) в пробах природной, питьевой и сточной воды флуориметрическим методом на анализаторе жидкости «Флюорат-02»: Утв. 2000-03-15. М., 2000. 21 с.
- Практикум по микробиологии/А.И. Нетрусов, М.А. Егорова, Л.М. Захарчук и др. М.: Академия, 2005. 608 с.
- Ротмистров М.Н., Гвоздяк П.И., Ставская С.С. Микробиология очистки воды. Киев: Наукова думка, 1978. 268 с.
- Турковская О.В. Биологические и технологические аспекты микробной очистки сточных вод и природных объектов от поверхностно-активных веществ и нефтепродуктов: Дис. … докт. биол. наук. Саратов, 2000. 360 с.


