Изучение комплексообразующей способности пектина по отношению к меди и свинцу
Автор: Михеева Лариса Алексеевна, Февралева Марина Анатольевна, Брынских Галина Тимофеевна, Тры Анна Вячеславовна
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Медико-биологические науки
Статья в выпуске: 2, 2017 года.
Бесплатный доступ
Сопротивляемость организма к негативным факторам можно повысить лечебно-профилакти- ческим питанием. Пектин является уникальным биологически активным веществом, обладающим радиопротекторными и другими лечебно-профилактическими свойствами. Рядом исследований была подтверждена комплексообразующая способность пектина, основанная на взаимодействии молекулы пектина с катионами тяжелых металлов, что позволило использовать его в качестве детоксиканта при отравлениях солями тяжелых металлов. Цель. Изучение влияния различных факторов на комплексообразующую способность пектина по отношению к меди и свинцу. Материалы и методы. Связывающую способность яблочного пектина различных концентраций (0,5-2,0 %) определяли путем его взаимодействия с растворами солей меди и свинца в кислой и щелочной средах. Растворы выдерживали в термостате, а осадки отделяли фильтрованием. Измерения оптической плотности растворов проводили на спектрофотометре КФК-2МП, по результатам строили градуировочный график зависимости концентрации ионов металлов от оптической плотности. Результаты. В щелочной среде комплексообразующая способность яблочного пектина максимальна по сравнению с кислой средой. Наилучшее комплексообразование происходит при взаимодействии ионов меди и свинца с разбавленными растворами пектинов. Значение концентрации пектинового раствора, при котором происходит максимальное связывание ионов металла, находится в области 0,5±0,1 %. Наибольшее связывание идет в течение 1 ч. Заключение. Природа металла влияет на комплексообразующую способность пектинов, и по активности реакций комплексообразования с пектином ионы меди и свинца можно представить в виде ряда: Сu2+>Pb2+.
Пектин, ионы меди, ионы свинца, комплексообразующая способность
Короткий адрес: https://sciup.org/14113266
IDR: 14113266 | УДК: 547.466:543.544 | DOI: 10.23648/UMBJ.2017.26.6225
Study of complexing ability of pectin with respect to copper and lead
Body resistance to negative factors can be maintained by healthful and dietary meals. Pectin is a unique biologically active agent with radioprotective and other preventive properties. A number of studies confirmed the complexing ability of pectin. It was based on interaction of the pectin molecule with heavy metal cations. This fact made it possible to use pectin as a detoxicating agent in case of poisoning by salts of heavy metals. Objective. The aim of this paper was to study the influence of various factors on pectin complexing properties with respect to copper and lead. Materials and Methods. The binding affinity of apple pectin taken in various concentrations (0.5-2.0 %) was determined by its interaction with solutions of copper and lead salts in acidic and alkaline media. The solutions were incubated, and the precipitates were separated by filtration. Spectrophotometer KFK-2MP was used to measure the optical density of solutions. Graduated dependency diagram of metallic ion concentration on the optical density was constructed. Results. The complexing ability of apple pectin in alkaline medium (as opposed to acidic medium) is maximal. The best complexing occurs when copper and lead ions interact with dilute pectin solutions. The maximum metal ions binding takes place when pectic concentration readings fall within the range 0.5±0.1 %. The maximum binding occurs within the 1st hour. Conclusion. Metals affect the complexing ability of pectins. Copper and lead ions can be represented as a series: Cu2+>Pb2+ due to their complexing reaction with pectin.
Текст научной статьи Изучение комплексообразующей способности пектина по отношению к меди и свинцу
Введение. В современном мире проблема ограничения неблагоприятных воздействий окружающей среды на организм становится все более актуальной. Наиболее простым и действенным методом сохранения здоровья является лечебно-профилактическое питание, позволяющее повысить сопротивляемость организма к негативным факторам. Проблема рационального питания особенно актуальна для людей, работающих во вредных условиях труда, подверженных действию ионизирующего излучения вследствие инкорпорации радионуклидов, а также по- стоянно проживающих в экологически неблагоприятных условиях.
В связи с этим все более привлекательным становится пектин – уникальный биологически активный продукт, обладающий ра-диопротекторными и другими лечебнопрофилактическими свойствами. К преимуществам пектина относится также многообразное, недорогое и доступное сырье, из которого его можно получить.
Благодаря природному происхождению и уникальным свойствам пектин и пектинсодержащие продукты, не имеющие полноцен- ных заменителей, завоевали прочное место в современной технологии пищевой промышленности и некоторых областях медицины [1].
По международной классификации пектиновые вещества зарегистрированы под номером Е 440 и вошли как одна из главных пищевых добавок в очень широкий ассортимент продуктов питания, выпускаемых во всех странах Европы и США (кондитерские, молочные, хлебобулочные и консервные изделия). Согласно рекомендациям Минздрава России, суточное потребление пектина в лечебно-профилактических целях должно составлять 2–4 г [2].
Несмотря на постоянно растущую потребность в пектине, особенно в условиях осложненной экологической обстановки, в России в настоящее время имеются лишь опытные производства по его изготовлению. В связи с этим потребности страны полностью удовлетворяются за счет импорта данного продукта.
Структура пектина была установлена только в первой половине XX в., но задолго до этого достаточно быстро были выявлены многие его ценнейшие свойства. В середине XIX в. рядом исследователей (Браконно, Фе-ленберг, Стейвер, Ольсен) была открыта и экспериментально подтверждена способность яблочного пектина связывать ионы тяжелых металлов, что позволило использовать его в качестве детоксиканта при отравлениях солями тяжелых металлов [3]. Исследования по изучению химических, биохимических свойств этого удивительного вещества не прекращаются и по сей день.
Основной объем исследовательских работ промышленной токсикологии по практическому использованию пектина и пектино-продуктов посвящен изысканию методов обезвреживания токсических веществ, попавших в организм человека, и быстрого их выведения из него [4, 5]. Следует заметить, что комплексообразующая способность пектинов, основанная на взаимодействии молекулы пектина с катионами тяжелых металлов, является одним из важнейших свойств пектиновых веществ.
Цель исследования. Изучение комплексообразующей способности пектиновых веществ по отношению к меди и свинцу и исследование влияния различных факторов на комплексообразующие свойства пектина.
В соответствии с поставленной целью были определены следующие задачи:
-
1. Исследовать влияние природы металла на комплексообразующую способность пектина.
-
2. Определить влияние pH среды на комплексообразующую способность пектина.
-
3. Установить влияние концентрации пектина на комплексообразующую способность пектина.
-
4. Исследовать влияние времени на комплексообразующую способность пектина. Материалы и методы. Для исследования был взят яблочный пектин, полученный Всероссийским научно-исследовательским институтом консервной и овощесушильной промышленности (ВНИИКОП).
Концентрацию пектина варьировали в диапазоне 0,5–2,0 %. Связывающую способность определяли путем взаимодействия 15 мл раствора пектина с 4 % растворами солей меди и свинца; объем осаждающего реагента изменяли от 5 до 15 мл при увеличении концентрации пектина от 0,5 до 2,0 %. Исследования проводили в кислой и щелочной средах. Растворы выдерживали в термостате в течение 30 мин и 1 ч и при разных температурах (20, 37 °С). Полученные осадки отделяли фильтрованием, затем производили измерения оптической плотности растворов на стектрофотометре КФК-2МП.
Определение оптической плотности оставшихся ионов меди в растворе после образования комплекса с пектином проводили при длине волны 720 нм. Для соответствующих измерений оставшихся ионов свинца после образования комплекса с пектином использовали длину волны 570 нм. Предварительно построили градуировочный график зависимости концентрации ионов меди и свинца от оптической плотности. По найденным нами оптическим плотностям определили их концентрации в растворах. По разности взятого исходного количества меди или свинца и не связавшихся в комплекс их ионов определили, сколько миллиграммов металла связывается с пектином. По этим данным построили графики зависимости массы (в мг) связанного металла на грамм пектина от объема раствора соли CuSO4×5H2O или Pb(NO3)2.
Результаты и обсуждение. В результате эксперимента было установлено, что минимально необходимое время связывания пектина в комплекс с медью составляет 1 ч. Результаты связывания пектина с медью в кислой и щелочной средах представлены на рис. 1 и 2.
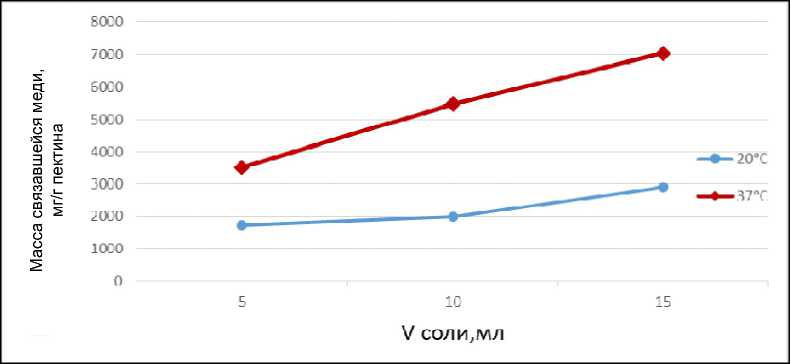
Рис. 1. Связавшиеся ионы меди с 0,5 % раствором пектина в кислой среде
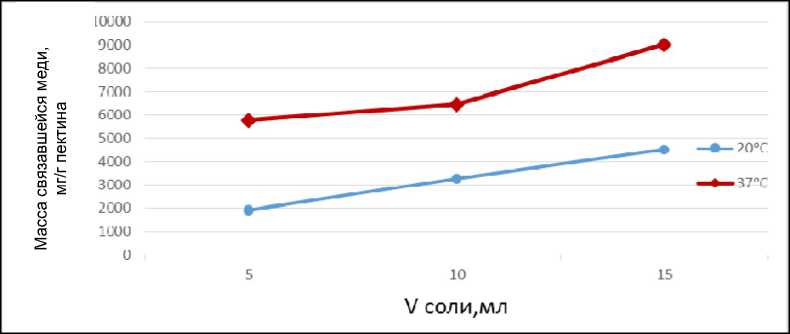
Рис. 2. Связавшиеся ионы меди с 0,5 % раствором пектина в щелочной среде
Из полученных графиков видно, что наилучшее связывание пектина происходит при температуре 37 °С.
Далее сравнили результаты связывания ионов меди пектином в течение 1 ч при температуре 37 °С в кислой и щелочной средах (рис. 3).
Из графика, представленного на рис. 3, видно, что наилучшее связывание пектина в комплекс с ионами меди происходит в щелочной среде.
Полученные экспериментальные данные позволяют сделать вывод о том, что наибольшее связывание пектина с медью в комплекс происходит в щелочной среде в течение 1 ч при температуре 37 °С. Было установлено, что пектин с медью образует комплекс состава 10:1 (одна молекула меди на десять моносахаридных фрагментов).
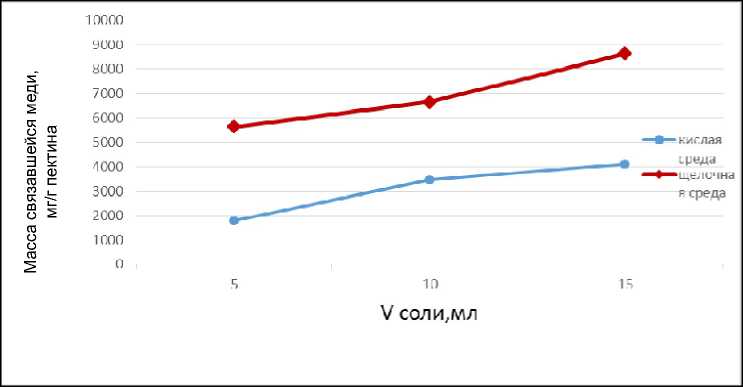
Рис. 3. Связавшиеся ионы меди с 0,5 % раствором пектина в кислой и щелочной средах
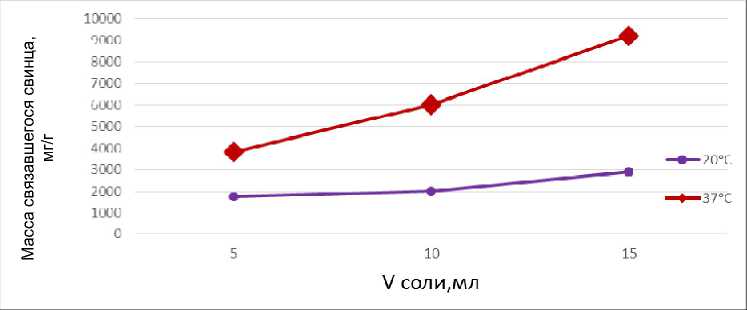
Рис. 4. Сравнение связавшихся ионов свинца с 0,5 % раствором пектина в кислой среде в течение 1 ч при температурах 20 и 37 °С
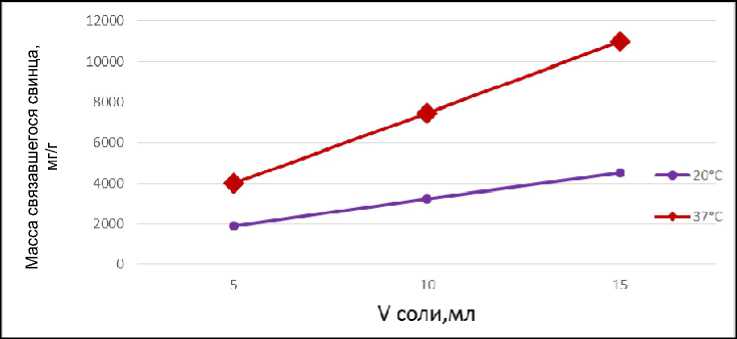
Рис. 5. Связавшиеся ионы свинца с 0,5 % раствором пектина в щелочной среде
Экспериментальные данные показывают, что максимальное связывание свинца происходит при концентрации пектина 0,5 % в кислой и щелочной средах. По этим данным по- строили графики зависимости массы (в мг) связанного металла на грамм пектина от объема раствора соли Pb(NO3)2. В результате установили, что минимальное время связыва- ния пектина в комплекс со свинцом составляет 1 ч.
Результаты связывания пектина с ионами свинца в кислой и щелочной средах пред- ставлены на рис. 4 и 5. Далее сравнили результаты связывания ионов свинца пектином в течение 1 ч при температуре 37 °С в кислой и щелочной средах (рис. 6).
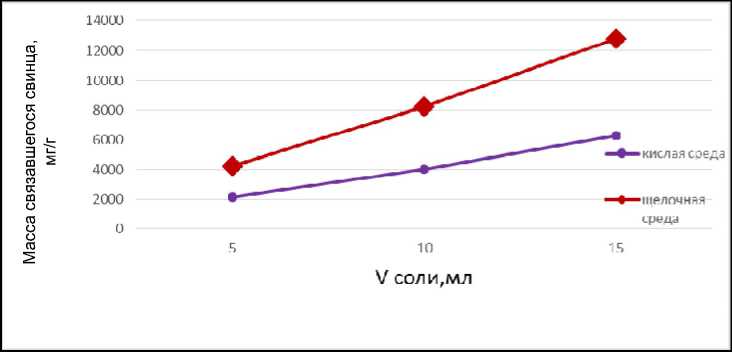
Рис. 6. Сравнение связавшихся ионов свинца с 0,5 % раствором пектина в кислой и щелочной средах при температуре 37 °С
По результатам экспериментальных данных можно сделать вывод о том, что наибольшее связывание пектина с ионами свинца происходит в щелочной среде в течение 1 ч при температуре 37 °С. Было установлено, что пектин со свинцом образует комплекс состава 6:1 (одна молекула свинца на шесть моносахаридных фрагментов).
Заключение. Таким образом, в ходе проделанной работы была определена зависимость комплексообразующей способности пектина от рН среды, в которой происходит связывание «металл – пектин». Показано, что в щелочной среде комплексообразующая способность максимальна по сравнению с ки- слой средой. Установлено, что наилучшее комплексообразование происходит при взаимодействии ионов меди и свинца с разбавленными растворами пектинов. Значение концентрации пектинового раствора, при котором происходит максимальное связывание ионов металла, находится в области 0,5±0,1 %. Установлено, что наибольшее связывание идет в течение 1 ч. Показано, что природа металла влияет на комплексообразующую способность пектинов и по активности реакций комплексообразования с пектином ионы меди и свинца можно представить в виде ряда: Сu2+>Pb2+.
Список литературы Изучение комплексообразующей способности пектина по отношению к меди и свинцу
- Новосельская И.Л., Воропаева Н.Л. Пектин. Тенденции научных и прикладных исследований. Химия природных соединений. 2000; 1: 3-11.
- Голубев В.Н., Шелухина Н.П. Пектин: химия, технология, применение. М.; 1995. 390.
- Михеева Л.А. Получение и некоторые химические свойства пектинов растений рода амарант: дис.. канд. хим. наук. Ульяновск; 2001. 205.
- Голубев В.Н., Чичева-Филатова Л.В., Шленская Т.В. Пищевые и биологически активные добавки. М.: Издательский центр «Академия»; 2003. 208.
- Ильина И.А. Научные основы технологии модифицированных пектинов. Краснодар; 2001. 312.


