Изучение методов получения метанола
Автор: Бозоров Г.Р., Суяров М.Т.
Журнал: Теория и практика современной науки @modern-j
Рубрика: Основной раздел
Статья в выпуске: 3 (45), 2019 года.
Бесплатный доступ
В статье изучены методы получения метанола для производства высокооктановых бензинов, топлива для электростанций, как сырья для синтеза белка и т.д.
Синтез-газ, метанол, эфир, товливо, катализатор, монооксид
Короткий адрес: https://sciup.org/140274423
IDR: 140274423 | УДК: 665.5
Studying methods for producing methanol
The article examines methods for producing methanol for the production of high-octane gasoline, fuel for power plants, as a raw material for protein synthesis, etc.
Текст научной статьи Изучение методов получения метанола
Метанол, один из основных продуктов многотоннажной химии, широко используется для получения множества ценных химических веществ: формальдегида, сложных эфиров, аминов, растворителей, уксусной кислоты. Мировое производство метанола превышает 20 млн. т в год, и спрос на него постоянно растет, что связано с наметившейся тенденцией использовать метанол в новых областях, например для получения высокооктановых бензинов, топлива для электростанций, как сырья для синтеза белка и т.д.
С этапами изучения химии метанола связаны имена величайших химиков. Впервые метанол был обнаружен еще в середине XVII века Робертом Бойлем при изучении продуктов перегонки дерева, однако в чистом виде метиловый спирт, или древесный, получаемый этим способом, был выделен только через 200 лет: тогда впервые удалось очистить его от примесей сопутствующих веществ, прежде всего уксусной кислоты и ацетона. В 1857 году Марселен Бертло получил метанол омылением хлористого метила. Процесс сухой перегонки древесины долгое время оставался, пожалуй, единственным способом производства метанола. Сейчас он полностью вытеснен каталитическим синтезом из оксида углерода и водорода. Получение метанола из синтез - газа впервые было осуществлено в Германии в 1923 году фирмой BASF
Процесс проводился под давлением 100-300 атм. на оксидных цинкхромовых катализаторах (ZnO-Cr 2 O 3 ) в интервале температур 320-4000С, производительность первой промышленной установки доходила до 20 т/сутки. Интересно, что в 1927 году в США был реализован промышленный синтез метанола, основанный не только на монооксиде, но и на диоксиде углерода. В настоящее время в результате развития и усовершенствования процесса получения метанола из синтез - газа используются реакторы большой мощности с производительностью до 2000 т метанола в сутки. Разработаны более активные катализаторы на основе оксидов цинка и меди, которые позволили смягчить условия синтеза - снизить давление до 50-100 атм., а температуру - до 2500C.
Суммарная реакция образования метанола:
CO + 2H2 ↔ CH3OH является сильно экзотермичной. Поскольку реакция протекает с уменьшением объема, повышение давления способствует увеличению конверсии синтез - газа.
Было предложено несколько механизмов образования метанола. Один из них предполагает ряд последовательных стадий гидрирования хемосорбированного на катализаторе монооксида углерода, при этом образуются промежуточные поверхностные соединения:
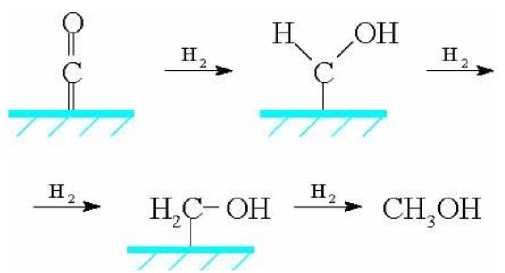
Второй механизм предполагает образование поверхностного гидрида, внедрение монооксида углерода в связь металл-водород с образованием поверхностного формильного производного, дальнейшее гидрирование которого приводит к образованию гидроксиметиленового производного, аналогичного приведенному в предыдущей схеме:
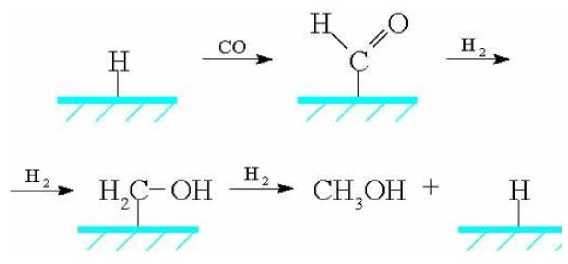
Согласно третьему механизму, СО внедряется в поверхностный гидроксил, при этом образуются промежуточные соединения, связанные с поверхностью катализатора через кислородный мостик. Последующее гидрирование образующегося формата и дегидратация приводят к метанолу:
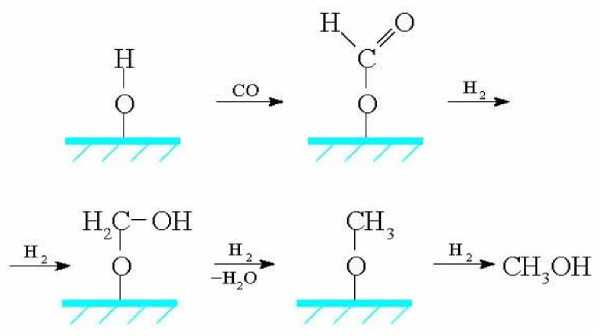
Следует отметить еще
один экспериментально обоснованный механизм синтеза, согласно которому метанол образуется при восстановлении диоксида углерода. Монооксид углерода является лишь источником CO2:
CO + H 2 O = CO 2 + H 2
CO 2 + 3H 2 = CH 3 OH + H 2 O
Как и во многих других случаях, однозначное установление истинных механизмов химических реакций представляет значительную трудность, и до сих пор в синтезе метанола имеются неразгаданные моменты.
Литературы
Список литературы Изучение методов получения метанола
- Караваев М.М. Технология синтеза метанола. М: Химия. 1984.-72 с.
- Лапидус А.Л. Газохимия. М. ЦентрЛитНефтеГаз, 2008. -357 с.


