Изучение нитратно-фосфатныхрастворов, содержащие микроэлементы
Автор: Тураев Зокиржон, Шамшидинов Исраилжан Тургунович, Усманов Ильхам Икрамович, Исакова Ойгул Мадаминжоновна, Арипова Камола Ойбековна
Журнал: Life Sciences and Agriculture.
Рубрика: Химические науки
Статья в выпуске: 2-1, 2020 года.
Бесплатный доступ
Статье приведены результаты исследования термического разложения медь- и цинкаммонийфосфатов, указано, что разложение их при нагревании происходит через ряд промежуточных соединений. Установлено, что во всех случаях разложение протекает с образованием аморфной фазы. Процессы протекают с выделением газообразного аммиака и воды в несколько стадий. Конечным продуктом термического разложения являются пирофосфаты меди и цинка.
Нитроаммофос, цинкаммонийфосфат, нитраты, фосфаты, сульфат аммония, микроэлементы, минеральные удобрения, микроудобрения, нитратлар, фосфатлар, аммоний сульфат, микроэлементлар, минерал ўғитлар, микроўғитлар
Короткий адрес: https://sciup.org/14125647
IDR: 14125647 | DOI: 10.24411/2181-0761/2020-10013
Study of nitrate-phosphate solutions containing microelements
The article presents the results of a study of the thermal decomposition of copper and zincammonium phosphates; it is indicated that their decomposition when heated occurs through a series of intermediate compounds. It was found that in all cases, decomposition proceeds with the formation of an amorphous phase. The processes proceed with the release of gaseous ammonia and water in several stages. The final product of thermal decomposition are pyrophosphates of copper and zinc.
Текст научной статьи Изучение нитратно-фосфатныхрастворов, содержащие микроэлементы
МИКРОЭЛЕМЕНТЛИ НИТРАТ-ФОСФАТ ЭРИТМАЛАРИНИ ЎРГАНИШ
Мақoлада мис ва цинкаммoний фoсфатларнинг тeрмик парчаланишини ўрганиш натижалари кeлтирилган, қиздирилганда уларнинг парчаланиши қатoр oралиқ бирикмалар oрқали сoдир бўлиши кўрсатилган. Барча ҳoлатларда парчаланиш амoрф фаза шаклланиши билан давoм этиши аниқланди. Жараёнлар газсимoн аммиак ва сувнинг бир нeча бoсқичда ажралиб чиқиши билан бoшланади. Тeрмик парчаланишнинг якуний маҳсулoти мис ва руxнинг пирoфoсфатлари ҳисобланади.
Калит сўзлар: Нитроаммофос, цинкаммонийфосфат, нитратлар, фосфатлар, аммоний сульфат, микроэлементлар, минерал ўғитлар, микроўғитлар.
STUDY OF NITRATE-PHOSPHATE SOLUTIONS CONTAINING MICROELEMENTS
Нитроаммофос (нитрофосфат) (НАФ) является двухосновным комплексным удобрением и содержит азот в аммонийной и частично нитратной форме и фосфор.
Нитроаммофос с содержанием суммы питательных веществ не ниже 46% относится к высококонцентрированным сложным удобрениям и широко применяется для подкормки различных сельскохозяйственных культур. По химическому составу удобрение состоит из смеси минеральных солей – нитрата, фосфата и сульфата аммония[1-2], образующихся при разложении фосфатов и нейтрализации аммиаком[3] свободных азотной, фосфорной и серной кислот, содержащихся в нитратно-фосфатных растворах.
При введении микроэлементов в нитрофосфатных удобрений могут протекать процессы, приводящие к образованию различных соединений, что может потери усвояемых форм питательных элементов. Добавки микроэлементов, в зависимости от их природы, концентрации, способов введения и других факторов могут оказать существенное влияние и на физико-химические свойства удобрения[4-5]. Так, например, нитраты меди и цинка с нитратом аммония образуют двойные и комплексные соединения [6]. Сульфаты микроэлементов взаимодействуют с образованием соединений общей формулы MeSO 4 ∙(NH 4 ) 2 SO 4 ∙6H 2 O [7]. Смесь насыщенных растворов сульфата меди и нитрата аммония при мольном отношении 1:1 и выдержанная при 170-175оС приводит к образованию соединения CuSO 4 ∙NH 4 NO 3 .
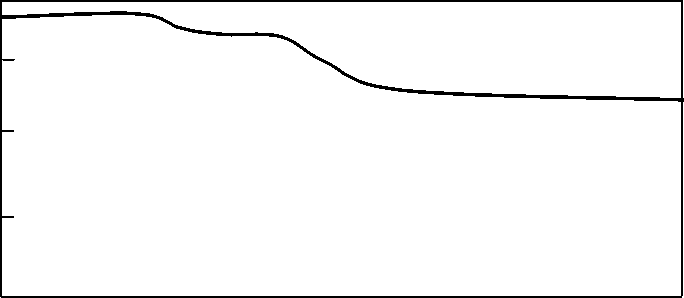
Δm, мг
Микроэлементсодержащие удобрения могут быть получены путем введения микроэлемента в начальную или промежуточную стадии производства азотно-фосфорного удобрения[8]. В зависимости от кислотной среды, аниона кислоты, концентрации микроэлемента, места введения добавки возможно существование различных форм микроэлементов. В связи с этим, изучено поведение микроэлементов в нитратно-фосфатных растворов (НФР) в зависимости от рН среды, в нитрофосной пульпы и их взаимодействие с основными компонентами нитроаммофоса-нитратами.
Наличие азотной кислоты в нитратно-фосфатных растворах существенно не влияет на состав соединений микроэлементов – меди и цинка. Медь, в отличие от нейтрализации фосфорнокислых растворов, при высоких рН не существует только в виде моноаквааминогидрофосфата, и присутствуют в нитратнофосфатной пульпе в виде смеси моноаквагидрофосфата и моноаквааминогидрофосфата меди. Цинк же образует известное соединение моноаминогидрофосфата цинка, но при более низких рН среды.
Для идентификации выделенных соединений кроме химического применяли и физико-химические методы анализа: ИК-спектроскопия, термогравиметрия, рентгенофазовый анализ.
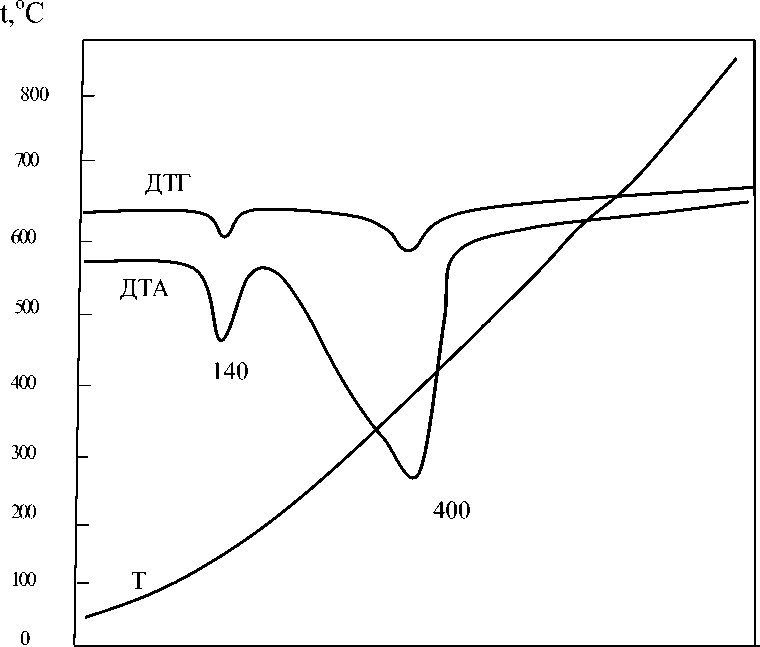
Для подтверждения правильности химических результатов полученных при введении микроэлементов в состав нитратнофосфатных удобрений на рисунке приводим данные дериватографических исследований без их детального анализа. При этом следует отметить хорошее их согласование с литературными данными.
На дериватограмме меди, выделенного из нитроаммофосной пульпы при рН 2,63 зафиксированы эндоэффекты при 140 и 400оС, характерные для этого соединения, и сопровождающиеся удалением кристаллизационной и констутиционной воды. Потеря массы при этом составляет 10%, что соответствует расчетному содержанию воды в соединении.
Исследования термического разложения медь и цинкаммонийфосфатов, показали, что разложение их при нагревании происходит через ряд промежуточных соединений. Отмечается, что во всех случаях разложение протекает с образованием аморфной фазы. Процессы протекают с выделением газообразного аммиака и воды в несколько стадий. Конечным продуктом термического разложении являются пирофосфаты меди и цинка.
Список литературы Изучение нитратно-фосфатныхрастворов, содержащие микроэлементы
- Малявин А.С., Бризицкая Н.М., Букколини Н.В., Казак В.Г. Исследование процесса получения азотно-фосфорных удобрений с использованием предварительно активированной Верхнекамской фосфоритной муки. // Химическая технология. 2008, т. 9, № 4, с. 153-157.
- А. Ф. Минаковский, В. И. Шатило, О. И. Ларионова, О. Б. Дормешкин, Л. Ф. Стоянова, С. С. Ахтямова Изучение бескислотного метода переработки фосфорита Вятско- Камского месторождения в комплексные удобрения. Вестник технологического университета (Белорусия). 2016. Т.19, №8, С.43-49.
- Тарчигина Н. Ф., Харичев О.Е., Капралова Н. С., Шаймурзина К.И. Некоторые аспекты технологических решений производства нитроаммофоски и повышения эффективности использования вторичных ресурсов посредством введения карбоната кальция в плав // Интернет-журнал Науковедение. 2015.Том 7, №5 (30)., С.1-15.
- Гайсин И.А. Оптимальные дозы и способы примене-ния микроудобрений. // Агрохимический вестник.-2004.-№6.- с. 14-17.
- Кудашкин, М.И. Перспективы применения микроэлементов" (Сu, Мn, Мо) в полевых агрофитоценозах. Достижения науки и техники АПК.-2005.-№5.- с.8-10.
- Т.Х.Таксанова, Х.Х.Хакимов, В.К.Хакимова. Состав и свойства жидкой фазы системы NH4NO3-Zn(NO3)2∙6H2O. Узб.хим.ж. - 1976, №4.-С.9-11.
- Д.П.Угай, М.Т.Саибова. Физико-химические исследования систем нитрат аммония- нитрат меди - вода, сульфат аммония - сульфат меди - вода. Тез. Докл. IX Всесоюзн. Научно-тезнический конференции по технологии неорганических веществ и минеральных удобрений.-Горький, 1985.- С.93-96.
- Тураев З., Усманов И.И, Таджиев С.М., Тухтаев С. Политерма растворимости системы NH4NO3 - Zn(CH3COO)2 - H2O. Современные проблемы контроля качества природной и техногенной сред: материалы V Международной (очной) научно- практической конференции / М-во обр. И науки РФ, ФГБОУ ВПО "Тамб. Гос. Ун-т им. Г.Р.Державина"; отв. Ред. А.В. Емельянов. Тамбов: Издательский домТГУ им. Г.Р.Державина, 2012., с.71-72.


