Изучение особенности лимфотропной терапии на фоне экспериментально созданной модели язвенного колита
Автор: Эгамов Ю. С., Рузиев А. Э., Дурдиев Х. Б.
Журнал: Московский хирургический журнал @mossj
Рубрика: Экспериментальная хирургия
Статья в выпуске: 1 (83), 2023 года.
Бесплатный доступ
Введение. Цель работы: изучить особенности лимфотропной терапии на фоне экспериментально созданной модели язвенного колита для улучшения результата хирургического лечения этой патологии с применением в комплексе лечения эндомезентериальной лимфотропной терапии в послеоперационном периоде.Материал и методы. Проведен анализ результатов 4-х серий экспериментальных опытов, выполненных на 24-х беспородных собаках. Задачей эксперимента было моделирование язвенного колита, и, на фоне созданной модели, изучение роли регионарной лимфатической системы органов брюшной полости в лечении с применением лимфотропной терапии. Подробно были изучены данные литературы по созданию модели язвенного колита в эксперименте. Наиболее оптимальным и приемлемым являлась химически индуцированная модель язвенного колита, которая вызывалась ректальным введением уксусной кислоты.Результаты. Полученные результаты созданной модели язвенного колита у подопытных животных показывают резкое замедление скорости лимфооттока в брыжейке кишечника в два и более раза по сравнению с нормальной. После лимфостимуляции, на фоне созданной модели язвенного колита, лимфоотток в брыжейках кишечника улучшается, устраняя при этом лимфостаз в «лимфатическом коллекторе», который развивается при воспалительном процессе. На фоне лимфостимуляции лимфотропно применяемые лекарственные препараты способствуют предупреждению возможно развивающихся нежелательных осложнений в послеоперационном периоде. Проведенные эксперименты убедительно доказывают позитивные стороны применения лимфотропной терапии в послеоперационном периоде.
Моделирование язвенного колита, язвенный колит, лимфотропная терапия
Короткий адрес: https://sciup.org/142237463
IDR: 142237463 | УДК: 616.348-003-08-12 | DOI: 10.17238/2072-3180-2023-1-73-81
Study of the peculiarities of lymphotropic therapy in the background of the experimentally developed model of ulcerant colitis
Introduction. Purpose of work: to study the features of lymphotropic therapy against the background of an experimentally created model of ulcerative colitis to improve the result of surgical treatment of this pathology using endomesentericlymphotropic therapy in the postoperative period in the complex treatment.Material and methods. The analysis of the results of 4 series of experimental experiments performed on 24 outbred dogs was carried out. The aim of the experiment was to model ulcerative colitis, and before and against the background of the created model to study the role of the regional lymphatic system of the abdominal organs in its treatment using lymphotropic therapy. Literature data on the creation of a model of ulcerative colitis in the experiment were studied in detail.The most optimal and acceptable was the chemically induced model of ulcerative colitis, which was caused by rectal administration of acetic acid.Results. The results obtained with the created model of ulcerative colitis in experimental animals show a sharp slowdown in the rate of lymphatic drainage in the intestinal mesentery by two or more times compared to normal. After lymphostimulation against the background of the created model of ulcerative colitis, lymphatic drainage in the intestinal mesentery improves, while eliminating lymphostasis in the "lymphatic collector", which develops during the inflammatory process.Against the background of lymphostimulation, lymphotropically used drugs contribute to the prevention of possibly developing undesirable complications in the postoperative period. The conducted experiments convincingly prove the positive aspects of the use of lymphotropic therapy in the postoperative period.
Текст научной статьи Изучение особенности лимфотропной терапии на фоне экспериментально созданной модели язвенного колита
Несмотря на совершенствование методов диагностики и улучшение качества лечебных мероприятий, послеоперационные осложнения и летальность при язвенном колите до сих пор остаются высокими. Основные сложности решения послеоперационных осложнений язвенного колита состоят в том, что недостаточно корригируются такие факторы, как борьба с интоксикацией организма в послеоперационном периоде [1, 2, 4, 11, 12, 13].
Порою язвенный колит способствует развитию грозных послеоперационных осложнений, путем переноса бактериальной флоры из кишечника в брюшную полость. Бактериальная флора благоприятствует усугублению патологического процесса, вовлекая органы и систем организма. На фоне таких трудно исправимых изменений развиваются глубокие метаболические расстройства организма, которые приводят к полиорганной недостаточности и гибели больного [1, 2, 4, 7, 12].
При язвенном колите первичным очагом инфекция валяются деструктивные изменения в кишечной стенке, этиологические факторы которых до сих пор не известны [1, 7, 11, 12].
Следующим этапом инфицирования и развития инфекции являются лимфатические узлы брюшной полости. В этих лимфатических узлах образуются микроабсцессы, приводящие в последующем к усилению интоксикации организма. При этом в лимфатической системе органов брюшной полости больных отмечается застойное явление, которое также способствует усилению интоксикации организма. Все это оказывает очень негативное воздействие на защитные механизмы кишечника, обеспечивающие его барьерную функцию. Перечисленные факторы способствуют нарушению функции желудочно-кишечного тракта как осложнения в послеоперационном периоде, которые больше усугубляют эндотоксикоз организма [4, 7, 11, 12].
В большинстве случаев, не смотря на полноценную ликвидацию первичного очага инфекции, продолжается ухудшение состояния больных и нарастание степени интоксикации организма. Вопрос о целесообразности антибактериальной терапии даже при таком тяжелом течении язвенного колита остается не решенным [1, 5, 6, 8].
Все же доказано, что одним из способов повышения эффективности антибиотикотерапии и коррекции иммунитета при язвенном колите является введение препаратов в лимфатическую систему [3, 5, 6, 9].
Разработки новых методов локальной доставки лекарственных препаратов в органы-мишени являются актуальными проблемами современной медицины [10, 13, 14].
Одним из методов локальной доставки лекарственных препаратов является лимфотропная терапия, обеспечивающая создание в лимфатическом регионе очага поражения патологическим процессом достаточных и стабильных терапевтических концентраций лекарственных препаратов, следовательно, и в органе-мишени. В связи с этим поиск и применение наиболее эффективных – лимфатических методов лечения в послеоперационном периоде при язвенном колите остается одним из приоритетных направлений данной сферы.
Цель работы: изучить особенности лимфотропной терапии на фоне экспериментально созданной модели язвенного колита для улучшения результата хирургического лечения этой патологии с применением в комплексе лечения эндомезентери-альной лимфотропной терапии в послеоперационном периоде.
Материал и методы
Нами проведен анализ результатов 4-х серий экспериментальных опытов, выполненных на 24-х беспородных собаках. Задачей эксперимента было моделирование язвенного колита и на фоне созданной модели изучение роли регионарной лимфатической системы органов брюшной полости в лечении с применением лимфотропной терапии. До этого нами были подробно изучены данные литературы по созданию модели язвенного колита в эксперименте. Наиболее оптимальным и приемлемым являлась химически индуцированная модель язвенного колита, которая вызывалась ректальным введением уксусной кислоты (Осиков М.В., 2016).
Эксперименты проведены на беспородных собаках, полученных из вивария аккредитованной центральной научно-исследовательской лаборатории Андижанского Государственного медицинского института на основании нормативных и методических документов республики Уз- бекистан с учетом требований Европейской конвенции по защите позвоночных животных, используемых для экспериментальных исследований или в иных целях (ЕТS № 123, Страсбург, 1986 г.), а также требований Национального руководства по содержанию и использованию лабораторных животных. Для проведения экспериментов взято одобрение этического комитета МЗ РУз.
Для экспериментов были сформированы группы, по 8 животных в каждой серии (табл. 1).
Таблица 1
Экспериментальные группы подопытных животных
Table 1
Experimental groups of experimental animals
|
№ серии опыта Experiment Series № |
Характер опыта The nature of the experience |
Задача Экспериментального опыта The task of experimental experience |
Количество подопытных животных Number of experimental animals |
|
Серия series 1 |
Хронический Chronic |
Исследование лимфооттока брыжейки кишечника в норме Examination of the lymphatic drainage of the mesentery of the intestine is normal |
8 |
|
2-серия series 2 |
Острый Sharp experience |
Моделирование язвенного колита Modeling of ulcerative colitis |
8 |
|
3-серия series 3 |
Острый Sharp experience |
Моделирование язвенного колита Modeling of ulcerative colitis |
8 |
|
4-серия series 4 |
Острый Sharp experience |
Исследование лимфооттока брыжейки кишечника на фоне модели язвенного колита и при этом определение эффективности лимфотропной терапии The study of the lymphatic drainage of the intestinal mesentery against the background of the model of ulcerative colitis and, at the same time, to determine the effectiveness of lymphotropic therapy |
8 |
|
Всего: |
24 (32) |
Примечание: подопытные животные, собаки, участвовавшие в 1-ой серии хронических опытов использованы для острых опытов 2-ой серии – моделирование острого язвенного колита. Исходя из этого количество подопытных животных составляло 24.
Note: experimental animals, dogs participating in the 1st series of chronic experiments were used for acute experiments of the 2nd series – simulation of acute ulcerative colitis. Based on this, the number of experimental animals was 24.
В 1-ой серии опытов изучали характер регионарной лимфатической системы органов брюшной полости в норме, который заключался в определении скорости лимфооттока в брыжейке кишечника. Для этого во время операции у подопытного животного в рану вывели часть петли тонкого кишечника с брыжейкой, которой изолировали от раны при помощи стерильных тампонов. В брыжейку этой части тонкого кишечника в трех местах: корень, срединная часть, краевая часть кишечника, дополнительно в стенку кишечника суб-серозно ввели 0,1 % раствор красителя синьки Эванса по 0,1 мл (рис. 1).
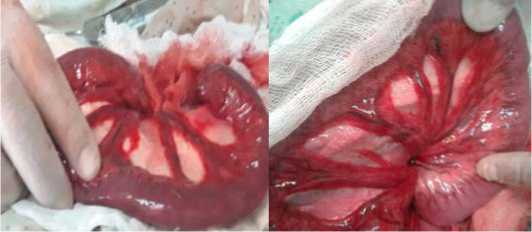
С момента введения синьки Эванса установили секундомеры для определения времени её всасывания. Время всасывания введенных в четырех точках раствора красителя определяли визуально, до полного исчезновения их цвета (рис. 2).
а б
Рис. 2. Визуально определяется время всасывания синьки Эванса в брыжейке кишечника до полного исчезновения их цвета
Fig. 2. Visually determine the absorption time of Evans blue in the mesentery of the intestine until their color disappears completely
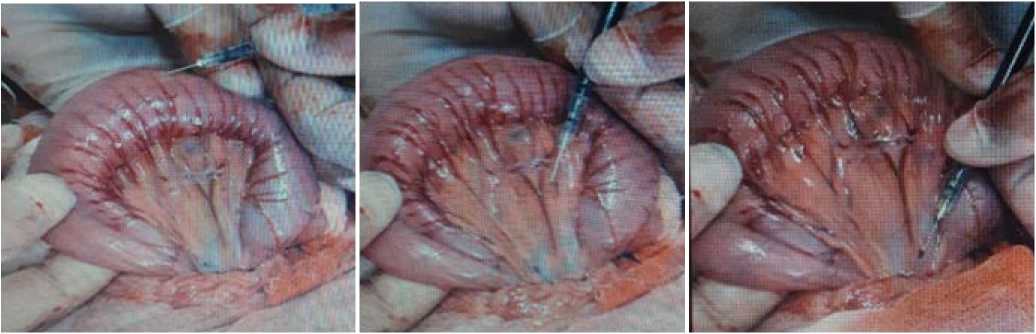
а
б
в
Рис. 1. Указаны места введения синьки Эванса (а – в стенку кишечника, б – в срединную часть брыжейки кишечника, в – в корень брыжейки кишечника) Fig. 1. The injection sites of Evans blue are indicated (a – into the intestinal wall, b – into the middle part of the mesentery of the intestine, c – into the root of the mesentery of the intestine)
После завершения 1-ой серии опытов начали проводить 2-ю серию. Задачей 2-ой серии опытов было: создать модель язвенного колита. Для этого промывали кишечник подопытного животного, применяя очистительную клизму. После полного опорожнения кишечника, ректально в полость толстого кишечника устанавливали специальный зонд-дренаж, смазывая его глицерином, на расстоянии 18–20 см от сфинктера ануса, через который ввели 1,0 мл 4 % раствора уксусной кислоты дробно, одновременно подтягивая зонд-дренаж на 2,0–4,0 см наружу. Экспозиция введенного раствора уксусной кислоты проводилась до одной минуты, как было указано в литературе, после чего при помощи 1,0 литра 0,9 % физиологического раствора промывали полость кишечника путем клизмы. По завершении манипуляции подопытного животного перевели в виварий, давая свободный доступ к питьевой воде и брикетированному корму.
На 7 день провели операцию. Во время ревизии органов брюшной полости не могли визуально найти патологически измененные участки толстого кишечника. Несмотря на это, решили резецировать ту часть толстого кишечника, куда предварительно 7 дней тому назад был введен 4 % раствор уксусной кислоты.
К сожалению, модель язвенного колита, химически индуцированного в эксперименте с 4 % раствором уксусной кислоты, не получилась. При гистологическом изучении под микроскопом, на слизистой оболочке резецированного участка толстого кишечника, явные патологические изменения не были выявлены (рис. 3).
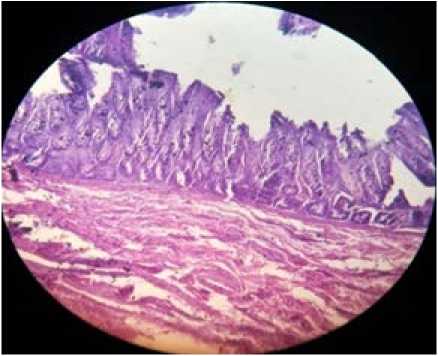
Рис. 3. Явные изменения слизистого слоя толстого кишечника не определяются. Окраска гемотоксилином и эозином, ок.10, об. 40 Fig. 3. There are no obvious changes in the mucous layer of the large intestineare determined. Stained with hematoxylin andeosin, eyepiece. 10, v. 40
Для моделирования язвенного колита во второй серии экспериментов, подопытным животным сначала промывали кишечник, путем очистительной клизмы, применяя «Энема
Клин» – микроклизму 120 мл ректально. До постановки очистительной клизмы подопытного животного – собаку доставили из вивария в наморднике и установили на специальный станок. Передние и задние конечности собаки при помощи специальных верёвок закрепили к станку и проводили очистительную клизму.
После полного опорожнения кишечника, ректально в полость толстого кишечника устанавливали специальный зонд-дренаж, смазывая его глицерином, на расстоянии 18–20 см от сфинктера ануса, через который вводили 2,0 мл 4 % раствора уксусной кислоты дробно, одновременно подтягивая зонд-дренаж на 1,0 – 2,0 см наружу.
Для поддержания одинакового распространения кислоты, задние лапы подопытного животного около минуты удерживали в вертикальном положении. Экспозиция введенного раствора уксусной кислоты проводилась до одной минуты, как было указано в литературе, после чего при помощи 1 литра 0,9 % физиологического раствора промывали полость кишечника путем клизмы. По завершении манипуляции, подопытного животного перевели в виварий, давая свободный доступ к питьевой воде и брикетированному корму.
Наблюдали за состоянием подопытного животного в течение 7 дней. Однако, никаких клинико-патологических изменений со стороны подопытного животного не наблюдалось: клинические признаки интоксикации, диарея с примесью слизи и крови, снижение массы тела. Тем не менее, решили оперировать и посмотреть состояние толстой кишки подопытного животного изнутри. На 7 день провели операцию в операционном блоке в условиях ЦНИЛ АГМИ под общим внутривенным наркозом. За 30 мин. до операции производилась премедикация внутримышечным введением фентанила (2,0 мл 0,005 % раствора) и дроперидола (4 мг 0,005 % раствора). Подопытного животного-собаку доставили из вивария в наморднике и установлен на специальный станок для наркоза. Передние и задние конечности собаки при помощи специальных верёвок закрепляли к станку. По задней наружной части левой конечности найден венозный сосуд, через который произведен внутривенный наркоз с дробным введением 0,1 % раствора калипсола из расчета 15 мг/кг. После наступления хирургического сна собака была взята на операционный стол. Произведена средне-срединная лапаротомия длиною 15 см. Гемостаз. Произвели ревизию органов брюшной полости, к сожалению, не могли визуально найти явно патологически измененные участки стенки толстого кишечника. Несмотря на это, решили резецировать ту часть толстого кишечника, в полость которой 7 дней тому назад был введен 4 % раствор уксусной кислоты. После наложения анастомоза конец в конец, операционная рана ушита послойно, наглухо. После выхода из состояния наркоза подопытное животное-собака переведена в виварий.
Макропрепарат из стенки толстого кишечника погружен в 10 % раствор формалина и отправлен для гистологического исследования в патологоанатомическое отделение клиники АндГосМИ.
При гистологическом изучении под микроскопом, на слизистой оболочке резецированного участка толстого кишечника явные патологические изменения не были выявлены. К сожалению, модель язвенного колита, химически индуцированная в эксперименте 4 % раствором уксусной кислоты, не получилась (рис. 4).
Решили продолжить эксперименты для создания модели язвенного колита прибегая к замене 4 % раствора уксусной кислоты на 6% раствор в третьей серии опытов. Все манипуляции были выполнены при тех же условиях, какие были во второй серии. Единственное отличие – в полость толстого кишечника вводили 6 % раствор уксусной кислоты.
На 7 день подопытного животного оперировали. Интраоперационно: в проекции толстого кишечника, в полость которой предварительно был введен 6 % раствор уксусной кислоты, стенки были незначительно отечны, а явных признаков воспалительного изменения визуально не было обнаружено, также не было обнаружено выпота в брюшной полости. Резецировали ту часть толстого кишечника, где имелась незначительная отечность.
При гистологическом изучении под микроскопом, на слизистой оболочке резецированных участков толстого кишечника выявлены незначительные некротические участки слизистой оболочки (рис. 4).
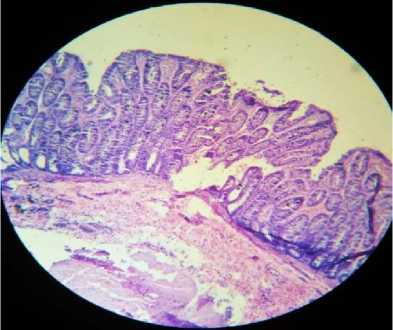
Рис. 4. Острая язва, незначительный некроз слизистого слоя толстого кишечника. Окраска гемотоксилином и эозином, ок.10, об. 40
Fig. 4. Acute ulcer, slight necrosis of the mucous layer of the colonin testines. Stained with hematoxylin andeosin, eyepiece. 10, v. 40
Решили продолжить эксперименты для создания модели язвенного колита прибегая к замене 4 % раствора уксусной кислоты на 6 % раствор в третьей серии опытов. Все манипуляции были выполнены при тех же условиях, какие были во второй серии. Единственное отличие – в полость толстого кишечника вводили 6 % раствор уксусной кислоты.
После чего за состоянием подопытного животного наблюдали в течение 7 дней. Начиная с третьего дня, были отмечены незначительные клинические признаки интоксикации, диарея с примесью слизи. Обогащённые клинические признаки не наблюдались. На 7 день подопытного животного взяли на операцию. Интраоперационно выявлено: в проекции толстого кишечника, в полость которой предварительно ректально был введен 6 % раствор уксусной кислоты, стенки были незначительно отечны, а явных признаков воспаления, а также выпота в брюшной полости визуально не было обнаружено. Решено резецировать ту часть толстого кишечника, где имелась незначительная отечность, что и было выполнено. После наложения анастомоза конец в конец операционная рана ушита послойно, наглухо. После того, как подопытное животное-собака вышла из состояния наркоза, была переведена в виварий.
Макропрепарат отправлен для гистологического исследования. При гистологическом изучении под микроскопом, на слизистой оболочке резецированного участка толстого кишечника явные патологические изменения не были выявлены, определялись лишь незначительные некротические участки слизистой оболочки (рис. 5).
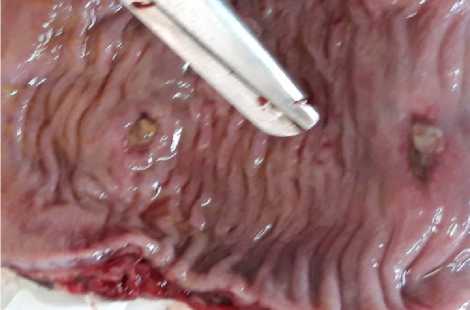
Рис. 5. Визуально определяются некротические участки слизистого слоя толстого кишечника
Fig. 5. Visually determined necrotic areas of the mucous layer large intestine
Так как нас не устраивали полученные результаты моделирования язвенного колита с применением 4 % и 6 % раствора уксусной кислоты, мы решили применить более концентрированный – 7,5 % раствор уксусной кислоты в четвертой серии опытов.
Все процедуры, проводимые во второй и третьей сериях экспериментов точно повторялись и при четвертой серии, но в отличие от предыдущих серий, применяли 7,5 % раствор уксусной кислоты в количестве 1,0 мл с экспозицией 15–20 секунд.
В виварии наблюдали за состоянием подопытного животного в течение 7 дней. Начиная со второго дня наблюдались значительные клинические признаки интоксикации: диарея с примесью слизи и элементами крови, подопытное животное-собака перестала есть.
На 7 день подопытных животных оперировали. Произвели ревизию органов брюшной полости и на проекции толстого кишечника, в полость которого был введен 7,5 % раствор уксусной кислоты, визуально определялись явные признаки воспаления, отечность стенок, гиперемия сосудов. Данный участок толстого кишечника резецировали. При разрезе резецированной части толстого кишечника визуально определялись некротические участки слизистой оболочки (рис. 6).
При гистологическом исследовании под микроскопом, определялись значительные некротические участки слизистой оболочки (рис. 6).
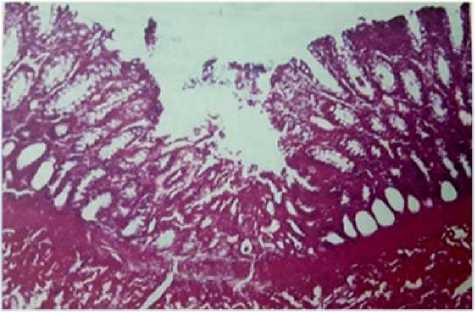
Рис. 6. Острая язва, некротический процесс слизистого слоя толстого кишечника. Окраска гемотоксилином и эозином, ок.10, об. 40
Fig. 6. Acute ulcer, necrotic process of the mucous layer of the thick intestines. Stained with hematoxylin and eosin, eyepiece. 10, v. 40
Макропрепарат отправлен в патологоанатомическое отделение для гистологического исследования. При гистологическом исследовании под микроскопом определялись значительные некротические участки слизистой оболочки (рис. 7).
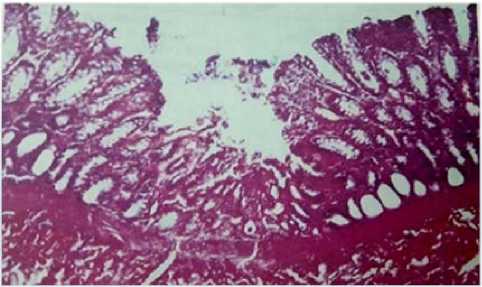
Рис. 7. Острая язва, некротический процесс слизистого слоя толстого кишечника. Окраска гемотоксилином и эозином, ок.10, об. 40
Fig. 7. Acute ulcer, necrotic process of the mucous layer of the thickintestines. Stainedwithhematoxylinandeosin, eyepiece. 10, v. 40
Таким образом, нам удалось создать модель язвенного колита в эксперименте на подопытных животных, давая возможность определить и характеризовать состояние лимфатической системы на фоне модели и при этом оценить эффективность лимфотропной терапии.
Методика определения эффективности лимфотропной терапии при созданной модели язвенного колита. При созданной модели язвенного колита, в четвертой серии опытов, была определена эффективность лимфотропной терапии. Для этого подопытных животных, участвовавших в четвертой серии, разделили на две группы, по 4 в каждой. Первая группа была контрольной, а вторая основной. Сущность методики заключалась в следующем: в брыжейку кишечника контрольной группы подопытных животных, на фоне созданной модели язвенного колита, ввели 0,1 мл 0,1 % раствора синьки Эванса, определяя при этом время ее всасывания по секундомеру.
Подопытным животным, входящим в основную группу, на фоне созданной модели язвенного колита, для стимуляции лимфатической системы в брыжейку кишки ввели смесь: 0,9 % изотонический раствор натрия хлорида в количестве 1,0 мл и гепарин в дозе 2000 ЕД. Через 10–15 минут после введения смеси повторно в брыжейку кишечника ввели 0,1 мл 0,1% раствора синьки Эванса, определяя при этом время ее всасывания по секундомеру.
Результаты
Изученные нами в эксперименте состояние лимфооттока в брыжейках кишечника в норме и при созданной модели язвенного колита были следующими (табл. 2 и 3).
Таблица 2
Время всасывания синьки Эванса из брыжейки кишечника в норме
Table 2
Absorption time of Evans blue from the intestinal mesentery is normal
|
Точки введения синька Эванса и время ее всасывания Points of injection of Evans blue and the time of its absorption |
|||
|
Корень брыжейки Closer to the root of the mesentery |
Срединная часть брыжейки |
Краевая часть брыжейки кишечника |
Стенка кишечника – субсерозная часть |
|
3 мин.22сек ± 16 sec 3 minutes. 22 sec ± 16 sec |
3 мин. 52сек. ± 9 sec 3 minutes. 52 sec ± 9 sec |
4 мин.15сек. ± 10 sec 4 minutes. 15 sec ± 10 sec |
4 мин. 22сек. ± 10 sec 4 minutes. 22 sec ± 10 sec |
Таблица 3
Время всасывания синьки Эванса из брыжейки и субсерозного слоя стенки толстого кишечника на фоне созданной модели язвенного колита
Table 3
Time of absorption of Evans’ blue from the mesentery and subserous layer of the colon wall against the background of the created model of ulcerative colitis
|
Точки введения синька Эванса и время ее всасывания Points of injection of Evans blue and the time of its absorption |
|||
|
Корень брыжейки Closer to the root of the mesentery |
Срединная часть брыжейки The middle part of the mesentery |
Краевая часть брыжейки кишечника The middle part of the mesentery |
Стенка кишечника – субсерозная часть The marginal part of the mesentery (closer to the intestinal wall) |
|
6 мин.39 сек. ± 10 sec 6 minutes. 39 sec ± 10 sec |
7 мин. 21сек. ± 10 sec 7 minutes. 21 sec ± 10 sec |
8 мин.35 сек. ± 10 sec 8 minutes. 35 sec ± 10 sec |
8 мин. 57сек. ± 10 sec 8 minutes. 57 sec ± 10 sec |
По полученным результатам видно, что при созданной модели язвенного колита у подопытных животных наблюдается резкое замедление скорости лимфооттока в брыжейке кишечника в два и более раз по сравнению с нормальной.
Проведенные эксперименты убедительно доказывают позитивные стороны применения лимфотропной терапии в послеоперационном периоде. Этому послужили результаты всасывания синьки Эванса из брыжейки кишечника в норме и на созданной модели язвенного колита после лимфостимуляции (табл. 4).
Из таблицы видно, что после лимфостимуляции лимфоотток в брыжейках кишечника улучшается, устраняя при этом лим-фостаз в «лимфатическом коллекторе», который развивается на фоне воспалительного процесса.
Таким образом, для создания экспериментальной модели язвенного колита у собак оптимальной дозой уксусной кислоты определено 7,5 % раствора. После моделирования язвенного колита региональной лимфоотток достоверно замедляется, что является показанием к проведению местной лимфостимуляции через брыжейки кишечника в послеоперационном периоде. При язвенном колите применяемая лимфотропная терапия в комплексе лечения больных в послеоперационном периоде на фоне лимфостимуляции сугубо положительно влияет на течение воспалительного процесса и восстановительную функцию организма, предотвращая при этом осложнение со стороны основного заболевания.
Таблица 4
Время всасывания синьки Эванса из брыжейки и субсерозного слоя стенки толстого кишечника на фоне созданной модели язвенного колита
Table 4
Time of absorption of Evans’ blue from the mesentery and subzero us layer of the colon wall against the background of the created model of ulcerative colitis
Результаты всасывания синьки Эванса на фоне созданной модели язвенного колита
Evans blue suction results against the background of the created model of ulcerative colitis
|
Точки введения синьки Эванса и время его всасывания Evans Blue Injection Points and its absorption time |
Ближе к корню брыжейки Closer to the root of the mesentery |
Время всасывания без лимфостимуляции Absorption time without lymphatic stimulation |
Время всасывания после лимфостимуляции Absorption time after lymphostimulation |
Ускорение всасывания в % Acceleration of absorption in % |
|
6 мин.39 сек ±10 сек. 6 minutes. 39 sec ± 10 sec |
4 мин.02 сек ±10 сек. 6 minutes. 02sec ± 10 sec |
36,2±1,4 |
||
|
Срединная часть брыжейки The middle part of the mesentery |
7 мин. 21сек. ±21сек. 7 minutes 21 sec ± 21 sec. |
4 мин. 32 сек. ±7 сек. 4 minutes 32 sec. ± 7sec. |
40,1±2,8 |
|
|
Краевая часть брыжейки (ближе к стенке кишечника) The marginal part of the mesentery (closer to the intestinal wall) |
8 мин.35 сек. ±13 сек. 8 minutes 35sec. ± 13sec. |
5 мин.02 сек. ±14 сек. 5 minutes 02 sec. ± 14sec. |
39,9±1,3 |
Список литературы Изучение особенности лимфотропной терапии на фоне экспериментально созданной модели язвенного колита
- Алексеева О.А., Ивашкин В.Т., Шелыгин Ю.А. и др. Проект клинических рекомендаций по диагностике и лечению язвенного колита. Колопроктология, 2019. Т. 18. № 4. С. 7-36.
- Борота А.А. Основные проблемы и перспективы хирургического лечения язвенного колита. Колопроктология, 2018. № 4 (66). С. 74-78.
- Брехов Е.И., Ягудаев Д.М., Саидов А.С. Лимфотропная терапия. Возможности и перспективы в клинической практике. Хирургическая практика, 2014. № 1. С. 20-25.
- Ватутин Н.Т., Шевелёк А.Н., Карапыш В.А., Василенко И.В. Неспецифический язвенный колит. Архивъ внутренней медицины, 2015. № 4(24). С. 62-65.
- Воробьев Г.И. Хирургическое лечение осложнений неспецифического язвенного колита. Российский журнал гастроэнтерологии, гепатологии, колопроктологии, 2003. Т. 13, № 1. С. 73-80.
- Вторенко В.И., Есипов А.В., Мусаилов В.А., Шишло В.К. Лимфатическая терапия в хирургической практике. Хирургическая практика, 2014. № 3. С. 29-34.
- Главнов П.В., Лебедева Н.Н, Кащенко В.А. Язвенный колит и болезнь Крона. Современное состояние проблемы этиологии, ранней диагностики и лечения (обзор литературы). Вестник СПбГУ, 2015. Сер. 11. Вып. 4. С. 49-54.
- Жуков Б.Н., Исаев В.Р., Андреев П.С., Каторкин С.Е., Чернов А.А. Комплексное лечение неспецифического язвенного колита с применением эндолимфатической терапии. Новости хирургии, 2013. Том 20. № 2. С. 49-54.
- Миннебаев М.М. Физиология и патофизиология лимфатической системы. Казанский медицинский журнал, 2015. Т. 96. № 1. С. 118-123.
- Осиков М.В., Симонян Е.В., Бакеева А.Е., Костина А.А. Экспериментальное моделирование болезни крона и язвенного колита. Современные проблемы науки и образования, 2016. № 4.
- Эгамов Ю.С., Рузиев А.Э. Значение эндомезентериальной лимфатической терапии в комплексном лечении неспецифического язвенного колита в послеоперационном периоде. Проблемы биологии и медицины, 2019. № 3 (111). С. 163-167.
- Эгамов Ю.С., Рузиев А.Э., Хайдаров С.А. Эндомезентериальная лимфотропная терапия как метод, предупреждающий осложнений в комплексном лечении неспецифического язвенного колита в послеоперационном периоде. Новый день в медицине, 2019. № 3. С. 299-303.
- Dignass A.U., Eliakim R., Magro F., Maaser C., Chowers Y., Geboes K., Mantzaris G., Reinisch W., Colombel Jean-Frederic, Vermeire S., Travis S., et al.Second European evidence-based consensus on the diagnosis and management of ulcerative colitis Part 1-3. Definitions and diagnosis Journal of Crohn’s and Colitis, 2012, № 6, рр. 965-990.
- Kiesler P., Fuss I.J., Strober W. Experimental Models of Inflammatory Bowel Diseases. Cell MolGastroenterolHepatol., 2015, № 1(2), рр. 154-170.


