Изучение влияния биостимуляторов на активность бактериальных и грибных гидролаз
Автор: Евдокимова К.В., Слащинина Я.А., Тумайкин Г.Г., Толкачева А.А., Черенков Д.А.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Биотехнология и бионанотехнология
Статья в выпуске: 4 (74), 2017 года.
Бесплатный доступ
Одним из перспективных направлений биотехнологии является биоконверсия растительного сырья, примером которой является твердофазное культивирование: выращивание микроорганизмов и высших грибов на растительном сырье с целью получения биологически активных веществ, в частности, целлюлаз. На данный момент существуют данные об исследованиях, посвященных методам усиления целлюлазной активности микроорганизмов путем модификации питательных сред: добавления витаминов, минеральных веществ, биорегуляторов. В представленной работе использовались штаммы микроорганизмов родов Bacillus, Alternaria, Trichoderma, способные к биодеградации целлюлозы, которые были получены из Всероссийской коллекции микроорганизмов. Данные культуры планируется использовать в качестве деструкторов клетчатки в подсолнечном шроте. В качестве усилителей целлюлолитической активности использовались биорегуляторы эпин (2,4-эпибрассинолид) и гетероауксин (?-индолилуксусная кислота). Для определения целлюлолитической активности были применены луночный метод на среде Гетчинсона с добавлением 10 г/л карбометилцеллюлозы, а также способность красителя конго-красный образовывать комплекс с целлюлозой. Оценкой наличия целлюлозолитической активности служил диаметр зоны просветления вокруг лунок. Выявлено, что биорегулятор эпин в разведении 10-1 проявил наибольшее усиление целлюлозолитической активности. Далее была проведена твердофазная ферментация на среде на основе подсолнечного шрота. Проанализировав полученные в ходе экспериментов данные, можно сделать вывод о положительном влиянии биостимуляторов эпин и гетероауксин на целлюлолитическую активность Alternaria alternate, Trichoderma reesei, Bacillus subtilis, при этом максимальное воздействие оказывал эпин.
Целлюлаза, целлюлолитическая активность, биостимулятор, эпин, гетероауксин
Короткий адрес: https://sciup.org/140229905
IDR: 140229905 | DOI: 10.20914/2310-1202-2017-4-204-209
Study of the influence of biostimulants on the activity of bacterial and fungal hydrolases
One of the promising areas of biotechnology is the bioconversion of plant raw materials, an example of which is solid-phase cultivation: the cultivation of microorganisms and higher fungi on plant raw materials in order to obtain biologically active substances, for example, cellulases. At the moment, there are data on studies on methods of enhancing the cellulase activity of microorganisms by modifying nutrient media: the addition of vitamins, minerals, bioregulators. In this work, strains of microorganisms of the genera Bacillus, Alternaria, Trichoderma were used. These microorganisms are capable of biodegradation of cellulose and were obtained from the All-Russian Collection of Microorganisms. These cultures of microorganisms are planned to be used as destructors of cellulose in sunflower meal. Appinee (2,4-epibrassinolide) and heteroauxin (?-indolylacetic acid) bioregulators were used as amplifiers of cellulolytic activity. To determine the cellulolytic activity, the Hutchinson medium method with the addition of 10 g / l of carbomethylcellulose was used, and the ability of the Congo-red dye to form a complex with cellulose. The diameter of the bleaching zone around the wells served as an estimate of the presence of cellulolytic activity. It was found that the appine bioregulator in the dilution 10-1 showed the greatest increase in cellulolytic activity. Further solid-phase fermentation was carried out on a medium based on sunflower meal. After analyzing the data obtained during the experiments, it can be concluded that the stimulant appine and heteroauxin have a positive effect on the cellulolytic activity of Alternaria alternate, Trichoderma reesei, Bacillus subtilis, with the maximum effect being on appine
Текст научной статьи Изучение влияния биостимуляторов на активность бактериальных и грибных гидролаз
Начало XXI века можно без преувеличения назвать эпохой биотехнологий, которые всё шире применяются в различных отраслях промышленности и науки.
Одним из основных направлений биотехнологии является применение ферментов (энзимов), которые являются белками-катализаторами, избирательно воздействующие и вызывающие многократное ускорение химических реакций.
В настоящее время ферменты применяют в составе синтетических моющих средств (для удаления загрязнений белковой, жировой природы, а также растительного происхождения); в производстве целлюлозно-бумажной продукции (отбеливание целлюлозы без применения хлора, вторичная утилизация целлюлозы); в пищевой промышленности (изготовление сыров и молока, не содержащего лактозу, мягчение мясного сырья, производство модифицированных жиров и масел); в производстве фармацевтических препаратов, комбикормов, текстиля.
Одним из перспективных направлений биотехнологии является биоконверсия растительного сырья. Популярность этого направления обусловлена прогрессирующим дефицитом невозобновляемых источников энергий и материалов.
Биоконверсия – это процесс переработки микроорганизмами сырья растительного происхождения, происходящий в аэробных или анаэробных условиях. Целлюлазы, как и многие другие биологически активные вещества, получают путем выращивания микроорганизмов и высших грибов на растительном сырье. Такой процесс является примером прямой биоконверсии растительного сырья – твердофазного культивирования.
Целлюлазами называют комплекс целлюлолитических ферментов, под действием которых происходит деструкция целлюлозы и ее производных до глюкозы и олигосахаридов. Во многих производствах, сырьем для которых служат отходы переработки растений, успешно применяют целлюлолитические ферменты. В таблице 1 приведены основные сферы применения целлюлаз.
Таблица 1.
Основные сферы применения целлюлаз
Table 1.
The main spheres of cellulase application
|
Область применения | Application area |
Способ применения | Wау of application |
|
Пищевая промышленность Food industry |
Экстракция и осветление соков, нектаров. Получение каротина и пищевых красителей. Размягчение сырья для виноделия. Добавка для омолаживания ячменя при пивоварении | Extraction and clarification of juices, nectars. Preparation of carotene and food colorings. Softening of raw materials for winemaking. Additive for barley rejuvenation during brewing |
|
Производство детергентов | Manufacture of detergents |
Энзимная добавка в синтетические моющие средства | Enzyme additive in synthetic detergents |
|
Текстильная промышленность | Textile industry |
Придание мягкости хлопчатобумажным тканям | Softening of cotton fabrics |
|
Целлюлозно-бумажная промышленность | Pulp and paper industry |
Размягчение целлюлозного сырья, отбеливание. Утилизация отходов | Softening of cellulose raw materials, bleaching. Recycling |
|
Сельское хозяйство | Agriculture |
Добавка к кормам, повышающая питательную ценность. Заготовка фуража | Additive to feed, increasing nutritional value. Procurement of forage |
Целлюлазы синтезируются исключительно микроорганизмами (бактериями, микроскопическими грибами и актиномицетами). Такие микроорганизмы, в большинстве своем, из всех компонентов питательных сред в качестве источника энергии используют только целлюлозу. В промышленности используется сравнительно небольшое количество видов микроорганизмов, в основном это штаммы грибов родов Trichoderma, Aspergillus, Phanerochaete .
Проведенный анализ литературных данных показал, что ранее были проведены исследования, посвященные методам усиления целлюлазной активности микроорганизмов путем модификации питательных сред: добавления витаминов, минеральных веществ, биорегуляторов. Также есть данные о повышении целлюлолитической активности базидиомицетов Lentinus edodes. (Berk. Sing.) под действием 2,4-эпибрассино-лид. В связи с эти целесообразными являются исследованию стимулирующего действия эпина на целлюлолитическую активность микроскопических грибов и бактерий.
Нами было изучено влияние регуляторов роста на целлюлолитическую активность грибов и бактерий, в зависимости от концентрации и времени воздействия вещества.
Вещества данного класса используют для предотвращения полегания культур, повышения урожайности и качества выращиваемой продукции, ускорения созревания и лучшей завязываемости плодов.
Материалы и методы исследования
В работе использовались штаммы микроорганизмов родов Bacillus, Alternaria, Tricho-derma , способные к биодеградации целлюлозы, которые были получены из Всероссийской коллекции микроорганизмов.
В качестве усилителей целлюлолитической активности использовались биорегуляторы эпин (2,4-эпибрассинолид) и гетероауксин (β-индоли-луксусная кислота) в различных концентрациях. Основным действующим веществом в эпине является 2,4-эпибрассинолид – стрессовый адаптоген растений. Эпин является полностью синтетическим, но безопасным для растений. Действующее вещество гетероауксина – β-индолилуксусная кислота – образуется в растениях и влияет на их ростовые процессы.
Культивирование микроорганизмов проводили в колбах Эрленмейера объемом 250 мл на жидкой питательной среде на основе подсолнечного шрота, в качестве источника азота добавляли мочевину. Колбы со средой автоклавировали при температуре 121 °С на протяжении 20 мин, перед засевом охлаждали до комнатной температуры.
Для эксперимента применяли растворы эпина и гетероауксина в следующих разведениях: 10-1, 10-6, 10-7. Каждый регулятор в каждом разведении добавляли в отдельную колбу со средой на основе шрота в количестве 1 мл.
Каждый штамм микроорганизмов выращивали на питательной среде на основе подсолнечного шрота с добавлением вышеуказанных биорегуляторов.
Для определения целлюлолитической активности были применены луночный метод на среде Гетчинсона с добавлением 10 г./л карбометилцеллюлозы (КМЦ), а также способность красителя конго-красный образовывать комплекс с целлюлозой.
Для бактерий рода Bacillus было произведено 3 параллельных эксперимента с различным временем культивирования на чашке Петри: 24, 48, 72 ч. В лунки вносили по 100 мкл суточного инокулята, инкубировали при 37 °С. После чего окрашивали среду 1% конго-красным, выдерживали 15 минут и смывали 1 М раствором NaCl. Оценкой наличия целлюлозолитической активности служил диаметр зоны просветления вокруг лунок.
Аналогичный эксперимент проводился для грибов родов Alternaria и Trichoderma с измененным диапазоном времени культивирования – от 24 до 168 ч.
Для проведения твердофазной ферментации (ТФФ) в колбы объемом 250 мл помещали по 25 г. подсолнечного шрота, доводили до влажности 40% дистиллированной водой, в качестве источника азота добавляли мочевину, закрывали фольгой и автоклавировали при температуре 121 °C на протяжении 20 мин.
Перед ТФФ микроорганизмы культивировали на жидкой питательной среде на основе подсолнечного шрота с добавлением эпина, разведение 10-1. Бактерии рода Bacillus культивировали в течение 24 ч, при 37 °C, грибы родов Alternaria и Trichoderma – в течение 72 ч при температуре 30 °C. В каждую колбу добавляли по 1 мл полученного инокулята. После ферментации в образцах подсолнечного шрота определяли массовую долю сырой клетчатки (СК)
Результаты исследования и их обсуждение
Важным фактором, определяющим целлюлолитическую активность, является концентрация вносимого биорегулятора и время последующего культивирования. Результаты экспериментов с наилучшими показателями целлюлолитической активности – наибольшими диаметрами зон лизиса – представлены в таблице 2.
Наглядно данные таблицы, отражающие зависимость целлюлолитической активности от концентрации эпина, представлены на рисунках 1 –3.
Таблица 2.
Максимальная целлюлолитическая активность исследуемых штаммов, выявленная в эксперименте
Table 2.
The maximum cellulolytic activity of the strains studied, revealed in the experiment
|
Микроогранизм Microorganism |
Диаметр зон лизиса, мм | The diameter of the lysis zones, mm |
||
|
Эпин | Appin |
Гетероауксин Heteroauxin |
Без стимулятора | Without stimulant |
|
|
р. Bacillus |
35 (48 ч.) |
22,25 (48 ч.) |
12,25 |
|
p. Alternaria |
38,75 (168 ч.) |
32,25 (144 ч.) |
29 |
|
p. Trichoderma |
40 (168 ч.) |
38 (120 ч.) |
30,25 |
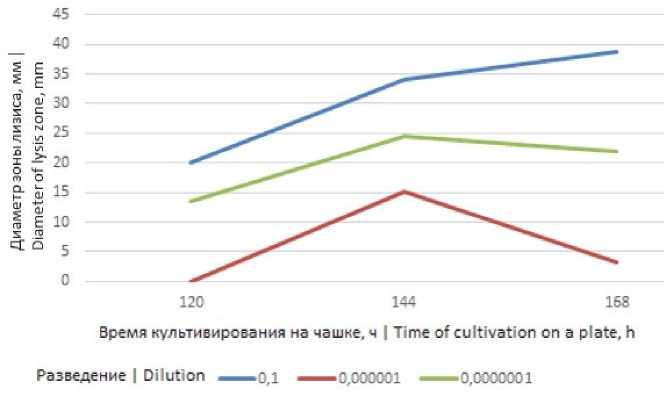
Рисунок 1. Зависимость диаметра зон лизиса грибов рода Alternaria от концентрации эпина в питательной среде
Figure 1. Dependence of the lysis zones diameter of Alternaria on the concentration of appine in a culture medium
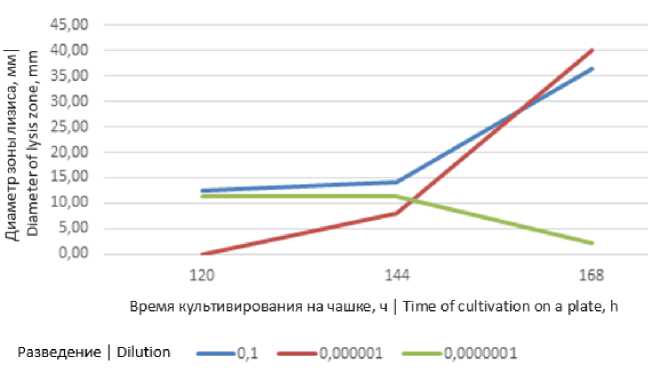
Рисунок 2. Зависимость диаметра зон лизиса грибов рода Trichoderma от концентрации эпина в питательной среде
Figure 2. Dependence of the lysis zones diameter of Trichoderma on the concentration of appine in a culture medium
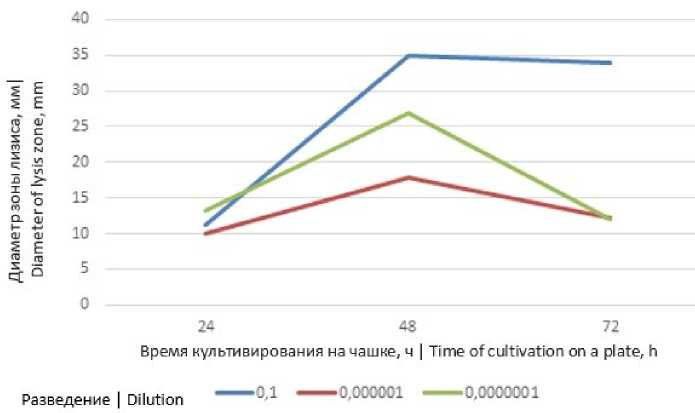
Рисунок 3. Зависимость диаметра зон лизиса бактерий рода Bacillus от концентрации эпина в питательной среде
Figure 3. Dependence of the lysis zones diameter of Bacillus on the concentration of appine in a culture medium
Из выше представленных рисунков видно, что биорегулятор эпин в разведении 10-1 проявил наибольшее усиление целлюлозолитической активности для бактерий рода Bacillus и грибов родов Alternaria и Trichoderma .
Далее была проведена твердофазная ферментация по схемам, продемонстрировавшим наибольшее усиление целлюлазной активности – максимальный диаметр зоны лизиса. Результаты представлены в таблице 3.
Таблица 3.
Содержание сырой клетчатки при твердофазном культивировании с добавлением эпина
Table 3.
The content of crude fiber in solid-phase cultivation with the addition of appine
|
Микроогранизм | Microorganism |
Содержание сырой клетчатки в подсолнечном шроте после ферментации | The content of raw fiber in sunflower meal after fermentation |
Содержание сырой клетчатки в исходном подсолнечном шроте | The content of raw fiber in the initial sunflower meal |
|
|
Эпин, разведение 10-1 | Appine, dilution 10-1 |
Контроль | Control |
||
|
Alternaria alternata |
12,5 |
13,26 |
14,07 |
|
Trichoderma reesei |
12,1 |
13,76 |
|
|
Bacillus subtilis |
13,4 |
11,37 |
|
Заключение
Проанализировав полученные в ходе экспериментов данные можно сделать вывод о положительном влиянии биостимуляторов
Список литературы Изучение влияния биостимуляторов на активность бактериальных и грибных гидролаз
- Компанцев Д.В. и др. Методические рекомендации по освоению дисциплины «Биотехнология (в том числе бионанотехнологии)». Пятигорск: ПМФИ, 2015. С. 72.
- Шевердин А.В. Создание и использование биотехнологий: история вопроса//Журнал российского права. 2012. С. 118-126.
- Описание основных технологий производства целлюлазы. URL: http://abercade.ru.
- ГОСТ 13496.2-91 Корма, комбикорма, комбикормовое сырье. Метод определения сырой клетчатки. М.: ИПК Издательство стандартов, 2002.
- Толкачева А.А., Черенков Д.А., Корнеева О.С. Скрининг продуцентов ферментов гидролаз в базе данных Национального центра биотехнологической информации (NCBI)//Актуальная биотехнология. 2015. № 3 (14). С. 63.
- Толкачева А.А., Черенков Д.А., Корнеева О.С. Получение рекомбинантных ферментов: протеазы и липазы для использования в качестве компонентов кормовых добавок//Биотехнология: состояние и перспективы развития. Материалы IX международного конгресса. 2017. С. 81-82.
- Звягинцев Д.Г. Методы почвенной микробиологии и биохимии. М.: Изд-во МГУ, 1991. 304 с.
- Аникеев В.В., Лукомская К.А. Руководство к практическим занятиям по микробиологии. М.: Просвещение, 1983. 127 с.
- Ngangi J., Pelealu J., Warouw J., Mandey L. Isolation and activity of cellulolytic bacteria isolated from hindgun of Odontotermes spa subteran termite on Wasian (Elmerrelia celebica L.) an Endemic Wood to North Sulawesi//International Journal of Science and Engineering Investigations. 2013. V. 2. № 22. P. 8-16.
- Алимова Ф.К., Тухбатова Р.И., Тазетдинова Д.И. Методы определения гидролаз почв и почвенных микроорганизмов. Казань: Казанский университет, 2010. 67 с.
- Усачева Р.В. Физиолого-биохимические особенности некоторых штаммов культивируемого гриба Lentinus edodes. (Berk. Sing.). Воронеж: ВГАУ, 2003. 128 с.


