Изучение возможности комплексного использования растения каланхоэ перистое
Автор: Маринина Тамара Филипповна, Савченко Людмила Николаевна, Саушкина Анна Степановна
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Биологические ресурсы: флора
Статья в выпуске: 5-1 т.17, 2015 года.
Бесплатный доступ
В работе приводятся результаты разработки стоматологической мази-пасты на основе сока каланхоэ. Для достижения выраженного анестезирующего, антимикробного, противовоспалительного действия в мазь введены тримекаин и фурацилин. Фармакогностическое исследование шрота каланхоэ позволило установить анатомо-морфологические признаки порошка шрота каланхоэ, определить наличие флавоноидов, полисахаридов, пектинов. На основе шрота каланхоэ разработана технология стоматологической гранулированной лекарственной формы. Установлена антимикробная и сорбционная активность гранул.
Сок и шрот каланхоэ, флавоноиды, полисахариды, пектины, стоматологическая мазь-паста, гранулы
Короткий адрес: https://sciup.org/148204002
IDR: 148204002 | УДК: 661.122:[615.322:582.374]:616.31
Studying the possibility of the plant Kalanchoe the plumose complex use
In work results of working out of stomatologic ointment-paste on the basis of juice Kalanchoe are resulted. For achievement of the expressed anaesthetising, antimicrobic, anti-inflammatory action into ointment are entered trimekain and furatsilin. Pharmacognostic research meal of kalanchoe has allowed to establish anatomo-morphological signs of a powder meal of kalanchoe, to define presence flavonoids, polysaccharides, pectins. On a basis meal of kalanchoe the technology of the stomatologic granulated medicinal form is developed. It is established antimicrobic and sorption activity of granules.
Текст научной статьи Изучение возможности комплексного использования растения каланхоэ перистое
Савченко Людмила Николаевна, кандидат фармацевтических наук, доцент кафедры технологии лекарств Саушкина Анна Степановна, кандидат фармацевтических наук, старший преподаватель кафедры военно-медицинского снабжения и фармации стимулирует их заживление (афтозные стоматиты, гингивиты, осложнённый пародонтоз и др.). Сок каланхоэ перистого обладает антибактериальной активностью в отношении широкого спектра грамположительных и грамотрицательных микроорганизмов [4]. После изготовления сока каланхоэ остаётся шрот, который не используется. В доступной литературе сведений о химическом составе шрота каланхоэ нами не найдено.
Цель исследований: разработать пролонгированную стоматологическую лекарственную мазь-пасту на основе сока каланхоэ, провести фармакогностическое исследование шрота каланхоэ и разработать стоматологическую гранулированную лекарственную форму (СГЛФ) на основе шрота каланхоэ.
На первом этапе исследований был получен сок каланхоэ по общепринятой методике. Получали из свежесобранного сырья – листья и побеги культивируемого растения каланхоэ перистого. Полученный сок отстаивали в течение суток при температуре 4°С, затем подвергали фильтрации, консервировали. Стандартизацию сока осуществляли согласно ВФС 42-1714-87. Полученный сок каланхоэ соответствовал требованиям ВФС. Содержание суммы кислот в пересчете на яблочную кислоту составляет 2,81%, рН сока каланхоэ 4,6; показатель преломления 1,345, содержание спирта (консерванта) 18,2%.
Следующим этапом исследований являлась разработка стоматологической пролонгированной лекарственной мази-пасты. При проведении лечения стоматологических заболеваний возникает необходимость обезболивания, a для снижения кариесогенной микрофлоры необходим доступный антисептик, например, фурацилин, который наряду с противомикробным действием обладает противо-отечными свойствами и широко применяется в виде аппликаций и лечебных повязок. Для проведения местного аппликационного обезболивания в стоматологии используют новокаин, анестезин, тримекаин, лидокаин, пиромекаин, артикаин. Наше внимание привлек анестетик тримекаин, т.к. он вызывает быстро наступающую, глубокую и продолжительную анестезию, и что весьма важно, вызывает поверхностную анестезию, но в отличие от новокаина, более продолжительную. Широко используется в стоматологической практике в виде растворов, орошений, аппликаций, пленок [3].
Определяющим фактором, который обеспечивает эффективное воздействие БАВ в мазях, является основа. Основообразующий состав мази должен быть многофункциональным: в полной мере высвобождать БАВ, входящие в состав мази, быть индифферентным по отношению к зубной эмали и тканям пародонта, но в то же время обеспечивать определенное терапевтическое воздействие на ткани пародонта, создавать пролонгированное действие. Пролонгированное действие мази-пасты предусматривает нахождение лекарственной формы в полости рта достаточно длительное время, поэтому лекарственные вещества не должны вымываться слюной, а постоянное смачивание должно служить дополнительным ув-лажн-ителем сохранения консистенции мази.
Принимая во внимание вышеизложенное, нами были избраны следующие основообразующие компоненты мази: консистентная эмульсия (вода очищенная + вазелин + эмульгатор Т2), метилцеллюлоза (МЦ), адсорбцинная основа (ланолин безводный + вазелин), композиционная основа (цинка оксид+белая глина+глицерин). С целью выбора оптимальной основы, обеспечивающей необходимую степень высвобождения фурацилина, тримекаина и БАВ из сока калан-хоэ, нами были приготовлены на изучаемых основах модельные образцы мазей, включающих каждый компонент отдельно.
Определение степени и скорости высвобождения фурацилина, тримекаина и органических кислот в пересчёте на яблочную кислоту осуществляли методом диализа через полупроницаемую мембрану. Навеска исследуемого образца мази составляла 1,0, средой для диализа служила вода очищенная 30 мл. Проба для анализа – 5 мл. Диализ проводили в термостате при температуре 37±1°С. Экспозиция 15'; 30'; 45'; 60'; 90' мин. Взятую для анализа пробу 5 мл восполняли 5 мл воды очищенной t=37°C. Количественное определение фурацилина и тримека-ина в диализатах осуществляли спектрофотометрически при длинах волн 230 и 260 нм соответственно [5]. Органические кислоты в диализатах определяли алкалиметрическим методом с предварительным использованием ионо-обменной хроматографии. Полученные данные представлены в табл. 1-3. Данные, представленные в табл. 1-3, сидетельствуют о том, что высвобождение лекар-ственных веществ и БАВ сока каланхоэ из изуча-емых основ находятся в прямой зависимости от природы используемой основы.
Таблица 1. Степень высвобождения фурацилина из различных мазевых основ
|
Вид основы |
Экспозиция, мин / высвобождение, % |
||||
|
15 |
30 |
45 |
60 |
90 |
|
|
композиционная |
- |
4,2 |
4,5 |
5,0 |
8,0 |
|
гель МЦ |
15,0 |
30,0 |
35,0 |
38,0 |
42,0 |
|
эмульсионная |
8,0 |
10,0 |
10,0 |
12,0 |
15,0 |
|
адсорбционная |
4,2 |
5,8 |
6,0 |
6,5 |
7,0 |
Таблица 2. Степень высвобождения тримекаина из изучаемых мазевых основ
|
Вид основы |
Экспозиция, мин / высвобождение, % |
||||
|
15 |
30 |
45 |
60 |
90 |
|
|
композиционная |
- |
5,5 |
6,2 |
8,8 |
11,9 |
|
гель МЦ |
38,4 |
45,6 |
54,2 |
63,0 |
65,0 |
|
эмульсионная |
12,2 |
21,1 |
30,0 |
41,1 |
42,0 |
|
адсорбционная |
10,4 |
12,0 |
12,0 |
13,2 |
14,0 |
Таблица 3. Степень высвобождения БАВ сока каланхоэ из мази в зависимости от вида основы
|
Вид основы |
Экспозиция, мин / высвобождение, % |
|||
|
15 |
30 |
45 |
60 |
|
|
композиционная |
5,9 |
8,1 |
10,1 |
11,8 |
|
гель МЦ |
2,2 |
2,8 |
3,2 |
4,0 |
|
эмульсионная |
1,08 |
2,2 |
2,5 |
3,0 |
|
адсорбционная |
- |
1,2 |
1,52 |
1,7 |
Мы остановили свой выбор на основах: композиционной, адсорбционной и консистентной эмульсии, т.к. гель МЦ высвобождает достаточно полно лекарственные вещества (90 мин), что не позволяет получить пролонгированное действие. Исследования по выбору оптимального носителя лекарственных веществ в мазях были продолжены: изучали антимикробную активность мазей. Были изучены образцы мазей и основы (плацебо). Антимикробную активность изучали методом диффузии в агар способом «колодцев» на восьми тест-культурах. 1. Staphylococcus aureus 209-Р; 2. Staphylococcus aureus; 3. Staphylococcus Type; 4. Staphylococcus epider-midis Wood 46; 5. Escherichia coli 675; 6. Shigella flexneri 266; 7. Bacillus subtilis L – 1; 8. Bacillus anthracoides. Полученные результаты представлены в табл. 4.
Таблица 4. Зоны задержки роста микроорганизмов
|
Исследуемые образцы |
Тест-культуры / зоны угнетения роста микроорганизмов, мм |
|||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
|
адсорбционная основа |
- |
- |
- |
- |
- |
- |
- |
- |
|
мазь на адсорбционной основе |
8 |
11 |
8 |
8 |
10 |
9 |
9 |
9 |
|
композиционная основа - плацебо |
9 |
10 |
10 |
10 |
10 |
9 |
10 |
10 |
|
мазь на композиционной основе |
20 |
22 |
23 |
20 |
18 |
18 |
20 |
35 |
|
эмульсионная основа |
6 |
7 |
6 |
7 |
- |
- |
- |
- |
|
мазь на эмульсионной основе |
15 |
18 |
15 |
14 |
12 |
12 |
15 |
15 |
|
сок каланхоэ + фурацилин + тримекаин |
15 |
15 |
12 |
14 |
12 |
12 |
15 |
20 |
Полученные результаты определения антимикробной активности мазей на различных основах и основ (плацебо) свидетельствуют о том, что наиболее выраженной активностью обладает мазь-паста на композиционной основе. Выраженная антимикробная активность мази-пасты на композиционной основе на 4 вида тест-культур стафилококков является весьма важным показателем для стоматологических мазей, т.к. до 50% микробной флоры полости рта соответствуют стафилококки. Установлено что основа композиционная (плацебо) обладает антимикробной активностью, что обеспечивает потенцирование антимикробной активности.
На основе проведенных исследований по выбору оптимальной композиции основы нами предлагается состав на 100,0 мази: тримекаина 0,25; фурацилина 0,20; сока каланхоэ 30,0; основы композиционной до 100,0. Композиционная основа включает: цинка оксид и белая глина поровну (по 40,0), глицерин – 20,0. Технология: предварительно измельченный цинка оксид смешивали с глицерином, затем с белой глиной. В подогретом соке каланхоэ растворяли фурацилин и тримекаин. Вводили в основу частями при тщательном дис-пергировании до однородной массы. Далее мазь стандартизировали по следующим показателям: качественное и количественное определение тримекаина [7], фура-цилина, органических кислот в пересчёте на яблочную кислоту. Для количественного определения компонентов мази использовали модифицированный метод Фирордта (тримекаина и фурацилина) [1]. Полученные результаты представлены в табл. 5. Количест-венное определение цинка оксида показано в табл. 6. Таким образом, методом комплексонометрии проведено количественное определение цинка оксида в мази с погрешностью 100,0±0,1%.
Таблица 5. Результаты количественного определения тримекаина и фурацилина в модельной мази на композиционной основе модифицированным методом Фирордта (А ст 230=0,561; А ст 260=0,503).
|
А 230 |
А 260 |
Найдено, % |
Хi – X |
(Хi -Х)2 |
Метрологические характеристики |
|
тримекаин |
|||||
|
0,534 |
0,492 |
103,88 |
3,2 |
10,2400 |
V = 100,68 S = 2,48 Су = 0,79 Δ = 1,79 _ = 1,8 У У ±Δ =100,7 ±1,8 |
|
0,543 |
0,435 |
102.04 |
1,36 |
1,8496 |
|
|
0,555 |
0,503 |
102,29 |
1,61 |
2,5921 |
|
|
0,530 |
0,483 |
99,49 |
-1,19 |
1,4161 |
|
|
0,535 |
0,482 |
96,65 |
-4,03 |
16,2409 |
|
|
0,555 |
0,503 |
109,29 |
1,61 |
2,5921 |
|
|
0,548 |
0,498 |
101,91 |
1,23 |
1,5129 |
|
|
0,543 |
0,495 |
102,04 |
1,36 |
1,8496 |
|
|
0,538 |
0,484 |
96,71 |
-3,97 |
15,7609 |
|
|
0,530 |
0,483 |
99,49 |
-1,19 |
1,4161 |
|
|
фурацилин |
|||||
|
0,534 |
0,492 |
98,73 |
-1,63 |
2.6569 |
у = |
|
0,543 |
0,435 |
100,64 |
0,28 |
0,0767 |
S = 1,78 |
|
0.555 |
0,503 |
103.01 |
2,65 |
7,0225 |
|
|
0,530 |
0,483 |
98,24 |
-2,12 |
4,4944 |
= 0,56 |
|
0,535 |
0,482 |
99,44 |
-0,92 |
0,8464 |
у Δ = 1,27 |
|
0.555 |
0,503 |
103,01 |
1,29 |
1.6641 |
|
|
0,548 |
0,498 |
101,65 |
2.65 |
7.0225 |
= 1,3 |
|
0,543 |
0,495 |
100,64 |
0,28 |
2,0784 |
±Δ = 100,7 ±1,8 |
|
0,538 |
0,484 |
100,03 |
-0,33 |
0,1089 |
|
|
0,530 |
0,483 |
98,24 |
-2,12 |
4,4944 |
|
Таблица 6. Результаты количественного определения цинка оксида в мази на композиционной основе (а=3,5000 г)
|
Объем титранта, мл |
Найдено цинка оксида |
V Хi- |
(Хi – )2 |
Метрологические характеристики |
|
|
Хi: % по прописи |
Хi: % к прописанному количеству |
||||
|
13,80 |
40,11 |
100,28 |
0,25 |
0,0625 |
= 100,03 S = 0,30 ^ V = 0,12 Δ = 0,12 = 0,119 ±Δ = 100,7 ±1,8 |
|
13,80 |
40,11 |
100,28 |
0,25 |
0,0625 |
|
|
13,80 |
40,11 |
100,28 |
0,25 |
0,0625 |
|
|
13,75 |
39,96 |
99,90 |
-0.13 |
0,0169 |
|
|
13,75 |
39,96 |
99,90 |
-0,13 |
0,0169 |
|
|
13,70 |
39,82 |
99,55 |
-0,48 |
0,2304 |
|
Следующим этапом наших исследований являлось фармакогностическое изучение побегов каланхоэ и шрота. Согласно ФС 42-1782-82 сырьё состоит из облиственных побегов, листьев и их частей. В статье отсутствует раздел «измельченное и порошкованное сырьё». По данному разделу отсутствует как характеристика внешних признаков, так и анатомические микроскопические диагностические признаки порошкообразного сырья – шрота. Поэтому мы поставили перед собой задачу – изучить влияние дисперсности на прояв-ляемость характерных анатомических признаков в шроте побегов каланхоэ.
Порошок шрота каланхоэ перистого содержит: фрагменты клеток эпидермиса листа; клетки мезофилла; зерна хлорофилла; фрагменты клеток эпидермиса над жилкой; обрывки проводящих элементов; фрагменты клеток эпидермиса стебля; фрагменты клеток пигментного слоя стебля;
клетки мезофилла стебля с кристаллическими включениями оксалата кальция; фрагменты клеток сердцевины с бурым содержимым; группы сте-реид. С помощью качественных реакций и хроматографии мы обнаружили в шроте побегов каланхоэ наличие флавоноидов (рутина). Для количественного определения суммы флавоноидов нами был выбран спектрофотометрический метод анализа с использованием реакции комплексообра-зования с алюминия хлоридом в среде 95% этанола [6]. Результаты количественного определения сум-мы флавоноидов в пересчёте на рутин в шроте каланхоэ представлены в табл. 7. Определение полисахаридов в шроте побегов каланхоэ проводили по методикам Н.К. Кочеткова, А.Г. Горина. Установлено, что фракция водорастворимых полисахаридов составила 9,4-10,1%, пектиновая – 2,7-3,1%, гемицеллюлоза А – 1,81,9%; гемицеллюлоза Б – 5,1-5,2%.
Таблица 7. Содержание флавоноидов в шроте каланхоэ
|
Масса сырья, г |
А 405 |
Найдено флавоноидов %, (Xj) |
Xi- |
(Xi- )2 |
Метрологические характеристики |
|
1,0322 |
0,305 |
0,422 |
-0,09 |
81∙10-6 |
= 0,43 S2 = 68∙10-6 S = 0,008246 = 0,003688 Δ = 0,01 Δ = 0,43±0,01 = 1,07 |
|
1,0120 |
0,302 |
0,437 |
+0,006 |
36∙10-6 |
|
|
1,01350 |
0,202 |
0,428 |
-0,003 |
9∙10-6 |
|
|
1,0262 |
0,297 |
0,426 |
-0,005 |
25∙10-6 |
|
|
0,9803 |
0,210 |
0,442 |
+0,011 |
121∙10-6 |
|
|
Σ 272∙10-6 |
Важным фармакологическим свойством полисахаридов и пектиносодержащих продуктов является адсорбция и выведение из организма тяжелых металлов. Наличие в шроте каланхоэ полисахаридов послужило основанием для определения их комплексообразующей способности. Комплексообразующая способность полисахаридов шрота составляет 91,01%, что свидетельствует о возможности использования этого показателя с терапевтической направленностью лекарственной формы.
Определение антимикробной активности шрота каланхоэ показало, что он обладает не выраженной активностью на 4 штамма стафилококков, но выраженной активностью на бациллы. Полученные результаты позволили разработать на основе шрота каланхоэ СГЛФ.
Полость рта, как экологическую нишу, можно разделить на несколько более мелких, но достаточно отличных друг от друга биотопов, одним из которых является десневая жидкость и зона десневого желобка. Десневая жидкость представляет собой транссудат, который секретируется в области десневого желобка и практически сразу контаминируется микрофлорой слизистой оболочки десны и ротовой жидкости. В данном биотопе преобладают нитевидные и извилистые облигатно-анаэробные виды бактерий, также встречаются дрожжеподобные грибы и др. Концентрация перечисленных микроорганизмов в десневой жидкости резко увеличивается при формировании десневого кармана при парадонтите [2]. Сведения литературы свидетельствуют о том, что сотрудниками Киевского института усовершенствования врачей предложена СГЛФ «Флавотин», действующими веществами которой являются кверцетин и пектины. Принимая во внимание вышеизложенное, а также сведения литературы о лечении стоматологических заболеваний средствами неспецифического действия, нами был разработан состав и технология гранул для введения их в над- и поддесневые патологические карманы, кариозные полости, в зону десневого желобка или для местного лечения заболеваний полости рта.
Разработку технологии и состава СГЛФ проводили с использованием измельчённого и высушенного шрота каланхоэ, остающегося после получения сока каланхоэ. Измельчённый порошок просеивали через шёлковое сито. В качестве вспомогательных веществ были изучены растворы производных целлюлозы, поливиниловый спирт, т.к. известно, что они снижают угнетающее действие некоторых лекарственных средств на мерцательный эпителий, удлиняют время контакта со слизистой. В качестве гранулирующих жидкос-тей изучали воду очищенную, 4% раствор жела-тина, 40% раствор сорбита и 50% спирт этиловый. С целью усиления антимикробной активности гранул в их состав был введён фурацилин, наибо-лее доступный и обладающий широким диапа-зоном действия антисептик.
Наиболее простым и эффективным является влажное гранулирование, а именно, метод формования (протирания массы через сито), т.к. для данного метода не требуется дорогостоящее оборудование и высокие энергозатраты.
Гранулы получали методом влажного гранулирования путём протирания увлажнённой массы измельчённого шрота, фурацилина и вспомогательных веществ с последующей сушкой и сухим гранулированием. Формование гранул осуществляли протиранием увлажнённой массы через протирочное сито (гранулятор с диаметром отверстий 2,5 мм). Сушку гранул осуществляли при температуре 40°-50°С в сушильном шкафу. После высушивания гранулы вновь протирали через гранулятор с размером отверстий 2,0 мм. Из гранулирующих агентов после проведения эксперимента исключили в качестве вспомогательных веществ метилцеллюлозу, т.к. гранулы долго сохли и легко отсыревали. Использование 50% спирта этилового приводило к тому, что масса слишком быстро высыхала с образованием большого количества частиц менее 0,2 мм. Дальнейшему исследованию были подвергнуты гранулы состава: порошок шрота каланхоэ + №КМЦ + фурацилин + сорбит + вода очищенная.
Стандартизация СГЛФ. В качестве основных показателей для стандартизации предлагаются подлинность, гранулометрический состав, потеря в массе при высушивании, растворение и распа-даемость, количественное содержание действую-щих веществ.
Проведение реакций на подлинность: 0,5 г гранул растворяли при нагревании в 10 мл воды очищенной и фильтровали. К 2,0 мл фильтрата приливали 2,0 мл раствора гидроксида натрия, перемешивали, нагревали. Постепенно появлялось оранжево-красное окрашивание. Растворимость гранул определяли в приборе «вращающаяся корзинка». Фурацилин, высвободившийся из гранул, определяли спектрофотометрически. Через 45 минут растворяется 78% фурацилина, что отвечает требованиям ГФ XI. Полученные результаты говорят о том, что распадаемость гранул составляет 12 минут.
Способ применения СГЛФ: гранулы 8-10 штук с помощью специальной стоматологи-ческой гладилки вносят в пародонтальные карманы или в кариозные полости. Гранулы смачиваются слюной, набухают и адсорбируют экссудат.
Определение дренажной способности СГЛФ: с целью определения сорбционной спо-собности гранул использовали диализтор. Навеску гранул 1,0 помещали на мембрану диализной трубки и опускали трубку в воду так, чтобы она была погружена на 3-4 мм. Через определённые промежутки времени извлекали трубку и взвешивали, предварительно промокнув фильтровальной бумагой остатки воды. Экспозиция 30, 60, 90, 120 минут. Полученные результаты представлены на рис. 1. На рис. 1 чётко прослеживается количественная характеристика сорбции жидкости во времени. Вначале сорбционная способность увеличивается, а к 120 минутам начинает падать. Этот показатель имеет важное значение: предлагаемая СГЛФ способна осуществлять капиллярный дренаж, сорбцию экссудата.
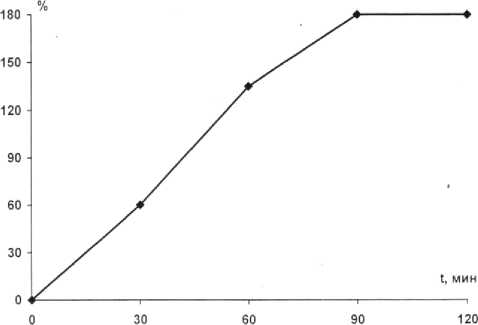
Рис. 1. Зависимость сорбционной способности СГЛФ от времени
Выводы:
-
1. Проведено фармакогностическое исследование шрота после получения сока каланхоэ и установлено наличие в шроте полисахаридов 9,410,1%, пектинов 2,7-3,4%, флавоноидов (в пересчёте на рутин) 0,43±0,01.
-
2. Разработаны состав и технология стоматологической гранулированной лекарственной формы на основе шрота каланхоэ.
-
3. Предлагается пролонгированная лекарственная форма – мазь-паста, включающая в себя сок каланхоэ, фурацилин и тримекаин.
Список литературы Изучение возможности комплексного использования растения каланхоэ перистое
- Батлюк, Г.Я. Разработка физико-химических методов контроля сульфаниламидных препаратов и их многокомпонентных лекарственных форм. -Дисс… канд.фарм.наук. -Пятигорск, 1994. 170 с.
- Боровский, Е.В. Биология полости рта/Е.В. Боровский, В.К. Леонтьев. -М.: Медицина, Н.Новгород: НГМА, 2001. 301 с.
- Вебер, В.Р. Клиническая фармакология для стоматологов/В.Р. Вебер, Б.Т. Мороз. -СПб.: Изд-во «Человек», 2003, 352 с.
- Волжанова, М.И. Каланхоэ перистое и Деграмона: химический состав, применение в медицине (обзор)/М.И. Волжанова, Р.А. Байльман, В.А.Быков//Вопросы биологической, медицинской и фармацевтической химии. 2010. №7. С. 14-20.
- Манджиголадзе, Т.Ю. Использование метода ВЭЖХ для установки качества мази с густым экстрактом солодкового корня и хлоргексидина биглюконата/Т.Ю. Манджиголадзе, Т Ю. Арчинова, В.И.Погорелов//Вопросы биологической медицинской и фармацевтической химии. 2013. №2. С. 31-34.
- Темирбулатова, А.М. Фитохимическое исследование и разработка технологии жидкого экстракта из листьев лимонника китайского/А.М. Темирбулатова, Э.Ф. Степанова, В.А. Садоян и др.//Научные ведомости Белгородского государственного университета. Серия: Медицина. Фармация. 2010. Т16, №12-2. С. 141-144.
- ФС42-2390-92. Тримекаин. 5 с.


