Являются ли однопортовые эндоскопические технологии реальной альтернативой «традиционным» лапароскопическим вмешательствам?
Автор: Восканян С. Э., Лащик М. Г., Найденов Е. В., Бажанова Ю. А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Абдоминальная хирургия
Статья в выпуске: 3 (73), 2020 года.
Бесплатный доступ
Введение. Лапароскопическая холецистэктомия является «золотым стандартом» лечения пациентов с доброкачественной патологией желчного пузыря. В последние годы отмечена динамика к уменьшению количества разрезов для оперативного вмешательства до однопортовых технологий. Материалы и методы. Было проведено сравнение результатов выполнения однопортовой лапроскопической холецистэктомии у 300 пациентов по сравнению со стандартной лапароскопической холецистэктомией у 1150 пациентов. Результаты. Длительность операции при ЛХЭ составила 40 (35-60) минут, длительность операции при SILS составила 55 (45-65) минут. Необходимость конверсии однопрокольной технологии в «традиционное» 4-прокольное лапароскопическое вмешательство отмечены у 2,3% пациентов, в «традиционную» холецистэктомию - у 0,3%, после ЛХЭ у 0,7% пациентов выполнена конверсия лапароскопического доступа в лапаротомию. Общая частота послеоперационных осложнений после ЛХЭ составила 0,8%, после SILS - 1%. Госпитальная летальность после ЛХЭ составила 0,17% (в результате массивной тромбоэмболии легочной артерии). После SILS госпитальной летальности не было. Болевой синдром после ЛХЭ составлял 6 (4-7) баллов, после SILS - 4 (3-5) баллов (p function show_abstract() { $('#abstract1').hide(); $('#abstract2').show(); $('#abstract_expand').hide(); }
Желчнокаменная болезнь, холецистит, лапароскопическая холецистэктомия, однопортовая лапароскопическая холецистэктомия
Короткий адрес: https://sciup.org/142226437
IDR: 142226437 | УДК: 616.366-089.87 | DOI: 10.17238/issn2072-3180.2020.3.12-16
Are single-port endoscopic technologies a real alternative to «traditional» laparoscopic procedures?
Introduction. Laparoscopic cholecystectomy is the «gold standard» of the treatment for patients with benign gallbladder diseases. In recent years, there has been a trend towards a decrease in the number of incisions for surgical intervention to single-port technologies. Material and methods. In our study the results of single-port laparoscopic cholecystectomy at 300 patients were compared with standard laparoscopic cholecystectomy at 1150 patients. Results. The duration of the laparoscopic cholecystectomy was 40 (35-60) minutes, the duration of the SILS was 55 (45-65) minutes. The conversion of SILS for «traditional» 4-puncture laparoscopic intervention was noted in 2.3% of patients, for open cholecystectomy in 0.3%, after LCE conversion of laparoscopic access to laparotomy was performed in 0.7% patients. Morbidity after laparoscopic cholecystectomy was 0.8%. Morbidity after SILS was 1%. Mortality after laparoscopic cholecystectomy was 0.17% (as a result of massive pulmonary embolism). Mortality after SILS was not. Pain syndrome after laparoscopic cholecystectomy was 6 (4-7) points, after SILS - 4 (3-5) points (p function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Являются ли однопортовые эндоскопические технологии реальной альтернативой «традиционным» лапароскопическим вмешательствам?
Конкременты в желчном пузыре выявляют примерно у 10% взрослого населения, чаще у женщин в возрасте старше 40 лет, при этом число осложненных форм калькулезного холецистита остается стабильно высоким [1].
В настоящее время лапароскопическая холецистэктомия (ЛХЭ) является «золотым стандартом» лечения пациентов с доброкачественной патологией желчного пузыря [2, 3], ведущее место в структуре которой занимает желчнокаменная болезнь (ЖКБ). При этом основным вопросом при выборе доступа для ЛХЭ является адекватная визуализация, однако возрастают требования к косметическому результату у определенной группы пациентов [2, 3, 4]. Эволюция операционного доступа от лапаротомии к 4-х портовой ЛХЭ логически продолжилась уменьшением количества вводимых троакаров до единого доступа [4].
На сегодняшний день четко обозначено три вектора развития лапароскопических технологий:
-
1) уменьшение диаметра троакаров и манипуляторов (минилапароскопия);
-
2) уменьшение количества разрезов, через которые осуществляется оперативное вмешательство (Single Incision Laparoscopic Surgery — SILS);
-
3) использование естественных доступов для осуществления технологии (Natural Orifice Transluminal Endoscopic Surgery — NOTES) [5, 6].
Цель исследования. Изучить результаты выполнения однопортовых эндоскопических технологий при лапароскопической холецистэктомии и оценить их преимущества по сравнению со стандартной лапароскопической холецистэктомией.
Материал и методы
В Центре хирургии и трансплантологии ФГБУ ГНЦ ФМБЦ им. А.И. Бурназяна ФМБА России однопортовые лапароскопические холецистэктомии выполняются с января 2012 [7]. За этот период по август 2020 было пролечено 300 пациентов, из них по поводу острых и подострых форм калькулезного холецистита 18 (6%) пациентов, хронических — 257 (85,7%); по поводу полиповидных образований желчного пузыря 25 (8,3%) пациентов (Таблица 1).
В 3 наблюдениях вмешательство носило симультанный характер — 1 пациентке по поводу сопутствующего хронического аппендицита выполнена аппендэктомия и 2 пациенткам по поводу гидросальпинкса произведена тубэктомия из имеющегося трансумбиликального доступа.
Женщины составили 262 наблюдения (87,3%), мужчины — 38 (12,7%), при этом 62 пациента (20,6%) были старше 60 лет, однако без выраженной сопутствующей патологии.
Группу сравнения составили 1150 пациентов, которым была выполнена лапароскопическая холецистэктомия в стандарт- ном варианте (Таблица 1). Группы больных были однородны по всем параметрам.
Таблица 1
Сравнительная характеристика оперированных больных
|
Показатель |
Вид вмешательства |
||
|
ЛХЭ |
SILS |
||
|
Количество пациентов |
1150 |
300 |
|
|
Нозология |
ОХ |
103 (8,9%) |
18 (6%) |
|
ХХ |
970 (84,3%) |
257 (85,7%) |
|
|
Полипоз ЖП |
77 (6,7%) |
25 (8,3%) |
|
|
Пол (ж/м) |
1033 (89,8%)/117 (10,2%) |
262 (87,3%)/38 (12,7%) |
|
|
Возраст |
40 (35-57) |
43 (38-57) |
|
Всем пациентам на дооперационном этапе проводилось стандартизированное обследование, включающее УЗИ органов брюшной полости, ЭГДС, по показаниям МРТ-холангиографию. При острых формах калькулезного холецистита длительность заболевания колебалась от 3-х до 5 суток, при этом, по результатам обследования, в 6 наблюдениях на дооперационном этапе был диагностирован перивезикальный инфильтрат.
В ходе вмешательств при SILS применяли набор инструментов «X-cone» фирмы «Karl Storz» со стандартной технологией транс-умбиликальной установки системы, прошиванием и лигатурной фиксацией дна желчного пузыря в 7–8 межреберье (рис. 1).

Рис. 1. Прошивание и фиксация дна желчного пузыря лигатурой к передней брюшной стенке при SILS
Интраоперационно при SILS в ходе пересечения пузырных протока и артерии в 97 наблюдениях (32,3%) были применены «clipless»-технологии с использованием генератора «Liga Sure» фирмы «Valleylab» 5 мм, а в остальных 203 (67,8%) стандарт- ное клипирование 8 мм клипсами. Выбор варианта пересечения трубчатых структур преимущественно определялся их диаметром, степенью инфильтрации стенки (особенно при острых формах холецистита) и длиной. Таким образом, мы применяли только клипирование пузырного протока, если его длина не превышала 7 мм и толщина составляла от 5 мм. На фоне проводившейся полноценной интраоперационной санации брюшной полости дренирование её не выполнялось ни в одном из наблюдений.
Интенсивность послеоперационной боли оценивали с помощью специальной шкалы, где 0 полное отсутствие болевого синдрома, а 10 — нестерпимая боль [8].
Результаты
Длительность операции при ЛХЭ составила 40 (35–60) минут, длительность операции при SILS составила 55 (45–65) минут (Таблица 2).
Интраоперационно при SILS у 3 (1%) пациентов было отмечено интенсивное кровотечение из ложа желчного пузыря и печеночно-двенадцатиперстной связки, которое было остановлено прошиванием, не потребовавшего установки дополнительного оборудования.
Таблица 2
Результаты оперативного лечения заболеваний желчного пузыря
|
Показатель |
Вид вмешательства |
|
|
ЛХЭ |
SILS |
|
|
Длительность операции, мин. |
40 (35–60) |
55 (45–70) |
|
Частота конверсий* |
0,7% |
2,3%/0,3% |
|
Частота послеоперационных осложнений |
0,8% |
1% |
|
Госпитальная летальность |
0,17% |
– |
|
Болевой синдром |
6 (4–7) |
4 (3–5)^ |
|
Длительность послеоперационного койко-дня |
3 (2–5) |
1 (1–2)^ |
|
Удовлетворенность результатами лечения |
95% |
98%^ |
* ― для группы больных ХЛЭ переход в лапаротомию, для группы больных SILS – переход в ЛХЭ/переход в лапаротомию; ^ ― p<0,05 по сравнению с группой больных после ЛХЭ.
Необходимость конверсии однопрокольной технологии в «традиционное» 4-х прокольное лапароскопическое вмешательство отмечена в 7 наблюдениях (в 3 — по поводу хрониче- ского и в 4 — по поводу острого калькулезного холецистита), а также в «традиционную» холецистэктомию в 1 наблюдении (в связи с интраоперационно диагностированным пузырнотолстокишечным свищом) и была вызвана технической невозможностью полноценной идентификации и мобилизации элементов печеночно-двенадцатиперстной связки.
У 8 пациентов (0,7%), подвергнутых ЛХЭ, возникла необходимость конверсии лапароскопического доступа в лапаротомию (у 1 пациента в результате пересечения общего желчного протока, у 3-х пациентов в результате массивного инфильтративно-воспалительного перивези-кального процесса при остром холецистите, у 3-х пациентов в результате внутрибрюшного кровотечения из правой печеночной артерии).
Общая частота послеоперационных осложнений после ЛХЭ составила 0,8%, после SILS — 1%. Основными осложнениями после ЛХЭ являлись массивная тромбоэмболия легочной артерии (2 пациента), приведшая к гибели пациентов, внутрибрюшное кровотечение (7 пациентов), что потребовало выполнения лапаротомии, остановки внтурибрюшного кровотечения у 3-х пациентов, дренирования гематомы под УЗ-контролем — у 4-х пациентов.
В 2 наблюдениях после SILS интенсивное внутрибрюшное кровотечение было отмечено в раннем послеоперационном периоде (в первом случае источником явилось коагуляционное повреждение стенки задней ветви правой печеночной артерии в ходе мобилизации шейки желчного пузыря, во втором — добавочная ветвь пузырной артерии). Была выполнена лапаротомия, остановка кровотечения. В 1 наблюдении на 3-и сутки после вмешательства диагностирована несостоятельность культи пузырного протока (интраоперационно применялись «clipless»-технологии) с последующим выполнением эндоскопического стентирования ОЖП выше уровня впадения пузырного протока, дренирования сформировавшейся биломы под УЗ-контролем. Пациентка была выписана на 15-е сутки после операции в удовлетворительном состоянии, стент удален на 50-е сутки после установки. Причиной желчеистечения явилось интраоперационное точечное повреждение стенки пузырного протока эндокрючком в ходе его мобилизации ниже уровня формирования биологической пломбы, но не дефект технологии электротермического воздействия.
Госпитальная летальность после ЛХЭ составила 0,17% (2 пациента в результате массивной тромбоэмболии легочной артерии в раннем послеоперационном периоде). После SILS госпитальной летальности не было.
Болевой синдром после ЛХЭ составлял 6 (4–7) баллов, после SILS — 4 (3–5) баллов (p<0,05).
Удовлетворенность результатами лечения после ЛХЭ составила 95%, после SILS — 98% (p<0,05).
Длительность послеоперационного койко-дня после ЛХЭ составила 3 (2–5) койко-дней, после SILS — 1 (1–2) койко-дня (p<0,05).
По результатам выборочного осмотра пациентов спустя 6 месяцев после операции грыжевых дефектов не отмечено, послеоперационный рубец, расположенный интраумбиликально, визуально не отличим от окружающих тканей (рис. 2). Спустя 2 года, у 2-х пациенток после SILS и у 7 пациентов после ЛХЭ, диагностированы рецидивы грыжевых выпячиваний в умби-ликальной области (на дооперационном этапе определялись дефекты пупочного кольца).
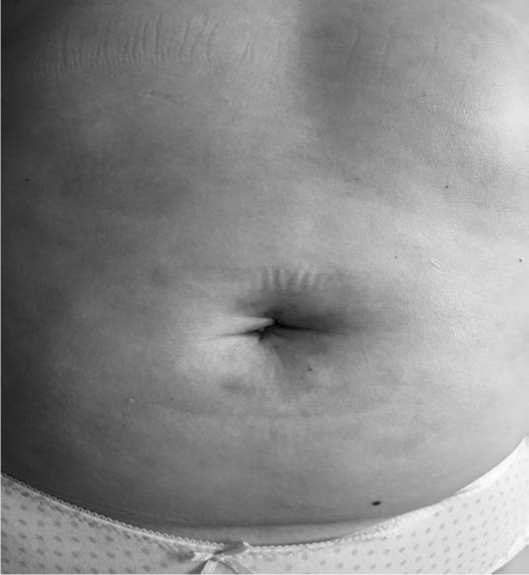
Рис. 2. Интраумбиликальный послеоперационный рубец после SILS
Заключение
По нашему мнению, однопрокольные методики хирургического лечения пациентов по поводу различных форм ЖКБ позволяют добиться оптимального косметического результата, умеренно выраженного послеоперационного болевого синдрома, быстрой послеоперационной реабилитации, а также увеличения общей удовлетворенности лечением у пациентов. Кроме того, при выполнении SILS имеется возможность перехода в традиционную ЛХЭ при возникновении технических трудностей при операции. Однако технологические возможности их выполнения существенно ниже при острых формах калькулезного холецистита, сопряжены с существенно большими рисками травмы элементов печеночно-двенадцатиперстной связки, чем при «стандартных» лапароскопических вмешательствах. Возможности выполнения симультанных вмешательств из единого трансумбиликального доступа в случаях сопутствующей хирургической и/или гинекологической патологии требуют дальнейшего изучения.
Список литературы Являются ли однопортовые эндоскопические технологии реальной альтернативой «традиционным» лапароскопическим вмешательствам?
- Курбанов Ф.С., Аббасова С.Ф., Алиев Ю.Г., Сушко А.Н., Добровольский С.Р. Холецистэктомия из лапароскопического доступа у больных старшего возраста. Хирургия, 2012. № 9. С. 38-41.
- Дадвани С. А., Ветшев П. С., Шулутко А. М., Прудков М. И. Желчнокаменная болезнь. М.: Видар, 2000. 144 с.
- Pisanu A., Reccia I., Porceddu G., Uccheddu A. Meta-analysis of prospective randomized studies comparing single-incision laparoscopic cholecystectomy (SILC) and conventional multiport laparoscopic cholecystectomy (CMLC). J. Gastrointest. Surg., 2012. 16(9). С. 1790-1801.
- Яхин Р.Р., Славин Л.Е. 8-летний опыт применения однопортовой холецистэктомии. Практическая медицина, 2017. Т. 6. № 107. С. 66-68.
- Podolsky E.R., Curcillo P.G. 2nd. Single port access (SPA) surgery - a 24-month experience. J. Gastrointest. Surg., 2010, 14(5), pp. 759-767.
- Можаровский В.В., Мишарин В.М., Цыганов А.А., Можаровский К.В. Однопортовая холецистэктомия - за и против. Хирургия, 2016. № 8. С. 50-54.
- Лащик М.Г., Восканян С.Э., Найденов Е.В. Первый опыт применения однопрокольных эндоскопических технологий на примере лапароскопической холецистэктомии. Доктор. Ру, 2015. № S1. C. 7-8.
- Овечкин А.М., Баялиева А.Ж., Ежевская А.А., Еременко А.А., Заболотский Д.В., Заболотских И.Б., Карелов А.Е., Корячкин В.А., Спасова А.П., Хороненко В.Э., Уваров Д.Н., Ульрих Г.Э., Шадрин Р.В. Послеоперационное обезболивание. Клинические рекомендации. Вестник интенсивной терапии им. А.И. Салтанова, 2019. № 4. С. 9-33.


