Эффект кардиодепрессии и его связь с острым панкреатитом и панкреонекрозом
Автор: Чавга А.И., Мидленко О.В., Гурьянова И.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Абдоминальная хирургия
Статья в выпуске: 1 (95), 2026 года.
Бесплатный доступ
Введение. Пациенты, страдающие острым панкреатитом, подвержены высокому риску возникновения серьезных кардиальных осложнений. Эффект кардиодепрессии относится к категории потенциально опасных осложнений острого панкреатита. Цель исследования. Проанализировать особенности взаимосвязи между эффектом кардиодепрессии и острым панкреатитом. Материалы и методы исследования. Нами был проведен анализ результатов патологоанатомического исследования и гистологии сердца пациентов с диагнозом острый панкреатит в период с 2019 по 2023 гг. Результаты. Результаты проведенного нами исследования показали, что на втором месте по частоте встречаемости был такой диагноз, как некроз поджелудочной железы – 10,8 % пациентов. На третьем месте – хронический панкреатит – 8,8 %. У пациентов наблюдаются такие осложнения, как перитонит, интоксикация, различные виды шока, флегмона, некроз брюшины, что приводит к летальному исходу. Сочетанное проявление перитонита и интоксикации влекло тяжелые полиорганные нарушения, в том числе, нарушения функционирования сердечно-сосудистой системы, кардиодепрессия. Была выявлена достоверно значимая корреляционная зависимость между состоянием тканей сердечной мышцы и выраженностью отека. Прослеживалась прямая корреляционная зависимость между характеристиками ткани и выраженностью отека. Заключение. Полученные данные примерно сопоставимы с данными, полученными другими авторами. Неконтролируемый выброс провоспалительных цитокинов в системный кровоток в ответ на активацию протеолитических ферментов и деструкцию тканей при остром панкреатите являются пусковым механизмом формирования синдрома системного воспалительного ответа. Данный процесс сопровождается развитием патологических состояний, одним из которых является эффект кардиодепрессии.
Панкреатит, острый панкреатит, осложнения, перитонит, интоксикация, кардиодепрессия, отек, гистология сердца
Короткий адрес: https://sciup.org/142247235
IDR: 142247235 | УДК: 616.37 | DOI: 10.17238/2072-3180-2026-1-11-23
The effect of cardiodepression and its relationship with acute pancreatitis and pancreatic necrosis
Introduction. Patients suffering from acute pancreatitis are at high risk of serious cardiac complications. The effect of cardiodepression belongs to the category of potentially dangerous complications of acute pancreatitis. The purpose of the study is to analyze the features of the relationship between the effect of cardiodepression and acute pancreatitis. Materials and methods of research. We analyzed the results of pathological examination and histology of the heart of patients diagnosed with acute pancreatitis in the period from 2019 to 2023. Treatment results. The results of our study showed that the second most common diagnosis was pancreatic necrosis – 10,8 % of patients. Chronic pancreatitis is in third place – 8,8 %. Patients have complications such as peritonitis, intoxication, various types of shock, phlegmon, peritoneal necrosis, which leads to death. The combined manifestation of peritonitis and intoxication led to severe multiple organ disorders, including impaired functioning of the cardiovascular system, and cardiodepression. A significantly significant correlation was found between the condition of the heart muscle tissues and the severity of edema. There was a direct correlation between tissue characteristics and the severity of edema. Conclusions. The data obtained is approximately comparable to the data obtained by other authors. Uncontrolled release of proinflammatory cytokines into the systemic bloodstream in response to activation of proteolytic enzymes and tissue destruction in acute pancreatitis is a trigger mechanism for the formation of systemic inflammatory response syndrome. This process is accompanied by the development of pathological conditions, one of which is the effect of cardiodepression.
Текст научной статьи Эффект кардиодепрессии и его связь с острым панкреатитом и панкреонекрозом
В этиологии летальных исходов при панкреонекрозе ведущая роль отводится развитию сердечно-сосудистой и полиорганной недостаточности, спровоцированной инфекционно-токсическим шоком. Несмотря на совершенствование методов диагностики и терапевтических подходов, показатели смертности при данной патологии остаются стабильно высокими, варьируясь в диапазоне от 15 до 100 % в зависимости от степени поражения поджелудочной железы и наличия/от-сутствия инфицирования некротических зон. Заболеваемость острым панкреатитом демонстрирует неуклонную тенденцию к росту, при этом частота развития его деструктивных форм достигает 20–45 %. Особую актуальность проблема приобретает в случае коморбидной патологии, когда острый панкреатит может оказывать негативное влияние на функционирование других жизненно важных органов, включая сердце.
Патология поджелудочной железы относится к категории актуальных и значимых заболеваний по ряду факторов. Она зачастую становится причиной временной нетрудоспособности пациентов, представляет собой неотложное состояние, требующее хирургического вмешательства. Несмотря на прогресс, достигнутый в области диагностики и лечения данной патологии за последние десятилетия, по-прежнему сохраняется необходимость в дальнейшем поиске эффективных средств и методов терапии острого панкреатита, профилактики возникающих осложнений, предупреждения риска развития воспалительных, дистрофических и гнойно-септических осложнений [1].
Исследование взаимосвязи между острым панкреатитом и феноменом кардиодепрессии представляет несомненный интерес не только с точки зрения клинической практики, но и для дальнейшего прогресса научных изысканий в данной области. Углубленное изучение этой проблематики может расширить современные представления о патофизиологических механизмах развития обоих состояний и послужить стимулом для разработки инновационных диагностических и терапевтических подходов. Понимание эффекта кардиодепрессии при остром панкреатите открывает перспективы для внедрения индивидуализированных схем ведения пациентов с данной патологией, что, в свою очередь, позволит оптимизировать прогноз заболевания и снизить риск развития сердечных осложнений [2].
Пациенты, страдающие острым панкреатитом, подвержены высокому риску возникновения серьезных кардиальных осложнений, включая аритмии, снижение сердечного выброса и другие нарушения функции сердечно-сосудистой системы. Изучение феномена кардиодепрессии на фоне острого панкреатита может способствовать более глубокому пониманию взаимосвязи между состоянием поджелудочной железы и сердечной функцией, а также определению факторов риска развития данного осложнения и разработке эффективных стратегий его лечения и профилактики. Эффект кардиодепрессии относится к категории потенциально опасных осложнений острого панкреатита, требующих пристального внимания со стороны клиницистов и исследователей.
Цель и задачи исследования . Проанализировать особенности взаимосвязи между эффектом кардиодепрессии и острым панкреатитом.
В ходе исследования решались следующие задачи:
-
1. Проанализировать этиопатогенез, классификацию, формы острого панкреатита.
-
2. Раскрыть этиопатогенетические механизмы кардиодепрессии.
-
3. Провести анализ структуры заболеваемости и исходов лечения пациентов с острым панкреатитом.
-
4. Определить особенности поражения сердца и проявления эффекта кардиодепрессии на фоне острого панкреатита и его осложнений по данным патологоанатомического исследования и гистологии сердца.
-
5. Сравнить полученные данные с результатами аналогичных исследований других авторов и сформулировать выводы.
Материалы и методы
Нами был проведен анализ результатов патологоанатомического исследования и гистологии сердца пациентов с диагнозом острый панкреатит в период с 2019 по 2023 гг. В период с 01.01.2019 по 31.12.2019 г на базе ГУЗ УОКБ вскрыт 791 пациент. В период с 01.01.2020 по 31.12.2020 г на базе ГУЗ УОКБ вскрыто 1413 пациентов. В период с 01.01.2021 по 31.12.2021 г. на базе ГУЗ УОКБ вскрыто 817 пациентов. В период с 01.01.2022 по 31.12.2022 г на базе ГУЗ УОКБ вскрыто 780 пациентов. В период с 01.01.2023 по 31.12.2023 г на базе ГУЗ УОКБ вскрыто 674 пациентов.
Результаты
Согласно статистическим данным, заболеваемость острым панкреатитом и обострениями хронического панкреатита в Российской Федерации составляет 23 % среди всех острых хирургических заболеваний органов брюшной полости, занимая третье место в общем перечне патологий данной локализации. В отдельных регионах и за определенные временные периоды острый панкреатит выходит на первое место по частоте встречаемости [3].
Несмотря на достижения в области интенсивной терапии, показатели летальности при тяжелых формах острого панкреатита остаются на высоком уровне и претерпевают незначительные изменения. Данная ситуация обусловлена сложностями в своевременной диагностике, особенно на ранних стадиях заболевания, а также риском развития серьезных осложнений, таких как некроз поджелудочной железы или инфекционные процессы. Именно поэтому важна ранняя диагностика – при появлении первых симптомов острого панкреатита (интенсивная боль в животе, рвота, лихорадка, повышенная чувствительность в области живота), выявление которых позволит предупредить прогрессирование заболевания и развитие угрожающих жизни осложнений. Тяжелые формы острого панкреатита характеризуются наличием гнойно-деструктивных осложнений, которые могут привести к летальному исходу. В последние годы наблюдается рост числа подобных клинических случаев, что может быть обусловлено изменениями в образе жизни и пищевых привычках населения.
Острый панкреатит является воспалительным заболеванием полиэтиологической природы. Чаще всего развивается на фоне коморбидной патологии желудочно-кишечного, гепа-то-биллиарного тракта, на фоне злоупотребления алкоголем, воспалительных и инфекционных процессов. Вне зависимости от этиологического фактора панкреатита, клиническая картина в целом примерно одинакова [4].
Развитию воспалительных процессов в поджелудочной железе могут способствовать различные причины, в том числе нерациональное питание, злоупотребление алкогольными напитками, прием лекарственных, наркотических или токсических веществ, оказывающих повреждающее воздействие на организм. В целом, несмотря на определенный прогресс в области диагностики и лечения, острый панкреатит по-прежнему остается одной из наиболее распространенных патологий органов брюшной полости. По данным некоторых авторов, показатели летальности при данном заболевании достигают 10–12 %, что диктует необходимость дальнейшего совершенствования терапевтических и профилактических мероприятий.
В отсутствие адекватных терапевтических мероприятий, прогрессирование острого панкреатита может привести к развитию обширного воспалительного процесса септической природы с неблагоприятным исходом [5]. Данная патологическая цепь событий инициируется чрезмерной системной воспалительной реакцией, обусловленной неконтролируемой активацией иммунных механизмов и аутоагрессией с повреждением клеток поджелудочной железы [5].
В результате деструкции панкреатоцитов происходит высвобождение внутриклеточных компонентов, активация провоспалительных цитокинов и медиаторов воспаления, что, в свою очередь, запускает миграцию иммунных клеток в очаг поражения. На фоне развивающегося молекулярного воспалительного синдрома постепенно изменяется состав микробиоты в зоне поражения, и первоначально не вовлеченные патогены становятся чужеродными антигенами, высвобождающими экзотоксины, белковые структуры и другие молекулы. Это приводит к формированию вторичного септического воспаления и дальнейшей выработке провоспалительных факторов, усугубляющих ситуацию.
Согласно клинической классификации, на начальной стадии развития острого панкреатита (стадия 1 – отечная форма) наблюдается выраженный отек окружающих тканей, накопление жидкости в паренхиме поджелудочной железы, формирование воспалительной реакции с возможным образованием очагов некроза.
Дальнейшее прогрессирование патологического процесса подразделяется на две подстадии 2А и 2Б, объединенные общим термином "секвестрация". Диагностика конкретной формы заболевания является одной из ключевых задач на втором этапе обследования пациентов с подозрением на острый панкреатит. На данном этапе основные усилия сосредоточены на детальной оценке состояния самой поджелудочной железы с использованием ультразвукового исследования для выявления специфических признаков, таких как нечеткость контуров, изменение эхогенности паренхимы, наличие отека, скопление жидкости в сальниковой сумке, брюшной или даже плевральной полости [6].
Первый этап диагностического поиска предполагает общую оценку состояния органов брюшной полости для определения объема необходимой хирургической помощи. На этом этапе могут быть выявлены такие острые хирургические патологии, как кишечная непроходимость, острый аппендицит или перфорация поджелудочной железы, требующие экстренного оперативного вмешательства.
Следует отметить, что в условиях острого панкреатита на 1–2 фазах заболевания существуют факторы риска, затрудняющие эффективную доставку лекарственных препаратов к очагу воспаления. К таким факторам относятся сладж-синдром, высокая скорость образования тромбов и микротромбозов в железе или парапанкреатической клетчатке, которые могут приводить к разрывам капиллярного русла и развитию серьезных осложнений [7].
В данной ситуации более предпочтительным представляется локальный метод введения лекарственных средств, например, установление катетера в чревный ствол под рентгенологическим контролем. Эффективность такого подхода обусловлена рядом факторов, включая скорость кровотока и, соответственно, проникновения действующего вещества непосредственно в клетки поджелудочной железы, экспозицию воздействия препарата на клетки и ткани, а также скорость его выведения из кровотока в целом [8].
Результаты многочисленных исследований, проведенных различными авторами, указывают на то, что патогенез острого панкреатита тесно связан с чрезмерной системной воспалительной реакцией, развивающейся вследствие неконтролируемой активации иммунной системы и аутоагрессии, приводящей к повреждению клеток поджелудочной железы.
В терминальной, заключительной стадии развития по-лиорганной недостаточности при остром панкреатите происходит срыв компенсаторных механизмов организма, что может привести к фатальному исходу. На предшествующем этапе запускаются резервные возможности организма для противодействия системной воспалительной реакции, представляющей собой компенсаторную противовоспалительную реакцию. Ранее, на стадии вторичной аутоагрессии, медиаторы воспаления индуцируют генерализованный воспалительный ответ и развитие острой сердечно-сосудистой недостаточности, проявляющейся в виде дистрибутивного шока.
Предшествующая каскадная стадия характеризуется вторичным повреждением органов и систем, начиная с поражения капиллярного русла вследствие дисфункции эндотелия. Инициирующим фактором служит локальное воспаление в поджелудочной железе, при котором происходит компенсаторное отграничение повреждающего агента посредством медиаторов воспаления (индукционная стадия).
Таким образом, прослеживается тесная взаимосвязь между системной воспалительной реакцией и развитием органной дисфункции при остром панкреатите. Переход локального воспалительного процесса в системную воспалительную реакцию способствует утяжелению течения заболевания.
Результаты современных исследований указывают на то, что одним из неблагоприятных осложнений при остром панкреатите является полиорганная недостаточность, развивающаяся на фоне генерализованного воспалительного процесса. Как правило, на первом этапе развивается выраженная почечная недостаточность, которая впоследствии может прогрессировать и значительно нарушать гомеостаз. Избыточная продукция трипсина, медиаторов воспаления, воспалительных цитокинов приводит к дальнейшему усугублению ситуации и развитию многочисленных повреждений органов и систем, включая миокард, сердечно-сосудистую систему с развитием сердечной недостаточности, а также печеночную и легочную недостаточность [9].
Развитию различных осложнений, таких, как тканевая гипоксия, токсемия, функциональная недостаточность, способствует эндогенная интоксикация. Ретенционная и реперфузионная недостаточность может приводить к развитию недостаточности детоксикационных систем, в связи с чем нарушаются процессы детоксикации, происходит накопление в организме продуктов интоксикации, которые продолжают и усиливают токсическое воздействие на организм. Особая опасность связана с воздействием инфекционного компонента. Некротизирующий панкреатит связан с воздействием на организм продуктов распада клеточных элементов. Панкреатит сопровождается снижением тканевой перкуссии, развитием тканевой гипоксии. Отмечается попадание в сосудистое русло вазодилататоров (эпинефрин, норэпинефрин), что рассматривается как компенсаторная реакция. Мощными вазодилататорами являются брадикинины, которые увеличивают сосудистую проницаемость, изменяют реологические свойства крови, способствуют выходу плазмы крови и форменных элементов в интерстициальное пространство. Панкреатические ферменты, простагландины, цитокины, другие медиаторы воспаления, биогенные амины, брадикинины – все это способствует нарушению гомеостаза, приводит к развитию оксидативного стресса. Как следствие – повреждаются клетки поджелудочной железы, происходит тканевая деструкция, высвобождение разрушенных субстанций, которые оказывают токсическое воздействие на организм [10].
На фоне интоксикации может развиваться феномен кар-диодиодепрессии, который представляет собой угнетение сократительной и метаболической активности миокарда. Это состояние сопровождает острый, хронический панкреатит, панкреонекроз, и другие заболевания поджелудочной железы. Кардиодепрессия впервые была описана в 1947 году при геморрагическом шоке. Также в отдельных исследованиях указывается на то, что КД может развиваться на фоне выраженной бактериемии, сепсиса, при ряде заболеваний воспалительно-инфекционного генеза.
Данное состояние характеризуется снижением или подавлением сердечной функции, что может привести к ухудшению работы сердца и развитию сердечной недостаточности. Это означает, что сердце не способно эффективно перекачивать кровь по организму, что может повлечь за собой различные сердечные осложнения. Кардиодепрессия может вызывать замедление сердечного ритма (брадикардию), ухудшающее общую сердечную эффективность и приводящее к симптомам, связанным с недостаточным кровоснабжением. Снижение способности сердца сокращаться и выдавать кровь эффективно может стать причиной усталости, одышки, отеков и других признаков сердечной недостаточности. Кардиодепрессия также может способствовать возникновению различных аритмий, что дополнительно ухудшает работу сердца и может потребовать специализированного лечения [11].
Неконтролируемый выброс провоспалительных цитокинов в системный кровоток в ответ на активацию протеолитических ферментов и деструкцию тканей при остром панкреатите являются пусковым механизмом формирования синдрома системного воспалительного ответа (ССВО). Данный процесс сопровождается развитием таких патологических состояний, как эндогенная интоксикация, оксидативный стресс, гипоксия, липидный дистресс-синдром и нарушения в системе гемостаза, приводящих к значительным расстройствам гомеостаза организма.
Степень выраженности ССВО находится в прямой зависимости от фазы и тяжести течения острого панкреатита. В свою очередь, формирование синдрома системного воспалительного ответа во многом обуславливает развитие полиорганных дисфункций, определяющих тяжесть клинического течения заболевания. Таким образом, тяжелое течение острого панкреатита с поражением органов и систем в значительной степени обусловлено синдромом системного воспалительного ответа, развитие которого связано с нарушениями гомеостаза, в том числе эндогенной интоксикацией, оксидативным стрессом, гипоксией, липидным дистресс-синдромом и расстройствами в системе гемостаза, сопровождающимися неконтролируемой продукцией про-воспалительных цитокинов вследствие активации протеолитических ферментов и деструкции тканей [9].
Цитотоксическое воздействие гипоксии, окислительного стресса и гипоэргоза на кардиомиоциты может быть опосредовано нарушением баланса кальция с избыточным накоплением данного катиона в саркоплазме этих клеток. Избыточное накопление кальция в саркоплазме кардиомиоцитов способно повреждать эти клетки при действии указанных повреждающих факторов. Механизмы дисбаланса внутриклеточного кальция при воздействии повреждающих агентов хорошо известны и постоянно уточняются. Чрезмерное поступление катиона кальция в цитоплазму кардиомиоцитов, опосредованное активацией потенциал-зависимых и рецептор-управляемых кальциевых каналов сарколеммы и мембран саркоплазматического ретикулума на фоне сниженной активности кальцийтранспортирующих систем клеток миокарда, может приводить к фатальным для клетки последствиям. Для воздействия на данное патогенетическое звено, связанное с нарушением кальциевого гомеостаза в кардиомиоцитах при повреждающем действии гипоксии, окислительного стресса и гипоэргоза, может быть использован блокатор L-потенциал-зависимых кальциевых каналов верапамил [12].
Выраженность системной воспалительной реакции ССВО напрямую определяется фазой течения панкреатита и степенью его тяжести. Максимально выраженная кардиодепрессия развивается на фоне нарушения обмена глюкозы (в первые дни после развития острого панкреатита), и примерно спустя месяц после индукции панкреонекро-за. В основе нарушения нормального функционального состояние сердечной мышцы лежат явления гипоксии, окислительный стресс, гипоэргоз, нарушение метаболических характеристик миокарда, нарушение энергетических потребностей, дисбаланс микроэлементов, дефицит макроэргических соединений [2].
Тот факт, что глюкоза неэкономно расходуется миокардом указывает на то, что в кардиомиоцитах наблюдается митохондриальная дисфункция, в связи с чем только усиливается дефицит синтеза макроэргических структур, и усугубляется дисбаланс внутриклеточного кальция. Мышца приобретает повышенную чувствительность к кислороду, происходит дальнейшая дестабилизация клеточных структур, дестабилизируются клеточные мембраны [1].
За последние годы было открыто и изучено множество механизмов миокардиальной депрессии. Термин «фактор миокардиальной депрессии» можно считать собирательным понятием, объединяющим эффекты ряда неспецифических веществ, роль которых в развитии кардиодепрессии была выявлена благодаря новым данным в области патогенеза этого состояния, таких как цитокины, бактериальные эндотоксины, ферментативные факторы, фактор некроза опухо- лей. Появление новых диагностических методик позволило изучить миокардиальную экспрессию цитокинов и действие на миокард бактериальных эндотоксинов. Одним из механизмов опосредованной миокардиальной депрессии является действие цитокинов на эндотелий сосудов, результатом которого становится диффузное нарушение микроциркуляции, оказывающее кардиодепрессивный эффект.
Гиперкоагуляция, вызванная активацией свертывающей системы крови, нарушением работы противосвертывающей системы, торможением фибринолиза и повышенной агрегацией тромбоцитов на фоне системного воспалительного ответа, может приводить к тромбозу коронарных артерий. Среди панкреатических ферментов, попадающих в системный кровоток при тяжелом остром панкреатите вследствие разрушения микро- и макроструктуры ткани поджелудочной железы, наиболее изучено действие трипсина на миокард [11].
В результате прямого повреждающего действия циркулирующих в кровяном русле панкреатогенных ферментов на кардиомиоциты при деструкции ткани поджелудочной железы происходит нарушение структурно-функциональной целостности миокарда, обусловленное увеличением проницаемости мембран кардиомиоцитов, некрозом клеток и развитием вторичных электрических нарушений. Другим патогенетическим механизмом депрессии сократимости миокарда является опосредованное действие цитокинов, продуцируемых иммунокомпетентными клетками в ответ на ферментативное повреждение поджелудочной железы и ее сосудистого русла. С одной стороны, цитокины индуцируют переход легкого острого панкреатита в тяжелую форму заболевания. С другой стороны, их действие на эндотелий сосудов приводит к диффузному нарушению микроциркуляции и оказывает кардиодепрессивный эффект. Кроме того, цитокины (ФНО, ИЛ-1β, ИЛ-18 и ИЛ-6) оказывают прямое негативное влияние на сократимость сердечной мышцы, что хорошо изучено при сепсисе.
Совокупность возможных причин нарушения сократимости миокарда объединяют термином «фактор депрессии миокарда», подразумевая некий фактор, вызывающий кардиодепрессию при взаимодействии с миокардом. Наличие такого фактора было предположено на основании результатов экспериментов с введением плазмы крови больного животного здоровому, в результате чего у последнего развивалась миокардиальная депрессия. Исходя из этого, можно сделать вывод, что таким фактором не могут являться нарушения вегетативной нервной системы, интраабдоминальная гипертензия, гиповолемия или нарушения водно-электролитного баланса. На данный момент не существует единой концепции патогенеза нарушения сократимости сердечной мышцы при остром панкреатите, однако выявленные механизмы позволяют объединить их в понятие «фактор депрессии миокарда» [8].
Нами были проанализированы основные диагнозы, с которыми пациенты поступали в отделение, была проведена оценка возникших осложнений, а также был проведен анализ патологоанатомического исследования, результаты гистологии. Было установлено, что в основном пациенты поступают с диагнозом острый панкреатит (64,8 % пациентов). Данные представлены на рисунке 1.
Гематома субдуральная1,8
Другие уточненные болезни ПЖ ■ 3,6
Цирроз ПЖ1,8
Некроз ПЖ10,8
Острый панкреатит64,8
Панкреонекроз ■ 3,6
Хронический панкреатит8,8
0 10 20 30 40 50 6070
Рис. 1 . Частота встречаемости различных первичных диагнозов Fig. 1. Frequency of occurrence of various primary diagnoses
Как видим из представленных данных, на втором месте по частоте встречаемости был такой диагноз, как некроз поджелудочной железы – 10,8 % пациентов. На третьем месте – хронический панкреатит – 8,8 %.
Далее нами была проанализирована структура осложнений. Результаты указывают на то, что у пациентов наблюдаются такие осложнения, как перитонит, интоксикация, различные виды шока, флегмона, некроз брюшины, что приводит к летальному исходу. Частота встречаемости анализируемых патологий представлена на рисунке 2.
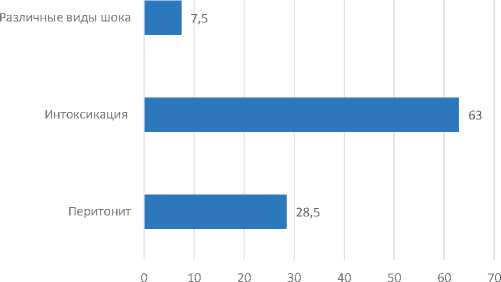
Рис. 2. Частота встречаемости различных типов осложнений
Fig. 2. Frequency of occurrence of various types of complications
Результаты указывают на то, что среди всех осложнений чаще всего встречается интоксикация (63 % случаев). На втором месте – перитонит (28,5 %), на третьем – различные другие виды шока (7,5 % случаев). Во многих клинических случаях наблюдалась сочетанное проявление перитонита и интоксикации, в связи с чем развивались тяжелые по-лиорганные нарушения, в том числе, нарушения функционирования сердечно-сосудистой системы, кардиодепрессия. Результаты гистологического исследования указывают на наличие у пациентов ряда изменений со стороны кардиомиоцитов, сердечной мышцы.
Далее нами был проведен корреляционный анализ, направленный на выявление корреляционной зависимости между исходным диагнозом, развившимся осложнением, состоянием кардиомиоцитов, отечностью сердечной мышцы (табл. 1).
Таблица 1
Корреляционная зависимость между исходным диагнозом, осложнением, результатами гистологии
Table 1
Correlation between the initial diagnosis, complication, and histology results
|
Исходный диагноз Initial diagnosis |
Осложнение Complication |
Гистология Histology |
Отек Edema |
|
|
Исходный диагноз / Initial diagnosis |
– |
–0,302455133 |
0,06415392 |
–0,017641288 |
|
Осложнение / A complication |
–0,302455133 |
– |
–0,10884956 |
–0,120273311 |
|
Гистология / Histology |
0,064153917 |
–0,108849563 |
– |
0,889708718* |
|
Выраженность отека / Severity of edema |
–0,017641288 |
–0,120273311 |
0,88970872* |
– |
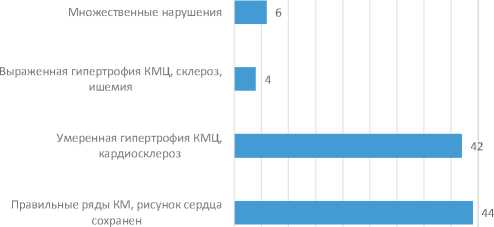
Как видим из представленных данных, была выявлена достоверно значимая корреляционная зависимость между состоянием тканей сердечной мышцы и выраженностью отека. У многих пациентов, которые изначально поступили с острым или хроническим панкреатитом, осложненным впоследствии перитонитом, интоксикацией, кардиомиоциты располагались правильными рядами, ядра были овальными, располагались в центре клеток. У таких пациентов наблюдался умеренный интерстициальный отек (рис. 3).
0 5 10 15 20 25 30 35 40 45 50
Рис. 3. Результаты гистологического исследования сердца
Fig. 3. Results of histological examination of the heart
Как видим, у большинства пациентов (44 %), наблюдались правильные ряды КМЦ, рисунок сердца сохранялся. У 42 % пациентов отмечалась умеренная гипертрофия КМЦ, склероз, ишемия (42 %). У пациентов с выраженным перитонитом и сильной интоксикацией наблюдалась умеренная гипертрофия кардиомиоцитов, полнокровие сосудов, умеренный межуточный и перидуктальный кардиосклероз. При этом у многих пациентов наблюдался выраженный отек межклеточного пространства. У пациентов с выраженной гипертрофией кардиомиоцитов, наблюдался выраженный интерстициальный отек. Во многих микропрепаратах сердца при этом наблюдались явления мелкоочагового кардиосклероза, явления очагового ишемического повреждения. Прослеживалась прямая корреляционная зависимость между характеристиками ткани и выраженностью отека. То есть, чем более тяжелыми были нарушения кардиомиоцитов, их гипертрофия, тем более выраженным и тяжелым был отек окружающих тканей. И наоборот, незначительные изменения кардиомиоцитов, сердечной ткани сопровождались незначительным, умеренным отеком. Частота встречаемости различных типов отека, по данным гистологического исследования, представлена на рисунке 4.
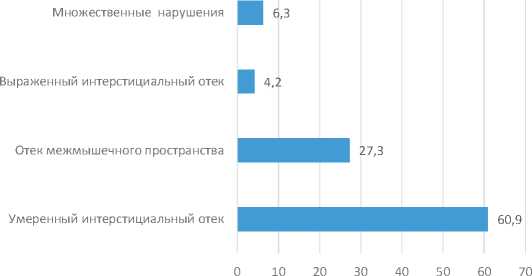
Рис. 4. Типы отеков сердечной ткани, по результатам гистологического исследования
Fig. 4. Types of edema of cardiac tissue, according to the results of histological examination
Как видим из представленных данных, чаще всего наблюдается умеренный интерстициальный отек (60,9 % случаев). В 27,3 % случаев наблюдается отек межмышечного пространства. Значительно реже отмечался выраженный интерстициальный отек и множественные нарушения в гистологической картине.
Была выявлена корреляция между состоянием тканей сердца
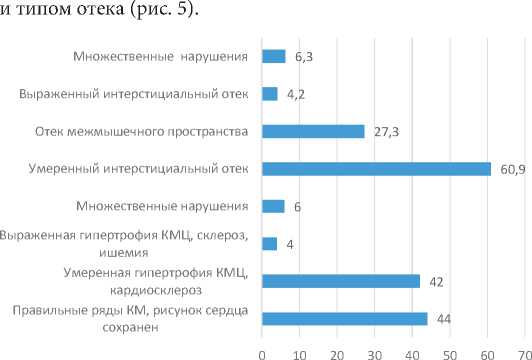
Рис. 5. Соотношение между гистологией сердца и типом отека
Fig. 5. The relationship between the histology of the heart and the type of edema
Как видим из представленных данных, правильные ряды кардиомиоцитов, сохраненный рисунок сердца сопровождался развитием умеренного интерстициального отека (рис. 6).
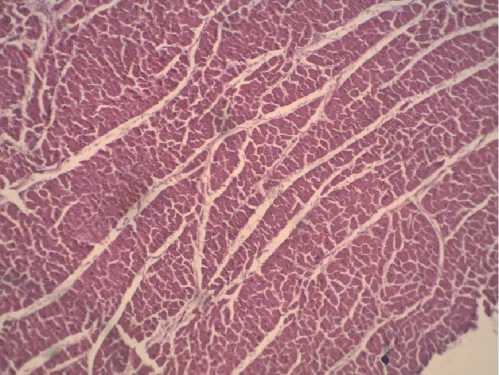
Рис. 6. Гистологическая картина сердца. Кардиомиоциты расположены правильными рядами, ядра овальные, в центре клеток. Умеренный интерстициальный отек (использовался микроскоп Leika DM E, фото сделано при помощи камеры микроскопа Leika EC3)
Fig. 6 . Histological picture of the heart. Cardiomyocytes are arranged in regular rows, the nuclei are oval, in the center of the cells.
Moderate interstitial edema (a Leika DM E microscope was used, the photo was taken using a Leika EC3 microscope camera)
Результаты показывают, что при умеренной гипертрофии кардиомиоцитов, измененном рисунке сердца, признаках склероза, развивался преимущественно отек межмышечного пространства (рис. 7).
Выраженная гипертрофия кардиомиоцитов, сопровождалась развитием выраженного интерстициального отека (рис. 8).
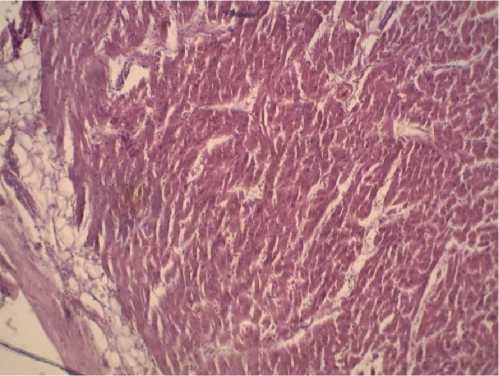
Рис. 7. Гистологическая картина сердца. Гипертрофия кардиомиоцитов, отек межмышечных пространств (использовался микроскоп Leika DM E, фото сделано при помощи камеры микроскопа Leika EC3)
Fig. 7 . Histological picture of the heart. Cardiomyocyte hypertrophy, swelling of the intermuscular spaces (a Leika DM E microscope was used, the photo was taken using a Leika EC3 microscope camera)
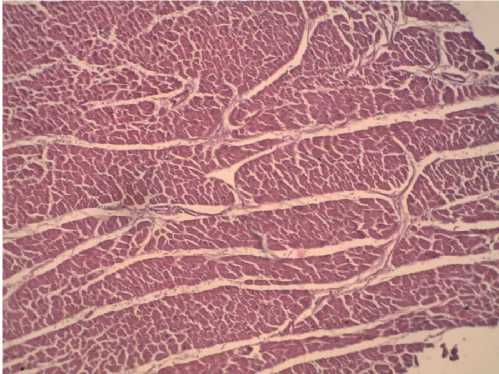
Рис. 8. Гистологическая картина сердца.
Выраженный интерстициальный отек, выраженная гипертрофия КМЦ (использовался микроскоп Leika DM E, фото сделано при помощи камеры микроскопа Leika EC3)
Fig. 8 . Histological picture of the heart. Pronounced interstitial edema, pronounced CMC hypertrophy (Leika DM E microscope was used, photo taken using a Leika EC3 microscope camera)
Множественные нарушения гистологической структуры сердца сопровождались выраженным отеком, наличием различных типов отека.
Рассмотрим случаи, в которых были выявлены наиболее значимые и многочисленные гистологические изменения.
Пациентка Л. Поступила с острым панкреатитом. Состояние осложнилось интоксикацией. Результаты гистологии сердца показали выраженный интерстициальный отек. Кардиомиоциты с явлениями умеренно выраженной гипертрофии, межмышечный отёк. В отдельных полях зрения наблюдались единичные кардиомиоциты с исчезновением поперечной ис-черченности, фрагментацией и лизисом ядер кардиомиоцитов. В отдельных полях зрения наблюдался периваскулярный фиброз, очаги мелкоочагового кардиосклероза. Сосуды капиллярного типа, полнокровны.
У пациентки Н. наблюдался некроз поджелудочной железы, состояние осложнилось интоксикацией. Результаты показали умеренный интерстициальный отёк и умеренное полнокровие сосудов, кардиомиоциты гипертрофированы с центрально расположенными ядрами, в состоянии белковой дистрофии по типу мутного набухания местами фрагментированы, в цитоплазме перинуклеарное скопление гранул липофусцина.
Пациентка Н. поступила с острым панкреатитом. Хирургическое лечение было осложнено перитонитом, интоксикацией. На результатах гистологического исследования наблюдалась умеренно выраженная дистрофия кардиомиоцитов в отдельных полях зрения. Кардиомиоциты фрагментированы, некоторые лишены поперечной исчер-ченности. Наблюдалась умеренно выраженная гипертро- фия кардиомиоцитов, интерстициальный отёк, очаговый периваскулярный фиброз, в кус из передней стенки левого желудочка от средней трети до верхушки участок по типу хронической аневризмы с явлениями крупноочагового кардиосклероза, полнокровие сосудов, очаговые диапе-дезные кровоизлияния.
Пациент М. поступил с циррозом поджелудочной железы. Состояние осложнилось перитонитом, интоксикацией. В микропрепаратах сердца наблюдалась умеренно выраженная дистрофия кардиомиоцитов в отдельных полях зрения. Кардиомиоциты в отдельных полях зрения фрагментированы, некоторые лишены поперечной исчерченности, умеренно выраженная гипертрофия кардиомиоцитов, интерстициальный отёк, очаговый периваскулярный фиброз, местами полнокровие сосудов.
Пациент Д. поступил с некрозом поджелудочной железы, острым панкреатитом. Состояние осложнилось интоксикацией, что привело к летальному исходу. По результатам гистологии было установлено, что рисунок строения сердца сохранён, умеренно выраженный межмышечный отек; нерезкая, местами умеренная гипертрофия кардиомиоцитов; в отдельных полях зрения, полнокровие сосудов капиллярного типа, местами кардиомиоциты лишены ядер, фрагментированы, с исчезновением поперечной исчерченности мышечных волокон, периваскулярный фиброз.
Пациент М. поступил с субдуральной гематомой, отеком. Наблюдались сопутствующие нарушения гепатобил-лиарного тракта. По результатам гистологии наблюдалась выраженная гипертрофия КМЦ, очаговый межуточный кардиосклероз, отек межуточного вещества, полнокровие сосудов, вторичные диамедезные кровоизлияния, участки ишемической дистрофии.
Пациентка Н. Поступила с хроническим панкреатитом. Состояние осложнилось выраженной интоксикацией. Результаты гистологического исследования показали, что кардиомиоциты были расположены правильными рядами, ядра овальные, в центре клеток. Умеренный интерстициальный отек
В целом, результаты изучения анамнеза пациентов и результаты гистологических исследований указывают на то, что у большинства пациентов с тяжелыми осложнениями в виде перитонита, интоксикации наблюдались выраженные изменения со стороны сердечной мышцы, кардиомиоцитов. Результаты гистологических исследований показали гипертрофию кардиомиоцитов, кардиосклероз, в некоторых случаях – ишемические процессы, участки кровоизлияния. У многих наблюдался умеренный и выраженный отек интерстициальной ткани.
Обсуждение
Полученные нами результаты исследования примерно сопоставимы с результатами исследований других авторов. Во многих исследованиях последних лет говорится о том, что при отсутствии адекватной энтеросорбции возникают многочисленные осложнения, являющиеся следствием интоксикации, в том числе, органные нарушения. Энтерособционная терапия способствует снижению эндотоксемии, энтерособ-ции. По характеру течения интоксикационного процесса и эффективности применения энтеросорбции, можно судить об особенностях течения острого панкреатита, о его прогнозе. Энтеросорбция представляет собой патогенетически обоснованное средство детоксикации, которое показывает высокую эффективность в составе комплексного лечения. Как правило, этот метод является важным дополнением к патогенетическому лечению, хирургической терапии.
Для оценки состояние пациента можно использовать ИЭИ – индекс эндогенной интоксикации, при помощи которого можно судить о состоянии поджелудочной железы, о тяжести острого панкреатита. Если показатели ИЭИ довольно низкие, это является неблагоприятным признаком и указывает на высокий риск развития осложнений, на неблагоприятный исход, и риск развития осложнений. Как правило, низкие показатели ИЭИ говорят о развитии осложнений и о морфологических изменениях, которые затрагивают поджелудочную железу, указывает на прогрессирование воспалительного процесса, на развитие системного воспалительного процесса. В большинстве случаев низкий ИЭИ сопровождается ограничениями, которые препятствуют дальнейшему проникновению токсических веществ в кровь. Состояние сопровождается развитием многочисленных осложнений, сопровождается эндогенной интоксикацией [14].
Определенный интерес представляют исследования, проведенные Пархомовой Р.А. и соавт. Авторами была отмечена клиническая картина, которая наблюдается у пациентов с острым панкреатитом, которые находятся в тяжелом состоянии. Так, у многих отмечается выраженное нарушение иммунного статуса, изменяются реологические свойства и характеристики крови. При тяжелом течении острого панкреатита отмечается абсолютная лимфопения. В первую очередь, обращает на себя внимание снижение содержания Т-хелперов (16,2±1,4). В гуморальном звене было отмечено уменьшение концентрации иммуноглобулинов А и М (2,4±0,08 и 1,4±0,03 соответственно). Было зарегистрировано незначительное снижение Т-супрессоров (26,8±1,8).
Состояние сопровождается развитием выраженных интоксикационных процессов, которые затрагивают все клетки и ткани организма. Это приводит к изменению морфологических характеристик клеточных мембран, к изменению молекулярной структуры, к развитию функциональных особенностей. Также происходит изменение содержания уровня макро- и микроэлементов в клетке. Внутри клетки развивается гипокалиемия. Отмечается достоверно значимое повышение уровня ионов кальция в крови, что может указывать на повреждение клеточных структур, на развитие апоптоза. По мере нарастания интоксикации, присоединения инфекционного и воспалительного процесса, гипокалиемия возрастает. Снижается уровень кислорода в крови, развивается гипоксия, гиперкапния, происходит разрушение клеточных структур. Наблюдается прямая корреляция между ростом выраженности эндогенной интоксикации и развитием гипоксии, так как по мере роста ИЭИ, резко снижается концентрация кислорода во внутриклеточном пространстве.
Воспалительная реакция усугубляет ситуацию, поскольку по мере развития воспаления в очаг воспаления проникают цитокины, факторы воспаления, тканеразрушающие энзимы. Уровень провоспалительных цитокинов находится прямой корреляционной зависимости с тяжестью состояния при остром панкреатите. При этом особенности патогенеза, степень тяжести, характер повреждения не зависят от этиологического фактора.
Доказаны процессы взаимосвязи воспаления, эндотелиальной дисфункции и иммунной недостаточности, приводящей к развитию полиорганной недостаточности и генерализации воспалительной реакции, являющиеся основными признаками тяжелого течения острого некротизирующего панкреатита. Проявлением синдрома системной воспалительной реакции является развитие эндотелиальной недостаточности, приводящей к синтезу и активации биологически активных веществ, оказывающих влияние на систему гемодинамики, гемостаза, иммунные реакции и процессы регенерации. Сложная взаимосвязь между синдромом системной воспалительной реакции и иммунной недостаточностью приводит к развитию генерализации инфекции и развитию полиорганной недостаточности при остром некротическом панкреатите в раннюю фазу.
Перитонит, интоксикация, различные виды шока являются следствием системной воспалительной реакции, снижения иммунитета [15].
Согласно клиническим рекомендациям, наиболее распространенной формой перитонита, с которой сталкиваются хирурги, является разлитой гнойный перитонит. Помимо этого, выделяют отдельную категорию – холецисто-панкреатиче-ский перитонит, возникающий при холециститах, желчном перитоните без перфорации желчного пузыря, деструктивном панкреатите и других сопутствующих заболеваниях. Его частота составляет 10–12 % случаев [16].
Перитонит развивается в несколько этапов. На начальном реактивном этапе в первые часы болезни доминирует болевой синдром, сопровождающийся тошнотой, задержкой стула и газов, напряжением мышц живота, появлением симптомов раздражения брюшины, тахикардией, повышенной температурой и сухостью во рту [17].
На следующей, токсической стадии (2–3 сутки) состояние пациента ухудшается: он становится беспокойным, появляется одышка, лицо приобретает заостренные черты, язык пересыхает. Развиваются признаки пареза кишечника: вздутие живота, снижение тонуса брюшной стенки по сравнению с реактивным этапом, отсутствие перистальтики, запор, усиление рвоты с примесью кофейной жидкости. Нарастают лейкоцитоз с выраженным сдвигом лейкоформулы влево, нарушения функций органов, печеночная и почечная недостаточность вследствие интоксикации [18].
На терминальной стадии (3–4 сутки) создается ложное впечатление улучшения из-за ослабления болей в животе [19]. Однако фактически признаки интоксикации нарастают: заостряются черты лица, глаза западают, появляется страдальческое выражение, усиливается сухость языка, вздутие живота, пациент неподвижен, участились эпизоды рвоты желчью или кишечным содержимым, пульс учащается и становится слабым, дыхание поверхностным без участия мышц передней брюшной стенки [20].
Заключение
Типичными признаками, которые оказывают на развитие острых форм панкреатита, выступает острая боль в животе, рвота, высокая температура, лихорадка, повышенная чувствительность и сенсибилизация в области живота. Неконтролируемый выброс провоспалительных цитокинов в системный кровоток в ответ на активацию протеолитических ферментов и деструкцию тканей при остром панкреатите являются пусковым механизмом формирования синдрома системного воспалительного ответа (ССВО). Данный процесс сопровождается развитием таких патологических состояний, как эндогенная интоксикация, оксидативный стресс, гипоксия, липидный дистресс-синдром и нарушения в системе гемостаза, приводящих к значительным расстройствам гомеостаза организма. Эндогенная интоксикация, в свою очередь, является ключевым звеном в развитии различных осложнений, включая токсемию, тканевую гипоксию и функциональную недостаточность систем детоксикации организма. Одним из осложнений является эффект кардиодепрессии.
Острый деструктивный панкреатит сопровождается нарушением силовых и скоростных параметров сократимости миокарда, что клинически проявляется снижением систолического давления, замедлением скоростей сокращения и расслабления миокарда левого желудочка, повышением диастолического давления вследствие контрактурных сокращений кардиомиоцитов.
Результаты проведенного нами исследования показали, что на втором месте по частоте встречаемости был такой диагноз, как некроз поджелудочной железы – 10,8 % пациентов. На третьем месте – хронический панкреатит – 8,8 %. У пациентов наблюдаются такие осложнения, как перитонит, интоксикация, различные виды шока, флегмона, некроз брюшины, что приводит к летальному исходу. Среди всех осложнений чаще всего встречается интоксикация (63 % случаев). На втором месте – перитонит (28,5 %), на третьем – различные другие виды шока (7,5 % случаев). Во многих клинических случаях наблюдалась сочетанное проявление перитонита и интоксикации, в связи с чем развивались тяжелые полиорганные нарушения, в том числе, нарушения функционирования сердечно-сосудистой системы, кардиодепрессия.
Результаты гистологического исследования указывают на наличие у пациентов ряда изменений со стороны кардиомиоцитов, сердечной мышцы. Была выявлена достоверно значимая корреляционная зависимость между состоянием тканей сердечной мышцы и выраженностью отека. У многих пациентов, которые изначально поступили с острым или хроническим панкреатитом, осложненным впоследствии перитонитом, интоксикацией, кардиомиоциты располагались правильными рядами, ядра были овальными, располагались в центре клеток. У таких пациентов наблюдался умеренный интерстициальный отек.
У пациентов с выраженным перитонитом и сильной интоксикацией наблюдалась умеренная гипертрофия кардиомиоцитов,полнокровие сосудов, умеренный межуточный и перидуктальный кардиосклероз. При этом у многих пациентов наблюдался выраженный отек межклеточного пространства. У пациентов с выраженной гипертрофией кардиомиоцитов, наблюдался выраженный интерстициальный отек. Во многих микропрепаратах сердца при этом наблюдались явления мелкоочагового кардиосклероза, явления очагового ишемического повреждения. Прослеживалась прямая корреляционная зависимость между характеристиками ткани и выраженностью отека. То есть, чем более тяжелыми были нарушения кардиомиоцитов, их гипертрофия, тем более выраженным и тяжелым был отек окружающих тканей. И наоборот, незначительные изменения кардиомиоцитов, сердечной ткани сопровождались незначительным, умеренным отеком.


