Эффективность, безопасность и переносимость генноинженерного биологического препарата инфликсимаба у больных анкилозирующим спондилитом
Автор: Тюрин В.П., Мезенова Татьяна Валентиновна, Давидьян С.Ю., Елонаков А.В.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 2 т.7, 2012 года.
Бесплатный доступ
Представлены результаты изучения эффективности, безопасности и переносимости инфликсимаба у больных анкилозирующим спондилитом.
Анкилозирующий спондилит, лечение
Короткий адрес: https://sciup.org/140188079
IDR: 140188079 | УДК: 616.711-002:615.36
Текст научной статьи Эффективность, безопасность и переносимость генноинженерного биологического препарата инфликсимаба у больных анкилозирующим спондилитом
Анкилозирующий спондилит (АС) относится к группе хронических воспалительных ревматических заболеваний, объединенных по патофизиологическим, клиническим и рентгенологическим чертам. В 1963 году Американская Ассоциация Ревматологов официально одобрила термин анкилозирующий спондилит [1].
Боль в спине воспалительного характера с возможным воспалением периферических суставов и определенные внескелетные проявления являются характерными признаками этих заболеваний [2]. Распространенность АС составляет в настоящее время от 0,2% до 1,1% [3], а ежегодная заболеваемость АС – 0,5–8,2 случаев на 100 000 населения. Мужчины заболевают в 3–4 раза чаще женщин [4].
Высокая степень риска развития заболевания ассоциированна с геном главного комплекса гистосовместимости (HLA)-B27 [5, 6, 7, 8]. Корреляция была доказана для различных рас и этнических групп [6].Укрепилась концепция семейного характера АС и его связь с определенным генетическим маркером [7]. В первую очередь это позволило разделить АС и ревматоидный артрит (РА) на две разные группы заболеваний, что дало начало новой классификации. В отличие от РА, воспалительный процесс при АС поражает так называемое твердое вещество кости и хряща, и в меньшей степени синовиальную ткань. Воспалительный процесс имеет тенденцию к затуханию с образованием новой костной ткани и формированием фиброзного рубца, и, как следствие, ведет к анкилозу или необратимой оссификации аксиальных и периферических суставов [9, 10, 11].
Принципы лечения АС в настоящий момент претерпевают значительные изменения, в связи с получением более детальной информации о процессе болезни и ее исходах, совершенствованием диагностической техники, уточнением классификационных критериев и более глубоким пониманием молекулярных механизмов хронического воспаления. У пациентов АС выявлены поврежденные цитокиновые функции, особенно в отношении фактора некроза опухоли ФНО [12]. Множественные исследования в Шотландии и Германии имели своей целью изучение влияния полиморфизма ФНО-308 [13, 14, 15]. ФНО-α прямо или косвенно влияет на образование воспалительного инфильтрата и процессы деструкции хряща и костной ткани. В эндотелии ФНО-α вызывает повышение экспрессии молекул адгезии и увеличение проницаемости, сопровождающееся массивной инфильтрацией воспаленных тканей лейкоцитами. Вследствие увеличения выработки сосудистого эндотелиального фактора роста (VEGF) ФНО-α усиливает ангиогенез, стимулирует выброс матриксных металлопротеиназ – ферментов, которые вызывают разрушение тканей и приводят к необратимым изменениям.
С 2001 г. накопленный клинический опыт длительного применения ингибиторов ФНО- α в лечении РА свидетельствовал о высокой эффективности, хорошей переносимости и способности индуцировать развитие ремиссии заболевания. Близость иммунных механизмов в патогенезе РА и АС позволило применить генно-инженерные биологические препараты (ГИБП) и при АС. В настоящее время для лечения АС в России зарегистрировано три ингибитора ФНО- α – инфликсимаб, адалимумаб и этанерцепт. Инфликсимаб (ИФ) – химерное моноклональное антитело к ФНО- α изотипа IgG1 используется с 2004 г. Адалимумаб (АДА) – первое моноклональное антитело к ФНО- α , структурно и функционально полностью идентичное человеческому иммуноглобулину G1 (IgG1),

Тюрин В.П., Мезенова Т.В., Давидьян С.Ю., Елонаков А.В.
ЭФФЕКТИВНОСТЬ, БЕЗОПАСНОСТЬ И ПЕРЕНОСИМОСТЬ ГЕННО-ИНЖЕНЕРНОГО БИОЛОГИЧЕСКОГО ПРЕПАРАТА ИНФЛИКСИМАБА У БОЛЬНЫХ АНКИЛОЗИРУЮЩИМ СПОНДИЛИТОМ применяется для лечения АС с 2006 г. Этанерцепт является растворимым рецептором ФНО-α, зарегистрирован для лечения АС в 2009 г. Высокая эффективность, хорошая переносимость препаратов были доказаны в двойных слепых, плацебо-контролируемых, рандомизированных исследованиях у больных АС и подтверждены при многолетних (более 8 лет) наблюдениях [16, 17, 18,19].
В 2010 г. опубликованы результаты первого многоцентрового открытого 54-недельного исследования в России по применению ИФ у 42 больных АС. Результаты исследования свидетельствовали о высокой эффективности ИФ у большинства больных АС [20].
Целью нашего исследования является оценка эффективности ИФ у пациентов АС, уделяя особое внимание на клинические проявления болезни, лабораторные маркеры воспаления, а также уточнение частоты и спектра нежелательных явлений.
Материал и методы исследования
Обследовано 53 пациента с АС, у которых на протяжении последних 3-х месяцев установлена неэффективность (непереносимость) НПВП в максимально переносимых дозах, сульфасалазина, метотрексата, ГКС и сохранялась активная фаза заболевания в течение 4-х недель (индекс активности BASDAI>4). ИФ вводили внутривенно в дозе 3–5 мг/кг массы тела с интервалом введения 0, 2, 6 недель и далее каждые 8 недель. Характеристика больных АС до начала генно-инженерной терапии ИФ представлена в таблице 1.
Эффективность терапии оценивали по индексам активности заболевания BASDAI, ASDAS; индексам повседневной функциональной активности суставов и позвоночника BASFI, BASMI; критериям ремиссии по Международной ассоциации по изучению АС (ASAS).
Индекс BASDAI (Bath Ankylosing Spondylitis Disease Activity Index) позволяет оценить выраженность основных клинических проявлений заболевания по визуальной аналоговой шкале (ВАШ) от 0 до 10 за последнюю неделю. Он включает утомляемость, боль в шее, спине, тазобедренных суставах, боль и припухание в других суставах, локальную болезненность, общий уровень утренней скованности, длительность и интенсивность утренней скованности.
Табл. 1. Общая характеристика больных АС
|
Мужчины / женщины, n |
42 / 11 |
|
Возраст, лет |
35 ± 9 |
|
Длительность заболевания, лет |
13,9 ± 7,5 |
|
Периферический артрит, % |
36 (67%) |
|
Системные проявления,% |
37 (69%) |
|
Сульфасалазин/метотрексат |
27 / 18 |
|
ГКС внутрь |
13 |
|
Активность по ASDAS. Умеренная/Высокая |
23 / 34 |
|
Индекс BASDAI (0–10) |
8,3 ± 3,7 |
|
Индекс BASFI (0–10) |
6,2 ± 2,5 |
|
Индекс BASMI |
19,4 ± 8,1 |
Индекс ASDAS (Ankylosing Spondylitis Disease Activity Score), включает: боль в шее, спине или тазобедренных суставах за последнюю неделю; боль/припухлость периферических суставов; продолжительность утренней скованности; общую оценку активности заболевания пациентом и уровень СРБ. Высокой активности заболевания соответствовали значения ASDAS более 4,5; умеренной активности – менее 4,5 и более 1,9; низкой активности – менее 1,9 [21].
Индекс BASFI (Bath AS Functional Index) оценивает физическую функцию, способность больных АС справляться с повседневными делами по ВАШ (от 0 до 10).
Оценка динамики позвоночных индексов основана на изучении объема движений в шейном, грудном и поясничном отделах позвоночника, а также тазобедренных суставов, мягких тканей таза.
Индекс BASMI (Bath Ankylosing Spondylitis Metrology Index) определяет изменения двигательной функции локомоторного аппарата, включающих 5 клинических измерений: ротация в шейном отделе позвоночника – измерение угла поворота головы вправо и влево (от 0 до 90 градусов), расстояние от затылка до стены, боковое сгибание позвоночника, модифицированный тест Шо-бера, расстояние между лодыжками (оценка функции тазобедренных суставов) по 10-бальной шкале. Чем выше индекс BASMI, тем более ограничены движения пациента.
Критерии ремиссии по ASAS при АС, включали глобальную оценку самочувствия пациента по ВАШ (0–10), боль – оценка по ВАШ за последние 2 дня (0–10), функцию локомоторного аппарата по BASFI (0–10), выраженность и продолжительность утренней скованности (2 последних вопроса индекса BASDAI) [22].
Лабораторные параметры представлены клиническими анализами крови и мочи, биохимическими исследованиями крови, СРБ, типированием HLA-B27.
На основании клинико-лабораторной динамики регистрировали нежелательные явления терапии ИФ.
Оценку эффективности терапии проводили через 12, 24 и 48 недель.
Результаты собственных исследований
Через 12 недель терапии ИФ отмечена выраженная клинико-лабораторная динамика: снижение СОЭ, СРБ более чем в 2 раза, повышение уровня гемоглобина. На протяжении 24 и 48 недель терапии более существенная лабораторная динамика достигнута в группе ИФ и к концу 48 недели лечения в этой группе достигнуто снижение СОЭ более чем в 3 раза, СРБ – в 6 раз.
Исходно высокая активность АС по индексу ASDAS установлена у 34 (62%) пациентов. Спустя 12 недель от начала терапии существенно уменьшилась активность АС у 69% (37 из 53) и стала минимальной – у 49% (18 из 37) пациентов. Через 24 недели высокая активность воспалительного процесса сохранялась у 2 (4%) пациентов, умеренная – у 21 (50%) и низкая – у 19 (45%) пациентов.
Тюрин В.П., Мезенова Т.В., Давидьян С.Ю., Елонаков А.В.
ЭФФЕКТИВНОСТЬ, БЕЗОПАСНОСТЬ И ПЕРЕНОСИМОСТЬ ГЕННО-ИНЖЕНЕРНОГО БИОЛОГИЧЕСКОГО ПРЕПАРАТА ИНФЛИКСИМАБА У БОЛЬНЫХ АНКИЛОЗИРУЮЩИМ СПОНДИЛИТОМ
К концу 48 недели наблюдения показатели индекса ASDAS оставались стабильными (рис.1).
Анализ эффективности терапии по индексу болезни BASDAI спустя 12 недель от начала лечения и на протяжении 24 и 48 недель терапии также показал значительное снижение клинической активности АС. Среднее значение к концу 12 недели лечения составило 5,5 ± 2,5 балла, через 24 недели – 4,3 ± 2,0 и 48 недель – 3,8 ± 2,0 баллов. Спустя 48 недель терапии частичная ремиссия (BASDAI < 4 баллов) достигнута у 24 (64%) пациентов (рис. 2).
Функциональное состояние опорно-двигательного аппарата, оцениваемое с помощью индекса BASFI (рис. 2) показало, что существенные изменения произошли уже через 12 недель лечения. Среднее значение индекса уменьшилось более чем в 2 раза и составило 4,2 ± 2,2 балла. Через 24 и 48 недель лечения было стабильное улучшение функциональной способности по сравнению с исходными значениями. Низкий уровень BASFI констатирован у 25 (67%) пациентов, у 9 (24%) – функциональные нарушения отсутствовали.
Результаты исследования двигательной функции локомоторного аппарата, определяемые по индексу BA-SMI, показали снижение ограничения объема движений у пациентов. На терапии ИФ через 12 недель лечения индекс BASMI уменьшился до 16,1 ± 7,3 балла, через 24 и 48 недел – до 14,1 ± 5,3 и 13,6 ± 4,8 балла соответственно (рис. 2).
Клинически и статистически значимая положительная динамика констатирована в отношении большинства анализировавшихся позвоночных индексов.
На фоне терапии ИФ установлено достоверное увеличение объема движений в позвоночнике уже в ранние сроки лечения. Статистически достоверно улучшились ротация шейного отдела (на 6 градусов), экскурсия грудной клетки (на 1 см), боковое сгибание в позвоночнике (на 5 см), снизился симптом Томайера (более 20 см). Такая положительная динамика подтверждает, что ограничение функции позвоночника у данных пациентов были вследствие активного воспаления, а не из-за структурных изменений в нем.
Суммарный эффект лечения ИФ в нашем исследовании оценивался с помощью критериев ремиссии ASAS. Уже к концу 24 недели терапии констатирована положительная динамика (клиническое улучшение на 20% или
Табл. 2. Динамика лабораторных показателей больных АС при терапии ИФ
|
Показатели |
До лечения n=53 |
12 недель n=53 |
24 недели n=42 |
48 недель n=37 |
|
СОЭ, мм/час |
37,7 ± 18,9 |
19,6 ± 13,4 p < 0,001 |
17,9 ± 14,7 p < 0,001 |
19,0 ± 16,8 p < 0,001 |
|
СРБ, мг/л |
39,8 ± 37,2 |
10,5 ± 15,5 p < 0,001 |
9,4 ± 28,8 p < 0,001 |
7,8 ± 24,0 p < 0,001 |
|
Гемоглобин г/л |
125,9 ± 18,8 |
133,2 ± 17,0 p < 0,001 |
134,7 ± 18,4 p < 0,001 |
137,5 ± 20,4 p < 0,001 |
Примечание: n – число больных, p – стандартное отклонение по сравнению с исходными данными.
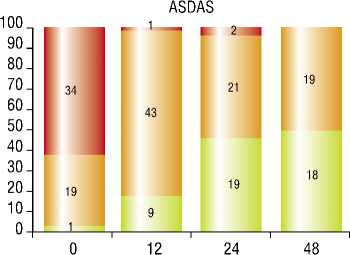
I ■ Высокая (> 4,5)
Умеренная (> 1,9; < 4,5)
Низкая (< 1,9)
Рис. 1. Динамика индекса ASDAS на фоне терапии ИФ
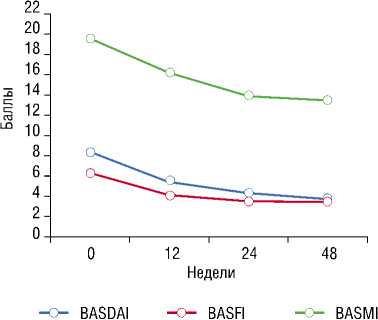
Рис. 2. Динамика индексов BASDAI, BASFI, BASMI больных АС при терапии ИФ
Табл. 3. Динамика позвоночных индексов больных АС при терапии ИФ
|
Показатели |
До лечения n=53 |
12 недель n=53 |
24 недели n=42 |
48 недель n=37 |
|
Ротация шейного отдела позвоночника, ° |
36,3 ± 14,9 |
42,5 ± 14,8 p < 0,001 |
41,0 ± 12,4 p < 0,001 |
37,5 ± 20,1 p > 0,07 |
|
Симптом подбородок-грудина, см |
1,4 ± 2,0 |
1,0 ± 1,8 p < 0,02 |
1,1 ± 1,7 p < 0,01 |
1,0 ± 1,5 p < 0,01 |
|
Симптом Томайера, см |
33,6 ± 38,9 |
18,9 ± 34,0 p < 0,01 |
10,8 ± 18,5 p < 0,002 |
10,5 ± 18,7 p < 0,01 |
|
Экскурсия грудной клетки, см |
4,1 ± 2,1 |
4,9 ± 1,8 p < 0,001 |
4,6 ± 1,6 p < 0,002 |
4,8 ± 1,5 p < 0,003 |
|
Расстояние затылок-стена, см |
3,7 ± 5,3 |
2,9 ± 4,9 p < 0,01 |
3,5 ± 5,2 p < 0,001 |
3,5 ± 5,3 p < 0,001 |
|
Боковое сгибание позвоночника, см |
12,2 ± 6,8 |
15,3 ± 7,3 p < 0,001 |
15,1 ± 7,9 p < 0,001 |
16,8 ± 7,2 p < 0,001 |
|
Тест Шобера, см |
2,8 ± 1,4 |
3,6 ± 1,3 p < 0,001 |
3,8 ± 1,5 p < 0,001 |
4,0 ± 1,2 p < 0,001 |
Примечания: n – число больных, p – стандартное отклонение по сравнению с исходными данными.

Тюрин В.П., Мезенова Т.В., Давидьян С.Ю., Елонаков А.В.
ЭФФЕКТИВНОСТЬ, БЕЗОПАСНОСТЬ И ПЕРЕНОСИМОСТЬ ГЕННО-ИНЖЕНЕРНОГО БИОЛОГИЧЕСКОГО ПРЕПАРАТА ИНФЛИКСИМАБА У БОЛЬНЫХ АНКИЛОЗИРУЮЩИМ СПОНДИЛИТОМ на >10 единиц, как минимум 3 из 4 показателей). Среднее значение снизилось с 33,1 ± 9,5 до 19,4 ± 9,0 единиц у 69% (37 из 53) пациентов (рис. 3).
Оценка переносимости и безопасности инфликсимаба
Переносимость ИФ была удовлетворительной. Серьезные нежелательные явления (НЯ) были отмечены только у 2-х пациентов. На 12-й неделе лечения развилась аллергической реакции в виде припухлости левого века, першения в горле, в связи с чем препарат был отменен. После 24 недель терапии у 1-го больного развился периодонтит, что послужило поводом для временной отмены ИФ до полного выздоровления (табл. 4).
После 12 и 24 недель терапии у 2 пациентов отмечено умеренное повышение лейкоцитов, тромбоцитов в клиническом анализе крови. У 6 пациентов констатировано транзиторное повышение печеночных ферментов более 2-х норм, нормализовавшиеся после курса лечения «ге-патопротекторами». Терапия блокаторами ФНО- α была продолжена. У 2-х больных через 24 недели терапии ИФ установлено нарастание клинико-лабораторной активности, в связи с чем ИФ был заменен на АДА. У 6-х пациентов после 24-х недель и 48-ми недель отмечено транзиторное нарастание уровня креатинина до 153м-кмоль/л (норма до 120). Терапия ИФ временно прекращена только у 1-го больного в связи с госпитализацией в стационар и проводимым оперативным вмешательством: биопсией почки. Таким образом, частота НЯ установлена у 37% (20) пациентов. Случаев смерти, злокачественных опухолей или туберкулеза в нашем исследовании зарегистрировано не было.
Обсуждение результатов
Результаты исследования показали, что ИФ высоко эффективны у большинства больных АС. К концу 12 недели лечения ИФ достигнута нормализация СОЭ у 69% пациентов. Через 24 недели и 48 недель уровень СОЭ оставался стабильно низким у 67% пациента. Уровень СРБ после 12 недель терапии нормализовался у 64%, после 24-х и 48 недель – у 78% и 72% больных соответственно. Через 12 недель лечения ИФ снижение индекса активности болезни BASDAI на 50% было достигнуто у 47% больных (р < 0,05), а после 24-х недель – у 66% пациентов (р < 0,05). Положительный эффект терапии сохранялся и через 48 недель у 70%. После 12-недельной терапии существенно уменьшилась активность АС, определяемая по индексу ASDAS, у 69% и стала минимальной у 49% больных к окончанию исследования. Улучшение физической функции (индекс BASFI) на 2 балла констатировано у 56% больных (р < 0,05) после 12 недель лечения, у 64% пациентов через 24 недели лечения.
У пациентов на терапии ИФ установлена положительная динамика в отношении анализировавшихся позвоночных индексов. Отмечено увеличение ротации шейного отдела позвоночника (с 36,3 ± 14,9 до 42,5 ± 14,8 и 41,0 ± 12,4 соответственно через 12 и 24 недель, р < 0,001);
Критерии ремиссии
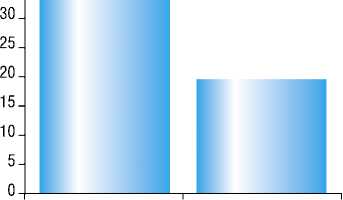
Рис. 3. Динамика критериев ремиссии по ASAS при терапии ИФ
Табл. 4. НЯ, зарегистрированные у пациентов на фоне терапии ИФ
Переносимость ИФ была, в целом, удовлетворительной. Частота развития серьезных НЯ в нашем исследовании меньше по сравнению с данными регистра BIOBADASER (Испания), где НЯ выявлены у 5,8% (102 из 1915) больных различными спондилоартропатиями, в том числе АС [23]. Общая частота НЯ установлена нами у 38% (20 из 53) пациентов была меньше, чем в сообщениях других авторов. M. Breban и соавт. (2002) выявили НЯ у 80% (40 из 50), а Schiff M. и соавт. (2008) – у 52,1% (86 из 165) больных [24, 25]. Наиболее частыми НЯ было повышение печеночных ферментов у 11% пациентов. Серьезные НЯ, послужившие причиной отмены ИФ, наблюдали у 1-го пациента – это развитие аллергической реакции по типу крапивницы. Уменьшение эффективности терапии ИФ установлена у 2 (3%) из 53 больных потребовавшее замены ИФ на адалимумаб.
Выводы
-
1. На ранних сроках лечения достигнуты нормализация острофазовых показателей воспаления и достоверное улучшение по индексам BASDAI, ASDAS и BASFI.
-
2. Эффективность ИФ констатирована уже в течение первых 12 недель лечения. 50% улучшение отмечали
-
3. Нежелательные явления, связывавшиеся с применением ИФ, выявлены у 38%пациентов. Для предотвращения НЯ, побочных эффектов необходимо предварительное исключение сопутствующих инфекций, постоянное повышенное внимание к возможному развитию инфекций в процессе лечения, динамический контроль лабораторных показателей.
Тюрин В.П., Мезенова Т.В., Давидьян С.Ю., Елонаков А.В.
ЭФФЕКТИВНОСТЬ, БЕЗОПАСНОСТЬ И ПЕРЕНОСИМОСТЬ ГЕННО-ИНЖЕНЕРНОГО БИОЛОГИЧЕСКОГО ПРЕПАРАТА ИНФЛИКСИМАБА У БОЛЬНЫХ АНКИЛОЗИРУЮЩИМ СПОНДИЛИТОМ у 47% пациентов, сохранявшееся на протяжении всего периода терапии.
Список литературы Эффективность, безопасность и переносимость генноинженерного биологического препарата инфликсимаба у больных анкилозирующим спондилитом
- Russel AS. History. In: Hochberg M, et al., eds. Rheumatology. Section 9: Spondylоarthropathies. Spain: Elsevier 2003; 1145.
- Khan MA. Clinical features of ankylosing spondylitis. In: Hochberg M, et al., eds. Rheumatology. Section 9: Spondylоarthropathies. Spain: Elsevier 2003; 1161-1181.
- Cruyssen B.V., Ribbens C., Boonen A. et al. The epidemiology of ankylosing spondylitis and the commencement of anti-TNF therapy in daily rheumatology practice. Ann Rheum Dis 2007; 66: 1072-1077.
- Lee W., Reveille J.D., Weisman M.H. Women With Ankylosing spondylitis: A Review. Arthr & Rheum. March 15, 2008; 59: N.3. 449-454.
- Brown M, Wordworth В, Reveille J. Genetics of ankylosing spondylitis. Clin Exp Rheumatol 2002; 20 (Suppl. 28): 43-49.
- David CS. The mystery of HLA-B27 and disease. Immunogenetics. 1997; 46: 73-77.
- Bluestone R. Identification of associations with HLA-B27. Milestones Rheumatol Patient Care 1988; 31: 15-24.
- Khan MA. Thoughts concerning the early diagnosis of ankylosing spondylitis and related diseases. Clin Exp Rheumatol 2002; 20: S6-S10.
- Vernon-Roberts B, Hochberg М, et al. Ankylosing spondylitis: pathology. Rheumatology. Section 9: Spondylarthropathies. Spain: Elsevier 2003; 1205.
- Koehler L, Hochberg M, Kuipers J, et al. Enthesopathy. Rheumatology. Section 9: Spondylarthropathies. Spain: Elsevier 2003; 1275-1281.
- Morris R, Metzger A, Bluestone R. HLA B27-a useful discriminator in the arthropathies of inflammatory bowel disease. N Engl J Med 1974; 290: 1117-1119.
- Rudwaleit M, Siegert S, Yin Z, et al. Low T cell production of TNFa and IFNa in ankylosing spondylitis: its relation to HLA B27 and influens of the TNF-308 gene polymorphism. Ann Rheum Dis. 2001; 60: 36-42.
- Milicic A, Lindheimer F, Laval S, et al. Interethnic studies of the TNF polymorphism confirm the likely presense of a second MHC susceptibility locus in ankylosing spondylitis. Genes Immun 2000; 1: 418-422.
- McGarry F, Walker R, Sturrock R, Field M. The-308.1 polymorphism in the promoter region of the tumor necrosis factor gene is associated with ankylosing spondylitis independent of HLA B27. J Rheumatol 1999; 26: 1110-1116.
- Hohler T, Schaper T, Schneider PM, Meyer zum Buschenfelde KH, MarkerHermann E. Association of different tumor necrosis factor a promoter allele frequencies with ankylosing spondylitis in HLA B27 positive individuals. Arthritis Rheum. 1998;41:1489-1492.
- Braun J, Brandt J, Listing J, et al. Treatment of active ankylosing spondylitis with infliximab: a randomized controlled multicentr trial Lancet. 2002; Vol. 359: 1187-1193.
- Van den Bosch F, Kruithof E, Baeten D, et al. Effects of a loading dose regimen of three infusions of chimeric monoclonal antibody to tumor necrosis factor a (infliximab) in spondylarthropathies an open pilot study. Ann Rheum Dis 2000; Vol. 59: 428-433.
- Baraliakos X, Listing J, Brandt J, et al. Clinical response to discontinuation of anti-TNF therapy in patients with ankylosing spondylitis after 3 years of continuous treatment with infliximab. Arthritis Res Therapy 2005; Vol. 7: 439-444.
- Baraliakos X, Listing J, Brandt J, et al. Persistent clinical response to the anti TNF-a antibody infliximab in patients with ankylosing spondylitis over 3 years. Rheumatol. 2005. Vol. 44: 670-676.
- Бунчук Н.В., Румянцева О.А., Логинова Е.Ю., и др. Эффективность и безопасность инфликсимаба у больных анкилозирующим спондилитом: результаты открытого многоцентрового исследования. Терапевтический архив 2010; №10: С. 41-46.
- Pedersen S.J. Responsiveness of the Ankylosing spondylitis Disease Activity Score (ASDAS) and clinical and MRI measures of disease activity in a 1-year follow-up study of patients with axial spondyloarthritis treated with tumor necrosis factor a inhibitors/S. J. Pedersen, I.J. Sorensen, O.R. Madsen//Ann Rheum Dis. 2010; 69: 1065-1071.
- Anderson JJ, Baron G, van der Heijde D et al. Ankylosing spondylitis assessment group preliminary definition of shorttrm improvement in ankylosing spondylitis. Arthritis Rheum 2001; 44: 1876-86.
- Loreto Carmona, Juan J Gomez-Reino and on behalf of the BIOBADASER Group Survival of TNF antagonists in spondyloarthritis is better than in rheumatoid arthritis Data from the Spanish registry BIOBADASER Arthritis Research & Therapi. 2006; R:72 () DOI: 10.1186/ar1941
- Breban M. Efficacy of infliximab in refractori ankylosing spondylitis results of a six-month open-label stady. Rheumatology 2002; 41: 1280-1285.
- Schiff M, Keiserman M, Codding С, et al. Efficacy and safety of abatacept or infliximab vs placebo in ATTEST: a phase III, multi-centre, randomised, double-blind, placebo-controlled study in patients with rheumatoid arthritis and an inadequate response to methotrexate. Ann Rheum Dis 2008; 67: 1096-1103.


