Эффективность и безопасность комбинированной хирургии катаракты и глаукомы у пациентов с подвывихом хрусталика и псевдоэксфолиативным синдромом
Автор: Ходжаев Н.С., Сороколетов Г.В., Колышева О.С., Таевере М.Р.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4S1 т.20, 2025 года.
Бесплатный доступ
Цель: Оценить эффективность и безопасность комбинированного хирургического подхода при лечении пациентов с ПОУГ и катарактой, осложненных подвывихом хрусталика I-II степени на фоне псевдоэксфолиативного синдрома. Материалы и методы: В исследование включены 40 пациентов (40 глаз) с ПОУГ II-III стадии, катарактой и подвывихом хрусталика I-II степени на фоне ПЭС. Всем пациентам выполнено одномоментное комбинированное вмешательство: ФЭК с имплантацией ИОЛ по технологии «optic capture» и НГСЭ с имплантацией коллагенового дренажа Healaflow. Результаты: Через 12 месяцев наблюдения отмечено значительное улучшение НКОЗ с 0,12±0,04 до 0,38±0,06 при II стадии и с 0,04±0,02 до 0,40±0,08 при III стадии глаукомы (p<0,001). ВГД снизилось до 16,4±2,1 мм рт.ст. и 17,0±1,9 мм рт.ст. соответственно (p<0,001). Гипотензивная терапия отменена у 85% пациентов со II стадией и 80% с III стадией заболевания. Заключение: Комбинированное хирургическое лечение продемонстрировало высокую эффективность и безопасность у пациентов с сочетанной патологией.
Катаракта, глаукома, подвывих хрусталика, псевдоэксфолиативный синдром, комбинированная хирургия, непроникающая глубокая склерэктомия
Короткий адрес: https://sciup.org/140312700
IDR: 140312700 | DOI: 10.25881/20728255_2025_20_4_S1_4
Efficacy and safety of combined cataract and glaucoma surgery in patients with lens subluxation and pseudoexfoliation syndrome
Objective: To evaluate the efficacy and safety of a combined surgical approach in patients with primary open-angle glaucoma and cataract complicated by grade I–II lens subluxation in the setting of pseudoexfoliation syndrome. Materials and methods: The study included 40 patients (40 eyes) with POAG stages II–III, cataract, and grade I–II lens subluxation associated with PEX. All patients underwent simultaneous combined surgery: phacoemulsification with IOL implantation using the optic capture technique and non-penetrating deep sclerectomy with implantation of a Healaflow collagen drain. Results: At 12 months after surgery, a significant improvement in uncorrected visual acuity (UCVA) was observed: from 0.12±0.04 to 0.38±0.06 in stage II glaucoma and from 0.04±0.02 to 0.40±0.08 in stage III glaucoma (p<0.001). Intraocular pressure (IOP) decreased to 16.4±2.1 mmHg and 17.0±1.9 mmHg, respectively (p<0.001). Antihypertensive therapy was discontinued in 85% of patients with stage II and 80% with stage III glaucoma. Conclusion: Combined surgical treatment demonstrated high efficacy and safety in patients with this complex ocular pathology.
Текст научной статьи Эффективность и безопасность комбинированной хирургии катаракты и глаукомы у пациентов с подвывихом хрусталика и псевдоэксфолиативным синдромом
Хирургическое лечение пациентов с такой сочетанной патологией сопряжено со значительными техническими трудностями и высоким риском интра- и послеоперационных осложнений [4,5,8]. В частности, при слабости цинновой связки стандартная факоэмульсификация катаракты требует серьезной модификации, включая использование капсульных колец или ретракторов для стабилизации капсульного мешка. Выбор оптимального метода фиксации интраокулярной линзы (ИОЛ) – будь то имплантация в капсульный мешок, транссклеральная фиксация или ирис-фиксация – является предметом дискуссий и требует индивидуального подхода, основанного на степени подвывиха и выраженности слабости связочного аппарата [4; 8].
Не менее важен вопрос выбора антиглаукомной операции при комбинированном вмешательстве. Непроникающая глубокая склерэктомия (НГСЭ) демонстрирует хорошие результаты, однако их эффективность в условиях нестабильности хрусталика требует дальнейшего изучения [8; 10]. В настоящее время общепризнанным преимуществом обладает подход одномоментного хирургического лечения катаракты и глаукомы, который

позволяет снизить совокупный хирургический риск, сократить период реабилитации и уменьшить медикаментозную нагрузку на пациента [10].
Несмотря на существующий объем знаний по отдельности в области хирургии катаракты и глаукомы, комбинированные операции у пациентов с ПОУГ, осложненной подвывихом хрусталика на фоне ПЭС, остаются недостаточно изученными. Это диктует необходимость проведения дальнейших исследований, направленных на разработку стандартизированных хирургических алгоритмов и оценку их долгосрочной эффективности и безопасности.
Цель исследования
Оценить эффективность и безопасность комбинированного хирургического подхода при лечении пациентов с первичной открытоугольной глаукомой и катарактой, осложненных подвывихом хрусталика I-II степени на фоне псевдоэксфолиативного синдрома.
Материалы и методы
В исследовании участвовали 40 пациентов (40 глаз) с сочетанием ПОУГ II–III стадии, катаракта и подвывих хрусталика I–II степени на фоне ПЭС. Исследуемую группу составили 23 мужчины (57,5%) и 17 женщин (42,5%) в возрасте от 65 до 82 лет. По стадиям глаукомного процесса распределение было следующим: II стадия диагностирована у 25 глаз (62,5%), III стадия – у 15 глаз (37,5%). Период наблюдения составил 12 месяцев.
Всем пациентам до операции и в послеоперационном периоде проводился комплекс стандартных офтальмологических исследований в установленные сроки наблюдения (1 сутки, 1, 3, 6 и 12 месяцев). Программа обследования включала: визометрию с определением некорригированной (НКОЗ) и максимально корригированной (МКОЗ) остроты зрения с последующим раздельным анализом для II и III стадий глаукомы; исследование полей зрения (периметр Oculus Centerflield 2); тонометрию по Маклакову; биомикроскопию переднего отрезка; тонография (GlauTest-60), подсчет плотности эндотелиальных клеток роговицы (Tomey EM-3000); для оптической биометрии использовали прибор IOL-ma-ster 700; оптическую когерентную томографию (ОКТ) переднего отрезка на приборе Casia 2 (Tomey) для оценки положения интраокулярной линзы (ИОЛ) и состояния фильтрационных структур; а также ОКТ диска зрительного нерва и слоя нервных волокон сетчатки на аппарате RTVue 100 (Optovue).
Всем пациентам было выполнено одномоментное комбинированное хирургическое вмешательство. Первым этапом проводилась факоэмульсификация катаракты с последующей имплантацией трехчастной интраокулярной линзы модели MA60AC (Alcon) по технологии «optic capture». Вторым этапом выполнялась непроникающая глубокая склерэктомия (НГСЭ) с имплантацией коллагенового дренажа Healaflow. Для интраоперационной стабилизации капсульного мешка, в условиях слабости цинновой связки, использовалась установка четырех капсульных ретракторов с имплантацией внутрикапсульного кольца. В связи с часто встречающейся недостаточностью медикаментозного мидриаза, обусловленной сочетанным влиянием ПЭС и глаукомы, интраоперационно применяли механический дилататор – кольцо Малюгина.
Статистическую обработку полученных данных проводили с использованием программного пакета Microsoft Excel. Для всех количественных показателей рассчитывали среднее арифметическое значение (M) и стандартное отклонение (SD). Для оценки динамики изменений в послеоперационном периоде использовали парный t-критерий Стьюдента. Статистически значимыми считали различия при уровне p<0,05.
Результаты
До операции все пациенты характеризовались значительным снижением зрительных функций и повышением офтальмотонуса. У пациентов со II стадией глаукомы исходная НКОЗ составляла 0,12±0,04, МКОЗ – 0,36±0,08, ВГД – 26,93±3,2 мм рт.ст.; при III стадии показатели достигали 0,04±0,02, 0,14±0,06 и 27,0±2,8 мм рт.ст. соответственно. Все пациенты получали комбинированную гипотензивную терапию в среднем из 3,04±0,45 препаратов (Таблица 1).
Послеоперационный период у всех 40 пациентов протекал без интра- и ранних послеоперационных осложнений, и на протяжении 12-месячного периода наблюдения отмечалась стабильная положительная динамика функциональных и морфометрических показателей.
После выполнения комбинированного хирургического вмешательства отмечалась значительная положительная динамика зрительных функций. Через 12 месяцев наблюдения у пациентов со II стадией глаукомы НКОЗ увеличилась до 0,38±0,06 (p<0,001), МКОЗ – до 0,78±0,05 (p<0,001); при III стадии показатели улучшились до 0,40±0,08 и 0,63±0,07 соответственно (p<0,001).
Статистически значимое улучшение отмечено и в динамике офтальмотонуса. При II стадии глауко-
Табл. 1. Сравнительная характеристика пациентов до операции в зависимости от стадии первичной открытоугольной глаукомы
|
Параметр / Parameter |
Стадия II (n = 25) |
Стадия III ( n = 15) |
p-value |
|
НКОЗ |
0.12±0.04 |
0.04±0.02 |
<0.001 |
|
МКОЗ |
0.36±0.08 |
0.14±0.06 |
<0.001 |
|
ВГД мм рт.ст. |
26.93±3.2 |
27.0±2.8 |
0.941 |
|
Кол-во гипотензивных препаратов |
3.0±0.4 |
3.1±0.5 |
0.485 |
|
Длина глаза, мм |
23.75±1.05 |
23.90±1.22 |
0.678 |
|
Плотность эндотелия, кл/мм 2 |
2180±580 |
2050±710 |
0.521 |
Примечание : Данные представлены как M±SD. p-value рассчитан по t-критерию Стьюдента (для количественных).

Табл. 2. Динамика основных функциональных и морфометрических показателей через 12 месяцев после комбинированного хирургического лечения
|
Параметр |
Стадия II (n = 25) |
p-value |
Стадия III (n = 15) |
p-value |
||
|
До операции |
12 месяцев |
До операции |
12 месяцев |
|||
|
НКОЗ |
0.12±0.04 |
0.38±0.06 |
<0.001 |
0.04±0.02 |
0.40±0.08 |
<0.001 |
|
МКОЗ |
0.36±0.08 |
0.78±0.05 |
<0.001 |
0.14±0.06 |
0.63±0.07 |
<0.001 |
|
ВГД, мм рт.ст. |
26.93±3.2 |
16.4±2.1 |
<0.001 |
27.0±2.8 |
17.00±1.9 |
<0.001 |
|
MD, дБ |
-7.5±4.1 |
-6.36±4.9 |
0.038 |
-9.4±5.8 |
-7.64±7.1 |
0.026 |
|
PSD, дБ |
4.5±1.1 |
3.49±1.5 |
0.012 |
5.0±1.4 |
3.71±1.9 |
0.009 |
|
Плотность эндотелия, кл/мм 2 |
2180±580 |
2023±540 |
0.015 |
2050±710 |
1848±650 |
0.021 |
|
Толщина GCC, мкм |
68.2±7.9 |
69.8±8.1 |
0.032 |
67.2±8.4 |
68.5±8.7 |
0.041 |
|
% пациентов без терапии |
- |
85% |
- |
- |
80% |
- |
мы ВГД снизилось до 16,4±2,1 мм рт.ст., при III стадии – до 17,00±1,9 мм рт.ст. (p<0,001). Достигнутый контроль ВГД позволил полностью отменить гипотензивную терапию у 85% пациентов со II стадией и 80% с III стадией заболевания. Параллельно зарегистрировано улучшение показателей гидродинамики: коэффициент легкости оттока (С) увеличился на 68% при II стадии и на 72% при III стадии глаукомы (p<0,001), минутный объем влаги (F) снизился на 25% и 31% соответственно (p<0,001) (Таблица 2).
Оценка состояния роговицы выявила ожидаемое снижение плотности эндотелиальных клеток на 7,2% при II стадии и 9,8% при III стадии глаукомы (p<0,05), что соответствует параметрам хирургической безопасности при комбинированных вмешательствах.
При анализе ОКТ-параметров через 12 месяцев после операции отмечены следующие изменения. У пациентов со II стадией глаукомы толщина ганглиозноклеточного комплекса (GCC) увеличилась с 68,2±7,9 мкм до 69,8±8,1 мкм (p = 0,032), тогда как при III стадии зарегистрирован рост с 67,2±8,4 мкм до 68,5±8,7 мкм (p = 0,041). Динамика толщины слоя нервных волокон сетчатки (RNFL) не достигла статистической значимости: при II стадии – с 63,2±6,5 мкм до 64,1±6,9 мкм (p = 0,215), при III стадии – с 62,4±7,2 мкм до 63,2±7,4 мкм (p = 0,193). Аналогичная картина наблюдалась для площади экскавации ДЗН: при II стадии - с 0,60±0,17 мм2 до 0,58±0,15 мм2 (р = о,184), при iii стадии — с 0,62±0,19 мм2 до 0,60±0,17 мм2 (р = 0,165). Учитывая удаление катаракты и улучшение оптических сред, выявленные изменения, особенно статистически значимое увеличение толщины GCC в обеих группах, вероятнее всего, связаны с улучшением качества визуализации и точности ОКТ-измерений, а не с истинными структурными изменениями.
Анализ периметрических показателей выявил достоверное улучшение: средний дефект (MD) уменьшился на 15,2% при II стадии (p = 0,038) и на 18,7% при III стадии (p = 0,026), стандартное отклонение паттерна (PSD) снизилось на 22,4% и 25,8% соответственно (p<0,05).
Применение техники optic capture обеспечило надежную фиксацию даже в условиях исходной слабости цинновой связки: значения наклона (Tilt) сохранялись на уровне 6,91±3,26°, а децентрация (Decentration) не пре-
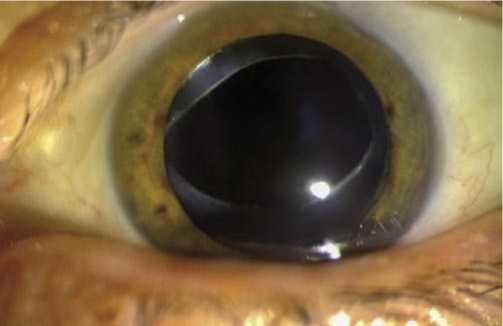
Рис. 1. Положение ИОЛ через 12 месяцев после операции.
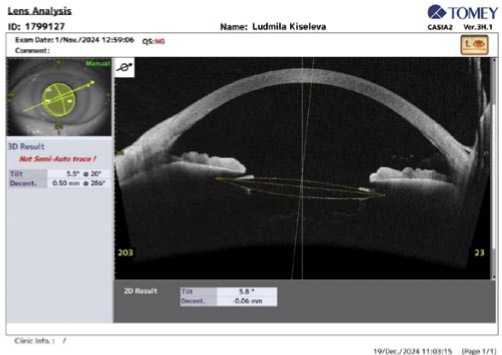
Рис. 2. ОКТ переднего отрезка глаза через 12 месяцев после операции.
вышала 0,38±0,18 мм. Статистический анализ не выявил достоверной динамики этих показателей в течение всего периода наблюдения (p > 0,05), что свидетельствует об эффективности выбранного метода фиксации (Рис. 1–2).
ОКТ зоны НГСЭ через 12 месяцев наблюдения выявила закономерное прогрессирование фиброзных изменений в зависимости от стадии глаукомы. При II стадии ПОУГ отмечалось умеренное уменьшение высоты ФП до 0,31±0,07 мм и сокращение протяженности ИСП до 1,630±0,68 мм. При III стадии эти изменения были

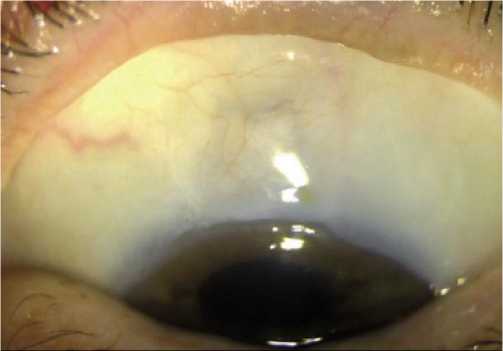
Рис. 3. Фильтрационная подушка через 12 месяцев после НГСЭ.
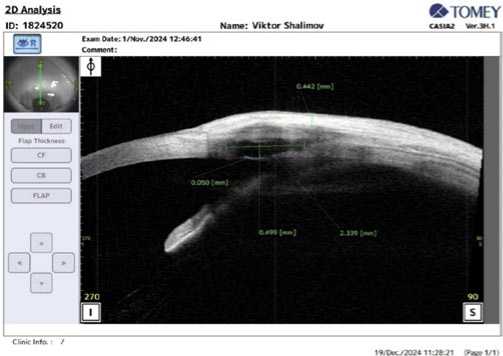
Рис. 4. ОКТ зоны НГСЭ через 12 месяцев после операции.
значительно более выражены: высота ФП уменьшилась до 0,28±0,08 мм, а протяженность ИСП составила 1,210±0,55 мм. Параллельно наблюдалось прогрессирующее утолщение ТДМ: с 0,079±0,004 мм при II стадии, до 0,086±0,005 мм при III стадии заболевания. Эта закономерность подтверждает, что исходно более тяжелое состояние дренажной системы глаза при далекозашедших стадиях глаукомы определяет менее благоприятные морфологические характеристики формирующегося фильтрационного комплекса (Рис. 3–4).
Заключение
Комбинированное хирургическое лечение продемонстрировало высокую эффективность у пациентов с сочетанной патологией. Метод обеспечил стабильное снижение ВГД с возможностью отмены гипотензивной терапии у большинства пациентов, значительное улучшение зрительных функций и надежную фиксацию ИОЛ. Полученные результаты подтверждают перспективность применения данной методики в хирургической практике. Для оценки отдаленных результатов целесообразно проведение дальнейших исследований.


