Эффективность применения феназепама в составе комплексной терапии у больных с тревожно-депрессивными расстройствами в раннем постинфарктном периоде
Автор: Стаценко М.Е., Спорова О.Е., Говоруха О.А., Бурлай С.В., Лемперт Б.А.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Рубрика: Клиническая медицина
Статья в выпуске: 3 (23), 2009 года.
Бесплатный доступ
В исследование включено 40 пациентов с тревожно-депрессивными расстройствами. Результаты исследования свидетельствуют о высокой анксиолитической активности и вегетонормализующем действии феназепама в дозе 1 мг/сутки уже через две недели терапии у пациентов с тревожным расстройством в раннем постинфарктном периоде.
Инфаркт миокарда, тревога, депрессия, феназепам
Короткий адрес: https://sciup.org/142148777
IDR: 142148777 | УДК: 616.127
The efficiency of phenazepam in combine therapy of patients with anxious and depressive disorders in the early period after myocardial infarction
40 patients with anxiety and depression were included in the research. The results of the research are testify positive influence of 1 mg phenazepam per day on anxiety and vegetative disorders in patients with anxious disorders in the early period after myocardial infarction.
Текст научной статьи Эффективность применения феназепама в составе комплексной терапии у больных с тревожно-депрессивными расстройствами в раннем постинфарктном периоде
Тревожно-депрессивные расстройства являются частыми спутниками у больных с инфарктом миокарда, при рецидивах стенокардии, прогрессировании симптомов сердечной недостаточности. Данное состояние существенно повышает уровень стрессогенности, содержание в крови катехоламинов, что нередко сопровождается увеличением частоты ангинозных приступов, аритмических событий и фатальных исходов. Поэтому своевременное выявление и устранение тревожнодепрессивных расстройств является важной задачей лечения ишемической болезни сердца (ИБС), в частности инфаркта миокарда.
Среди препаратов психотропного действия транквилизирующие (анксиолитические) средства являются одними из наиболее широко применяемых как в клинической, так и в амбулаторной практике [9].
В середине прошлого века в качестве анксиолитиков использовали барбитураты. Однако побочные эффекты и недостаточная эффективность барбитуратов как анксиолитиков активизировали поиски новых лекарственных средств для лечения тревоги. И в начале 1960-х годов появились препараты бензодиазепинового ряда, которые благодаря высокой эффективности и относительной безопасности заняли лидирующее положение в группе анксиолитиков [9].
Ярким представителем высокоэффективных анксиолитиков бензодиазепиновой структуры является отечественный препарат «Феназепам». Экспериментально установлено, что феназепам защищает миокард от гипоксии и уменьшает миокардиальную ишемию, вызванную окклюзией коронарной артерии [4], значительно подавляет эктопическую активность сердца, восста- навливает нарушение электрической проводимости сердца и уменьшает гибель животных при остром инфаркте миокарда и постинфарктном кардиосклерозе [5].
Феназепам также оказался эффективным при лечении больных с ишемической болезнью сердца [11]. При ИБС применение феназепама уже в первые дни приводит к нормализации ночного сна, уменьшению выраженности тревоги и страха за свое здоровье и жизнь, а также раздражительности и возбудимости, фиксации внимания на различных проявлениях заболевания, снижению выраженности кардиалгий, улучшению настроения и формированию более адекватной оценки своего здоровья. Отчетливое купирующее действие феназе-пам оказывает на вегетативно-сосудистые дисфункции — головную боль, потливость, дыхательную аритмию [9]. Наиболее выраженный терапевтический эффект феназепама — в 70 % случаев — был установлен при неврозоподобных расстройствах у больных ИБС [3, 7].
Важное значение для лечения пациентов с ИБС имеют установленные факты, что транквилизаторы могут обладать самостоятельным корона-ролитическим эффектом [6, 13, 15].
Транквилизаторы позволяют мягко, быстро и достаточно избирательно воздействовать на эмоциональную сферу, не вызывая при этом отрицательного влияния на гемодинамику и нормализуя ее у лиц с нарушениями вегетативной регуляции [9]. Показано, что короткие курсы анксиолитической терапии не приводят к возникновению побочных эффектов и не вызывают лекарственной зависимости [10].
В доступной нам литературе мы не встретили сообщений об исследованиях, посвященных возможности применения феназепама у пациентов с тревожно-депрессивными расстройствами в раннем постинфарктном периоде.
Таким образом, представляется целесообразным изучить терапевтическую эффективность и безопасность феназепама в составе комплексной терапии больных с тревожно-депрессивными расстройствами в раннем постинфарктном периоде.
МЕТОДИКА ИССЛЕДОВАНИЯ
В исследование включено 40 пациентов с тревожно-депрессивными расстройствами. Все включенные в исследование больные проходили стационарный этап реабилитации после инфаркта миокарда. Средний возраст — (60,4 ± 2,82) лет. Структура диагноза складывалась следующим образом: инфаркт миокарда с зубцом Q имели 62,5 %, а инфаркт миокарда без зубца Q — 37,5 % больных; постинфарктный кардиосклероз в анамнезе определялся у 20 % исследуемых. Течение подострого периода инфаркта миокарда осложнилось развитием аневризмы левого желудочка у
-
7, 5 % больных, постинфарктной стенокардией — у 20 %, нарушениями ритма (частая желудочковая и предсердная экстрасистолия, пароксизмы мерцательной аритмии) — у 12,5 %. Артериальная гипертензия отмечалась у 87,5 % пациентов.
Объективные данные о состоянии пациентов были получены при физикальном исследовании, а также с помощью эхокардиографии (ЭхоКГ) и электрокардиографии (ЭКГ). Функциональный класс хронической сердечной недостаточности (ХСН) устанавливался согласно Российским национальным Рекомендациям ВНОК и ОССН по диагностике и лечению ХСН (второй пересмотр) и теста шестиминутной ходьбы (ТШХ) [8]. Для оценки психоэмоционального состояния, проявлений вегетативной дисфункции, а также нарушений сна использовались неспецифические опросники и шкалы:
-
А. Шкала бальной оценки проявлений вегетативной дистонии — данная шкала позволяет диагностировать наличие синдрома вегетативной дисфункции. Общая сумма баллов, полученная при изучении признаков по вопроснику, у здоровых лиц не должна превышать 15, в случае повышения можно говорить о наличии синдрома вегетативной дисфункции [2].
Б. Госпитальная шкала тревоги и депрессии (HADS) — предназначена для выявления тревоги и депрессии в общесоматической практике. HADS содержит 2 подшкалы: «тревога» и «депрессия». При интерпретации результатов учитывается суммарный показатель по каждой подшкале, при этом выделяются три области его значений: 0—7 — «норма», 8—10 — «субклинически выраженная тревога/депрессия», 11 и выше — «клинически выраженная тревога/деп-рессия» [14].
-
В. Анкета субъективной оценки нарушений сна. Суммарная оценка 22 и более баллов — сон нормальный, 19—21 балл — пограничные значения, менее 19 баллов — сон нарушен [12].
Г. Анкета для скрининга синдрома апноэ во сне — при значениях более 4 баллов позволяет с большой вероятностью подозревать у больного присутствие синдрома апноэ во сне. Шкала позволяет определить наличие противопоказаний к назначению лекарственных средств, а также оценить их безопасность [12].
Исходно включенные в исследование пациенты с тревожно-депрессивными расстройствами были рандомизированы на 2 группы.
Первая группа ( n = 20) — пациенты, которые в дополнение к базисной терапии (бета-адреноблокатор — бисопролол, ингибитор АПФ — эналаприл, антиагрегант — аспирин, статин — симвастатин, при необходимости диуретики и нитраты) получали по 1 мг препарата «Феназепам» на ночь в течение (14 ± 2) дня.
Вторая группа ( n = 20) — пациенты, которые получали только базисную терапию в течение (14 ± 2) дня.
Обе группы сопоставимы по возрасту, полу, тяжести заболевания, основным клинико-гемодинамическим параметрам (табл. 1).
ТАБЛИЦА 1
Характеристика групп пациентов с хронической сердечной недостаточностью в раннем постинфарктном периоде ( M ± m )
|
Параметр |
1-я группа |
2-я группа |
|
Количество больных |
20 |
20 |
|
Возраст больных, лет |
61,80 ± 2,73 |
58,90 ± 2,86 |
|
Мужчины/женщины |
14/6 |
16/4 |
|
Инфаркт миокарда с зубцом Q / без зубца Q |
11/9 |
14/6 |
|
Пациенты с ГБ /без ГБ |
18/2 |
17/3 |
|
Функциональный класс ХСН по NYHA |
2,45 ± 0,71 |
2,15 ± 0,69 |
|
Систолическое артериальное давление, мм рт.ст. |
127,30 ± 3,55 |
125,80 ± 3,15 |
|
Диастолическое артериальное давление, мм рт.ст. |
78,00 ± 2,57 |
77,50 ± 2,26 |
|
Частота сердечных сокращений, мин-1 |
63,10 ± 2,68 |
64,60 ± 2,93 |
|
Конечный диастолический размер левого желудочка, мм |
56,70 ± 2,41 |
55,90 ± 2,32 |
|
Размер ЛП, мм |
38,90 ± 2,23 |
39,20 ± 1,97 |
|
Фракция выброса по Тейкхольцу, % (ФВ) |
55,0 ± 2,88 |
54,4 ± 2,45 |
|
DT, мс |
230,80 ± 6,13 |
224,70 ± 5,66 |
|
IVRT, мс |
142,80 ± 6,10 |
145,50 ± 5,55 |
ТАБЛИЦА 2
Оценка эффективности и безопасности проводилась исходно и через (14 ± 2) дня от начала исследования. Для оценки безопасности регистрировались все побочные эффекты проводимой терапии, установленные как по жалобам, так и при целенаправленном расспросе и анализе динамики стандартных инструментальных данных (продолжительность ЭКГ-интервалов).
Компьютерная статистическая обработка полученных результатов проводилась на основе пакета анализов программ «Microsoft Excel».
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Исследование завершили все пациенты. Результаты проведенного исследования представлены в табл. 2.
У пациентов 1-й группы была установлена высокая анксиолитическая эффективность препарата «Феназепам» в составе базисной терапии — тревожность уменьшилась на 48,6 % ( р < 0,05), рис. 1. В то же время снижение показателей депрессии не достигло статистической значимости (Δ%= -16,3, р > 0,05), рис. 2.
Необходимо отметить, что показатели депрессии в конце периода наблюдения у пациентов 2-й группы не изменились, а тревоги — снизились, но недостоверно (Δ % = -19,3, р > 0,05).
Динамика объективных данных и вегетативной дисфункции, оцениваемых у больных ХСН (M ± m)
|
Показатели |
1-я группа ( n = 20) |
2-я группа ( n = 20) |
р * |
||||||
|
исходно |
14 ± 2 дн. |
Δ % |
р |
исходно |
(14 ± 2) дн. |
Δ% |
р |
||
|
САД, мм рт.ст. |
127,30±3,55 |
119,30 ± 3,19 |
-6,3 |
>0,05 |
125,80±3,15 |
120,50 ± 2,62 |
-4,2 |
>0,05 |
>0,05 |
|
ДАД, мм рт.ст. |
78,00±2,57 |
75,30 ± 2,36 |
-3,5 |
>0,05 |
77,50±2,26 |
74,00 ± 2,02 |
-4,5 |
>0,05 |
>0,05 |
|
ЧСС, мин -1 |
63,10±2,68 |
60,30 ± 2,36 |
-4,4 |
>0,05 |
64,60±2,93 |
59,90 ± 2,56 |
-7,3 |
>0,05 |
>0,05 |
|
Тревога (HADS) |
14,80 ± 1,58 |
7,60 ± 1,39 |
-48,6 |
<0,05 |
14,00 ± 1,71 |
11,30 ± 2,27 |
-19,3 |
>0,05 |
0,022 |
|
Депрессия (HADS) |
6,45 ± 1,17 |
5,40 ± 1,13 |
-16,3 |
>0,05 |
6,85 ± 1,53 |
6,85 ± 1,55 |
0 |
>0,05 |
0,004 |
|
Сон |
16,20 ± 1,47 |
22,40 ± 1,35 |
38,3 |
<0,05 |
16,10 ± 1,18 |
18,10 ± 1,49 |
11,4 |
>0,05 |
<0,05 |
|
Апноэ |
7,35 ± 1,43 |
4,85 ± 1,32 |
-34,0 |
>0,05 |
6,95 ± 1,53 |
5,60 ± 1,44 |
-19,4 |
>0,05 |
0,29 |
|
Вегетативная дисфункция |
47,90 ± 2,42 |
29,50 ± 2,61 |
-38,4 |
<0,05 |
46,20 ± 2,97 |
39,60 ± 2,79 |
-14,3 |
>0,05 |
<0,05 |
|
Индекс Кердо |
-30,30 ± 4,82 |
-25,60 ± 4,01 |
15,5 |
>0,05 |
-22,00 ± 4,12 |
-23,5 ± 4,1 |
-6,8 |
>0,05 |
0,38 |
|
Ангинозные приступы, количество |
4,40 ± 1,59 |
1,55 ± 1,22 |
-64,8 |
>0,05 |
3,75 ± 1,36 |
1,95 ± 1,29 |
-48 |
>0,05 |
0,28 |
|
Нитроглицерин, кол-во табл. |
3,90 ± 1,86 |
1,00 ± 0,78 |
-74,4 |
>0,05 |
2,85 ± 1,32 |
1,30 ± 1,12 |
-54,4 |
>0,05 |
0,092 |
Примечание, р — достоверность различий между исходными и конечными результатами; р* — достоверность различий между конечными результатами в 1-й и 2-й группах.
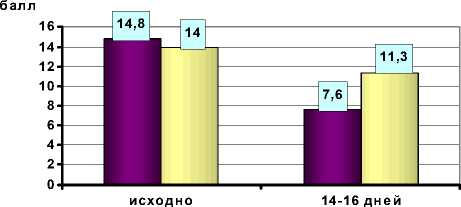
■1-я группа □2-я группа
Рис. 1. Показатели тревоги у больных в 1-й и 2-й группах
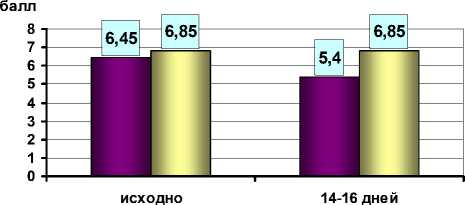
□ 1-я группа □ 2-я группа
Рис. 2. Показатели депрессии у больных в 1-й и 2-й группах
Так как у пациентов с тревожно-депрессивной симптоматикой имеется нарушение баланса между симпатическим и парасимпатическим отделом вегетативной нервной системы, это опосредованно может приводить к нарушениям ритма сердца. В связи с этим проводилась оценка вегетативного статуса пациентов с помощью шкалы балльной оценки проявлений вегетативной дистонии. На момент включения в исследование у пациентов обеих групп был одинаковый уровень проявлений вегетативной дисфункции (см. табл. 2).
На фоне применения феназепама в течение 14—16 дней в составе базисной терапии уровень вегетативной дисфункции снизился на 38,4 % ( р < 0,05), а во 2-й группе (прием только базисных препаратов) — на 14,3 % (межгрупповые различия достоверны, р < 0,05) (рис. 3), что свидетельствует о вегетонормализующем действии феназепама у пациентов в раннем восстановительном периоде инфаркта миокарда.
В ходе проведенного исследования установлено, что переносимость феназепама в целом хорошая. Случаев преждевременной отмены фена- ТАБЛИЦА 3
зепама у больных, перенесших инфаркт миокарда, из-за побочных эффектов не было. После отмены феназепама не обнаружено признаков лекарственной зависимости.
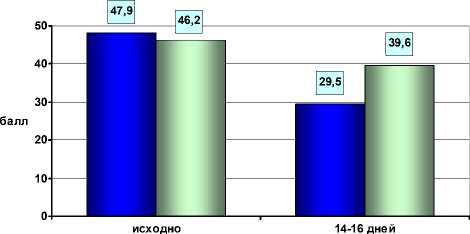
■ 1-я группа □ 2-я группа
Рис. 3. Показатели синдрома вегетативной дисфункции у больных в 1-й и 2-й группах
В ходе исследования не отмечено клинически значимого изменения артериального давления, а также существенных изменений частоты сердечных сокращений на фоне приема феназепама (табл. 2).
Показатели электрокардиограммы у больных, перенесших инфаркт миокарда (M ± m)
|
Показатели |
1-я группа ( n = 20) |
2-я группа ( n = 20) |
||||||
|
исходно |
(14 ± 2) дня |
Δ % |
р |
исходно |
(14 ± 2) дня |
Δ % |
р |
|
|
PQ, мсек |
151 ± 100 |
162,1 ± 91,2 |
7,4 |
>0,05 |
163,2 ± 91,0 |
171,6 ± 93,1 |
5,1 |
>0,05 |
|
QT, мсек |
400,1 ± 161,3 |
402,4 ± 162,0 |
0,6 |
>0,05 |
401,1 ± 160,0 |
420,2 ± 145,7 |
4,8 |
>0,05 |
Примечание. р — достоверность различий между исходными и конечными результатами
Анализ ЭКГ пациентов 1-й и 2-й группы в начале и в конце исследования показал, что применение феназепама в сочетании с базисными препаратами не влияет на продолжительность основных ЭКГ-интервалов (PQ, QT) (табл. 3).
Многие психотропные препараты противопоказаны при наличии у пациента синдрома апноэ во сне, так как могут усугубить его проявления. Поэтому в ходе настоящего исследования оценивались показатели шкалы для выявления апноэ во сне до и после окончания приема препарата. Анализ полученных данных показал, что применение феназепама в течение короткого периода ([14 ± 2) дня] не влияет на выраженность апноэ во сне (рис. 4). В обеих группах показатели по шкале «Апноэ во сне» снижались, при этом более выраженная положительная динамика наблюдалась в 1-й группе.
Данное исследование демонстрирует благоприятное влияние короткого курса [(14 ± 2) дня] терапии препаратом «Феназепам» на качество сна у пациентов в раннем постинфарктном периоде (нормализация сна по результатам анкеты субъективной оценки нарушений сна) (рис. 5). При этом у пациентов 1-й группы в отличие от 2-й (прием только базисных препаратов) в конце периода наблюдения достоверно уменьшалось время засыпания (р < 0,05), количе- ство ночных пробуждений и сновидений (р < 0,01), а также улучшалось качество пробуждения утром (р < 0,01). В тоже время короткий курс терапии фе-назепамом не оказывал существенного влияния на продолжительность ночного сна.
балл 4
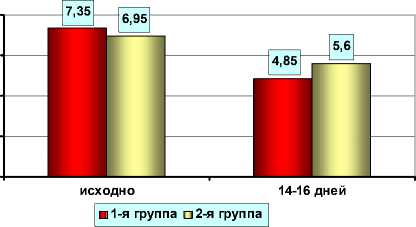
Рис. 4. Показатели опросника «Апноэ во сне» у больных в 1-й и 2-й группах
В двух исследуемых группах больных на фоне проводимой терапии отмечалось недостоверное уменьшение количества ангинозных приступов и кратности приема таблеток нитроглицерина. При этом лучшая динамика отмечена в 1-й группе пациентов, что может быть связано с более выраженным снижением исходного уровня тревоги и уменьшением степени вегетативной дисфункции (табл. 2).
балл
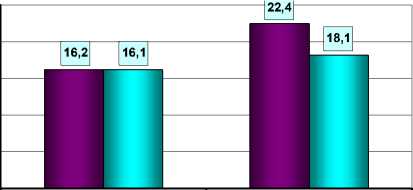
исходно
14-16 дней
□ 1-я группа □ 2-я группа
Рис. 5. Показатели качества сна у больных в 1-й и 2-й группах
За время наблюдения (14—16 дней) признаков неблагоприятного лекарственного взаимодействия феназепама с базисными препаратами для лечения ИБС (нитраты, бета-адреноблокаторы, ингибиторы АПФ, статины, антиагреганты, мочегонные) у пациентов в раннем постинфарктном периоде не отмечено.
ЗАКЛЮЧЕНИЕ
-
1. Результаты исследования свидетельствуют о высокой анксиолитической активности уже через две недели терапии феназепамом в дозе 1 мг/сутки у пациентов с тревожным расстройством в раннем постинфарктном периоде.
-
2. Установлено вегетонормализующее действие феназепама в дозе 1 мг/сутки у пациентов с тревожно-депрессивным расстройством в раннем постинфарктном периоде.
-
3. Выявлена способность феназепама в дозе 1 мг/сутки эффективно и быстро редуцировать различные нарушения сна у больных с тревожно-депрессивным расстройством в раннем постинфарктном периоде.
-
4. Показана безопасность, хорошая переносимость и отсутствие лекарственной зависимости короткого курса [(14 ± 2) дня] лечения феназепа-
- мом в дозе 1 мг/сутки у больных с тревожно-депрессивным расстройством в раннем постинфарктном периоде.


