Эффективность применения искусственной активации ооцитов ионофорами кальция в программах ВРТ у пациентов с неблагоприятным репродуктивным анамнезом: эмбриологические и клинические исходы
Автор: Попова О.О., Шурыгина О.В., Юхимец С.Н., Сараева Н.В., Петрова А.А., Минаева Т.В., Шурыгин С.А.
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 4 т.33, 2025 года.
Бесплатный доступ
Актуальность. Компетентность ооцита является определяющим фактором успешного оплодотворения и развития эмбриона. Низкое качество ооцитов может приводить к отсутствию оплодотворения или остановке развития эмбрионов in vitro. Для преодоления недостаточной активации ооцитов у пациенток с неудачами оплодотворения и неудовлетворительным качеством эмбрионов в анамнезе предлагается проведение искусственной активации ооцитов с помощью ионофоров кальция (АОА). Анализ эффективности использования данной технологии представляет интерес для специалистов фундаментальной медицины, а также клиник вспомогательных репродуктивных техно-логий (ВРТ). Цель исследования: оценить эффективность активации ооцитов ионофором Ca²⁺ на эмбриологическом этапе про-грамм ВРТ у пациентов с предыдущими неудачными попытками лечения бесплодия. Материалы и методы. Проведено ретроспективное когортное сравнительное исследование на базе ЗАО «Клинический госпиталь "Мать и дитя"» (Самара) в период с января по декабрь 2024 года. Группа исследования (n=35): циклы с применением АОА ионофором кальция (A23187, Sigma) после ИКСИ по медицинским показаниям (низкий процент оплодотворения в анамнезе). Контрольная группа (n=61): циклы со стандартной процедурой ИКСИ без применения активации. Критерии включения: возраст 18–43 лет, использование спермы партнёра, наличие полных данных о культивировании до 5-х суток. Для подготовки клеток и проведения ИКСИ использовали среды Vitrolife (Sweden). Клетки получали путём трансвагинальной аспирации фолликулов через 36–37 часов после триггера овуляции. После ИКСИ клетки выдерживали в среде с ионофором Ca²⁺ (концентрация 10 мМ) 8–10 минут при 6% CO₂, 5% O₂ и температуре +37°C. Для оценки качества эмбрионов использовали балльную систему, основанную на критериях Gardner et al. (1999), модифицированную с учётом дополнительных морфологических параметров. Результаты. Основные параметры – частота оплодотворения, частота дробления и частота формирования бластоцист – не имели значимых отличий между группами (p>0,05). Существенное отличие отмечено только по среднему баллу эмбрионов на перенос (2,91±2,09 vs 3,98±1,41, p=0,008). Показатели частоты наступления клинической беременности, подтверждённой УЗИ (36,0% vs 30,4%), и частоты имплантации (27,3% vs 23,8%) оставались сопоставимыми (p>0,05). Выявлен клинически значимый тренд к снижению разницы между показателями беременности, установленной по определению положительного уровня ХГЧ, и частотой клинической беременности (4% vs 10,7% в контроле), что может свидетельствовать о более высокой компетенции эмбрионов в группе АОА и снижении ранних репродуктивных потерь. Заключение. Искусственная активация ооцитов ионофорами кальция не приводит к статистически значимому улучшению основных эмбриологических показателей, но демонстрирует тенденцию к снижению разницы между биохимической и клинической беременностью, что может указывать на повышение качества эмбрионов у пациентов с неблагоприятным репродуктивным анамнезом. Для получения более достоверных выводов требуется накопление информации и проведение мультицентровых рандомизированных исследований с увеличенным объёмом выборки.
Ооцит, человек, ИКСИ, ионофоры кальция, ВРТ
Короткий адрес: https://sciup.org/143185413
IDR: 143185413 | УДК: 618.177-089.888.11:612.621.31 | DOI: 10.20340/mv-mn.2025.33(4).991
Effectiveness of calcium ionophore artificial oocyte activation in ART programs for patients with adverse reproductive history: embryological and clinical outcomes
Background. Oocyte competence is a determinant of successful fertilization and embryo development. Poor oocyte quality may lead to fertilization failure or in vitro embryo developmental arrest. Artificial oocyte activation (AOA) using calcium ionophores has been proposed to overcome oocyte activation deficiency in patients with fertilization failure and unsatisfactory embryo quality. The effectiveness of this technology is of interest to fundamental medicine specialists and ART clinics. Aim. To evaluate the effectiveness of calcium ionophore-mediated oocyte activation at the embryological stage of assisted reproductive technology (ART) programs in patients with previous unsuccessful infertility treatments. Materials and Methods. A retrospective cohort comparative study was conducted at the Clinical Hospital "Mother and Child" (Samara) from January to December 2024. Study group (n=35): cycles with AOA using calcium ionophore (A23187, Sigma) after ICSI by medical indications (low fertilization rate in history). Control group (n=61): cycles with standard ICSI procedure without activation. Inclusion criteria: age 18–43 years, partner sperm use, complete data on culture up to day 5. Vitrolife media (Sweden) were used for cell preparation and ICSI. Cells were obtained by transvaginal follicular aspiration 36–37 hours after ovulation trigger. After ICSI, cells were in-cubated in medium with Ca²⁺ ionophore (10 mM concentration) for 8–10 minutes at 6% CO₂, 5% O₂, and +37°C. Embryo quality was assessed using a scoring system based on Gardner et al. (1999) criteria, modified with additional morphological parameters. Results. Main parameters–fertilization rate, cleavage rate, and blastocyst formation rate–showed no significant differences between groups (p>0.05). A significant difference was observed only in mean embryo score at trans-fer (2.91±2.09 vs 3.98±1.41, p=0.008). Clinical pregnancy rate confirmed by ultrasound (36.0% vs 30.4%) and implantation rate (27.3% vs 23.8%) remained comparable (p>0.05). A clinically significant trend toward re-duced difference between positive hCG and clinical pregnancy rate (4% vs 10.7% in control) was revealed, sug-gesting higher embryo competence in the AOA group and reduced early reproductive loss. Conclusion. Calcium ionophore artificial oocyte activation does not lead to statistically significant improvement in main embryological parameters but demonstrates a trend toward reducing the gap between biochemical and clinical pregnancy, which may indicate improved embryo quality in patients with adverse reproductive history. Data accumulation and multicenter randomized studies with increased sample size are required for more reliable conclusions.
Текст научной статьи Эффективность применения искусственной активации ооцитов ионофорами кальция в программах ВРТ у пациентов с неблагоприятным репродуктивным анамнезом: эмбриологические и клинические исходы
(4).991
В последние десятилетия применение вспомогательных репродуктивных технологий (ВРТ) стало мировым стандартом терапии бесплодия: ежегодно проводится более 2,5 миллионов циклов [1]. С развитием технологий всё большую популярность приобретают дополнительные процедуры, направленные на повышение эффектив- ности эмбриологического этапа программ ВРТ. К числу наиболее востребованных вмешательств относятся видеомониторинг развития эмбрионов (time-lapse), вспомогательный хетчинг, использование среды, обогащённой гиалуроновой кислотой (PICSI или физиологическое ICSI – предварительный отбор сперматозоидов на основе взаимодействия рецепторов мембраны их головки с гиалуроновой кислотой), искусственная активация ооцитов ионофором Ca²⁺ (АОА) и др.
Тем не менее, результаты систематических обзоров показывают противоречивые результаты их эффективности [2]. Исключение может составлять комбинация ИКСИ и искусственной активации ооцитов, для которой ряд авторов отмечает достоверное увеличение вероятности оплодотворения и наступления беременности [3–7]. АОА с применением ионофоров Ca²⁺ представляет собой стратегию преодоления отсутствия оплодотворения или снижения его показателя, низкого качества эмбрионов в предыдущих программах. Причины данных проблем, как правило, связаны с отклонениями в гаметогенезе и образованием компетентных сперматозоидов и ооцитов. Это приводит к нарушению взаимодействия гамет в процессе оплодотворения и, как следствие, к нарушению формирования качественных эмбрионов.
Мы предлагаем рассматривать распространённый в практической эмбриологии термин «качество эмбриона» как совокупность морфологических и цитофизиологических характеристик, позволяющих реализовать его способность к имплантации и дальнейшему развитию.
Механизм действия искусственной активации ооцитов
Метод искусственной активации ооцитов (АОА) целенаправленно воспроизводит ключевые этапы оплодотворения – завершение мейо-тического деления ооцита и кортикальную реакцию. Однако динамика кальциевого сигнала при АОА отличается от естественной. Механизм действия заключается в следующем: ионофор в культуральной среде связывается с ионами кальция (Ca²⁺ ). Образовавшийся комплекс проходит через клеточную мембрану ооцита, доставляя внутрь него Ca²⁺ . Этот искусственный приток кальция служит триггером для запуска последующих процессов развития. Таким образом, АОА эффективно инициирует процесс оплодотворения, хотя и использует для этого упрощённую, по сравнению с природной, кальциевую сигнализацию.
В цитоплазме, где базальная концентрация свободного Ca²⁺ составляет ~100 нМ, происходит диссоциация комплекса с высвобождением ионов кальция. Важно отметить, что ионофор при этом рециркулирует к внешней поверхности мембраны, обеспечивая многократный транспортный цикл [5]. Данный процесс индуцирует резкий транзиент (от англ. transient – временный, преходящий) внутриклеточного кальция (>1 мкМ), имитирующий начальную фазу физиологической кальциевой волны, инициируемой спермальным фактором PLCζ (phospholipase C zeta) при естественном оплодотворении.
Возросшая концентрация цитоплазматического Ca²⁺ активирует каскад кальций-зависимых сигнальных путей внутри ооцита. Ключевым событием является конформационное изменение кальмодулина (CaM) при связывании с Ca²⁺ [8], что в свою очередь приводит к активации каль-модулин-зависимой киназы II (CaMKII) через фосфорилирование остатка Thr286 [9]. Активированная CaMKII инициирует фосфорилирование компонентов комплекса, стимулирующего анафазу (APC/C), запуская убиквитин-опосредованную протеасомальную деградацию циклина B1 – регуляторной субъединицы M-фазного стимулирующего фактора (MPF) [10].
Деградация циклина B1 приводит к инактивации MPF (комплекса Cyclin B1/CDK1), что снимает блок метафазы II мейоза. Последующее завершение второго мейотического деления включает сегрегацию хроматид, экструзию второго полярного тельца и формирование женского пронуклеуса посредством деконденсации хромосом и образования ядерной оболочки [11]. Параллельно кальциевый сигнал индуцирует экзоцитоз кортикальных гранул, чьё содержимое (включая ово-трансферазу и N-ацетилглюкозаминидазу) модифицирует гликопротеины блестящей оболочки (ZP2/ZP3), создавая биохимический барьер против полиспермии.
Следует подчеркнуть, что в отличие от физиологических Ca²⁺ -осцилляций при оплодотворении (15–30 волн за 4–6 часов), ионофор индуцирует монофазный транзиент [12].
Введение ионофора Са2+

Связывание внеклеточного Са2+

Транспорт Са2+через мембрану ооцита

Высвобождение Са2+ в цитоплазму резкое повышение его концентрации

Активация Са2-завсисимых сигнальных путей

Кальмодулин (СаМ)

Активация СаМК II

Инактивация MPF

Деградация циклина В1

Снятие блока метафазы II

Завершение мейоза II
Сегрегация хроматид и изгнание 2-го полярного тельца
Образование женского пронуклеуса

Модификация zona pellucida

Блок полиспермии
Рис. 1. Механизм искусственной активации яйцеклеток человека ионофорами Ca²⁺ (систематизация литературных данных): MPF – митоз-стимулирующий фактор; СаМК II-кальмодулин – зависимая протеинкиназа II; Zona pellucida – блестящая оболочка


Клиническое значение АОА
Особое значение АОА приобретает при полной неудаче оплодотворения (Total Fertilization Failure, TFF) – полной неспособности любого из полученных зрелых ооцитов на стадии MII к оплодотворению в цикле экстракорпорального оплодотворения (ЭКО) или ИКСИ. В настоящее время одной из главных причин возникновения TFF считается недостаточная активация ооцитов, напрямую связанная с нарушением кальциевой сигнализации. После оплодотворения в ооцитах должны развиваться специфические осцилляции Ca²⁺ , критично важные для триггера активации; нарушение этих процессов может объяснять TFF [13].
Отдельные работы демонстрируют, что сперматозоиды, неспособные активировать ооцит даже в условиях ИКСИ, частично или полностью лишены потенциала к запуску осцилляций Ca²⁺ , либо вызывают только редуцированные или аномальные амплитуды кальциевых колебаний [14, 15].
Тем не менее, окончательный вопрос о влиянии АОА на частоту наступления беременности и рождение живого ребёнка остаётся нерешённым. Согласно части работ, эффективность метода проявляется в основном у пациентов со снижением способности к оплодотворению, а для других категорий статистически значимых различий не выявляется. Современные метаанализы отмечают: для пациентов с трудностями или невозможностью оплодотворения применение АОА может позитивно сказываться на клинических перспективах беременности и её пролонгировании.
Однако следует отметить, что большинство работ по положительному влиянию АОА носили характер отдельных наблюдений и небольших серий [16, 17]. В исследовании Яхьяровой М.П. была продемонстрирована эффективность применения ионофора Ca²⁺ для коррекции локализации пронуклеусов в ооцитах после ИКСИ у пациенток с недостаточной активацией и неудачными попытками оплодотворения в анамнезе [18]. Однако систематический обзор Sfontouris и соавт. [19] подчёркивает отсутствие убедительных доказательств эффективности АОА, а вопросы безопасности процедуры до сих пор не решены. В связи с этим необходимо дальнейшее накопление данных.
ЦЕЛЬ ИССЛЕДОВАНИЯ: оценить эффективность активации ооцитов ионофором Ca²⁺ на эмбриологическом этапе программ ВРТ у пациентов с предыдущими неудачными попытками лечения бесплодия.
МАТЕРИАЛЫ И МЕТОДЫ
Проведено ретроспективное когортное сравнительное исследование на базе ЗАО «Клинический госпиталь "Мать и дитя"» (Самара) в период с января по декабрь 2024 года.
Критерии включения в исследование: возраст пациенток от 18 до 43 лет, использование спермы партнёра (без применения донорских программ), наличие полных данных об исходе культивирования до 5-х суток.
Единицей наблюдения являлся цикл ИКСИ. Для исключения статистической зависимости данных в случаях повторных обращений одной и той же пациентки в анализ включался только первый цикл, проведённый в указанный период времени.
Группы исследования:
-
• Группа I (группа исследования, n=35) – циклы с применением метода искусственной активации ооцитов (АОА) ионофором кальция после ИКСИ по медицинским показаниям (низкий процент оплодотворения в анамнезе).
-
• Группа II (контрольная группа, n=61) – циклы со стандартной процедурой ИКСИ без применения активации, соответствующие критериям включения.
Исследование одобрено локальным Комитетом по биоэтике при Самарском государственном медицинском университете (протокол №240 от 19 ноября 2021 года).
Эмбриологические процедуры
Для подготовки клеток и проведения процедуры ИКСИ использовали среды производства 30
Vitrolife (Sweden). Клетки получали путём трансвагинальной аспирации фолликулов через 36–37 часов после назначения триггера овуляции. Сбор ооцит-кумулюсных комплексов (ОКК) проводили в стерильных условиях ламинарного потока воздуха при соблюдении температурного режима +37°C.
ОКК идентифицировали под контролем стереомикроскопа (Nikon SMZ18, Япония), помещали в среду для сбора ооцитов Gmops Plus (Vitrolife, Sweden). После отмывки от фолликулярной жидкости и крови в буферном растворе ОКК выдерживали 2–3 часа в культуральной среде IVF Plus (Vitrolife, Sweden) при концентрации 6% CO₂, 5% O₂ и температуре +37°C до момента денудации.
После окончания предварительной инкубации проводили денудирование ооцитов (механическое и энзимное удаление клеток кумулю-са). Сначала ОКК помещали на 20–30 секунд в раствор гиалуронидазы (Vitrolife, Sweden), затем отмывали от фермента в буферной среде механическим путём. Для предотвращения повреждения ооцита использовали пипетки с соответствующим размером просвета (d=175 мкм), избегая слишком энергичного пипетирования. После денудации ооциты тщательно промывали в буферном растворе Gmops Plus для удаления остатков гиалуронидазы.
Оценку степени зрелости ооцитов фиксировали в эмбриологическом протоколе. Процедуру ИКСИ производили только ооцитам на стадии MII через 20–30 минут после денудации. В качестве среды для проведения процедуры ИКСИ использовали Gmops Plus (Vitrolife, Sweden). Для оплодотворения использовали морфологически нормальные сперматозоиды. Инъекцию сперматозоида в цитоплазму ооцита производили стандартным способом.
Процедура искусственной активации ооцитов
Чашки с каплями среды, содержащей ионофор Ca²⁺ , за 2–3 часа до начала процедуры ИКСИ помещали в инкубатор для уравновешивания при концентрации CO₂ 6%. Непосредственно после завершения процедуры ИКСИ клетки выдерживали в среде с добавлением ионофора Ca²⁺ (calcium ionophore A23187, Sigma) при концентрации CO₂ 6%, O₂ 5% и температуре +37°C на протяжении 8–10 минут в соответствии с рекомендациями производителя.
Для приготовления базового раствора 5 мг ионофора Ca²⁺ разводили в 1250 мкл DMSO (Sigma). Приготовленный базовый раствор алик-вотировали по 25 мкл в пробирки Эппендорфа и хранили в морозильной камере при –20°C. Для достижения рабочей концентрации раствора к 25 мкл базового раствора добавляли 475 мкл буферного раствора. Для достижения разведения ×40 и необходимой концентрации 10 мМ к 25 мкл подготовленного раствора добавляли 975 мкл культуральной среды.
По окончании инкубирования клетки тщательно промывали и переносили в капли со свежей средой GTL (Vitrolife, Sweden) при концентрации O₂ 5% и температуре +37°C. Через 16–18 часов проводили оценку оплодотворения.
Оценка качества эмбрионов
Для оценки качества развивающихся эмбрионов использовали собственную балльную систему, основанную на критериях оценки бластоцист по D.K. Gardner et al. (1999), модифицированную с учётом дополнительных морфологических критериев (табл. 1) [20, 21].
Таблица 1. Система оценки качества эмбрионов 5–6-х суток развития
|
Оценка качества эмбриона |
Морфологическая характеристика эмбриона |
|
Эмбрион отличного качества |
Бластоциста категории АА, АB, BA 3,4,5,6 степени экспансии, с фрагментацией 0-10%, без вакуолей, фрагментации и атрезивных клеток |
|
Эмбрион хорошего качества |
Бластоциста категории BB, CA, AC, 3,4,5,6 степени экспансии, ранняя бластоциста, начало кавитации с фрагментацией (0–10%), с единичными вакуолями в ТБ или ВКМ, единичными атрезивными клетками |
|
Эмбрион удовлетворительного качества |
Бластоциста категории BC, CB, CC, 3,4,5,6 степени экспансии, ранняя бластоциста, начало кавитации с множественными вакуолями в ТБ/ВКМ или фрагментацией (более 25%), с атрезивными клетками (более 25%), наличие аномалий формы |
|
Эмбрион посредственного качества |
Бластоциста категории СС, ранняя бластоциста, морула, начало кавитации с множественными вакуолями в ТБ/ВКМ или фрагментацией (более 50%), с атрезивными клетками (более 50%), наличие аномалий формы |
|
Эмбрион, остановившийся в развитии |
Эмбрион с признаками тотальной атрезии, без прогрессивных морфологических изменений в развитии |
Статистический анализ
Для оценки эффективности эмбриологического и клинического этапов использовали стандартные критерии в соответствии с рекомендациями Vienna Consensus (2017) [22].
Использовались описательные статистические показатели: среднее значение, медиана, стандартное отклонение, 95% доверительный интервал для среднего, межквартильный размах. Для сравнения двух групп применяли различные статистические методы в зависимости от типа данных. Для параметрических переменных использовали независимый t-критерий Стьюдента. В случае непараметрических показателей использовали критерий Манна – Уитни.
Для количественных непараметрических данных применяли z-тест для пропорций с поправкой на непрерывность. Различия считали статистически значимыми при p<0,05.
РЕЗУЛЬТАТЫ
Группы исследования и контроля были сопоставимы по основным демографическим и анамнестическим характеристикам: средний возраст женщин и среднее число предшествующих попыток лечения бесплодия методами ВРТ статистически не различались между группами (табл. 2).
Однако обращает на себя внимание показатель продолжительности бесплодия. В группе исследования средняя продолжительность бесплодия была выше. Статистический анализ продемонстрировал существенные различия в медианной длительности бесплодия между группами. Так, в контрольной группе медианная длительность бесплодия составила 4,0 года [межквартильный размах (IQR): 2,0–7,0], в то время как в группе исследования этот показатель был достоверно выше – 7,5 года (IQR: 4,0–10,0; p<0,001 по U-критерию Манна – Уитни).
Распределение длительности бесплодия в контрольной группе было правоасимметричным. Большинство пациенток (65,0%, n=41) имели историю бесплодия продолжительностью ≤5 лет. Случаи с длительностью ≥12 лет были редки (6,4%, n=4). Контрольная группа репре- зентирует когорту пациенток, которые в среднем обратились за помощью на более ранних сроках наступления бесплодия по сравнению с группой исследования. Учёт этого значимого различия является критически важным для последующего сравнительного анализа исходов лечения между группами.
Результаты анализа свидетельствуют о том, что по большинству ключевых эмбриологических и клинических параметров существенных различий между группами не выявлено (табл. 3). Доля зрелых ооцитов, частота оплодотворения, дробления и формирования бластоцист статистически значимо не отличались между группами (p>0,05).
Таблица 2. Сравнительная характеристика клинико-анамнестических данных групп исследования и контроля
|
Показатель |
Группа исследования |
Группа контроля |
|
Сp.количество попыток |
2,6 |
2,4 |
|
Ср.возраст (лет) |
33,97 ±4,37 |
34,51 ±4,68 |
|
Ср продолжительность бесплодия (лет) |
7,86 ± 4,00 |
5,90 ± 4,28 |
|
Количество полученных ооцитов |
6,1 |
5,9 |
|
Количество MII ооцитов |
4,5 |
4,6 |
Таблица 3. Сравнительная характеристика эмбриологических и клинических показателей
|
Показатель |
Группа |
N |
Медиана |
Среднее ± SD |
95% ДИ среднего |
25-й перц. |
75-й перц. |
IQR |
p-value |
|
Доля МII ооцитов при ИКСИ (%) |
исследования |
35 |
83,33 |
78,85 ± 20,97 |
72,17–85,53 |
66,67 |
100,00 |
33,33 |
0,567 |
|
контроль |
61 |
83,33 |
81,21 ± 20,39 |
76,25–86,17 |
66,67 |
100,00 |
33,33 |
||
|
Доля оплодотворения (%) |
исследования |
35 |
100,00 |
85,74 ± 19,78 |
78,87–92,61 |
76,39 |
100,00 |
23,61 |
0,479 |
|
контроль |
61 |
87,50 |
82,67 ± 20,15 |
77,35–87,99 |
75,00 |
100,00 |
25,00 |
||
|
Доля дробления (%) |
исследования |
35 |
100,00 |
95,70 ± 7,87 |
92,68–98,73 |
100,00 |
100,00 |
0,00 |
0,968 |
|
контроль |
61 |
100,00 |
95,59 ± 7,81 |
91,59–99,59 |
100,00 |
100,00 |
0,00 |
||
|
Доля дорастания до бластоцисты (%) |
исследования |
35 |
50,00 |
43,59 ± 30,93 |
32,10–55,07 |
17,14 |
66,67 |
49,52 |
0,827 |
|
Доля дорастания до бластоцисты (%) |
контроль |
61 |
40,00 |
41,92 ± 38,23 |
32,34–51,50 |
0,00 |
75,00 |
75,00 |
|
|
Средний балл эмбриона на перенос (ПЭ) |
исследования |
35 |
3,50 |
2,91 ± 2,34 |
2,23–3,60 |
0,00 |
4,75 |
4,75 |
0,008 |
|
контроль |
61 |
4,00 |
3,85 ± 1,01 |
3,50–4,20 |
3,00 |
5,00 |
2,00 |
||
|
Частота положительных ХГЧ (%) |
исследования |
35 |
40,0 |
40,0 ± 8,4 |
23,9–54,9 |
40,0 |
40,0 |
0,0 |
0,500 |
|
контроль |
61 |
41,1 |
41,1 ± 6,6 |
28,3–53,9 |
41,1 |
41,1 |
0,0 |
||
|
Частота наступления клин. беременности (ЧКБ, %) |
исследования |
35 |
36,0 |
36,0 ± 9,8 |
23,9–57,1 |
36,0 |
36,0 |
0,0 |
0,200 |
|
контроль |
61 |
30,4 |
30,4 ± 8,1 |
16,8–49,4 |
30,4 |
30,4 |
0,0 |
||
|
Частота имплантации (ЧИ, %) |
исследования |
35 |
27,3 |
27,3 ± 7,6 |
16,8–47,2 |
27,3 |
27,3 |
0,0 |
0,300 |
|
контроль |
61 |
23,8 |
23,8 ± 5,7 |
12,0–35,6 |
23,8 |
23,8 |
0,0 |
Однако средний балл эмбрионов на перенос составил 2,91±2,09 (95% ДИ: 2,23–3,60) в группе исследования и 3,98±1,41 (95% ДИ: 3,50–4,20) в контрольной группе (рис. 2); при этом единственное статистически значимое различие было отмечено именно по этому показателю (t-критерий Стьюдента: p=0,008).
Клинические исходы также были сопоставимы. Частота биохимической беременности (ХГЧ+) составила 40,0% в группе исследования против 41,1% в контрольной; частота клинической беременности (визуализация плодного яйца на УЗИ) – 36,0% против 30,4%; частота имплантации – 27,3% против 23,8%. Для всех этих показателей статистические тесты не выявили значимых различий (p>0,05).
Тем не менее, были обнаружены позитивные тенденции при использовании АОА. Последова- тельное повышение ключевых показателей в группе исследования (формирование бластоцист +1,7%, частота клинической беременности +5,6%, частота имплантации +3,5%) показывает биологически значимый тренд. Различия ≥5% по частоте клинической беременности считаются клинически важными (рис. 2).
Разница между показателями положительного ХГЧ и частоты клинической беременности в группе, где ооцитам была проведена АОА (4% vs 10,7% в контроле), указывает на снижение частоты биохимических беременностей (OR 0,37, 95% CI 0,16–0,85 в косвенном расчёте). Это свидетельствует о более высоком потенциале эмбрионов к имплантации и снижении ранних репродуктивных потерь (рис. 3).
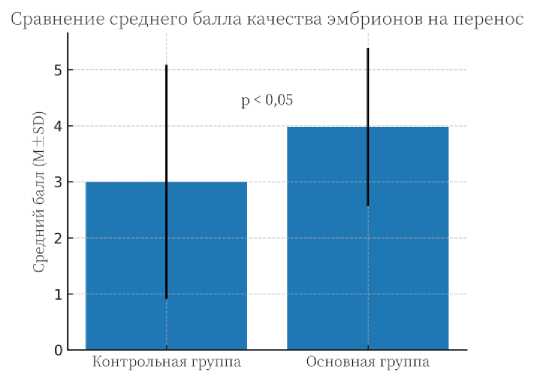
Рис. 2. Сравнение среднего балла качества эмбрионов на перенос в группах сравнения (M ± SD).
Примечание: различия статистически значимы (p < 0,05)
Сравнение клинических исходов с акцентом на тренд
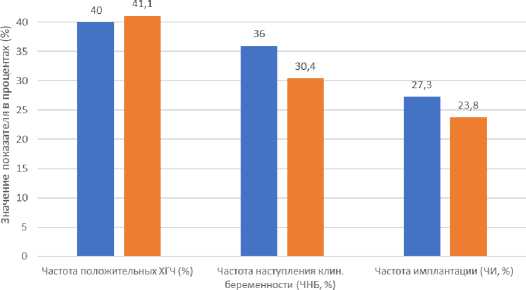
■ Исследования ■ Контроль
Рис. 3. Сравнение клинических исходов с акцентом на тренд
ОБСУЖДЕНИЕ
Искусственная активация ооцитов с использованием ионофоров Ca²⁺ обеспечивает приток ионов кальция в цитоплазму ооцита. Это приводит к инициации процессов экзоцитоза кортикальных гранул, окончанию мейоза и запуску молекулярных каскадов дальнейшего оплодотворения. Искусственная активация ооцитов компенсирует дефекты кальциевой сигнализа- ции и позволяет избежать полной неудачи оплодотворения (TFF).
На молекулярном уровне преимущество АОА заключается во включении сигнальных путей, ответственных за завершение второго мейотиче-ского деления, экспрессию ранних инициационных генов эмбриона, а также структурную реорганизацию пронуклеусов. Она может восполнить недостаточную мобилизацию кальция и вызвать активацию кальций-зависимых ферментов, в том числе кальмодулин-киназ, необходимых для формирования и развития эмбриона в случаях, когда естественные механизмы нарушены.
Тем не менее, искусственная активация не полностью имитирует природный паттерн повторяющихся быстрых кальциевых осцилляций, что может иметь значение для точности регуляции экспрессии ряда генов или процессов ком-партментализации в ооплазме. Однако в строго определённых патологических сценариях её применение позволяет достичь наступления оплодотворения и ранних стадий эмбриогенеза, что не было бы возможно исключительно при физиологической кальциевой сигнализации.
Полученные данные, несмотря на ограниченный объём выборки, выявляют клинически значимую тенденцию к улучшению репродуктивных исходов в группе АОА. Ключевые индикаторы эффективности программ ВРТ, а именно уменьшение дельты между ХГЧ и частотой клинической беременности, рост частоты имплантации, свидетельствуют о повышении качества эмбрионов. Вероятнее всего, это является следствием вклада искусственной активации ооцитов как биологического механизма, направленного на коррекцию сигнальных дефектов.
Развитие специальных дополнительных технологий (add-on) в ВРТ предопределено высоким спросом как со стороны пациентов, так и медицинских специалистов, стремящихся повысить успех программ лечения бесплодия. Несмотря на это, внедрение инноваций должно базироваться на принципах безопасности, доказательности и рационального распределения ресурсов. Применение большинства специальных техник характеризуется слабой клинически доказанной базой. Тем не менее, выявление положительных тенденций предполагает использование искусственной активации ооцитов в индивидуальных случаях.
Полученные результаты демонстрируют целесообразность АОА в селективных когортах (повторные неудачи ВРТ) и необходимость дальнейших проспективных исследований с увеличенной выборкой. Накопление данных и их анализ является важнейшей задачей для специалистов в области репродуктивной медицины.
ЗАКЛЮЧЕНИЕ
Искусственная активация ооцитов ионофорами кальция позволяет, по всей вероятности, улучшить их цитофизиологические характеристики и приводит к формированию качественных эмбрионов, способных к имплантации, у пациентов с предыдущими неудачными попытками лечения бесплодия.
Полученные данные свидетельствуют о том, что основные эмбриологические показатели (частота оплодотворения, дробления, формирования бластоцист) и клинические исходы в группах АОА и контроля сопоставимы. Однако выявлен клинически значимый тренд к снижению разницы между биохимической и клинической беременностью в группе АОА (4% vs 10,7% в контроле), что может указывать на повышение качества эмбрионов и снижение ранних репродуктивных потерь.
Для получения более достоверных выводов требуется накопление информации и проведение мультицентровых рандомизированных исследований с увеличенным до расчётного объёмом выборки.


