Эффективность применения коллагеновых мембран для реконструкции полнослойных дефектов гиалинового хряща в эксперименте
Автор: Лазишвили Г.Д., Егиазарян К.А., Никишин Д.В., Воронцов А.А., Храменкова И.В., Тен Г.С., Клинов Д.В.
Журнал: Кафедра травматологии и ортопедии @jkto
Рубрика: Оригинальное исследование
Статья в выпуске: 4 (46), 2021 года.
Бесплатный доступ
Статья посвящена анализу результатов экспериментального исследования - изучению эффективности применения коллагеновых мембран при хирургическом лечении полнослойных дефектов гиалинового хряща. Цель исследования - изучить биологический потенциал коллагеновых мембран и их способность к трансформации в хрящевую ткань. Исследование проводилось на 4-х свиньях. На суставах правых задних конечностей формировался полнослойный дефект хряща и имплантировалась коллагеновая мембрана Ortokeep. На суставах левых задних конечностей формировались по 2 полнослойных дефекта хряща. На один дефект имплантировалась коллагеновая мембрана Chondro-Gide, на 2-й дефект мембрана не имплантировалась. Животные выводились из эксперимента в сроки 2,3,4,6 месяцев после операции. В статье представлены макроскопический и микроскопический анализ характера регенерации хрящевой ткани в различные сроки после операции. Исследование показало высокий биологический потенциал коллагеновых мембран и их возможность трансформироваться в хрящевую ткань.
Хрящ, локальные дефекты хряща, коленный сустав, технология amic, костно-хрящевой дефект, коллагеновая мембрана, мозаичная пластика
Короткий адрес: https://sciup.org/142234233
IDR: 142234233 | УДК: 617.3
The effectiveness of the use of collagen membranes for the reconstruction of full-layer defects of hyaline cartilage in the experiment
The article is devoted to the analysis of the results of an experimental study - the study of the effectiveness of the use of collagen membranes in the surgical treatment of full-thickness defects of hyaline cartilage. The aim of the study is to study the biological potential of collagen membranes and their ability to transform into cartilage tissue. The study was carried out on 4 pigs. A full-thickness cartilage defect was formed on the joints of the right hind limbs and the Ortokeep collagen membrane was implanted. Two full-thickness cartilage defects were formed on the joints of the left hind limbs. A collagen membrane Chondro-Gide was implanted on one defect, a membrane was not implanted on the second defect. The animals were withdrawn from the experiment at 2,3,4,6 months after the operation. The animals were withdrawn from the experiment at 2,3,4,6 months after the operation. The articlepresents a macroscopic and microscopic analysis of the nature of the regeneration of cartilage tissue at various times after the operation. The study showed a high biological potential of collagen membranes and their ability to transform into cartilage tissue.
Текст научной статьи Эффективность применения коллагеновых мембран для реконструкции полнослойных дефектов гиалинового хряща в эксперименте
Введение. За последнее годы для восстановления полнослойных дефектов гиалинового хряща широкую популярность получила технология индуцированного матрицей аутохондрогенеза - AMIC (autologous matrix indused chondrogenesis) [1,2,3,4]. Технология AMIC основана на формировании отверстий в субхондральной кости (обеспечивающих транспорт костного мозга на поверхность дефекта) и репаративной способности стромальных клеток костного мозга, поступающего через сформированные отверстия. Образующийся в результате этого «суперсгусток» из красного костного мозга стабилизируется коллагеновой мембраной, имплантируемой в зону дефекта хряща. Естественный клеточный каркас защищает и связывает прогениторные клетки внутри «биологической камеры», стимулируя их дифференциацию для репарации хряща [3,5]
Преимущества технологии AMIC очевидны. Это: мало инвазивная одноэтапная процедура, не требующая культивирования хондроцитов; возможность восстановления крупных дефектов хряща (≥ 6-8 см²); простая хирургическая техника; подтвержденная эффективность в отношении купирования болевого синдрома, восстановления функции сустава и удовлетворенности больных исходами лечения.
Несмотря на широкую популярность технологии AMIC, остается много спорных и нерешенных вопросов, а именно: сроки деградации мембраны, характер её трансформации в хрящевую ткань, качество вновь образованной на месте имплантации мембраны хрящевой ткани и др. [6,7]
В настоящее время коллагеновая мембрана является одним из наиболее востребованных биологических материалов для восстановления хрящевой ткани. К сожалению, высокая стоимость импортных коллагеновых мембран не позволяет внедрить технологию AMIC в широкую клиническую практику отечественных медицинских учреждений. В тоже время потребность в выполнении операций по восстановлению хряща остается высокой. Этот факт определил необходимость разработки отечественного аналога, отвечающего всем современным требованиям, предъявляемым клиницистами к коллагеновым мембранам.
Цель исследования: экспериментальным путем изучить биологический потенциал коллагеновых мембран, их способность к трансформации в хрящевую ткань, оценить качество вновь образованной хрящевой ткани.
В работе использовалось два вида коллагеновых мембран, отличающихся по составу, структуре и характеру производства.
В качестве основной, использовалась разработанная российскими учеными мембрана Ortokeep (Рис.1а). Мембрана сформирована методом электроспиннинга из нановолокон диаметром 300-500 нм, состоящих из смеси полилактида и бычьего коллагена I-го типа (Рис.1б). Мембрана имеет одинаковый микрорельеф и смачиваемость с обеих сторон. Метод формирования мембраны и структура нановолокон радикально отличают ее от зарубежных аналогов, что позволяет произвести объективный сравнительный анализ их биологического потенциала.
В качестве контрольной, использовалась коллагеновая мембрана Chondro-Gide, производства зарубежной компании, синтезированная из свиного коллагена I и III типа, который резорбируется естественным путем (Рис.1г). Мембрана имеет двухслойную структуру (Рис.1д). Плотный слой имеет гладкую, не проницаемую поверхность, что обеспечивает стабилизацию сгустка костного мозга на поверхности субхондральной кости и исключает проникновение клеток костного мозга через мембрану в полость сустава. Пористый слой мембраны состоит из рыхлых коллагеновых волокон, способствующих адсорбции клеток в мембрану (Рис.1е). Структура мембраны имеют высокую устойчивости к растяжению, что препятствует её разрыву. Мембрана Chondro-Gide является наиболее популярным биопродуктом и широко используется для восстановления полнослойных дефектов хряща. Именно поэтому данная мембрана была выбрана нами в качестве контрольной.
Модель эксперимента: исследование проводилось на 4-х свиньях породы «русская белая». Настоящее экспериментальное исследование не противоречило этическим нормам и Международным требованиям по гуманному отношению к лабораторным (экспериментальным) животным, а также ГОСТ Р ИСО 10993-1-2009 «Изделия медицинские».
Исследование выполнено с использованием анальгетиков системного действия, применяемых в ветеринарии и клинической медицине в соответствующих для конкретного животного дозировках. Респираторная поддержка при помощи наркозно-дыхательного аппарата осуществлялась путем ингаляции кислородно-воздушной смеси по полузакрытому контуру.

Рис. 1. Внешний вид и строение коллагеновых мембран: а – мембрана Ortokeep; б - нановолокнистая структура мембраны Ortokeep (электронная микроскопия); в - рост клеток на мембране в эксперименте; г – мембрана Chondro-Gide; д - двухслойная структура мембраны Chondro-Gide (электронная микроскопия, увеличение в 100 раз); е - пористая, адгезирующая клетки поверхность мембраны Chondro-Gide (увеличение в 1500 раз).
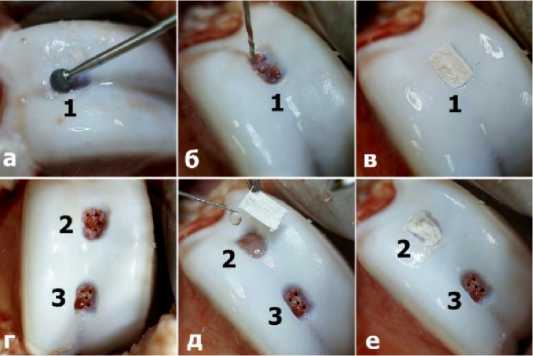
Рис. 2 Этапы формирования полнослойных дефектов и имплантации коллагеновых мембран (разъяснения см. в тексте). Примечание: 1 – дефект № 1 (имплантация мембраны Ortokeep); 2 – дефект № 2 (имплантация мембраны Chondro-Gide); 3 – дефект № 3 (без имплантации мембраны).
Результаты собственных исследований
На суставах правых задних конечностей каждого животного, с помощью круглого бора формировалось по одному полнослойному дефекту хряща (дефект №1) прямоугольной формы, размером 1х0,5 см, доходящего до субхондральной кости (Рис.2 а). Тонким сверлом диаметром 1,5 мм производилось рассверливание субхондральной кости на глубину 1 см, что позволило обеспечить транспорт костного мозга на поверхность дефекта (Рис.2 б). Коллагеновая мембрана Ortokeep моделировалась по форме и размеру дефектов, и фиксировались к субхондральной кости с помощью фибринового клея (Рис.2 в).
На суставах левых задних конечностей формировали по два дефекта: дефект (№2) – для имплантации мембраны Chondro Gide и контрольный дефект (№3) - без имплантации мембраны (Рис.2 г). Коллагеновая мембрана моделировалась по форме и размеру дефекта. После рассверливания субхондральной кости на дефект №2 наносился фибриновый клей и имплантировалась коллагеновая мембрана Chondro Gide (Рис.2 д). На контрольный дефект №3 имплантация мембраны не осуществлялась (Рис.2 е).
Животные выводились из эксперимента в сроки 2,3,4,6 месяцев после операции. Для последующего гистологического исследования предоставлялись крупные костно-хрящевые фрагменты, с расположенными на них исследуемыми дефектами. Для последующего микроскопического исследования из центральной части каждого дефекта производился забор одного фрагмента-биоптата.
Используя микроскоп с разрешением 12 мегапикселей, с каждого гистологического препарата производили микросъемку препарата, с последующим исследованием: воспалительной реакции, клеточного состава, коллагеновых волокон, остеогенеза. Изучаемые характеристики представлены в таблице.
При макроскопическом исследовании дефекта 3 (без имплантации мембран) отмечалось прогрессирующее увеличение его размеров без признаков регенерации хрящевой ткани на поверхности дефекта (Рис.3). Микроскопическое исследование показало признаки прогрессирующей деструкции костной ткани и отсутствие признаков хондрогенеза. Исходы таких операций были расценены как неудовлетворительные. Именно поэтому мы не будем представлять результаты гистологического исследования биоптатов из зоны дефекта 3, а представим лишь сравнительные с другими группами результаты морфометрии (таблица). Это экспериментальное наблюдение еще раз подтверждает низкую эффективность одной лишь туннелизации субхондральной кости, что ставит под сомнение целесообразность выполнения подобных операций в клинической практике.
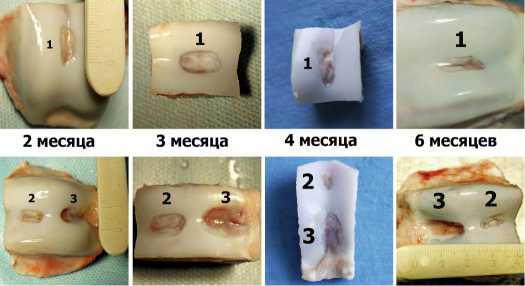
Рис.3. Макро препараты на различных сроках после операции.
Примечание: 1 – дефект № 1 после имплантации мембраны
Ortokeep; 2 – дефект № 2 после имплантации мембраны
Chondro-Gide; 3 – дефект № 3 – без имплантации мембран.
В тоже время в экспериментальных группах (дефекты № 1 и 2) выраженного увеличения размеров дефекта не выявлено. Дно дефектов ровное, но не равномерное. При пальпации дна, ткани на ощупь упруго-эластичные. Оба дефекты покрыты жизнеспособной, стабильной хрящевой тканью. (Рис.3)
Микроскопическое исследование дефекта № 1
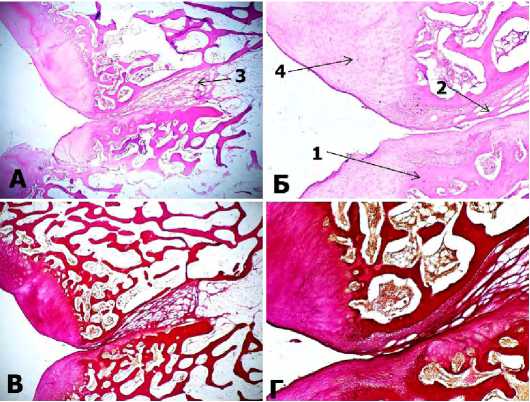
Рис.4 Микроскопия центральной части дефекта № 1 через 6 месяцев после имплантации мембраны Ortokeep. А-окраска гематоксилином и эозином, х40; Б-окраска гематоксилином и эозином, х100; В-окраска по методу Ван-Гизона, х40; Г- окраска по методу Ван-Гизона, х100.
Примечание: 1 – формирование остеоида (новообразованной костной ткани); 2 – грубоволокнистая соединительная ткань; 3 – адипоциты (жировые клетки); 4 – неохондрогенез (новообразованные хондроциты).
При исследовании гистологических стекол, окрашенных гематоксилином и эозином, во всех сроках вывода, воспалительного процесса, лейкоцитарной инфильтрации, не выявлено. Четкая граница интактного хряща выявлялась до срока 4 месяца, а на 6-м месяце граница стирается. Подлежащая костная ткань подверглась значительной резорбции в непосредственной близости от дефекта. Но признаков остеодистрофии в окружающем губчатом веществе не выявлено. На месте удаленного хряща и резорбированной костной ткани формировалась грубоволокнистая соединительная ткань. Начиная с 1-го месяца наблюдалось образование и созревание соединительной ткани и как следствие уменьшения ее объема (табл.). Параллельно по краям дефекта костной ткани происходили активные репаративные процессы – неостеогенез. Дефект первоначально имел колбообразную форму, но в дальнейшем приобретал цилиндрическую форму и к 6 месяцам становился клиновидным. Причем если с 1 месяца до 4 месяца дефект в основном был заполнен грубой волокнистой тканью, то на 6 месяце дефект практически полностью закрылся костной тканью. Формирование неохондроцитов (хонрогенез) проис- ходило активно и не только у края неповрежденного хряща, также выявлялись островки хондроцитов по центру дефекта (Рис. 4). В центре дефекта имелось глубокое щелевидное пространство, уходящее относительно глубоко в губчатое вещество. Процессы неоангиогенеза выраженные. Результаты морфометрии представлены в таблице.
Таким образом, при гистологическом исследовании центральной части образца дефекта № 1 выявлены активные репаративные процессы, направленные на восстановление резорбированной костной ткани, закрытие дефекта, а также восстановление гиалинового хряща. Причем, хондрогенез протекал не только по краю неповрежденного хряща, но и в виде отдельных островков в толще соединительной ткани.
Микроскопическое исследование дефекта № 2
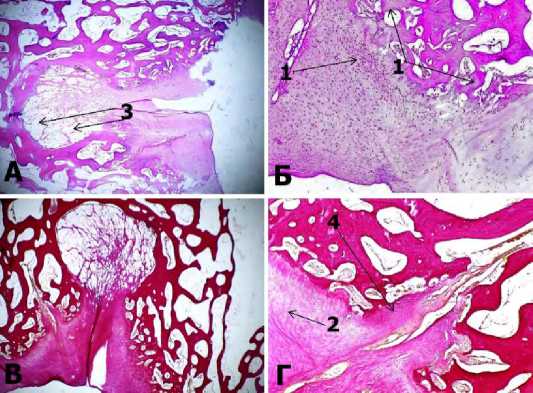
Рис.5 Микроскопия центральной части дефекта № 2 через 6 месяцев после имплантации мембраны Chondro-Gide. А-окраска гематоксилином и эозином, х40; Б-окраска гематоксилином и эозином, х100; В-окраска по методу Ван-Гизона, х40; Г- окраска по методу Ван-Гизона, х100.
Примечание: 1 – формирование остеоида (новообразованной костной ткани); 2 – грубоволокнистая соединительная ткань; 3 – адипоциты (жировые клетки); 4 – неохондрогенез (новообразованные хондроциты).
При исследовании гистологических стекол, окрашенных гематоксилином и эозином, воспалительного процесса, лейкоцитарной инфильтрации, не выявлено. Граница разрушенного хряща нечеткая. По центру сформировалась щелевидная полость, образованная на месте дефекта, подлежащая костная ткань подверглась резорбции (глубина резорбции несколько уменьшилась по сравнению с 3-х месячным результатом), на месте резорбированной костной ткани сформировалась грубоволокнистая соединительная ткань, с тенденцией к образованию костной ткани по краю дефекта и множественными островками хондроцитов в толще дефекта. Дефект имел колбообразную форму, и формирование неохондроцитов происходило активнее в направлении от периферии к центру. Имелсь отдельные щелевидные полости в толще грубоволокнистой соединительной ткани. На дне дефекта между соединительной тканью и костной тканью сформировалась довольно выраженная прослойка, состоящая из жировых клеток. Процессы неоангиогенеза выраженные. Также в толще соединительной ткани формировались островки хондроцитов. Результаты морфометрии представлены в таблице.
Таким образом, при гистологическом исследовании центральной части образца из дефекта № 2 отмечены ускоренные репаративные процессы, формирование островков хрящевой ткани в непосредственной близости к суставной поверхности. Также отмечены изменения глубины дефекта. Из негативных моментов отмечается образование прослойки жировых клеток между соединительно-тканной мозолью и костной тканью. А также наличие щелевидной полости.
Таблица 1
Размерные характеристики гистологического строения центра дефекта при различных видах вмешательств
|
Группа |
2 месяца (M±m) |
3 месяца (M±m) |
4 месяца (M±m) |
6 месяцев (M±m) |
|
|
Толщина интактного хряща, мкм |
Контроль |
734,0±16,12 |
2247,5±36,94 |
2359,8±38,79 |
842,10±21,23 |
|
Chondro-Gide |
1118,5±21,81 |
1230,4±23,99 |
1291,9±25,19 |
838,67±19,12 |
|
|
Ortokeep |
1519,0±38,42 |
1670,5±42,26 |
1341,3±25,08 |
886,35±10,44 |
|
|
Толщина хряща в центре вмешательства, |
Контроль |
0,0 |
0,0 |
0,0 |
0,0 |
|
мкм |
Chondro-Gide |
0,0 |
503,9±22,74 |
571,4±29,96 |
252,68±12,19 |
|
Ortokeep |
0,0 |
534,0±36,42 |
657,1±34,46 |
335,94±13,47 |
|
|
Толщина соединительной ткани в области |
Контроль |
1635,2±187,33 |
1152,2±124,80 |
1094,6±118,56 |
2406,98±178,05 |
|
имплантации, мкм |
Chondro-Gide |
1648,2±137,34 |
1615,2±134,60 |
1534,5±127,87 |
900,58±72,43 |
|
Ortokeep |
2072,0±339,89 |
1968,6±322,90 |
2905,7±204,92 |
1688,66±71,60 |
|
|
Толщина кортикальной пластинки в |
Контроль |
162,9±6,33 |
121,9±7,27 |
134,0±8,00 |
53,22±4,08 |
|
интактной области, мкм |
Chondro-Gide |
162,2±8,37 |
181,6±9,38 |
199,8±10,32 |
102,18±6,60 |
|
Ortokeep |
181,0±9,92 |
198,6±10,91 |
226,0±12,03 |
84,53±5,15 |
|
|
Толщина кортикальной пластинки в цен- |
Контроль |
121,6±7,73 |
96,8±5,53 |
106,5±6,08 |
147,54±18,67 |
|
тре вмешательства, мкм |
Chondro-Gide |
140,4±13,67 |
157,3±15,31 |
173,0±16,84 |
184,76±5,48 |
|
Ortokeep |
149,0±11,01 |
164,4±12,11 |
163,9±14,81 |
142,66±19,93 |
|
|
Объем костной ткани, % |
Контроль |
18,9±0,63 |
18,5±0,62 |
20,4±0,68 |
10,42±0,67 |
|
Chondro-Gide |
16,3±028 |
19,2±0,33 |
21,1±0,36 |
17,41±0,36 |
|
|
Ortokeep |
27,0±0,67 |
29,8±0,73 |
27,1±0,57 |
30,23±0,34 |
|
|
Объем хрящевой ткани, % |
Контроль |
15,4±0,51 |
22,4±0,74 |
24,6±0,82 |
10,64±0,38 |
|
Chondro-Gide |
23,1±0,29 |
25,8±0,33 |
28,4±0,36 |
15,04±0,72 |
|
|
Ortokeep |
27,0±0,57 |
29,4±0,63 |
32,1±1,88 |
19,99±0,43 |
|
|
Объем соединительной ткани, % |
Контроль |
53,3±0,70 |
52,3±0,69 |
44,4±0,58 |
13,31±1,04 |
|
Chondro-Gide |
53,2±0,50 |
40,4±0,48 |
34,4±0,41 |
17,03±0,56 |
|
|
Ortokeep |
43,0±0,47 |
33,7±0,47 |
31,2±0,46 |
18,19±0,53 |
|
|
Объем кровеносных сосудов, % |
Контроль |
5,8±0,16 |
7,1±0,20 |
6,8±0,19 |
8,39±0,42 |
|
Chondro-Gide |
7,5±0,45 |
8,9±053 |
8,4±0,50 |
11,91±0,42 |
Выводы. Подводя итог, хотим отметить, что оба исследуемых материала (коллагеновые мембраны Ortokeep и Chondro-Gide) показали отличные результаты в регенерации полнослойного дефекта хряща. В обеих группах были получены практически идентичные макро и микроскопические результаты. Однако более детальный анализ данных гистологического исследования выявил следующие особенности:
-
• В обеих группах зона имплантации коллагеновых мембран была представлена волокнистой соединительной тканью с включениями хондроцитов.
-
• Коллагеновые мембраны в месте дефекта создавали более благоприятные условия для репаративных процессов, что подтверждается самыми короткими сроками закрытия дефекта собственной соединительной тканью. Созревание соединительной ткани протекало в более короткие сроки.
-
• В зоне имплантации мембран хондрогенез протекал по «рассыпному» типу – в сформированной грубоволокнистой соединительной ткани появлялись «островки» гиалинового хряща. Данные островки первоначально располагались на удалении друг от друга, но имели тенденцию к слиянию между собой. И процессы неохондрогенеза протекали не только на границе со здоровой тканью, но и в толще соединительнотканной мозоли.
-
• Эффективность применения коллагеновых мембран подтверждается цифровыми значениями объема костной и хрящевой тканей.
Таким образом, проведенное исследование подтвердило высокую эффективность коллагеновых мембран для регенерации хрящевой ткани. В тоже время считаем важным изучить данные с более отдаленными сроками исследованиями. Также, были бы весьма ценными исследования с различными по составу мембранами, что является предметом нашей дальнейшей работы.
Список литературы Эффективность применения коллагеновых мембран для реконструкции полнослойных дефектов гиалинового хряща в эксперименте
- Гаркави А.В., Блоков М.Ю. Артроскопическая хондропластика локальных хрящевых дефектов коленного сустава с использованием коллагеновой мембраны Chondro-Gide. Кафедра травматологии и ортопедии. 2015, №3 (15). С.4 - 7. [Garkavi A.V., Blokov M.U. Artroskopicheskaja hondroplastika lokalnih hriachevih defektov kolennogo sustava s ispolzovaniem kollagenovoi membrani Chondro-Gide. Kafedra travmatologii i ortopedii. 2015, No 3 (15). pp.4-7 [In Russ].
- Gao L., Orth P., Cucchiarini M., Madry H. Autologous Matrix-Induced Chondrogenesis: A Systematic Review of the Clinical Evidence. Am J Sports Med, 2019, № 1 (47), pp. 222-231.
- Benthien J.P., Behrens P. Autologous Matrix-Induced Chondrogenesis (AMIC) combining Microfracturing and a Collagen I/III Matrix for Articular Cartilage Resurfacing. Cartilage, 2010, №1, vol.1, рр. 65-68.
- Girolamo L., Schönhuber H.I., Vigano M. et al. Autologous Matrix-Induced Chondrogenesis (AMIC) and AMIC Enhanced by Autologous Concentrated Bone Marrow Aspirate (BMAC) Allow for Stable Clinical and Functional Improvements at up to 9 Years Follow-Up: Results from a Randomized Controlled Study. Journal of Clinical Medicine, 2019, vol.8, №3, рр.392-405.
- Kon E., Filardo G., Brittberg M., Busacca M. et al. Multilayer biomaterial for osteochondral regeneration shows superiority vs microfractures for the treatment of osteochondral lesions in a multicentre randomized trial at 2 years. Knee Surgery Sports Traumatology Arthroscopy, 2018, Vol. 26, рр. 2704 - 2715.
- Егиазарян К.А., Лазишвили Г.Д., Храменкова И.В., Шпак М.А., Бадриев Д.А. Алгоритм хирургического лечения больных с рассекающим остеохондритом коленного сустава. Вестник РГМУ. 2018, №2. C.77-83. [Egiazaryan K.A., Lazishvili G.D., Hramenkova I.V., Shpak M.A., Badriev D.A. Algoritm hirurgicheskogo lechenija bolnich s rassekajushim osteochondritom kolennogo sustava. Vestnik RGMU. 2018. No2. pp.77-83 [In Russ].
- Лазишвили Г.Д., Егиазарян К.А., Ратьев А.П., Гордиенко Д.И., Бут-Гусаим А.Б., Чуловская И.Г., Сиротин И.В., Шпак М.А. Гибридная костно-хрящевая трансплантация - инновационная технология для хирургического лечения обширных костно-хрящевых дефектов коленного сустава. Хирургическая практика. 2019, №4 (40). С.10-18. [Lazushvili G.D., Egiazaryan K.A., Ratyev A.P., Gordienko D.I., But-Gusaim A.B., Chulovskaja I.G., Sirotin I.V., Shpak M.A. Gibridnaja kostnohriashevaja transplantacija - innovacionnaja technologija dla hirurgicheskogo lechenija obshirnih kostno-hriashevich defektov kolennogo sustava // Hirurgicheskaja Praktika. 2019, No4 (40). pp.10-18 [In Russ].


