Эффективность применения сетчатых имплантов при лапароскопической пластике грыж пищеводного отверстия диафрагмы
Автор: Ищенко Р.В., Совпель И.В., Гринцов А.Г., Совпель О.В.
Журнал: Хирургическая практика @spractice
Рубрика: Статьи
Статья в выпуске: 1 (41), 2020 года.
Бесплатный доступ
Цель исследования. Анализ непосредственных и отдаленных результатов хирургического лечения больных грыжей пищеводного отверстия диафрагмы, осложненной гастроэзофагеальной рефлюксной болезнью.Материаллы и методы. В исследовании проведен ретроспективный анализ результатов хирургического лечения 98 пациентов за период 2009-2016 гг., оперированных по поводу грыж пищеводного отверстия диафрагмы, с размером грыжевого дефекта 5 и более см. В первую группу вошли 69 пациентов, которым пластика грыжевого дефекта выполнена шовным способом. Во вторую группу вошли пациенты, которым выполнена аллопластика - 29 пациентов.Результаты исследования. Отличий между группами пластики швом и аллопластики по частоте интраоперационных осложнений - 7(10,1%) против 2(6,9%), послеоперационных осложнений - 6(8,7%) против 3(10,4%), длительности оперативного вмешательства - 141±21,1 минут против 179±28,4 минут, длительности пребывания в стационаре - 6,7±1,6 дней против 6,9±1,8 дней, частоте послеоперационной дисфагии - 11(15,9%) против 6(20,7%) не отмечено. Через 5 лет после оперативного вмешательства рецидивы в группе шовной пластики отмечены у 14(20,3%) пациентов, в группе аллопластики - у 4(13,8%) пациентов. Суммарный балл по шкале-опроснику GERD - HRQL в группе шовной пластики составил 6,4±1,8 балла, в группе аллопластики - 5,9±2,1 балла. Неудовлетворительно оценили свое состояние 9(13%) пациентов в группе шовной пластики и 5(17,2%) в группе аллопластики.Выводы. Анализ отдаленных результатов через 5 лет после проведенного исследования показал отсутствие преимущества использования сетчатого трансплантата при пластике больших грыж пищеводного отверстия диафрагмы в сравнении со стандартной шовной пластикой как по частоте рецидивов, так и при оценке качества жизни.
Грыжа пищеводного отверстия диафрагмы, лапароскопическая коррекция, аллопластика, непосредственные и отдаленные результаты
Короткий адрес: https://sciup.org/142226477
IDR: 142226477 | УДК: 617-089.844 | DOI: 10.38181/2223-2427-2020-1-33-44
The effectiveness of mesh reinforcement during laparoscopic hiatal hernia repair
Purpose. To analyze short-term and long-term results of surgical treatment of patients with hiatal hernia complicated by gastroesophageal reflux disease.Materials and methods. A retrospective analysis of short-term and long-term results of treatment of 98 patients for the period 2009-2016, who underwented surgical treatment of hiatal hernia with a hernia defect size 5 or more cm was performed. The first group included 69 patients underwent suture repair of hernia defect. The second group underwent mesh repair - 29 patients.Results. Intraoperative complications - 7 (10.1%) versus 2 (6.9%), postoperative complications - 6 (8.7%) versus 3 (10.4%), the duration of surgery - 141 ± 21.1 min versus 179 ± 28.4, duration of hospital stay - 6.7 ± 1.6 days versus 6.9 ± 1.8, postoperative dysphagia - 11 (15.9%) versus 6 (20.7%) were not noted. In 5 years after surgery, reccurence in the suture group were noted in 14 (20.3%) patients, in the mesh group - in 4 (13.8%) patients. The total GERD-HRQL questionnaire score was 6.4 ± 1.8 points in the suture repair group and 5.9 ± 2.1 points in the mesh group. 9 (13%) patients in the suture repair group and 5 (17.2%) in the mesh group evaluated their condition as unsatisfactorily.Conclusion. The analysis of long-term results in 5 years after the surgery showed the absence of benefit after using mesh reinforcement during laparoscopic repair of large hiatal hernias compared to usual suture cruroraphy both in recurrence rate and in assessing the quality of life.
Текст научной статьи Эффективность применения сетчатых имплантов при лапароскопической пластике грыж пищеводного отверстия диафрагмы
Подавляющее число ГПОД протекают бессимптомно и не требуют какого-либо лечения, однако появление клинических проявлений, в первую очередь развитие гастроэзофагеальной рефлюксной болезни (ГЭРБ), может достаточно существенно нарушать самочувствие пациента и ухудшать качество жизни. Основой патогенеза ГЭРБ является нарушение антирефлюксного механизма пищеводно-желудочного перехода как следствие анатомических изменений, развивающихся при ГПОД[1,4,5,6].
Лапароскопический метод на сегодняшний день «является золотым» стандартом в лечении ГПОД и ГЭРБ благодаря малой травматичности, более низкой частоте осложнений. Широкое повсеместное внедрение малоинвазивных лапароскопических методик и появление большого количества хирургических способов коррекции ГПОД не привело к выработке единого унифицированного подхода к лечению пациентов с данной патологией[7,8,9,10]. Одной из основных проблем после выполнения пластики ГПОД является высокая частота неудовлетвориттельных результатов и рецидивов, которые в отдаленном периоде выявляются в среднем в 15-25%, а по данным некоторых авторов достигают 40%-50%[4,9,11,12].
С целью снижения частоты рецидивов, проводя аналогии с пластиками грыж брюшной стенки, рядом хирургов предложено применения аллопластики[13], что, по мнению части авторов, на первых этапах освоения методики позволило резко сократить количество рецидивов после пластик ГПОД[14]. Однако, по мере более широкого распространения методики аллопластики, накопления опыта ее применения и анализ длительного наблюдения за пациентами, в литера- туре стали появятся сообщения об осложнениях, связанных с установкой стеки, а также работы, ставящие под сомнение эффективность использования различных вариантов аллопластики при ГПОД[4,15,16].
Обобщение имеющихся в литературе данных, на наш взгляд позволит стандартизировать подходы к хирургическому лечению пациентов, страдающих ГПОД.
Цель исследования — анализ непосредственных и отдаленных результатов хирургического лечения больных грыжей пищеводного отверстия диафрагмы, осложненной гастроэзофагеальной рефлюксной болезнью, в зависимости от выбора способа пластики грыжевого отверстия.
Материалы и методы
В настоящем исследовании проведен ретроспективный анализ результатов хирургического лечения 98 пациентов за период 2009–2016 гг., оперированных по поводу грыж пищеводного отверстия диафрагмы, с размером грыжевого дефекта 5 и более см. Все пациенты оперированы в объеме лапароскопической крурорафии и фундопликации.
В зависимости от способа пластики пищеводного отверстия диафрагмы пациенты разделены на 2 группы сравнения. В первую группу вошли 69 пациентов, которым пластика грыжевого дефекта выполнена шовным способом. Во вторую группу вошли пациенты, которым выполнена пластика грыжи ПОД сетчатым аллотрансплантатом - 29 пациентов.
Показаниями к оперативному лечению явились:
-
- клинически, рентгенологически и эндоскопически подтвержденные ГПОД;
-
- неэффективность в течении более 3 месяцев консервативной терапии гастроэзофагеального рефлюкса;
-
- наличие клинически значимых экстрапищеводных проявлений ГПОД и ассоциированной с ней ГЭРБ — кардиальных либо бронхолегочных;
-
- показанием к использованию сетчатого аллотрансплантата при выполнении ушивания дефекта пищеводного отверстия диафрагмы служили наибольший поперечный размер дефекта более 5 см.
В группе шовной крурорафии в зависимости от величины пищеводного отверстия диафрагмы производилась задняя крурорафия с использованием от 2 до 4 узловых не-рассасывающихся швов «Ethibond» 2–0, при необходимости задняя крурорафия дополнялась одним передне-латеральным швом. В группе крурорафии с аллопластикой, ножки диафрагмы во время сшивания укреплялись со стороны брюшной полости сетчатым трансплантатом, который располагался V-образно. В исследовании использованы 2 типа сетчатых трансплантатов: не рассасывающийся трансплантат Prolene (Ethicon) - у 12(41,4%) пациентов, и композитный частично-рассасывающийся трансплантат Ultrapro (Ethicon) - у 17(58,6%) пациентов. Этапы выполнения оперативного вмешательства представлены на Рис.1.
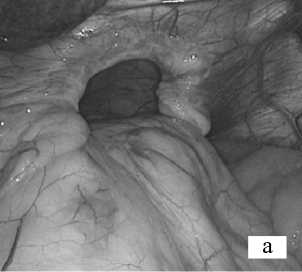
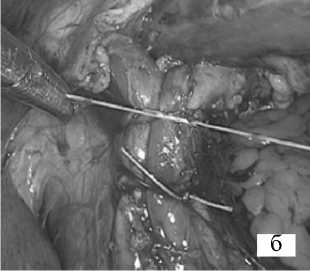
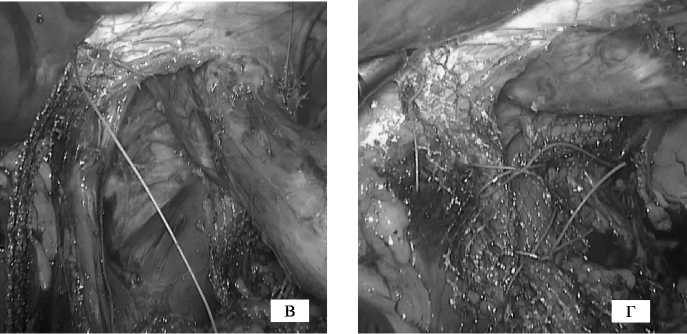
Рис.1. Этапы выполнения оперативного вмешательства: а - грыжа пищеводного отверстия диафрагмы; б - закрытие грыжевого дефекта шовным способом; в - фиксация аллотрансплантата к диафрагме; г - окончательный вид после аллопластики пищеводного отверстия диафрагмы.
В послеоперационном периоде проведена оценка непосредственных и отдаленных результатов хирургических вмешательств. Учитывая отсутствие единой общепринятой классификации неудовлетворительных результатов после хирургического лечения ГПОД, осложненной ГЭРБ, при оценке отдаленных неудовлетворительные результатов, последние разделены на 2 группы: рецидивы и стойкая длительная дисфагия. Рецидивы разделены на 2 подгруппы: анатомические рецидивы - пациенты, у которых в послеоперационном периоде рецидив подтвержден рентгенологически либо эндоскопически, и функциональные рецидивы - случаи, где клинически имеется появление жалоб, в первую очередь связанных с гастроэзофагеальным рефлюксом, имевшихся до операции, без подтвержденных рентгенологически либо эндоскопически признаков рецидива ГПОД, которые, вероятно, обусловлены недостаточной функцией сформированной анти-рефлюксной манжетки. Дисфагию в нашем исследовании мы разделяли на 2 подгруппы. Функциональная дисфагия (послеоперационная) - возникающая в раннем послеоперационном периоде, обусловленная реакцией и адаптацией пациента к сформированной фундопликационной манжетке, при которой симптомы сохраняются не более 2-3 месяцев и проходят самостоятельно. Стойкая длительная дисфагия -патологическое состояние, возникающее либо сохраняющееся в сроки более 3 месяцев, симптоматика может нарастать со временем и даже потребовать повторной операции.
Контрольные осмотры проводились через 3, 6 и 12 месяцев после операции, затем ежегодно в течении 5 лет либо внепланово при возникновении жалоб. Объективные методы обследования после операции включали полипозици-онное рентгенологическое исследование, эндоскопическое исследование и, при необходимости, для пациентов, имевших рецидив жалоб ГЭРБ, суточный внутрипищеводный рН-мониторинг с расчетом индекса DeMeester. При подозре- нии на анатомический рецидив либо у пациентов, имевших рецидив ГЭРБ, обязательным компонентом дообследования являлась компьютерная томография. Субъективные методы включали изучение соматического статуса при помощи специализированного опросника GERD-HRQL (GERD-Health Related Quality of Life Questionnaire). Общим недостатком всех аналогичных анкет-опросников качества жизни является невозможность оценки атипичных симптомов за-болеваниядання. Однако, предложенный Velanovich в 1996 году, опросник GERD-HRQL является наиболее специфичным при оценке результатов хирургического лечения ГПОД и ГЭРБ, что подтверждено в ряде публикаций [17].
Статистический анализ был проведен в программе RStudio Version 1.2.1335© 2009-2019 RStudio, Inc., GPL. Количественные переменные представлены в виде среднего и стандартного отклонения, т.к все они имели нормальное распределение (тест Шапиро - Уилка). При сравнении двух независимых групп с количественными переменными был использован T-критерий Стьюдента. Номинальные и порядковые переменные представлены в виде процентов. Для сравнения номинальных шкал применялся критерий Пирсона, если не более 20% ожидаемых частот было меньше 5, в противном случае применялся точный критерий Фишера.
Результаты исследования
По возрасту, полу, характеру жалоб, типу грыжи, выраженности рефлюкс-эзофагита, частоте симультанных операций и способу фундопликации группы пластики швом и аллотрансплантатом были сопоставимы (Таблица 1).
Возраст больных в исследовании колебался от 26 до 74 лет. Средний возраст в группе, где использовалась пластика швом составил 49±5,1 лет, в группе аллопластики - 54±6,4 года соответственно. Как в группе шва, так и группе аллопластики преобладали женщины - 55,1% и 58,6% соответственно.
Таблица 1
Характеристика групп на дооперационном этапе
|
Прогностический признак |
Пластика швом, n=69 |
Аллопластика, n=29 |
Уровень значимости |
|
Пол |
p=0,75 |
||
|
Мужской |
31(44,9%) |
12(41,4%) |
|
|
Женский |
38(55,1%) |
17(58,6%) |
|
|
Возраст, лет (SD) |
49±5,1 |
54±6,4 |
p=0,42 |
|
Основные жалобы |
|||
|
Изжога |
39(56,5%) |
14(48,3%) |
р=0,46 |
|
Боль в эпигастрии и за грудиной |
52(75,4%) |
20(69%) |
р=0,42 |
|
Дисфагия |
9(13%) |
5(17,2%) |
p=0,59 |
Продолжение Таблицы 1
|
Тип грыжи |
p=0,63 |
||
|
Параэзофагеальная |
32(46,4%) |
15(57,7%) |
|
|
Смешанная |
37(53,6%) |
14(48,3%) |
|
|
Способ фундопрликации |
|||
|
По Ниссену |
43(62,3%) |
17(58,6%) |
0,73 |
|
По Тупе |
26(37,7%) |
12(41,4%) |
|
|
Симультанные операции |
12(17,4%) |
4(13,8%) |
p=0,66 |
По типу грыжи по классификации Василенко пациенты распределились следующим образом: в группе, где применена пластика ножек швом параэзофагеальные грыжи отмечены у 32(46,4%) пациентов, смешанные у 37(53,6%) пациентов. В группе, где применялась аллопластика параэзофагеальные грыжи диагностированы у 15(57,7%) пациентов, смешанные у 14(48,3%) пациентов.
Наиболее часто отмечаемыми клиническими проявлениями ГПОД у данной категории больных явились тяжесть и боль в эпигастрии и за грудиной, усиливающаяся после еды или при наклоне туловища вперед. Данные жалобы на момент обращения предъявляли 52(75,4%) пациента в группе шва, в группе аллопластики - 20(69%) пациентов. Жалобы, связанные с ГЭРБ отмечены в группе шва у 39(56,5%)пациентов, в группе аллопластики - у 14(48,3%) пациентов. Жалобы на дисфагию различной степени отмечены у 9(13%) пациентов в группе шовной пластики и у 5(17,2%) пациентов в группе аллопластики. У всех пациентов при фиброгастродуоденоскопии был отмечен гастроэзофагеальный рефлюкс, преимущественно I-II степени (по классификации Савари-Миллера), однако в данной группе пациентов клинические проявления имелись лишь у 53(54%) больных.
При сочетании ГПОД с другой хирургической патологией выполнялись симультанные вмешательства. В группе шовной пластики по поводу желчекаменной болезни оперативное вмешательство дополнено холецистэктомией у 8(11,6%) пациентов, по поводу грыж передней брюшной стенки у 4(5,8%) пациентов выполнена лапароскопическая грыжепластика. В группе аллопластики симультанные операции по поводу желчекаменной болезни выполнены 2(6,9%), по поводу грыж передней брюшной стенки у 2(6,9%) пациентов. Как в группе пластики швом, так и аллопластики чаще применялась фундопликация по Ниссену - у 43(62,3%) и 17(58,6%) пациентов соответственно. Фундопликация по Тупе в группе шва и группе аллопластики применена у 26(37,7%) и 12(41,4%) пациентов соответственно.
Летальных исходов после оперативных вмешательств в обеих группах исследования отмечено не было.
В группе шовной пластики ПОД интраоперационные осложнения отмечены у 7(10,1%) пациентов, в группе аллопластики ПОД - у 2(6,9%) пациентов. В обеих группах интраоперационно имели место случаи острой кровопотери -у 7(7,1%) пациентов, и травмы пищевода во время выделения грыжевого мешка и мобилизации в средостении - у 2(2%) пациентов. Во всех случаях объем острой кровопотери не превышал 125 мл (25-125 мл), кровотечение было остановлено коагуляцией кровоточащего сосуда. При травме пищевода дефект ушивался.
Во время высокой мобилизации пищевода либо при выделении грыжевого мешка в средостении достаточно часто отмечается травма плевры с развитием интраоперационного карботоракса. Травма плевры в группе с пластикой швом отмечена у 5(7,2%) пациентов, в группе аллопластики - у 4(13,8%) пациентов. Данная ситуация, на наш взгляд, не требует отдельного дренирования плевральной полости, у всех пациентов в течении суток карботоракс разрешался самостоятельно путем удлинения абдоминального дренажа по Бюлау.
Частота послеоперационных осложнений в группе с фундопликацией по Тупе составила 6,5% (4 пациента), а в группе с фундопликацией по Ниссену - 8,3% (9 пациентов) (Таблица 2).
Таблица 2
Структура послеоперационных осложнений после хирургического лечения пациентов с ГПОД, осложненных ГЭРБ
|
Причина осложнения |
Пластика швом, n=69 |
Аллопластика, n=29 |
|
Пароксизм фибрилляции предсердий, n(%) |
1(1,5%) |
1(3,5%) |
|
Гастростаз, n(%) |
1(1,5%) |
1(3,5%) |
|
Нижнедолевая пневмония, n(%) |
1(1,5%) |
- |
|
Фебрильная лихорадка, n(%) |
2(2,9) |
1(3,5%) |
|
Полная дисфагия |
1(1,5%) |
- |
|
Всего, n(%) |
6(8,7%) |
3(10,4%) |
Из тяжелых осложнений следует отметить у 1 пациентки в группе шовной пластики на 2-е сутки послеоперационного периода развилась полная дисфагия, подтвержденная рент-генконтрастным исследованием, что потребовало повторного оперативного вмешательства и переформирования фун-допликационной манжетки. Остальные послеоперационные осложнения не носили тяжелого характера и были купированы назначением симптоматического лечения. Так у 1 пациента так в группе шовной пластики и 1 пациента в группе аллопластики в раннем послеоперационном периоде отмечен пароксизм фибрилляции предсердий, у 1 пациента так в группе шовной пластики и 1 пациента в группе аллопластики длительно сохранялись симптомы гастростаза, не смотря на проводимое лечение, что потребовало продолжения терапии прокинетиками в позднем послеоперационном периоде. У 1 пациента в группе пластики швом на 4 сутки после- операционного периода на фоне сохраняющейся лихорадки диагностирована левосторонняя нижнедолевая пневмония. Так же у 2 пациентов в группе шовной пластики и 1 пациента в группе аллопластики отмечены случаи фибрильной лихорадки, причину которой при помощи дополнительных обследований установить не удалось, что потребовало продолжения антибиотикотерапии до 7 суток.
Длительность оперативного вмешательства в группе шовной пластики составила 141±21,1 мин, в группе аллопластики - 179±28,4 мин. Длительность пребывания в стационаре в группе шовной пластики составила 6,7±1,6 дня, в группе аллопластики - 6,9±1,8 дня. Послеоперационный койко-день в общем в обеих группах составил 4,3±1,2 дня. Непосредственные результаты хирургического лечения грыж пищеводного отверстия диафрагмы с использованием вышеуказанных методик фундопликации отображены в Таблице 3.
Таблица 3
Непосредственные результаты хирургического лечения пациентов с ГПОД, осложненных ГЭРБ
|
Пластика швом, n=69 |
Аллопластика, n=29 |
Уровень значимости |
|
|
Длительность операции, мин (SD) |
141±21,1 |
179±28,4 |
p=0,41 |
|
Длительность пребывания в стационаре, дней (SD) |
6,7±1,6 |
6,9±1,8 |
p=0,82 |
|
Частота интраоперационных осложнений, n(%) |
7(10,1%) |
2(6,9%) |
p=0,6 |
|
Частота послеоперационных осложнений, n(%) |
6(8,7%) |
3(10,4%) |
p=0,8 |
|
Функциональная дисфагия, n(%) |
11(15,9%) |
6(20,7%) |
p=0,58 |
При оценке непосредственных результатов выполненных операций случаи функциональной дисфагии не включались в структуру послеоперационных осложнений и оценивались отдельно. Функциональная дисфагия легкой степени тяжести отмечена у 11(15,9%) пациентов в группе шовной пластики и у 6(20,7%) в группе аллопластики.
Отдаленные результаты выполненных оперативных вмешательств оценены при помощи совокупности субъективных и объективных методов в сроки от 12 месяцев до 6,5 лет, в среднем период наблюдения за пациентами составил 4,5 года (Таблица 4).
Таблица 4
Отдаленные результаты пластики ГПОД
|
Пластика швом, n=109 |
Аллопластика, n=62 |
Уровень значимости |
|
|
Анатомический рецидив |
8(11,6%) |
2(6,9%) |
p=0,47 |
|
Функциональный рецидив |
6(8,7%) |
2(6,9%) |
p=0,76 |
|
Рецидив в целом |
14(20,3%) |
4(13,8%) |
p=0,44 |
|
Дисфагия |
2(2,9%) |
4(13,8%) |
p=0,053 |
|
Бал по GERD – HRQL |
6,4±1,8 |
5,9±2,1 |
p=0,84 |
|
Неудовлетворительный результат по GERD – HRQL |
9(13%) |
5(17,2%) |
Р=0,59 |
Через 1 год рецидивы в группе шовной пластики отмечены у 6(8,7%) пациентов. Среди них у 4(5,8%) пациентов имел место анатомический рецидив, подтвержденный рентгенологически. У 2(2,9%) пациентов имелся рецидив ГЭРБ без подтвержденного рентгенологически анатомического рецидива. В группе аллопластики через 1 год наблюдения рецидив отмечен у 1(3,5%) пациента и был связан с возвратом гастроэзофагеального рефлюкса. Через 5 лет после оперативного вмешательства рецидивы в группе шовной крурорафии отмечены у 14(20,3%) пациентов. Среди них анатомический рецидив диагностирован у 8(11,6%) пациентов, рецидивы функционального характера, связанные с появлением клиники ГЭРБ выявлены у 6(8,7%) пациентов. В группе крурорафии с аллопластикой рецидивы диагностированы у 4(13,8%) пациентов. Из них анатомический рецидив отмечен у 2(6,9%) пациентов, функциональный рецидив - у 2(6,9%) пациентов.
Стойкая длительная дисфагия при приеме плотной пищи в позднем послеоперационном периоде как ведущий симптом отмечена у 2(2,9%) пациентов в группе шовной круро-рафии. В группе крурорафии с аллопластикой стойкая длительная дисфагия отмечена у 4(13,8%) пациентов. В группе аллопластики дисфагия носила более тяжелый, рефрактерный к терапии (баллонной дилятации) характер. Однако стоит отметить, что у 4(66,7%) пациентов с наблюдаемой стойкой длительной дисфагией в последующем был диагностирован анатомический рецидив ГПОД.
При изучении функциональных результатов хирургического лечения пациентов, страдающих ГПОД были получены следующие результаты. В группе пластики швом суммарный балл по шкале-опроснику GERD – HRQL через 5 лет после операции составил 6,4±1,8 в сравнении с исходным доопера-ционным показателем 29,4±6,1 балла. Через 5 лет после опе- ративного лечения 45(65,2%) пациента были удовлетворены своим состоянием, нейтрально результаты оперативного вмешательства оценили 15(21,7%) пациентов, неудовлетворены были 9(13%) пациентов. В группе аллопластики суммарный балл по шкале-опроснику GERD – HRQL через 5 лет после операции составил 5,9±2,1 в сравнении с исходным до-операционным показателем 27,8±5,7 балла. Через 5 лет после оперативного лечения 17(58,6%) пациента были удовлетворены своим состоянием, нейтрально результаты оперативного вмешательства оценили 17(24,1%) пациентов, неудовлетворены были 5(17,2%) пациентов.
Обсуждение
Одной из основных проблем после лапароскопической пластики ГПОД является высокая частота возникновения рецидива, частота которого колеблется от 10%-40%[4,9], а в отдельных источниках достигая 50%-60% [11,12]. Хотя сразу стоит отметить, что четкого определения рецидива в настоящий момент в литературе не имеется. Так часть авторов под рецидивом после пластики ГПОД понимают только непосредственно пролабирование содержимого брюшной полости в средостение в следствие расширения ранее редуцированного пищеводного отверстия диафрагмы. Наиболее часто встречаемый параметр анатомического рецидива -пролабирование в средостение более 2 см [11,18]. Часть авторов под рецидивом после пластики ГПОД понимают любое нарушение ранее сформированной анатомической конструкции, в том числе, помимо рецидива грыжевого дефекта ПОД, миграцию либо разрушение фундопликационной манжетки [4,9,16]. Так же часть хирургов под рецидивом понимает любой неудовлетворительный результат ранее выполненной операции, к выше указанному добавляя и так называемые рецидивы функционального характера, при которых имеется рецидив клиники ГЭРБ либо появление упорной дисфагии без рентгенологически либо эндоскопически подтвержденного случая анатомического рецидива [4].
С целью улучшения отдаленных результатов, некоторые хирурги, по аналогии с пластикой грыж передней брюшной стенки, предложили использовать сетчатые протезы при пластике больших дефектов ПОД, в особенности в случаях, где закрытие хиатального отверстия без натяжения имеет опе-ределенные трудности. Первая хиатопластика с использованием аллотрансплантата была описана в 1993 году Kuster и Gilroy [13], в последующем данная методика приобрела широкое распространение. Так по данным Society of American Gastrointestinal Endoscopic 23% опрошенных хирургов рутинно используют сетку при пластике ГПОД, 67% предпочитают использовать рассасывающиеся материаллы [20]. При первых аллопластиках ГПОД с использовались нерассасываю-щиеся сетчатые импланты, в частности полипропиленовые или политетрафторэтиленовые (ПТФЭ) [4,14,19]. По мере накопления опыта по применению аллопластики, появились публикации посвященные отсроченным осложнениям, наиболее тяжелыми из которых являются аррозия сетки в желудок или пищевод и дисфагия, требующих повторных, а иногда и инвалидизирующих, оперативных вмешательств, таких как эзофагэктомия или гастрэктомия, что подвигло хирургов к разработке и внедрению полностью рассасывающихся и биологических сетчатых имплантов, позволяющих нивелировать осложнения синтетических материалов [12,16].
Первое рандомизированное исследование, посвященное эффективности синтетической сетки при пластике ГПОД, опубликованно Frantzides et al. [14] в 2002 году, где показано значительное снижение частоты рецидива - 0/36 в группе аллопластики в сравнении с шовной пластикой – 8/36 (22%). Похожие данные опубликованы в рандомизированном исследовании Granderath et al. [19] в 2005 году, где частота рецидива в группе аллопластики синтетической не рассасывающейся сеткой 8%(4\50) против и 26%(13\50) в группе простой шовной пластики. В рандомизированном многоцентровом исследовании Oelschlager et al. [12], опубликованном в 2006 году, отмечено значимое снижение частоты рецидивов в группе биологической сетки (small intestinal submucosa) 8,9%(4\45) в сравнении с группой шовной пластики 24%(12\50). Однако во всех исследованиях период наблюдения за пациентами не превышал 2 лет. В раномизированном исследовании, опубликованном Watson et al. [16] в 2015 году, проведена оценка эффективности использования синтетического и биологического сетчатых протезов в сравнении с обычным шовным методом, где было показано отсутствие различий между группами по частоте рецидивов в отдаленном периоде – 12,8%, 30,8% и 23,1% соответственно. Более того, в 2011 году Oelschlager et al. опубликовал отдаленные результаты вошедших в рандомизированное исследование пациентов и про- слеженных 4 и более года (медиана наблюдения 58 месяцев) и отметил отсутствие разницы между группами шовной пластики и аллопластики, при этом показав высокую частоту рецидива 59%(20\39) в группе шовной пластики и 54%(14\33) после пластики биологической сеткой. В остальных трех рандомизированных исследованиях отдаленные результаты в последующем не обновлялись.
Практически все метаанализы, опубликованные на сегодняшний день, отмечают преимущество использования сетчатых имплантов в сравнении с шовной пластикой. Наиболее крупными за последние несколько лет являются Tam et al. [21] (2016) проанализировавший 13 исследований, 1194 пациента: 673 с пластикой сеткой и 521 с пластикой швом. Частота рецидива составила 13% в группе пластики сеткой против 24% пластики швом (ОР 0.51, 95%; ДИ 0.30–0.87; p=0.014). В метаанализе Huddy et al. [22] (2016) проанализированы 9 исследований, 676 пациентов: 310 пациентов с пластикой швом, 214 пациентов с пластикой синтетической сеткой, и 152 пациента с пластикой биологической сеткой. Применение сетки при пластике ГПОД позволило снизить частоту рецидива до 14.5% в сравнении с пластикой швом 24.5%, ОР=0.36(95 % ДИ 0.17–0.77); р=0.009. В этом же исследовании показано отсутствие преимуществ биологического сетчатого импланта перед обычной пластикой швом, где частота рецидива составила 17.1 % против 23.4% соответственно (95% ДИ 0.26–1.83; р=0.457). Частота повторных операций статистически не отличалась. В этом же исследовании при опросе хирургов 67% респондентов отметили, что постоянно используют сетку при пластиках больших ГПОД, отдавая предпочтение синтетическому нерассасывающемуся материалу, но 21% респондентов хотя бы один раз в своей практике встречался с эрозией сетчатого импланта. Аналогичные результаты получены в последних метаанализах. В опубликованном исследовании Zhang et al. [23] (2017), где проанализированы результаты лечения 719 пациентов с использованием сетчатого импланта и 755 с первичной пластикой швом, частота рецидива составила 2.6% против 9.4% соответственно (ОШ 0.23, 95% ДИ 0.14–0.39, р=0.00001). В метаанализе Sathasivam et al. [24] (2019) проанализированы результаты лечения 942 пациентов (пластика сеткой - 517 пациентов, шовная круропла-стика - 425 пациентов), где так же отмечено преимущество пластики сетчатым имплантом (ОШ 0.48, 95% ДИ:0.32-0.73, р<0.05). Во всех вышеуказанных исследованиях не отмечено существенной разницы по частоте интраоперационных и послеоперационных осложнений.
Тем не менее, как в самих метаанализах, так и при анализе имеющихся в литературе данных, нами, как и рядом других авторов, отмечен главный недостаток - медиана наблюдения за пациентами в большинстве опубликованных исследований не превышает 1-2 года, не смотря на то, что многие исследования на данный момент могли бы быть дополнены более точными отдаленными результатами с более длительным периодом наблюдения, повторные публикации отсутствуют. При этом, в большинстве публикаций период наблюдения за пациентами с пластикой швом иногда существенно превышает период наблюдения при использовании сетки. Большинство использованных для метаанализа публикаций имеют уровень доказательности 2В и ниже [18]. Возникновение ассоциированных с имплантацией сетки осложнений, как правило, отмечается авторами в более поздние сро-ки[15,18]. Более того, в последние годы появляется все больше отдельных публикаций, имеющих период наблюдения более 3 лет, отмечающих отсутствие преимущества пластики сеткой в сравнении с шовным методом[11,16,25]. Главным выводом анализа литературы является то, что исследования по эффективности применения сетчатых имплантов при пластике ГПОД должны продолжаться в направлении уточнения отдаленных результатов с медианой наблюдения 5 лет и более, что отмечается и в некоторых метаанализах [21,22,23,24].
Из отмеченных в исследовании 9(9,2%) послеоперационных осложнений 8(88,9%) относились I стадии по классификации Clavien-Dindo и были без особых усилий купированы консервативно. Лишь 1(1%) послеоперационное осложнение потребовало повторного оперативного вмешательства. По данным литературы частота послеоперационных ослож- нений колеблется в среднем от 5% до 20%[4,9,20,21,22,23]. По данным Kaplan et al. [26] при анализе результатов 10273 пациентов частота послеоперационных осложнений составила 5,2% при плановых операциях. В одном из последних рандомизированных исследований Oor et al. послеоперационные осложнения отмечены в 11,1% (8\72) [25]. По данным Tam et al.[21] при анализе результатов 753 пациентов при плановых операциях данный показатель составил 18%, однако в результаты включена послеоперационная дисфагия. В целом в проведенном нами исследовании показатели частоты интраоперационных и послеоперационных осложнений не отличалась между группами исследования и соответствовали имеющимся литературным данным.
Заключение
Лапароскопические операции по поводу ГПОД, осложненных ГЭРБ являются высокоэффективным и безопасным методом лечения данной категории пациентов, имеют минимальную летальность, низкий процент осложнений. Полученные в нашем исследовании отдаленные результаты сравнения эффективности использования сетчатых имплантов не показали преимущества перед обычной шовной пластикой дефекта ПОД. Учитывая так же возможное появление тяжелых осложнений в позднем послеоперационном периоде, таких как аррозия сетчатого импланта или тяжелой дисфагии, мы не можем рекомендовать рутинное применение аллопластики при лапароскопической коррекции ГПОД. Однако, беря во внимание имеющиеся противоречивые литературные данные, исследования по эффективности использования сетчатых имплантов нуждаются в уточнении и должны быть продолжены.
Список литературы Эффективность применения сетчатых имплантов при лапароскопической пластике грыж пищеводного отверстия диафрагмы
- Пучков К.В., Филимонов В.Б. Грыжи пищеводного отверстия диафрагмы. М.: Медпрактика-М, 2003. 172 с.
- Andolfi C., Jalilvand A., Plana A., Fisichella P.M. Surgical Treatment of Paraesophageal Hernias: A Review. J Laparoendosc Adv Surg Tech A. 2016, 26(10), pp. 778-783. DOI: 10.1089/lap.2016.0332
- Родин А.Г., Базаев А. В, Никитенко А.И. Хирургическое лечение грыж пищеводного отверстия диафрагмы у больных пожилого возраста // Медицинский альманах. 2014. 3. C.117-120.
- Грубник В.В., Малиновский А.В. Критические аспекты лапароскопической хирургии гастроэзофагеальной рефлюксной болезни и грыж пищеводного отверстия диафрагмы: монография / Грубник В.В., Малиновский А.В. Одесса: ВМВ-типография, 2015. 106 с., илл. - 34 с.
- Зябрева И.А., Джулай Т.Е. Грыжи пищеводного отверстия диафрагмы: спорные, нерешенные и перспективные аспекты проблемы (обзор литературы) // Верхневолжский медицинский журнал. 2015.14(4). C. 24-28.
- Калинина Е.А., Пряхин А.Н. Технические аспекты лапароскопической пластики грыж пищеводного отверстия диафрагмы: обзор литературы и собственный опыт // Вестник Южно-Уральского ГУ. Серия "Образование, здравоохранение, физическая культура". 2014. 14(3). C. 54-60.
- Грубник В.В., Малиновский А.В. Анализ отдаленных результатов лапароскопической пластики грыж пищеводного отверстия диафрагмы и фундопликации по Ниссену // Клiнiчна хiрургiя. 2012. 10. C. 34-36.
- Lebenthal A., Waterford S.D., Fisichella P.M. Treatment and controversies in paraesophageal hernia repair. Front Surg. 2015, 2(13).
- DOI: 10.3389/fsurg.2015.00013
- Kohn G.P., Price R.R., DeMeester S.R., Zehetner J. Guidelines for the management of hiatal hernia. Surgical endoscopy. 2013, 27(12), pp. 44094428.
- DOI: 10.1007/s00464-013-3173-3/
- Повторные лапароскопические операции при рецидиве гастроэзофагеальной рефлюксной болезни и грыжи пищеводного отверстия диафрагмы / Э.А. Галлямов// Хирургия. Журнал им. Н.И. Пирогова. 2019. 2. C. 26-31.
- DOI: 10.17116/hirurgia201902126
- Dallemagne B, Kohnen L, Perretta S, Weerts J, Markiewicz S, Jehaes C. Laparoscopic repair of paraesophageal hernia. Long-term follow-up reveals good clinical outcome despite high radiological recurrence rate. Ann Surg. 2011. 253. pp. 291- 296.
- Oelschlager BK, Pellegrini CA, Hunter JG, Brunt ML, Soper NJ, Sheppard BC et al. Biologic prosthesis to prevent recurrence after laparoscopic paraesophageal hernia repair: long-term follow-up from a multicenter, prospective, randomized trial. J Am Coll Surg. 2011, 213, pp. 461-468.
- DOI: 10.1016/j.jamcollsurg.2011.05.017
- Kuster G.G., Gilroy S. Laparoscopic technique for repair of paraesophageal hiatal hernias. J Laparoendosc Surg. 1993, 3, pp. 331-338.
- DOI: 10.1089/lps.1993.3.331
- Frantzides C.T., Madan A.K., Carlson M.A., Stavropoulos G.P. A prospective, randomized trial of laparoscopic polytetrafluoroethylene (PTFE) patch repair vs simple cruroplasty for large hiatal hernia. Arch Surg. 2002, 137, pp. 649-652.
- DOI: 10.1001/archsurg.137.6.649
- Li J., Cheng T. Mesh erosion after hiatal Hernia repair: the tip of the iceberg? Hernia. 2019 Dec, 23(6), pp. 1243-1252.
- DOI: 10.1007/s10029-01902011-w
- Watson DI, Thompson SK, Devitt PG, Smith L, Woods SD, Aly A et al. Laparoscopic repair of very large hiatus hernia with sutures vs a able vs non-absorbable mesh - A randomized controlled trial. Ann Surg. 2015, 261, pp. 282-289.
- DOI: 10.1097/SLA.0000000000000842
- Velanovich V. Comparison of generic (SF-36) vs. disease-specific (GERD-HRQL) quality-of-life scales for gastroesophageal reflux disease. J Gastrointest Surg. 1998, 2, pp. 141-5.
- DOI: 10.1016/s1091-255x(98)80004-8
- Balague C., Fdez-Ananı'n S., Sacoto D., Targarona E.M. Paraesophageal Hernia: To Mesh or Not to Mesh? The Controversy Continues. J Laparoendosc Adv Surg Tech. 2020 Feb, 30(2), pp. 140-146.
- DOI: 10.1089/lap.2019.0431
- Granderath FA, Schweiger UM, Kamolz T, Asche KU, Pointner R. Laparoscopic Nissen fundoplication with prosthetic hiatal closure reduces postoperative intrathoracic wrap herniation: Preliminary results of a prospective randomized functional and clinical study. Arch Surg. 2005, 140, pp. 40-48.
- DOI: 10.1001/archsurg.140.1.40
- Bernabé M.Q., Adelina E.C. Use of absorbable meshes in laparoscopic paraesophageal hernia repair. World J Gastrointest Surg. 2019, 11(10), pp. 388-394.
- DOI: 10.4240/wjgs.v11.i10.388
- Tam V., Winger D.G., Nason K.S. A systematic review and metaanalysis of mesh versus suture cruroplasty in laparoscopic large hiatal hernia repair. Am J Surg. 2016 Jan, 211(1), pp. 226-38.
- DOI: 10.1016/j.amjsurg.2015.07.007
- Huddy J.R., Markar S.R., Ni M.Z., Morino M., Targarona E.M., Zaninotto G. et al. Laparoscopic Repair of Hiatus Hernia: Does Mesh Type Influence Outcome? A Meta-Analysis and European Survey Study. Surg Endosc. 2016, 30(12), pp. 5209-5221.
- DOI: 10.1007/s00464-0164900-3
- Zhang C., Liu D., Li F., Watson D.I., Gao X., Koetje J.H. Systematic review and meta-analysis of laparoscopic mesh versus suture repair of hiatus hernia: objective and subjective outcomes. Surg Endosc. 2017, 31(12), pp. 4913-4922.
- DOI: 10.1007/s00464-017-5586-x
- Sathasivam R, Bussa G, Viswanath Y, Obuobi RB, Gill T, Reddy A et al. Mesh hiatal hernioplasty versus suture cruroplasty in laparoscopic paraoesophageal hernia surgery; a systematic review and meta-analysis. Asian J Surg. 2019, 42. pp. 53-60.
- DOI: 10.1016/j.asjsur.2018.05.001
- Oor J.E., Roks D.J., Koetje J.H., Broeders J.A., Westreenen H.L., Nieuwenhuijs V.B. et al. Randomized clinical trial comparing laparoscopic hiatal hernia repair using sutures versus sutures reinforced with nonаbsorbable mesh. Surg Endosc. 2018, 32(11), pp. 4579-4589.
- DOI: 10.1007/s00464-018-6211-3
- Kaplan J.A., Schecter S., Lin M.Y., Rogers S.J., Carter J.T. Morbidity and Mortality Associated With Elective or Emergency Paraesophageal Hernia Repair. JAMA Surg. 2015, 150(11), pp. 1094-1096.
- DOI: 10.1001/jamasurg.2015.1867
- Müller-Stich B.P., Holzinger F., Kapp T., Klaiber C. Laparoscopic hiatal hernia repair: long-term outcome with the focus on the influence of mesh reinforcement. Surg Endosc Other Interv Tech. 2006, 20(3), pp. 380-384.
- DOI: 10.1007/s00464-004-2272-6


