Эффективность радикальных реконструктивных операций при мочепузырном кровотечении
Автор: Латыпов В.Р., Дамбаев гЦ., Вусик А.Н., Воробьев В.М., Хурсевич Н.А.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Лекции
Статья в выпуске: 2 (26), 2008 года.
Бесплатный доступ
Устранение мочепузырного кровотечения, обусловленного местно-распространенным раком мочевого пузыря, опухолевыми поражениями органов брюшной полости, лучевыми повреждениями, геморрагическим циститом - сложная клиническая задача. Выделена группа риска, состоящая из 40 пациентов, у которых консервативные и малоинвазивные способы лечения МПК оказались не эффективны. Из этой группы 22 пациентам проведено лечение в объеме радикальной цистэктомии и уретерокутанеостомии, остальным пациентам - цистэктомия с последующей одно- и многоэтапной кишечной мочевой диверсией по различным методикам. По результатам статистического анализа определены 4 прогностических критерия: возраст (р=0,027), болевой синдром (р=0,008), уретерогидронефроз (р=0,038), местная распространенность опухолевого процесса (для РМП) (р=0,05), на основании которых предложен алгоритм определения тактики оперативного лечения. При оценке отдаленных результатов лечения, согласно разработанной хирургической тактике, установлено, что показатели 3- и 5-летней безрецидивной выживаемости составили - 55,8 % и 47,8 %, общей - 71,2 % и 58,0% соответственно. Обоснованность предложенной оперативной тактики определена показателями выживаемости пациентов с различными видами деривации мочи, у пациентов с кишечными вариантами деривации 3- и 5-летняя выживаемость составили - 61,4 %, в то время как при уретерокутанеостомии 3-летняя равнялась 39,2 %, а 5-летняя не определялась.
Мочепузырное кровотечение, хирургическое лечение
Короткий адрес: https://sciup.org/14054838
IDR: 14054838 | УДК: 616.62-006.6-005.1-089
Efficacy of radical reconstructive surgeries in bladder hemorrhage
Despite considerable progress in recent years, medical management of bladder hemorrhage resulted from locally advanced bladder cancer, radiation-induced damages and hemorrhagic cystitis still remains a major problem. The study included 40 patients who previously received conservative and mini-invasive treatment for bladder hemorrhage, which appeared to be ineffective. Out of them, there were 22 patients who underwent radiacal cystectomy and uretherocutaneostomy and 18 patients who underwent cystectomy followed by one-or multi-stage intestinal urinary diversion according to various techniques. Results of statistical analysis showed 4 prognostic factors on the base of which the algorythm for the surgical treatment technique was suggested: age (p=0.027), pain syndrome (p=o.008), uretherohydronephrosis (p=0.038) and local tumor dissemination (for bladder cancer) (p=0.05). The 3-and 5-year recurrence-free survival rates were 55.8%) and 47.8%, respectively. The overall survival rates were 71.2% and 58.0%, respectively. The 3-and 5-year survival rates were 61.4% for patients with intestinal urinary derivation, while the 3-year survival rate was 39.2% and the 5-year survival rate was not determined for patients with uretherocutaneoustomy.
Текст научной статьи Эффективность радикальных реконструктивных операций при мочепузырном кровотечении
Мочепузырное кровотечение (МПК) – проявление самых разнообразных заболеваний как доброкачественной, так и злокачественной этиологии. Кровотечение при раке мочевого пузыря (РМП) является ведущим симптомом и встречается в 95–98 % случаев. Наиболее склонны к кровотечениям папиллярные образования, однако в случаях инвазивных и солидных образований с явлениями распада кровотечения часто принимают угрожающий для жизни пациента характер [1, 4–6]. Мультифокальная распространенность опухоли, стадии опухоли T2b–4aNxM0 являются показанием к радикальной цистэктомии (РЦЭ) [2, 3, 5]. Геморрагический цистит (ГЦ) – полиэтиологическое заболевание, проявляющееся кровотечением из слизистой мочевого пузыря (МП) различной степени интенсивности. Три фактора являются ведущими в этиологии ГЦ: химический, лучевой и инфекционный [9, 11]. Лучевую терапию на органы малого таза проводят при различных опухолевых поражениях, ГЦ после лучевой терапии может развиваться через 6 мес–10 лет. Патогенез кровотечения при этом состоянии обусловлен развитием облитерирующего эндартериита и развивающейся на этом фоне хронической ише- мии в подслизистом слое и стенке пузыря [7]. Лечение ГЦ осуществляется преимущественно консервативно, однако до 10–12 % пациентов требуют хирургического лечения [7, 10].
Цель исследования – на основании определенных прогностических факторов разработать последовательность лечебных мероприятий, определить тактику и объем оперативного лечения пациентам группы риска с МПК различной этиологии. Данное исследование является продолжением ранее проведенного исследования, связанного с лечением осложненных форм РМП (патент на изобретение № 2257856 от 10 августа 2005 г.).
Материал и методы
С сентября 1996 г. по февраль 2006 г. оперировано 40 пациентов с МПК. Критериями включения в анализируемую группу, которая расценена нами как группа риска, были следующие состояния: опухоль МП больших размеров (более 5 см) или мультифокальный рост опухоли; неэффективность гемостатической терапии на этапах предыдущего лечения; ранние рецидивы МПК; ранее перенесенные различные варианты органосохранного лечения; поражение МП опухолью органов брюшной полости; тяжелые лучевые повреждения МП и органов малого таза, как следствие лечения злокачественных опухолей; пациенты с развившимся геморрагическим шоком. У 30 (75 %) пациентов кровотечение обусловлено РМП, у 10 (25 %) – связано с другими вариантами поражения МП (рак ободочной кишки с вовлечением МП – 2 пациента, геморрагический цистит – 8 пациентов). Причиной развития ГЦ у 4 пациентов были лучевые поражения (лучевая терапия по поводу злокачественных новообразований матки), ишемический цистит был у 3 пациентов, интерстициальный цистит – в 1 случае. В исследуемой группе было 27 мужчин и 13 женщин. Средний возраст пациентов составил 61,1 года, от 43 до 82 лет; 40 пациентов группы имели 148 сопутствующих заболеваний, в среднем 3,7 заболевания на 1 пациента. Основную часть сопутствующих заболеваний составили поражения сердечно-сосудистой системы – 54 случая, заболевания желудочно-кишечного тракта выявлены у 52 пациентов. Большая часть пациен- тов предварительно получали консервативное или органосохранное хирургическое лечение по поводу МПК в хирургических стационарах. Пациенты с РМП обращались в среднем 0,9 (0–3) раза, а пациенты с другими заболеваниями МП – 5,1 (0–21) раза (p=0,001). Интенсивность кровотечения, эффективность гемостатической терапии в большой степени были обусловлены степенью поражения стенки МП и вовлечением в опухолевый процесс слизистой МП. В группе пациентов с РМП у 22 (73,3 %) имелось мультифокальное поражение стенки МП или очаговое поражение стенки больших размеров (более 5 см). В структуре распространенности опухолевого процесса у пациентов с РМП преобладали местно-распространенные формы – 26 пациентов, у 11 пациентов выявлено поражение регионарных лимфатических узлов, у 6 пациентов – отдаленные метастазы. У 29 пациентов опухоль была представлена переходноклеточным РМП, в 1 случае – плоскоклеточным РМП. Умеренно- и низкодифференцированные опухоли были у 27 (90 %) пациентов. В двух наблюдениях у пациентов с РМП и в одном, – у пациентов с другими поражениями на фоне продолжающегося кровотечения и неэффективности консервативных методов гемостаза наблюдался геморрагический шок. Всего осложнения дооперационного периода у пациентов с МПК имели место 63 раза (болевой синдром – 21, уретерогидронефроз – 17, ХПН – 6, анемия – 16). При обследовании выполнялись рутинные лабораторные исследования, УЗИ почек, печени, МП. Обязательным методом исследования являлась экскреторная урография, магниторезонансная или рентгеновская компьютерная томография. Цистоскопия выполнялась больным под наркозом с мультифокальной биопсией опухоли и слизистой МП с последующим морфологическим исследованием. Статистическая обработка выполнена программным пакетом Statistica 6,0 для Windows. Анализ выживаемости произведен по методу Каплана–Майера, для сопоставления групп применялся критерий Гехана–Вилкоксона. Сравнение результатов лечения различных групп пациентов проводилось параметрическим методом, используя t-критерий для зависимых выборок.
Результаты и обсуждение
При лечении МПК в стационаре использовался комплексный подход. Принцип ведения данной категории больных выстраивался следующим образом: всем пациентам в день поступления назначалось консервативное лечение или малоинвазивные вмешательства (постельное положение и покой; катетеризация МП, отмывание сгустков крови, постоянная ирригация физиологическим раствором хлористого натрия; медикаментозная терапия – антибиотики, спазмолитики, внутривенное введение этамзилата, 5 % р-ра аминокапроновой кислоты; внутрипу-зырное введение 0,5 % азотнокислого серебра; в случае анемии тяжелой степени – трансфузия препаратов крови. Если на момент поступления причина кровотечения не была известна, проводились диагностические мероприятия на фоне проведения гемостатической терапии. При возможности осуществлялась ТУР-коагуляция источника кровотечения. Неэффективность консервативных и малоинвазивных методов гемостаза, развитие опасных для жизни пациента осложнений служили показанием к выполнению операции удаления МП. Сравнивая показатели пациентов с РМП, подвергшихся различным способам устранения МПК, можно отметить, что наиболее молодой возраст был у пациентов, которым удалось добиться гемостаза консервативными мероприятиями, у этой же категории больных был наиболее короткий период кровотечения до госпитализации в стационар (табл. 1).
Характер радикального оперативного лечения представлен следующими подходами:
одноэтапное лечение – РЦЭ + кишечная деривация мочи – 10 (25 %) больных;
многоэтапное лечение – РЦЭ + УКС – консервативное лечение – варианты кишечной деривации мочи – 8 (20 %) больных;
РЦЭ + УКС как окончательный вариант лечения – 22 (55 %) больных.
Варианты кишечной деривации мочи в конечном итоге выполнены 18 пациентам, в том числе гетеротопический вариант мочевой диверсии – в 7 случаях (операция Бриккера – 2, операция Морра – 1, формирование резервуара низкого давления с механизмом удержания мочи – 3 (патент на изобретение № 2286098 от 27 октября 2006 г.), перевод ортотопического резервуара в гетеротопический операцией Китинга – 1). Ортотопический вариант мочевой диверсии использован в 11 наблюдениях (I-образная сигмокишечная пластика – 2, U-образный резервуар (патент на изобретение № 2279254 от 10 июля 2006 г.) – 6, Studer – 2, Reddy – 1). Показатели, отражающие пребывание пациентов в стационаре в зависимости от особенностей оперативного лечения, приведены в табл. 2.
Особенностью оперативного лечения пациентов с МПК являлось то, что сразу же после доступа в брюшную полость для уменьшения кровотечения выполнялось клипирование внутренней подвздошной артерии (использование конструкции из материала с памятью формы; патент на изобретение № 2218111 от 10 декабря
Таблица 1
|
Методика лечения |
Диагноз |
Возраст (лет) |
Длительность заболевания (мес) |
Длительность кровотечения (сут) |
|
Консервативное |
РМП (n=14) |
57,3 (43–70) |
6,3 ± 7,2 (0,6–20,6) |
60,8 ± 26,1 (21–110) |
|
Прочие (n=8) |
62,3 (45–71) |
40,1 ± 43,7 (4,7–126,7) |
513,8 ± 848,1 (40–2589) |
|
|
ТУР МП |
РМП (n=3) |
73,0 (67–82) |
2,3 ± 0,9 (1,3–2,9) |
67,7 ± 25,9 (38–86) |
|
ЦЭ |
РМП (n=13) |
61,7 (45–77) |
11,0 ± 14,4 (0,6–56,3) |
76,4 ± 69,0 (10–222) |
|
Прочие (n=2) |
61,5 (43–80) |
31,5 ± 7,6 (26,1–36,9) |
700,0 ± 565,7 (300–1100) |
Таблица 2
Зависимость показателей, отражающих пребывание пациентов в стационаре, от особенностей оперативного лечения
Причины и сроки наступления летальных исходов в раннем послеоперационном периоде
|
ЦЭ (n=22) |
Одноэтапные операции (n=10) |
Многоэтапные операции (n=8)* |
|
|
Возраст (лет) |
64,5 (43–82) |
56,6 (45–67) |
57,4 (43–67) |
|
Пребывание в стационаре до операции (сут) |
17,5 ± 12,6 (4–49) |
18,4 ± 21,2 (3–67) |
14,5 ± 7,3 (6–30) |
|
Длительность операции (мин) |
208,4 ± 67,3 (100–385) |
370,0 ± 95,4 (265–585) |
201,9 ± 74,5 (110–370) |
|
Операционная кровопотеря (мл) |
454,5 ± 255,4 (200–1100) |
613,0 ± 254,6 (350–1200) |
526,3 ± 389,8 (150–1200) |
Примечание: * – показатели, характеризующие первый этап операции РЦЭ.
Таблица 3
Характеристика групп пациентов с МПК в зависимости от способа устранения осложнения
2003 г.). У пациентов анализируемой группы не отмечено ни одного серьезного интраоперационного осложнения, но было 4 (10 %) летальных исхода в раннем послеоперационном периоде, из 4 пациентов – 3 мужчины, все страдали РМП (табл. 3). Все пациенты с РМП имели местнораспространенную и диссеминированную формы заболевания и низкую степень дифференцировки опухоли. Причиной смерти явились осложнения, связанные с сопутствующими заболеваниями.
К моменту анализа результатов лечения получены данные об общей и безрецидивной выживаемости для всех пациентов данной группы. За период наблюдения умерло 22 (55,0 %) пациента, из них 4 – в раннем послеоперационном периоде, в результате постоперационных осложнений. Средний возраст умерших пациентов – 65,4 года (от 53 до 82 лет). Продолжительность жизни после радикальной операции (без учета послеоперационной смертности) составила 19,0
± 21,9 (от 3,3 до 98,7) мес, из них 10 пациентов прожили до 12 мес (средний возраст – 64,3 года), 8 пациентов – больше 12 мес (средний возраст - 66,8 года). Прогрессирование основного заболевания явилось причиной смерти 11, сопутствующие заболевания – 7 больных. Из умерших пациентов у 15 способом отведения мочи явилась УКС, 7 пациентам были выполнены различные варианты кишечной пластики. Характеристики в группе прооперированных больных были подвергнуты анализу по следующим 10 переменным: диагноз заболевания, возраст пациента, количество сопутствующих заболеваний у одного больного, наличие болевого синдрома, наличие уретерогидронефроза с одной или обеих сторон, уровень анемии, количество осложнений у одного пациента до начала лечения, для РМП - местная распространенность опухолевого процесса (T), наличие или отсутствие поражения регионарных лимфатических узлов (N), гистопатологическая
1 <60 пет
б
Выживаемость пациентов с мочепузырным кровотечением в зависимости от возраста р - 0,027
1 осложнение
2 и> осложнений
50 ео /о 80 ео изо но
Месяцы
Нет осложнений
Выживаемость пациентов с мочепузырным кровотечением в зависимости от числа осложнений
до начала лечения р - 0,084
Месяцы
Выживаемость пациентов РМП с МПК от стадии Т
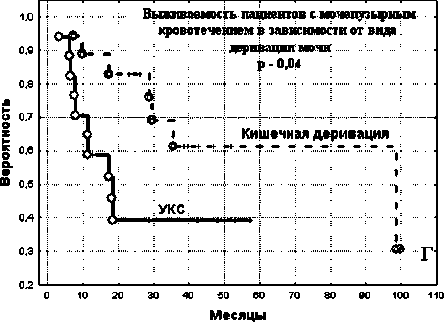
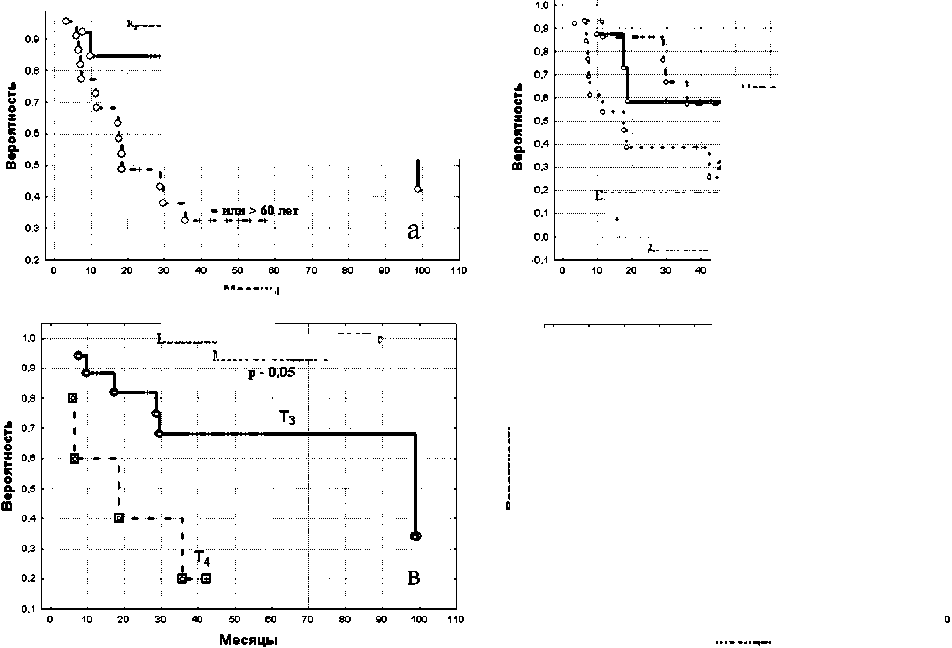
Рис. 1. Выживаемость пациентов с мочепузырным кровотечением, определенная по методу Каплана–Майера, в зависимости от статистически значимых прогностических факторов: а – в зависимости от возраста; б – в зависимости от количества осложнений на момент поступления в стационар (кроме кровотечения); в – в зависимости от местной распространенности опухолевого процесса (критерий Т); г – в зависимости от хирургического способа деривации мочи
дифференцировка опухоли (G). Статистически достоверными оказались 4 показателя: возраст пациента до 60 лет или от 60 лет и старше (p=0,027), наличие болевого синдрома (p=0,008), уретерогидронефроза (p=0,038), стадия T (для РМП) (p=0,05) (рис. 1а).
Выживаемость пациентов с МПК в зависимости от осложнений, развившихся до операции, представлена сравнением двух групп: в первую включены больные, имевшие 1 осложнение, во вторую - 2 и более (рис. 1б). Показатели выживаемости определялись методом Каплана–Майера. В нашем исследовании также показано, что прогностически значащим фактором является местная распространенность опухолевого процесса (критерий T). Выживаемость пациентов со стадией Т3 статистически была достоверно выше, чем при Т4 (рис. 1в). Однако этот показатель для определения тактики оперативного лечения нами не использовался, так как достоверно определяется только по результатам гистологического исследования операционного материала. Показаниями к радикальному оперативному лечению во всех случаях явились следующие состояния: неэффективность консервативных и малоинвазивных методов гемостаза, рецидив кровотечения, ранее перенесенные органосохранные способы лечения МПК, геморрагический шок. Основными критериями, определяющими тактику оперативного лечения, служили сочетания следующих факторов прогноза (рис. 2): диагноз заболевания, возраст пациента, количество сопутствующих заболеваний и количество осложнений, раз-
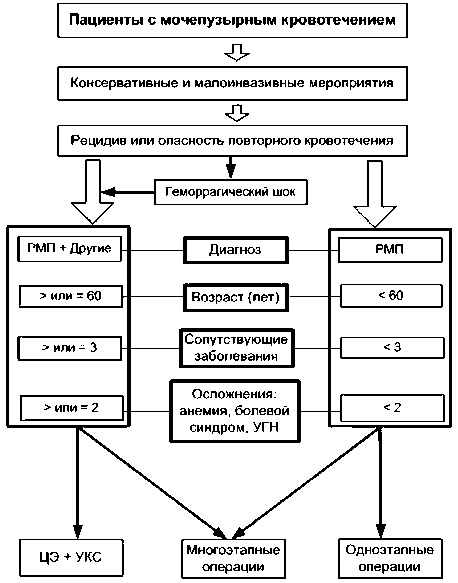
Рис. 2. Алгоритм определения тактики оперативного лечения у больных с мочепузырным кровотечением вившихся у пациента в результате основного заболевания (кроме МПК). При использовании предложенного алгоритма определения тактики лечения пациентов с МПК были получены следующие отдаленные результаты лечения: безрецидивная 3-летняя выживаемость составила 55,8 %, 5-летняя – 47,8 %; общая выживаемость соответственно – 71,2 % и 58,0 %. Правильность предложенной нами тактики подтверждается показателями выживаемости пациентов, которым выполнялись различные варианты кишечной мочевой диверсии и УКС.
У пациентов с кишечной деривацией мочи 3- и 5-летняя выживаемость равнялась 61,4 %, в то время как при УКС 3-летняя выживаемость составила 39,2 %, а 5-летняя выживаемость не определяется (p=0,04) (рис. 1г).
Таким образом, мочепузырное кровотечение в 85 % случаев имело опухолевую этиологию или явилось осложнением лучевой терапии по поводу злокачественной опухоли матки. Критерием, определяющим тактику оперативного лечения, является сочетание факторов прогноза: диагноза заболевания, возраста пациента, количества сопутствующих заболеваний и числа осложнений, развившихся у пациента до оперативного лечения.


