Эффективность терапии силденафилом у больных с легочной гипертензией различной этиологии: влияние на клинико-функциональный и гемодинамический статус, структурно-функциональное состояние правых и левых отделов сердца, сердечно-сосудистое сопряжение
Автор: Мартынюк Тамила Витальевна, Дадачева Заира Хаджимурадовна, Парамонов Виталий Михайлович, Саидова Марина Абдулатиповна, Наконечников Сергей Николаевич, Чазова Ирина Евгеньевна
Журнал: Евразийский кардиологический журнал @eurasian-cardiology-journal
Рубрика: Оригинальные статьи
Статья в выпуске: 1, 2017 года.
Бесплатный доступ
Цель: изучить эффективность терапии силденафилом при ЛГ различной этиологии, ее влияние на клинико-функциональный и гемодинамический статус, структурно-функциональное состояние правых и левых отделов сердца, сердечно-сосудистое (СС) сопряжение у больных с идиопатической легочной гипертензией (ИЛГ) и хронической тромбоэмболической легочной гипертензией (ХТЭЛГ). Материал и методы: в исследование включено 29 пациентов с ИЛГ в возрасте 42,8±10,6 лет, 28 больных с ХТЭЛГ в возрасте 43,4±10,4 лет II-IV функционального класса (ФК) (ВОЗ), получавших стабильную в течение 3 мес. стандартную терапию (антикоагулянты, диуретики, гликозиды) и антагонисты кальция. Силденафил назначался в стартовой дозе 10 мг 3 раза в сутки для оценки переносимости терапии с дальнейшим титрованием дозы через 1 нед. от начала лечения до 20 мг 3 раза в сут. Длительность лечения составила 16 недель. Исходно и через 16 недель оценивались ФК и тест 6-минутной ходьбы (Т6МХ), проводились трансторакальная эхокардиография (ЭхоКГ) и катетеризация правых отделов сердца (КПОС). Результаты: обе группы были сопоставимы по исходным функциональным характеристикам: ФК, дистанции в Т6МХ и индексу Борга. При анализе структурно-функциональных показателей сердца по данным ЭхоКГ исходно у всех пациентов с ИЛГ и ХТЭЛГ выявлено выраженное ремоделирование сердца по сравнению с контрольной группой (КГ), при сравнении 2-х групп ЛГ достоверных различий не выявлено. По данным КПОС у всех пациентов имелись критерии прекапиллярной ЛГ, обе группы были сопоставимы по уровню систолического давления в легочной артерии (СДЛА) и среднего давления в легочной артерии (ДсрЛА), сердечного выброса (СВ) и индекса (СИ), легочного сосудистого сопротивления (ЛСС), за исключением диастолического давления в легочной артерии (ДДЛА), которое в группе ИЛГ оказалось выше (38,3±13,7мм рт. ст.), чем в группе ХТЭЛГ (31,5±8,9мм рт. ст., p
Идиопатическая легочная гипертензия, хроническая тромбоэмболическая легочная гипертензия, ингибиторы фосфодиэстеразы типа 5, силденафил
Короткий адрес: https://sciup.org/14343384
IDR: 14343384
The efficacy of sildenafil therapy in patients with pulmonary hypertension of different etiology: influence on the clinical, functional, hemodynamic status, structure and function of the right and left heart, right ventricular-arterial coupling
Aim: to study the efficacy of sildenafil therapy in pulmonary hypertension of different etiology, its influence on the clinical, functional, hemodynamic status, structure and function of the right and left heart, right ventricular-arterial coupling (RVAC) in pts with idiopathic pulmonary hypertension (IPAH) and chronic thromboembolic pulmonary hypertension (CTEPH). Materials and methods: in the study we included 29 IPAH pts aged 42.8±10.6 yrs, 28 CTEPH pts aged 43.4±10.4 yrs II-IV functional class (FC) (WHO), receiving stable standard therapy (anticoagulants, diuretics, glycosides) and calcium channel blockers for at least 3 months. Sildenafil was started at the dose of 10 mg TID to assess the tolerability for further titration after 1 wk to 20 mg 3 times a day. The treatment duration was 16 wks. At baseline and at wk 16 FC (WHO), 6-minute walking test (6-MWT), transthoracic echocardiography (Echo) and right heart catheterization (RHC) were performed. Results: both groups were comparable in baseline functional parameters: FC, the distance in 6-MWT, Borg index. The analysis of baseline structural and functional cardiac parameters by Echo in IPAH and CTEPH pts revealed pronounced cardiac remodeling as compared to the control group. All pts had criteria precapillary PH by RHC with comparable systolic pulmonary artery pressure (SPAP), mean pulmonary artery pressure (PAPm), cardiac output (CO) and index (CI), pulmonary vascular resistance (PVR) except for diastolic PAP (DPAP), which was higher in IPAH group (38.3±13.7 mm Hg vs 31.5±8.9 mm Hg in CTEPH group (p
Текст научной статьи Эффективность терапии силденафилом у больных с легочной гипертензией различной этиологии: влияние на клинико-функциональный и гемодинамический статус, структурно-функциональное состояние правых и левых отделов сердца, сердечно-сосудистое сопряжение
фодиэстеразы типа 5 (ИФДЭ5) и стимуляторов растворимой гуанилатциклазы [4,5].
Хроническая тромбоэмболическая легочная гипертензия (ХТЭЛГ) представляет собой особую, потенциально излечимую патологию с помощью хирургического лечения – операции тромбэдартерэктомии [6,7]. Однако по результатам Европейского регистра операбельными являются примерно 60% пациентов [8]. В патогенезе неоперабельных форм важную роль играет дистальная васкулопатия за счет дисфункции эндотелия, когда включаются характерные для ЛАГ патофизиологические механизмы [6]. Вместе с тем, не все классы ЛАГ-специфической терапии доказали клиническую эффективность при неоперабельных формах ХТЭЛГ [1,8].
В 2011 г. для лечения пациентов с легочной гипертензией (ЛГ) Фармкомитетом РФ был одобрен ИФДЭ5 силденафил, который до настоящего времени является единственным представителем этого класса лекарственных препаратов [4]. Стандартная доза составляет 20 мг три раза в сутки.
Целью настоящего исследования явилось изучение эффективности терапии силденафилом у больных с ЛГ различной этиологии, ее влияния на клинико-функциональный и гемодинамический статус больных с идиопатической ЛГ (ИЛГ) и ХТЭЛГ, структурно-функциональное состояние и взаимосвязь правых и левых отделов сердца, сердечно-сосудистое сопряжение.
МАТЕРИАЛ И МЕТОДЫ
До включения в исследование пациентам с высокой ЛГ, госпитализированным для стационарного лечения в НИИ кардиологии им. А.Л. Мясникова ФГБУ «Российский кардиологический научно-производственный комплекс» МЗ РФ, проводилось комплексное клинико-инструментальное обследование для верификации диагноза ИЛГ и ХТЭЛГ.
Критериями включения явились: возраст >18 лет; верифицированный диагноз ИЛГ или ХТЭЛГ (неоперабельная форма); оценка гемодинамических параметров по данным катетеризации правых отдела сердца (КПОС) в течение последних 3 мес.; отрицательная острая фармакологическая проба на вазореактивность; функциональный класс (ФК) (ВОЗ) II-IV; прием стандартной лекарственной терапии ЛГ в течение последних 3-х мес.; стабильное течение заболевания на фоне проводимой терапии. Критериями исключения были: возраст <18 лет; ЛГ вследствие поражения сердца, лёгких, смешанная форма; несоблюдение методов контрацепции женщинами детородного возраста; беременность, лактация; хроническая обструктивная болезнь легких (FEV1 <70% от должного), рестриктивные заболевания легких (TLC <70% от должного); АГ или систолическое артериальное давление (САД) < 90 мм рт. ст.; заболевания опорно-двигательного аппарата, препятствующие проведению теста 6-минутной ходьбы (Т6МХ); изменения лекарственной терапии в течение последних 3-х мес., прием антагонистов рецепторов эндотелина, простаноидов, ингаляционного NO, ИФДЭ-5 в течение последних 3-х месяцев.
Всего в исследование по изучению эффективности терапии cилденафилом было включено 57 пациентов с ЛГ: 29 (50,8%) пациентов с ИЛГ (2 мужчины и 27 женщин) в возрасте от 19 до 62 лет; 28 (47,6%) пациентов с ХТЭЛГ (9 мужчин и 19 женщин) в возрасте от 20 до 63 лет. Группа контроля состояла из 22 здоровых добровольцев (5 мужчин и 17 женщин) в возрасте от 23 до 56 лет.
Таблица 1. Исходная характеристика групп больных с ЛГ
|
Показатели |
ИЛГ |
ХТЭЛГ |
|
Возраст, лет |
42,8±10,6 |
43,4±10,4 |
|
Пол, м/ж (n,%) |
2(6,8)/ 27(93,1) |
9 (33,3)/18 (66,6) |
|
Длительность периода от дебюта 1-х симптомов, годы |
2,1±0,8 |
1,8±1 |
Обе группы были сопоставимы по возрасту и длительности периода от дебюта 1-х симптомов, в них преобладали женщины. Различия между группами по полу соответствуют эпидемиологическим данным. Всем больным, соответствующим критериям включения/ исключения, назначался силденафил в стартовой дозе 10 мг 3 раза в сутки для оценки переносимости терапии с дальнейшим титрованием дозы через 1 нед. от начала лечения до 20 мг 3 раза в сутки. Длительность лечения составила 16 недель.
До начала лечения силденафилом, через 4 и 16 недель проводимой терапии у всех больных для оценки функционального состояния оценивался ФК в соответствии с классификацией ВОЗ, проводился Т6МХ с оценкой индекса одышки по Боргу, а также комплексная ЭхоКГ на ультразвуковом аппарате системы GE Vivid 9 (США). Стандартный протокол ЭхоКГ-исследования включал следующие методики: двухмерная ЭхоКГ, режим М-моde, допплерэхокардиография (режим им-пульсно- и постоянно-волнового допплера), режим цветного доплеровского картирования кровотока. Проводились измерения размеров камер сердца, внутрисердечных структур, аорты и легочной артерии, исключалось наличие врожденных и приобретенных аномалий развития структур сердца. Оценивались следующие показатели: систолическое, среднее, диастолическое давление в ЛА, диаметр НПВ, диаметр левого предсердия (ЛП), аорты; конечно-диастолический (КДР ЛЖ) и конечно-систолический размеры ЛЖ (КСР ЛЖ), индекс эксцентричности (ИЭ), конечно-диастолический и конечносистолический объемы (КДО, КСО) ЛЖ, выносящий тракт ЛЖ, переднезадний размер ПЖ (ПЗР ПЖ), проксимальный и дистальный ВТПЖ, ТПСПЖ, диаметр устья, ствола ЛА и ее ветвей; измеряли размеры и объемы обоих предсердий и желудочков, ФВ ЛЖ по Симпсону, FAC; TAPSE, пик Е, пик А, их соотношение Е/А.
Осуществлялась неинвазивная оценка легочного сосудистого сопротивления (ЛСС), давления заклинивания в легочной артерии (ДЗЛА), сердечного выброса (СВ). ЛСС оценивалось по формуле: ЛСС= 80 (ДсрЛА-ДЗЛА)/ СВ, где ДсрЛА – среднее давление в ЛА; ДЗЛА – давление заклинивания ЛА, СВ – сердечный выброс. Для расчета ДЗЛА использовалась формула Nagueh: Д3ЛA= 1,9 +1,24 х (Е/Em ) + 1,9, где E – максимальная скорость раннего диастолического наполнения ЛЖ, измеренная с помощью импульсно-волновой допплерографии, Em – максимальная скорость раннего диастолического смещения латерального сегмента кольца митрального клапана (МК).
Выполнялась количественная обработка ТМД с оценкой систолической и диастолической функции ПЖ в режиме off-line. Проводилась оценка глобальной и региональной сократимости продольных волокон миокарда (Tissue Velocity Imaging (TVI)), показатель деформации (Strain rate). Оценка глобальной функции производилась в области фиброзного кольца трикуспидального (ТК) и митрального (МК) на латеральной и септальной стенках. Оценка глобальной функции выполнена с помощью показателей стандартной ЭхоКГ: 1. индекс сократимости – FAC; 2. показатель экскурсии кольца ТК – TAPSE. Также оценивались показатель E' области кольца базального, среднего, апикального сегментов от латеральной стенки ПЖ и ЛЖ. Кроме этого, показатели транстрикуспидального потока и данным ТМД позволили рассчитать соотношение E/E', которое использовалось для оценки диастолической функции ПЖ. О дисфункции ПЖ говорили следующие показатели: соотношение Е/А (<0,8 или 2,1>), DT <120 мс, а также соотношение E/E' >6. При оценке региональной сократимости контрольный объем устанавливался по центру исследуемого сегмента, направление луча и исследуемой стенки было максимально параллельно (с погрешностью не более 20°).
Мы использовали метод определения сердечно-сосудистого (СС) сопряжения ЛЖ, предложенный Antonini-Canterin F. и Carerj S., и рассчитывали отношение жесткости аорты (Еа) к жесткости ЛЖ (Еs) [9]. Жесткость аорты определяли по формуле Еа = КСД ЛЖ/ УО ЛЖ, где КСД – конечно-систолическое давление в ЛЖ, УО – ударный объём ЛЖ, Еа – жесткость аорты. Жесткость ЛЖ (Еs) рассчитывали по формуле – КСД ЛЖ/ КСО ЛЖ, при этом КСД – конечно-систолическое давление ЛЖ = 0,9 х систолическое АД. Величина СС-сопряжения рассчитывалась по формуле как отношение КСО ЛЖ к УО ЛЖ, где КСО – конечно-систолический объем ЛЖ, УО – ударный объем ЛЖ.
КПОС выполнялась до начала терапии силденафилом и спустя 16 недель на аппарате "PhilipsAllureFD 10" с пакетным обеспечением HaemoSphere. Во время исследования оценивались давление в правом предсердии (ДПП), давление в легочной артерии (систолическое (СДЛА), диастолическое (ДДЛА), среднее (Дср.ЛА), ДЗЛА, СВ (по методу Фика), ЛСС, насыщение кислородом артериальной и венозной крови.
Стандартная терапия в группе ИЛГ включала: варфарин 2,5-7,5 мг – у 28 (96,5%); эноксапарин – у 2 (3,4%); петлевые диуретики (фуросемид 20-100 мг; торасемид 2,5-10 мг) – у 12 (41,7%), верошпирон 50-200 мг- у 14 (48,3%), дигоксин 0,25мг – у 1 (2,9%) больного (рис. 1). Сопутствующую терапию в группе ХТЭЛГ составили следующие препараты: вар-фарин 2,5-7,5 мг – у 24 (88,6%); эноксапарин – у 6 (22,4%); петлевые диуретики (фуросемид 20-100 мг; торасемид 2,5-10 мг) – у 15 (51,7%), верошпирон 50-200 мг – у 14 (50 %), дигоксин 0,25 мг – у 2 (7,14%), бисопролол 1,25 мг – у 3 (10,7%) больных (рис. 1). Для пациентов с ИЛГ целевыми уровнями МНО при назначении варфарина были 1,5-2,5, для пациентов с ХТЭЛГ – 2,5-3,5. Перечисленные лекарственные препараты в стабильных дозах больные получали в течение как минимум 3 мес., предшествующих включению в исследование.
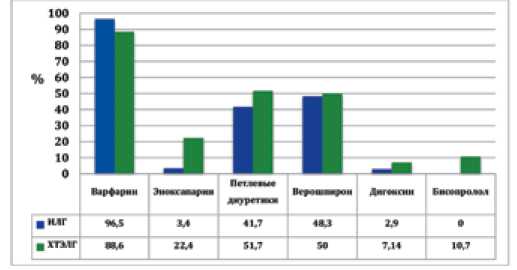
Рисунок 1. Стандартная лекарственная терапия у больных с ИЛГ и ХТЭЛГ
Статистическая обработка данных проводилась с использованием компьютерной программы Statistica v.10 для Windows (StatSoftInc., USA). При нормальном распределении значения определялись среднее (М) и стандартное отклонение (о ). Для сравнения количественных показателей разных групп пациентов для нормально распределенных переменных использовался t-критерий Стьюдента. Непараметрические статистические методы (критерий Манна-Уитни и критерий Вилкоксона) применялись при отличии закона распределения исследуемых величин от нормального. Различия считались статистически значимыми при уровне значимости p<0,05.
РЕЗУЛЬТАТЫ
На первом этапе исследования проводилась сравнительная оценка исходных клинических показателей у 29 пациентов ИЛГ и 28 пациентов ХТЭЛГ. Обе группы были сопоставимы по исходным функциональным характеристикам: ФК, дистанции в Т6МХ и индексу Борга. Характеристика функционального статуса больных представлена в таблице 2.
Таблица 2. Исходная характеристика функционального статуса у больных с ЛГ
|
Показатели |
Группа ИЛГ, (n=29) |
Группа ХТЭЛГ, (n=28) |
p |
|
ФК (ВОЗ) |
2,85±0,6 |
3±0,4 |
>0,05 |
|
Т6МХ, метры |
329±106 |
319,4±100 |
>0,05 |
|
Одышка по Боргу, баллы |
3,1±1,2 |
3,5±0,9 |
>0,05 |
В обеих группах не было больных с I ФК. Процентное распределение больных по ФК (ВОЗ) в группах ИЛГ и ХТЭЛГ не имело различий, как показано на рисунке 2.
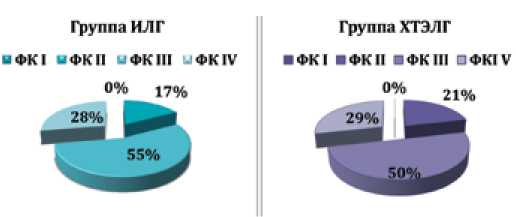
Рисунок 2. Исходный ФК (ВОЗ) у пациентов с ИЛГ и ХТЭЛГ
Основные жалобы и клинические проявления, характерные для пациентов с ЛГ, представлены в таблице 3. При сравнении данных показателей между группами ИЛГ и ХТЭЛГ достоверных различий получено не было.
Таблица 3. Жалобы и клинические проявления у больных ИЛГ и ХТЭЛГ
|
Жалобы |
Группа ИЛГ |
Группа ХТЭЛГ |
|
Одышка |
100 |
100 |
|
Головокружение,% |
90 |
92 |
|
Боли в сердце,% |
65 |
67 |
|
Сердцебиение,% |
79 |
75 |
|
Синкопе,% |
24 |
28 |
|
Отеки,% |
58 |
60 |
|
Гепатомегалия,% |
34 |
42 |
|
Гидроперикард,% |
11 |
21 |
При сравнительном анализе структурно-функциональных показателей сердца по данным эхокардиографии исходно у всех пациентов с ИЛГ и ХТЭЛГ отмечалась характерная картина: гипертрофия и дилатация ПЖ с признаками его перегрузки объемом и давлением, уменьшение объема ЛЖ, дилатация ствола ЛА и ее ветвей. Параметры ремоделирования сердца по данным ЭхоКГ представлены в таблице 4.
В обеих группах отмечалось увеличение ПЖ и ПП; уменьшение ЛЖ, увеличение ИЭ. Как в группе ИЛГ, так и ХТЭЛГ отмечалось уменьшение объемов ЛЖ (КДО, КСО и УО) при сохранной систолической функции ЛЖ (ФВ ЛЖ >60). Выраженность гипертрофии миокарда ПЖ, степень дилатации ствола ЛА и степень относительной недостаточности ТК также были сопоставимы в обеих группах больных.
Таким образом, у больных ИЛГ и ХТЭЛГ выявлено выраженное ремоделирование сердца по сравнению с контрольной группой (КГ), однако при сравнении этих групп между собой достоверных различий получено не было.
Таблица 4. Параметры эхокардиографии больных с ИЛГ и ХТЭЛГ
|
Показатели |
Группа ИЛГ, n=29 |
Группа ХТЭЛГ, n=28 |
Контрольная группа (КГ), n= 22 |
|
SПП, см |
23,4±7,07* |
23,9±6,95* |
12±1,56 |
|
ПЗР ПЖ, см |
3,8±0,64* |
3,7±0,62* |
2,4±0,22 |
|
БР ПЖ, см |
4,8±0,66* |
4,75±0,55* |
3,4±0,21 |
|
ВТПЖ прокс., см |
4,07±0,65* |
3,94±0,47* |
3,2±0,5 |
|
SПЖ диаст., см |
29,3±6,7* |
30,2±5,9* |
16±2,44 |
|
ТПСПЖ, см |
0,71±0,13* |
0,69±0,11* |
0,1±0,07 |
|
КДРЛЖ, см |
3,86±0,64* |
3,98±0,6* |
4,6±0,36 |
|
ИЭ ЛЖ |
1,46±0,30* |
1,42±0,25* |
1,01±0,03 |
|
КСО ЛЖ, мл |
21,5±5,47* |
24,5±8,8* |
41±5,1 |
|
КДО ЛЖ, мл |
61,4±17,7* |
64,2±19,8* |
98±22,7 |
|
ЛА ствол, см |
3,26±0,63* |
3,05±0,35* |
2,0±0,5 |
Примечание:* p<0.05 по сравнению с КГ, ^ по сравнению групп ИЛГ с ХТЭЛГ
У больных ИЛГ и ХТЭЛГ отмечалось существенное повышение систолического (СДЛА) и среднего давления (ДсрЛА) в ЛА, определенного по данным ЭхоКГ по сравнению с КГ (табл. 5). В обеих группах наблюдалось сопоставимое увеличение ЛСС до 1208±638 и 1153±424 дин*сек/см5, соответственно, в группах ИЛГ и ХТЭЛГ. ДЗЛА в пределах нормальных значений. УО ПЖ в группе ХТЭЛГ был достоверно выше, чем в группе ИЛГ (p<0.05).
Таблица 5. Внутрисердечная гемодинамика по данным допплерэхокардиографии у больных с ИЛГ и ХТЭЛГ
|
Показатели |
Группа ИЛГ, n=29 |
Группа ХТЭЛГ, n=28 |
КГ, n=22 |
|
ТК недостаточность, степень |
2,27±0,73* |
2,26±0,63* |
1±0,7 |
|
СДЛА, мм рт. ст. |
89,3±19,5* |
91,2±18,8* |
22,5±3,46 |
|
ДсрЛА, мм рт. ст. |
55,1±14,09 |
55,4±9,53 |
<18 |
|
ДЗЛА, мм рт. ст. |
8,1±1,5 |
7,64±1,74 |
<10 |
|
ЛСС, дин *сек/см5 |
1208±638 |
1153±424 |
<240 |
|
УО ЛЖ, мл |
45,4±10,7* |
46,9±12,2* |
65,1±4,3 |
|
УО ПЖ, мл |
49,9±16,6*^ |
60,8±11,8*^ |
64,1±4,9 |
Примечание:* p<0.05 по сравнению с КГ, ^ по сравнению групп ИЛГ с ХТЭЛГ
При оценке исходных показателей центральной гемодинамики у больных ИЛГ и ХТЭЛГ отмечалось выраженное повышение давления в ЛА и по данным КПОС. У всех пациентов, включенных в исследование, имелись критерии прекапиллярной ЛГ (ДсрЛА ≥ 25 мм рт. ст., ДЗЛА <15 мм рт. ст.). Больные обеих групп были сопоставимы по уровню СДЛА и ДсрЛА, СВ и СИ, ЛСС (табл. 6). Исключение составило ДДЛА, которое в группе ИЛГ оказалось выше (38,3±13,7 мм рт. ст.), чем в группе ХТЭЛГ (31,5±8,9 мм рт. ст., p<0,05).
Таблица 6. Исходная характеристика гемодинамики пациентов ИЛГ, ХТЭЛГ по данным КПОС
|
Показатель |
Группа ИЛГ, n=29 |
Группа ХТЭЛГ, n=28 |
|
СДЛА, мм рт. ст. |
82,5±21,7 |
84,9±18,6 |
|
ДДЛА, мм рт. ст. |
38,3±13,7* |
31,5±8,9 |
|
СрДЛА, мм рт. ст. |
49,4±16,4 |
51,7±10,2 |
|
СВ, КПОС, л/мин |
3,2±0,77 |
3,5±0,82 |
|
СИ, л/мин/м2 |
1,86±0,56 |
1,96±0,53 |
|
УО, мл. |
45,03±14,6 |
50,1±14,2 |
|
ДПП, мм рт. ст. |
9,65±5,1 |
8,85±3,79 |
|
ЛСС, дин*сек/см5 |
1315±680 |
1181±4,73 |
|
ДЗЛА, мм рт. ст. |
6,34±2,8* |
4,96±2,04 |
|
SvO2, % |
56,1±9,64 |
55,6±8,7 |
Примечание:* p<0.05 по сравнению с группой ИЛГ
На фоне терапии силденафилом в обеих группах отмечалось улучшение функционального статуса, гемодинамических показателей и параметров ремоделирования сердца. Спустя 16 недель терапии силденафилом в группе ИЛГ отмечался прирост дистанции в Т6МХ на 114 м, а в группе ХТЭЛГ на 108 м. При сравнении средних дельт от 16 недели к исходным значениям, достоверной разницы динамики дистанции при Т6МХ в обеих группах не получено (табл. 7). Положительная динамика Т6МХ сопровождалась уменьшением степени одышки по Боргу в обеих группах.
Спустя 16 недель терапии силденафилом пациенты с ИЛГ распределились по ФК следующим образом: I ФК – 12%, II ФК – 62,5%, III ФК – 25%, IV ФК – 0% (рис. 3). Все пациенты с IV ФК через 16 недель терапии соответствовали III ФК, значительная часть пациентов достигла ФК II.
Процентное распределение больных ХТЭЛГ по ФК до лечения было следующим: I ФК – 0 %, II ФК – 21,4%, III ФК – 50%, IV ФК – 28,5%. К 16 неделе лечения наблюдалась положительная динамика в виде достоверного улучшения ФК: I ФК – 28,5%, II ФК – 42,8%, III ФК – 28,5%, IV ФК – 0% (рис. 3).
Динамика выраженности процессов ремоделирования сердца и параметров гемодинамики на основании традиционной ЭхоКГ у больных, получавших терапию силденафилом, представлена в таблице 7. На фоне лечения силденафилом у всех пациентов с ИЛГ отмечалось улучшение исследуемых показателей по данным ЭхоКГ. Так, спустя уже 4 недели проводимой терапии отмечалось снижение СДЛА с 89,3±19,3 мм рт. ст. до 84,9±16,7 мм рт. ст. (p>0,05). К 16 неделе проводимой терапии отмечалось достоверное снижение СДЛА на 12,7 мм рт. ст. (абсолютное значение 76,6±12,9, p<0,01) и ДсрЛА на 8,3 мм рт. ст. (с 55,1±14,0 мм рт. ст. до 46,8±12,7 мм рт. ст., p<0,05). Несмотря на значимое снижение давления в ЛА, степень трикуспидальной регургитации практически не уменьшилась, достигнуто достоверное увеличение УО и КДР ЛЖ.
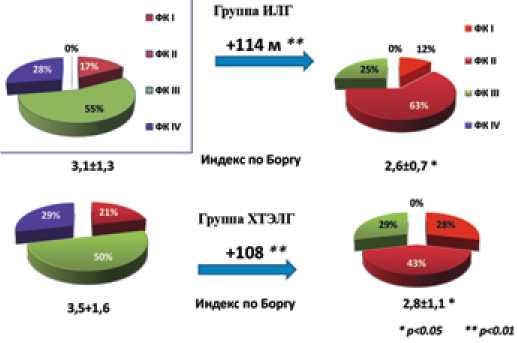
Рисунок 3. Динамика ФК у больных с ИЛГ и ХТЭЛГ на фоне 16-недельной терапии силденафилом
Через 16 недель терапии силденафилом у больных ИЛГ было выявлено достоверное увеличение УО ЛЖ с 45,4±10,7мл до 52,9±9,1 мл ( p<0,01), КДР с 3,8±0,64 см. до 4,2±0,4( p<0,05), КСО с 21,5±5,4 мл до 26±5,7 (p<0,01), которые все же оставались ниже нормальных значений. ФВ ЛЖ, которая исходно была в пределах нормальных значений, что характерно для пациентов ИЛГ, спустя 16 недель терапии увеличилась с 63,5±4,9 % до 66,2±5,5%. 16 недельная терпия силденафилом привела к изменению параметров: ПЗР ПЖ с 3,8±0,6 см уменьшился до 3,6±0,6 см (p<0,05) и апикальный размер ПЖ с 4,8±0,6 см уменьшился до 4,6±0,6 см (p<0,05). Выявлено улучшение сократительной функции ПЖ – TAPSE увеличился с 1,3±0,2 см до 1,6±0,2 см (p<0,05), FAC – c 25,8±6,0% до 34,2±5,6 (p<0,01). Тем не менее, показатели TAPSE и FAC оставались ниже нормальных значений. Позитивное влияние терапии силденафилом выразилось также в изменении показателя СС-сопряжения и жесткости ЛЖ. Отмечалось некоторое увеличение СС-сопряжения с 0,4±0,1 до 0,5±0,09 (+0,1,
Таблица 7. Сравнение групп ИЛГ и ХТЭЛГ на терапии
|
Показатели |
ИЛГ исходно |
ИЛГ 16 недель |
ХТЭЛГ исходно |
ХТЭЛГ 16 недель |
|
Т6МХ, м |
329,7±106,9 |
443,0±77,4 |
319,5±105,7 |
427,3±54,8 |
|
Данные ЭхоКГ: |
||||
|
БР ПЖ, см |
4,8±0,6 |
4,5±0,6* |
4,7±0,5 |
4,4±0,5 * |
|
ПЗР ПЖ, см |
3,8±0,6 |
3,6±0,6* |
3,7±0,6 |
3,4±0,5 |
|
SПП, см |
23,4±7,0 |
22±6,3 |
23,9±6,9 |
21,6±6,2 |
|
ТПСПЖ, см |
0,7±0,1 |
0,6±0,1 |
0,6±0,1 |
0,6±0,09 |
|
TAPSE ПЖ,см |
1,3±0,2 |
1,6±0,28 * |
1,3±0,1 |
1,5±0,2 ** |
|
FAC ПЖ,% |
25,8±6,0 |
34,2±5,6 ** |
28,4±8 |
37,4±6,9 ** |
|
ИЭ ЛЖ |
1,4±0,30 |
1,3±0,2 |
1,5±0,2 |
1,2±0,1 ** |
|
СС-сопряжение |
0,4±0,1 |
0,5±0,09 |
0,4±0,1 |
0,5±0,1 |
|
Данные КПОС: |
||||
|
СДЛА, мм рт. ст. |
82,5±21,7 |
70,8±15,4 * |
84,9±18,6 |
70,7±20,6 ** |
|
ДсрЛА, мм рт. ст. |
49,4±16,5 |
39,1±13,7 * |
51,7±10,2 |
40,6±12,5 ** |
|
ДДЛА,мм рт. ст. |
38,3±13,7^ |
30,5±12,1 *^^ |
31,5±8,9^ |
23,3±9,4 **^^ |
|
ЛСС |
1368,1±680 |
1051±465,5* |
1181±473 |
779,9±385,7 ** |
|
СВ, л/мин |
3,2±0,77 |
3,6±1* |
3,5±0,8 |
4,0±0,8 * |
|
SvO2,% |
56,1±9,6 |
58,7±10,4 |
55,6±8,7 |
62,2±8,2 * |
Примечание:* p<0.05 по сравнению с исходом,
** p<0.01по сравнению с исходом, ^ по сравнению групп ИЛГ с ХТЭЛГ исходно, ^^ по сравнению групп ИЛГ с ХТЭЛГ на лечении.
p<0,05) и значимое снижение жесткости ЛЖ с 4,7±0,9 до 3,9±0,6 (-0,8, p<0,01), что, по всей видимости, отражает улучшение функции ЛЖ: увеличение УО, сократительной функции. Однако эти показатели также остались ниже нормальных значений. Показатель Ea изменился недостоверно.
В результате 16-недельной терапии силденафилом в группе ХТЭЛГ также отмечалась положительная показателей ЭхоКГ (табл. 7). Отмечалось существенное снижение СДЛА с 91,2±18,8 мм рт. ст. до 75,6±20,3 мм рт. ст. (-15,63 мм рт. ст., p<0,01) и ДсрЛА с 55,4±9,5 мм рт. ст. до 44,3±9,9 мм рт. ст. (-11,33 мм рт. ст., p<0,01). Уменьшение степени трикуспидальной регургитации было несущественным (с 2,2±2,2 до 1,9±0,7, p>0,05). На фоне терапии силденафилом в группе ХТЭЛГ отмечалось улучшение не только УО ЛЖ (с 49,9±12,2 мл до 56,2±11,4 мл, p<0,05), как в группе ИЛГ, но и УО ПЖ (с 60,8±11,8 мл до 69,4±14,6 мл, p<0,05).
Исходно обе группы имели одинаковые ПЗР и БР ПЖ, однако в группе ХТЭЛГ, спустя 16 недель терапии, достоверно уменьшился только БР ПЖ (-0,3 см, p<0,05). У больных в результате терапии силденафилом выявлено улучшение сократительной функции ПЖ в виде увеличения TAPSE (c1,3±0,1 см до 1,5±0,2 см, p<0,05) и увеличения FAC (c 28,4±8% до 37,4±6,9%, p<0,05). Получена положительная динамика показателей, характеризующих изменение левых отделов сердца, таких как КДР и ИЭ. Отмечено увеличение КДР с 3,9±0,6 см до 4,3±0,5 см (p<0,05), и уменьшение ИЭ с 1,5±0,2 см до 1,2±0,2 см (p<0,05). Через 16 недель терапии в группе ХТЭЛГ значение жесткости ЛЖ достоверно снизилось с 4,5±1,2 до 3,6±0,7.
Анализ результатов КПОС при 16-недельной терапии у больных ИЛГ показал значимое снижение СДЛА с 82,5±21,7 мм рт. ст. до 70,8±15,4 мм рт. ст. (-11,7 мм рт. ст., p<0.05), ДсрЛА с 49,4±16,5 мм рт. ст. до 39,1±13,7 мм рт. ст.(-10 мм рт. ст., p<0.05), ДДЛА с 38,3±13,7 мм рт. ст. до 30,5±12,1 мм рт. ст. (-8,3 мм рт. ст., p<0.05), ЛСС с 1368,1±680 дин *сек/см5
Таблица 8. Сравнение дельт показателей теста 6-минутной ходьбы, ЭхоКГ и КПОС в результате терапии силденафилом в группах ИЛГ и ХТЭЛГ
|
∆ от 16 недели к исходным значениям |
Группа ИЛГ |
Группа ХТЭЛГ |
p |
|
∆ Т6МХ |
96,3 |
115,1 |
>0,05 |
|
Данные ЭхоКГ: |
|||
|
∆ ПЗР ПЖ |
-0,2 |
-0,4 |
>0,05 |
|
∆ SПП |
-1,92 |
-3,6 |
>0,05 |
|
∆ БР ПЖ |
-0,3 |
-0,5 |
>0,05 |
|
∆ ТПС ПЖ |
-0,01 |
-0,02 |
>0,05 |
|
∆ FAC ПЖ |
8,6 |
7,1 |
>0,05 |
|
∆ TAPSE ПЖ |
0,18 |
0,11 |
>0,05 |
|
∆ ИЭ ЛЖ |
-0,13 |
-0,23 |
<0,05 |
|
∆ СС-сопряжение |
0,05 |
0,05 |
>0,05 |
|
Данные КПОС: |
|||
|
∆ СДЛА |
-11,5 |
-18 |
<0,05 |
|
∆ ДсрЛА КПОС |
-9,5 |
-12,7 |
<0,05 |
|
∆ дДЛА КПОС |
-7,4 |
-10,4 |
>0,05 |
|
∆ ЛСС КПОС |
-266 |
-405 |
<0,05 |
|
СВ КПОС |
0,4 |
0,3 |
>0,05 |
Примечание: p>0,05 - ∆ на лечении в группах
ИЛГ и ХТЭЛГ достоверно не различны, p<0,05 - ∆ на лечении в группах ИЛГ и ХТЭЛГ достоверно различны до 1051±465,5 дин *сек/см5 (-317, p<0.05), увеличение СВ с 3,2±0,77 л/мин до 3,6±1 л/мин (+0,4, p<0.05), УО с 45,0±14,7 до 52,1±14* (+7,1, p<0.05) (табл. 7,8). По данным КПОС значение СИ после лечения силденафилом составило 2,1±0,9 л/ мин/м2, а ДПП достигло нормальных значений, снизившись с 9,6±5,1 мм рт. ст. до 5,7±1,9 (p<0,01).
Выраженное снижение ДЛА в группе ХТЭЛГ спустя 16 недель проводимой терапии, было подтверждено и данными КПОС (табл. 7). Так, СДЛА в среднем снизилось с 84,9±18,6 мм рт. ст. до 70,7±20,6 мм рт. ст. (p<0,01), ДДЛА с 31,5±8,9 мм рт. ст. до 23,3±9,4 мм рт. ст. (p<0,01), ДсрЛА с 51,7±10,2 мм рт. ст. до 40,6±12,5 мм рт. ст. (p<0,01). Отмечено также достоверное снижение ЛСС с 1181±473 дин *сек/см5 до 779,9±385,7 дин *сек/см5 (p<0,01), и ДПП с 8,8±3,7 мл до 5,5±2,4 мл (p<0,05). 16 недельная терапия силденафилом привела к увеличению УО с 50,1±14,2 мл до 57,1±12,4 мл (p<0,05) и СВ с 3,5±0,8 л/ мин до 4,0±0,8 л/мин (p<0,05).
В группах ИЛГ и ХТЭЛГ достоверно снизилось СДЛА по данным КПОС. Так, в группе ИЛГ снижение составило -11,7 мм рт. ст., в группе ХТЭЛГ -14,2 мм рт. ст. (табл. 7). При сравнении средних дельт СДЛА от 16 недели к исходу, также обнаружены достоверные различия. Размеры камер сердца на терапии уменьшились в равной степени в обеих группах. Исключение составил ИЭ ЛЖ, который достоверно улучшился только в группе ХТЭЛГ, что было подтверждено при статистическом анализе дельт. ДсрЛА в обеих группах также снизилось достоверно, на -10,3 мм рт. ст. и -11,1 мм рт. ст. в группе ИЛГ и ХТЭЛГ, соответственно. ЛСС в группе ХТЭЛГ снизилось на -402 дин *сек/см5, против -317 дин*сек/см5 в группе ИЛГ, дельты достоверно различались. Достоверное улучшение сатурации венозной крови кислородом на терапии отмечалось только в группе ХТЭЛГ.
ОБСУЖДЕНИЕ
В данном исследовании у больных ИЛГ и ХТЭЛГ в сравнительном аспекте были проанализированы результаты 16-недельной патогенетической терапии ИФДЭ5 силденафилом. На первом этапе был проведен анализ исходных данных клинико-функционального и гемодинамического статуса больных ИЛГ и ХТЭЛГ, а также структурно-функционального состояния и взаимосвязи правых и левых отделов сердца, сердечно-сосудистого сопряжения. В обеих группах выявлялись характерные для пациентов с ЛГ жалобы и клинические проявления. При сравнении частоты клинических проявлений и данных осмотра между группами ИЛГ и ХТЭЛГ, достоверных различий получено не было, что соответствует данным литературы [1,4]. Одышка отмечалась у 100% пациентов в группах ИЛГ и ХТЭЛГ, головокружение – у 90% и 92% больных, соответственно, боли в сердце – у 65% и 67%, сердцебиение – у 79% и 75%, синкопальные состояния – у 24% и 28% больных. Высокая частота и широкий спектр жалоб, выявленных на момент включения больных в исследование, соответствует длительности ИЛГ и ХТЭЛГ – 2,1±0,8 и 1,8±1 года. На развернутую стадию заболевания указывает частое выявление в группах ИЛГ и ХТЭЛГ при осмотре и ЭхоКГ признаков ПЖ сердечной недостаточности – периферических отеков (58% и 60%), гепатомегалии (34% и 43%), гидроперикарда (11% и 21%). При валидации опросника для скрининга ЛАГ и ХТЭЛГ проводился анализ симптомов у 81 больного ИЛГ и 36 больных ХТЭЛГ. При ИЛГ и ХТЭЛГ наиболее частой комбинацией клинических симптомов явились одышка (99% и 97%, соответственно), утомляемость (99% и 83%), сердцебиение (61% и 58%) [10]. Синкопе достоверно чаще отмечались при ИЛГ (29%) в сравнении с группой ХТЭЛГ (8%). Отеки на момент верификации диагноза чаще определялись при ХТЭЛГ (56% и 44%), чем в группе ИЛГ. Эти различия можно объяснить тем, что в нашу работу включались больные с большей длительностью заболевания, на что указывает высокая частота проявлений ПЖ сердечной недостаточности.
У пациентов с ИЛГ и ХТЭЛГ при проведении трансторакальной ЭхоКГ исходно мы отметили характерные признаки ЛГ такие, как гипертрофия и дилатация правых отделов сердца, компрессия ЛЖ дилатированным ПЖ. Пациенты обеих групп исследования были сопоставимы по размерам камер и объемам сердца – ПЖ и ПП. У больных ИЛГ и ХТЭЛГ было определено нарушение сократительной функции ПЖ при оценке показателя FAC по сравнению с КГ. Андреева Ю.А. и соавт. при оценке структурного состояния и систолической функции ПЖ у больных с ЛГ различной этиологии также описывали наиболее выраженное нарушение процессов ремоделирования в группах ИЛГ и ХТЭЛГ. У этих пациентов в сравнении с группами ЛГ вследствие ХОБЛ и ЛАГ на фоне системной склеродермии определялось наибольшее увеличение правых отделов сердца при уменьшении левых и снижении систолической функции ПЖ в соответствие с наибольшим уровнем СДЛА [11].
Средние значения TAPSE, отражающего глобальную сократимость ПЖ, были ниже, чем в контроле, без достоверных различий между группами ИЛГ и ХТЭЛГ. При изучении региональной систолической функции миокарда ПЖ у больных с ЛГ определялось уменьшение систолических скоростей от базальных сегментов к верхушечным, что было показано в ряде исследований [11-13]. При этом минимальные показатели во всех сегментах боковой стенки ПЖ обнаруживались у больных с ИЛГ.
По нашим данным при импульсно-волновом допплеровском исследовании транстрикуспидального потока у больных с ИЛГ и ХТЭЛГ была выявлена «псевдонормальная» диастолическая функция ПЖ, что ранее было показано у больных ЛАГ различной этиологии, ХТЭЛГ и ЛГ вследствие ХОБЛ [11].
Известно, что в дебюте заболевания отмечаются нарушения диастолической функции ПЖ по типу замедленной релаксации. Они усугубляются по мере прогрессирования дилатации ПЖ, развития изменений в его миокарде дистрофического и фиброзного характера, что приводит к нарушению наполнения ПЖ. В дальнейшем, страдает диастолическая функция ЛЖ вследствие сдавления его гипертрофированным и дилатированным ПЖ, при наличии «парадоксального» движения МЖП, которое выявлялось у большинства наших пациентов с ИЛГ и ХТЭЛГ без значимых различий в зависимости от этиологии ЛГ. Хотя при ИЛГ в отличие от ассоциированных форм ЛАГ и ХТЭЛГ описывается наиболее выраженное нарушение геометрии ЛЖ вследствие парадоксального движения межжелудочковой перегородки [14].
При ЛГ различной этиологии описаны особенности взаимодействия правого и левого желудочка. По результатам ЭхоКГ наиболее выраженное ремоделирование правых отделов сердца среди больных с ЛГ выявлено при ИЛГ [15].
На нарушение процессов ремоделирования сердца у наших больных с различными формами ЛГ указывало уменьшение размеров КДР ЛЖ и увеличение ИЭ в обеих группах по сравнению с КГ. Как в группе ИЛГ, так и в группе ХТЭЛГ отмечалось снижение КДО, КСО и УО при сохранной систолической функции ЛЖ. При оценке ФВ ЛЖ у пациентов с ИЛГ существенно не отличалась от таковой у больных с ХТЭЛГ и КГ. В работе Raymond R.J. и соавт. у больных с ЛАГ также выявлялась сохранная систолическая функция ЛЖ [16]. По данным допплеровского исследования трансмитрального потока снижение показателя Е/А<1 было обнаружено в обеих группах ЛГ без достоверных различий между ними. В литературе описываются выраженные нарушения диастолической функции ЛЖ при исследования трансмитрального потока у больных с ИЛГ [17].
С учетом вовлеченности ЛЖ в патологический процесс при ЛГ различной этиологии мы изучали сердечно-сосудистое сопряжение – феномен, который отражает взаимодействие ЛЖ с артериальной системой. В физиологических условиях он обеспечивает должный прирост СВ за счет регуляции системного АД и соответствующего увеличения ЧСС и, в свою очередь, зависит от функции сердца и сосудов, в которые осуществляется выброс крови. Если проблеме сердечно-сосудистого сопряжения при артериальной гипертонии посвящены единичные работы, подтверждающие клиническое значение этой взаимосвязи, то подобные взаимосвязи не изучались при ЛГ [9]. В обеих группах ЛГ независимо от этиологии исходно были получены достоверно более низкие и сопоставимые показатели сердечно-сосудистого сопряжения по сравнению с КГ. Показатели жесткости аорты Еа находились в пределах нормальных значений в обеих группах, но были достоверно выше, чем в КГ. Повышенные по сравнению с КГ значения Еs, отражающего жесткость ЛЖ, установлены как в группе ИЛГ, так и в группе ХТЭЛГ [18].
Нарушение СС-сопряжения, увеличение жесткости ЛЖ у пациентов с ЛГ отражает ухудшение систолической функции ПЖ, а также динамику дилатации камер сердца. Оценка сердечно-сосудистого сопряжения с помощью современных методов ЭхоКГ у больных ЛГ необходима для установления взаимосвязи правых и левых отделов сердца.
По данным КПОС гемодинамический профиль в целом в группах ИЛГ и ХТЭЛГ оказался сопоставимым по уровням ДЛА, СВ и СИ, ЛСС. При манометрии определялись значительно повышенные уровни СДЛА в обеих группах, несколько выше у больных с ХТЭЛГ. ДДЛА, напротив, оказалось достоверно выше в группе ИЛГ. Полученные данные в группе ИЛГ соответствовали результатам первого регистра больных с первичной ЛГ NIH (CША) по оценке гемодинамических параметров на момент установления диагноза, а также регистров, проведенных в последующие годы [4].
В нашем исследовании больные ИЛГ и неоперабельной ХТЭЛГ получали 16-недельную патогенетическую терапию ИФДЭ5 силденафилом. Роль эндогенного оксида азота (NO) в патогенезе ЛАГ и ХТЭЛГ связана с комплексным воздействием на сосудистый тонус, активность тромбоцитов и лейкоцитов, пролиферацию гладкомышечных клеток и фибробластов, а также иммунный и воспалительный ответ [1,4,19]. Механизм действия ИФДЭ5 осуществляется за счет ингибирования цГМФ-специфической фосфодиэстеразы типа 5. Уменьшение деградации цГМФ приводит к вазодилатирующему эффекту за счет расслабления гладкомышечных клеток легочных сосудов и активации калиевых каналов, а также антипролиферативному эффекту вследствие активации цГМФ-зависимых киназ [1,2].
В рандомизированных клинических исследованиях (РКИ) у больных ЛАГ ИФДЭ5 доказали способность улучшать функ-
I 40 I------------------------------------------ циональные возможности, показатели легочной гемодинамики, уменьшать выраженность ремоделирования легочных сосудов. У больных с ЛАГ в единственном РКИ SUPER-1 изучалось влияние 12-недельной терапии силденафилом в различных дозах на функциональный и гемодинамический статус больных [20]. При ХТЭЛГ выполнялись неконтролируемые исследования по оценке клинической эффективности силденафила [21].
Для первичной оценки переносимости терапии всем больным из 2-х групп назначалась терапия силденафилом в стартовой дозе 10 мг 3 раза в сутки. В дальнейшем через 1 неделю после начала лечения осуществлялась титрация дозы до 20 мг 3 раза в сутки. Поскольку исходно больные в группах ЛГ были сопоставимы по клиническому статусу, параметрам ЭхоКГ и гемодинамики, представлялось возможным оценить клинические результаты лечения силденафилом у больных в зависимости от этиологии ЛГ. В группе ИЛГ исходно преобладали больные с ФК III (55,1%) и IV (27,5%). Спустя 16 недель терапии силденафилом преобладающим стал ФК II (62,5%), только у 25% отмечался ФК III, ни у одного больного не сохранился ФК IV. Положительная динамика дистанции в Т6МХ сопровождалась уменьшением степени одышки к 16 неделе лечения.
Наши результаты подтверждаются данными ключевого РКИ SUPER-1, которое внесло важный вклад в доказательную базу, необходимую для официального одобрения препарата у больных с ЛАГ [20]. Оно было выполнено по дизайну двойного слепого, многоцентрового исследования с целью изучения эффективности и безопасности силденафила в дозах 20, 40 и 80 мг 3 раза в сутки в сравнении с плацебо. В исследовании SUPER-1 преобладали больные ИЛГ (63%), преимущественно ФК II-III. Следует отметить быстрое наступление эффекта: повышение толерантности к физическим нагрузкам у наших больных отмечалось уже к 4 неделе лечения, как и в РКИ SUPER-1. В последнем улучшение дистанции в Т6МХ в течение 12 недель составило, в среднем, +45 м. Более значительный прирост Д6МХ у наших пациентов видимо был обусловлен значительной долей больных с выраженным нарушением функционального статуса – 82% больных имели ФК III и IV.
В группе ХТЭЛГ в нашем исследовании также преобладали тяжелые больные с ФК III (50%) и IV (28,5%). Только 21,4% больных до лечения силденафилом имели ФК II. Спустя 4 недели проводимой терапии была замечена тенденция к улучшению ФК: 4% больных относились к ФК I, 17% - к ФК II, 65% - ФК III и 14% больных – ФК IV. К 16 неделе лечения в группе ХТЭЛГ также наблюдалась значительная положительная динамика с достижением ФК I и II у 28,5%, и 42,8% пациентов соответственно. ФК III сохранился у 28,5%, доля ФК IV составила 0%. Значительное увеличение толерантности к физической нагрузке у 28 пациентов с неоперабельной ХТЭЛГ в результате 16-недельной терапии силденафилом подтверждалось динамикой дистанции в Т6МХ: +17 м к 4-й неделе терапии и далее +107 м при снижении степени одышки по Боргу к 16 неделе терапии.
Важно отметить, что в группе ИЛГ мы отметили значительное улучшение Т6МХ уже на ранних сроках лечения силденафилом в отличие от группы ХТЭЛГ. В литературе имеются указания, что различные ЛАГ-специфические препараты у больных с неоперабельной формой ХТЭЛГ оказываются менее эффективными, чем при ЛАГ, в плане улучшения функционального статуса больных. Так, H.A. Ghofrani и соавт., обсуждая результаты 12-недельного РКИ фазы II с примене-
ТЕРАПИЯ ЛЕГОЧНОЙ ГИПЕРТЕНЗИИ СЕГОДНЯ И ЗАВТРА

еваиыо силденафила цитрат таблетки 20 мг
Ревацио® эффективен и безопасен у пациентов с легочной гипертензией:14
Повышает переносимость физических нагрузок1’2
Улучшает ФК Л Г1"3
Повышает выживаемость14
хорошо переносится1
КРАТКАЯ ИНФОРМАЦИЯ О ПРЕПАРАТЕ РЕВАЦИО®
Перед назначением ознакомьтесь с полной инструкцией по медицинскому применению препарата РЕВАЦИО®, одобренной М3 РФ. регистрационный номер ЛП 000197-270116 от 27.01.2016.
Список литературы Эффективность терапии силденафилом у больных с легочной гипертензией различной этиологии: влияние на клинико-функциональный и гемодинамический статус, структурно-функциональное состояние правых и левых отделов сердца, сердечно-сосудистое сопряжение
- Galie N, Hoeper MM, Humbert M, et al. Guidelines for the diagnosis and treatment of pulmonary hypertension: The Task Force for the Diagnosis and Treatment of Pulmonary Hypertension of the European Society of Cardiology (ESC) and the European Respiratory Society (ERS), endorsed by the International Society of Heart and Lung Transplantation (ISHLT). Eur Heart J 2016; 37(1): 67-119
- А.В. Волков, Е.В. Николаева, Н.Н. Юдкина, др. Влияние те рапии силденафилом на выживаемость пациентов с легочной артериальной гипертонией, ассоциированной с системными заболеваниями соединительной ткани (результаты проспективного наблюдения). Терапевтический архив 2015;11:62-67
- Волков А.В., Мартынюк Т.В., Юдкина Н.Н., др. Выживаемость пациентов с легочной артериальной гипертензией, ассоциированной с системной склеродермией. Терапевтический архив 2012; 5:24-28
- Чазова И.Е., Авдеев С.Н., Царева Н.А., др. Клинические рекомендации по диагностике и лечению легочной гипертензии. Терапевтический архив 2014; 9:4-23
- Волков А.В, Юдкина Н.Н., Курмуков И.А., др. Влияние силденафила на клинические проявления и гемодинамические показатели у больных легочной артериальной гипертензией, ассоциированной с системными ревматическими заболеваниями. Системные гипертензии 2014;3:61-66
- Hoeper MM, Madani MM, Nakanishi N, et al. Chronic thromboembolic pulmonary hypertension. LancetRespirMed 2014; 2:573-582
- Акчурин Р.С., Чазова И.Е., Мершин К.В., др. Случай сочетанного лечения тяжелой формы хронической тробоэмболической легочной гипертензии. Медицинский совет 2015; 8:10-13.
- Чазова И.Е., Мартынюк Т.В. от имени рабочей группы по разработке и подготовки текста Российских рекомендаций по диагностике и лечению ХТЭЛГ. Клинические рекомендации по диагностике и лечению хронической тромбоэмболической легочной гипертензии (II часть). Терапевтический архив 2016; 10: 63-74
- Antonini-Canterin F., Carerj S., Di Bello V. et al. Arterial stiffness and ventricular stiffness: a couple of diseases or a coupling disease? A review from the cardiologist's point of view. Eur J Echocardiogr 2009 10 (1): 36-43.
- Валиева З.С., Валеева Э.Г., Глухова С.И., др. Разработка скринингового опросника для улучшения ранней диагностики легочной артериальной гипертензии. Системные гипертензии. 2014;11(4):62-67.
- Андреева Ю.А. Оценка структурно-функционального состояния правых отделов сердца по данным тканевой миокардиальной допплерэхокардиографии и нейрогуморального статуса у больных с легочной гипертензией различной этиологии и определение влияния на них терапии ингибитором АПФ моэксиприлом. Автореф. дисс. канд. мед. наук-М., 2010
- Saxena N, Rajagopalan N, Edelman K, Lopez-Candales A. Tricuspid annular systolic velocity: a useful measurement in determining right ventricular systolic function regardless of pulmonary artery pressures. Echocardiography 2006;23:750-5
- Андреева Ю.А., Саидова М.А., Мартынюк Т.В., др. Ремоделирование сердца и легочной артерии в зависимости от уровня натрийуретических пептидов и активации ренин-ангиотензин -альдостероновой системы у больных с легочной гипертензией различной этиологии. Кардиоваскулярная терапия и профилактика 2008, №7, с.62-68
- Gan Ct, Lankhaar JW, Marcus JT, etal. Impaired left ventricular filling due to right-to-left ventricular interaction in patients with pulmonary arterial hypertension. Am J Physiol Heart CircPhysiol 2006;290:H1528 -33
- Андреева Ю.А., Саидова МА, Мартынюк Т.В., др. Тканевая миокардиальная допплерэхокардиография в оценке функции правого желудочка у больных с легочной гипертензией различной этиологии. Кардиоваскулярная терапия и профилактика 2010, №4, 27-34
- Raymond R.J., Hinderliter A.L., Willis P.W. et al. Echocardiographic predictors of adverse outcomes in primary pulmonary hypertension.//J Am Coll Cardiol 2002; 39:12141219.
- McGoon M.D. The assessment of pulmonary hypertension. Clin Chest Med 2001; 22:493-508.
- Gan CT, Lankhaar JW, Marcus JT, et al. Impaired left ventricular filling due to right-to-left ventricular interaction in patients with pulmonary arterial hypertension. Am J Physiol Heart CircPhysiol 2006;290:H1528 -33.
- Furchgott R.F., Vanhoutte P.M. Endothelium-derived relaxing and contracting factors. FASEB J 1989; 3:2007-2018.
- Galie N., Ghofrani H.A., Torbicki A., et al. Sildenafil citrate therapy for pulmonary arterial hypertension. N Engl J Med 2005; 353:2148-2157.
- Lang IM. Managing chronic thromboembolic pulmonary hypertension: pharmacological treatment options. EurRespirRev 2009; 18:24-28.
- H.A. Ghofrani, N. Galie, F. Grimminger, et al. Riociguat for the treatment of pulmonary arterial hypertension. N Engl J Med 2013;369:330-340.
- Reichenberger F., Voswinckel R., Enke B. et al. Long-term treatment with sildenafil in chronic thromboembolic pulmonary hypertension. Eur Respir J 2007; 30:922-927.
- Condliffe R., Kiely D.G., Gibbs J.S. etal. Improved outcomes in medically and surgically treated chronic thromboembolic pulmonary hypertension patients. AmJ Respir Crit Care Med 2008;177:1122-1127.


