Эффекты комбинированного действия гипертермии и УФ-света на клетки дрожжей: фактор времени и последовательность воздействия
Автор: Купцова П.С., Жураковская Г.П., Переклад О.В., Белкина С.В., Пронкевич М.Д.
Рубрика: Научные статьи
Статья в выпуске: 3 т.31, 2022 года.
Бесплатный доступ
В современных методах лечения онкологических заболеваний для достижения лучшего терапевтического эффекта широко используются сочетания воздействующих факторов различной природы: ионизирующее излучение, химиопрепараты, гипертермия, неионизирующее излучение и другие. Наибольший эффект достигается при одновременном применении воздействующих факторов. Увеличение интервала между воздействиями приводит к его снижению. Однако, как степень суммарного эффекта зависит от временного интервала, подробно не изучалось. В работе представлены результаты исследования такой зависимости при различной последовательности применяемых воздействий на примере комбинации УФ-света и гипертермии. Выбор воздействующих агентов обусловлен вниманием к свечению Вавилова-Черенкова, возникающего при действии ионизирующего излучения высоких энергий, используемого в онкотерапии и большая часть которого составляет непрерывный УФ-спектр. И если рассматривать свечение Вавилова-Черенкова ответственным за возникновение УФ-подобных повреждений, оказывающих своё влияние на конечный результат действия ионизирующего излучения высоких энергий, тогда становится ясной необходимость понимания поведения УФ-света при его применении в комбинации с другими воздействующими факторами. Таким образом, цель работы - изучить влияние последовательности воздействующих факторов и временного интервала между ними на величину суммарного эффекта при последовательном действии УФ-света и гипертермии на дрожжевые клетки. Полученная в работе зависимость носит разнонаправленный характер, изменяясь от синергизма к аддитивности, переходя в антагонизм. Показано, что эффект практически не зависит от последовательности применяемых агентов, но существенно зависит от интервала времени между воздействующими факторами. Подобные закономерности получены впервые. Но именно они указывают на то, что при использовании на практике сочетанного действия ионизирующего излучения или УФ-света с гипертермией следует помнить о том, что итоговый результат может существенно отличаться от ожидаемого.
Уф-свет, гипертермия, синергизм, антагонизм, аддитивность, комбинированное действие, радиобиология, дрожжевые клетки, свечение вавилова-черенкова, ионизирующее излучение, фактор времени
Короткий адрес: https://sciup.org/170195739
IDR: 170195739 | УДК: 576.3:615.832.8+615.831.4 | DOI: 10.21870/0131-3878-2022-31-3-111-120
Effects of the combined action of hyperthermia and UV light on yeast cells: time factor and sequence of exposure
In modern methods of cancer therapy, combinations of influencing factors having various nature are widely used to achieve the highest therapeutic effect: ionizing radiation, chemotherapy drugs, hyperthermia, non-ionizing radiation, etc. The greatest cells damaging effect is achieved when the treatments are applied simultaneously. An increase in the interval between the treatments leads to final effect decrease. However, how the degree of the total effect depends on the time gap has not been studied in detail. The paper presents the results of a study of this dependence with a different sequence of applied treatments. Combination of UV radiation and hyperthermia were examined. The choice of treatments is due to attention to the Vavilov-Cherenkov radiation, which arises when accompanies high-energy ionizing radiation used in oncotherapy and most of which is a continuous UV spectrum. And if we consider the Vavilov-Cherenkov radiation responsible for UV-like damages, which has its effect on the final result of the action of high-energy ionizing radiation, then it becomes clear that it is necessary to understand the behavior of UV light when it is used in combination with other damaging factors. Thus, the aim of the work is to study the effect of a sequence of applied treatments and the time gap between them on the magnitude of the final effect of the sequential action of UV light and hyperthermia on yeast cells. The dependence obtained in the work is of a multidirectional nature, changing from synergism to additivity, turning into antagonism with time gap rising. It is shown that the effect practically does not depend on the sequence of the treatments application, but significantly depends on the time gap between them. Such patterns were obtained for the first time. But it is indicates that when using in practice the combined action of ionizing radiation or UV light with hyperthermia, it should be remembered that the final effect can differ from expected.
Текст научной статьи Эффекты комбинированного действия гипертермии и УФ-света на клетки дрожжей: фактор времени и последовательность воздействия
Гипертермия, являясь модификатором клеточной радиочувствительности, широко используется в лечении онкологических заболеваний [1-3]. Она применяется не только в комбинации с ионизирующим излучением, но и с другими факторами химической и физической природы, о чём свидетельствуют многочисленные данные литературы [4-6]. Хорошо известно, что результат комбинированного воздействия может носить синергический, антагонистический или аддитивный характер. При этом величина, в частности, синергического эффекта зависит от степени нагрева, мощности дозы ионизирующего излучения или концентрации химического препарата. Максимальный синергизм наблюдается только при строго определённых соотношениях параметров воздействующих агентов. Также известно, что синергический эффект больше при одновременном применении агентов, а увеличение временного интервала ведёт к его снижению [6].
Антагонизм, или защитный эффект, представляет особый интерес в связи с тем, что такое взаимодействие некоторых факторов не всегда поддаётся объяснению [5]. Примером антагонизма может служить результат одновременного комбинированного действия УФ-света и
Купцова П.С.* – мл. науч. сотр.; Жураковская Г.П. – вед. науч. сотр., д.б.н..; Переклад О.В. – науч. сотр.; Белкина С.В. – зав. лаб., к.б.н.; Пронкевич М.Д. – ст. науч. сотр., к.б.н. МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
гипертермии. Более того, при одновременном действии УФ-света и гипертермии на эукариотические клетки, может наблюдаться и синергизм, и антагонизм в зависимости от соотношения параметров, воздействующих на клетки факторов [7].
Исследование результата комбинированного действия УФ-света с гипертермией интересно ещё и потому, что при действии ионизирующего изучения на биологические объекты возникают УФ-подобные повреждения, которые инициируются свечением Вавилова-Черенкова, большая часть которого находится в непрерывном коротковолновом УФ-спектре [8-10]. Поэтому знания всех особенностей, наблюдаемых при действии УФ-света в присутствии модификатора, могут быть полезны с точки зрения понимания влияния УФ-составляющей свечения Вавилова-Черенкова на конечный эффект действия ионизирующего излучения высоких энергий.
Эффект Вавилова-Черенкова в настоящее время в медицине используют в новых методах мониторинга результатов применения лучевой терапии in vivo - люминесцентной черенковской визуализации [11-18]. Также этот эффект используется для наблюдения за изменениями, происходящими у пациентов, получающих радиофармпрепараты [19, 20].
Таким образом, целью работы было исследование влияния последовательности воздействующих факторов и временного интервала между ними на величину суммарного эффекта при последовательном действии УФ-света и гипертермии.
Материалы и методы
Объект. Эукариотические клетки - диплоидные дрожжи Saccharomyces cerevisiae дикого типа, штамм XS800 . Тест. Анализ клоногенной активности (выживаемость). Физические факторы и условия облучения . Источником УФ-света служил аппарат UVstar 15 Biometra с длиной волны 254 нм и плотностью потока 4,5 Вт/м2. Во избежание фотореактивации облучение УФ-светом и другие манипуляции с суспензией клеток проводили в темноте. Гипертермическое воздействие осуществляли в водяном термостате (ELMI, TW-2.03), в котором выбранная для эксперимента температура 55 °С находилась в пределах ±0,1 °С. Интервал времени между окончанием действия УФ-света и размещением клеток в предварительно прогретую стерильную воду при последовательном комбинированном действии УФ-света и гипертермии составлял не более 15 сек. При комбинированном последовательном действии гипертермии и затем УФ-света суспензию клеток после действия гипертермии охлаждали до комнатной температуры, после чего клетки подвергали облучению УФ-светом. По окончании воздействия клетки высевали на полную питательную среду YEPD для роста дрожжей.
Каждая серия опытов повторялась 3-5 раз. Статистическая обработка результатов выполнялась с применением критерия Стьюдента. Наблюдаемые различия считали статистически значимыми (достоверными) при уровень значимости p<0,05.
Результаты и обсуждение
Для оценки эффекта комбинированного действия УФ-света и гипертермии обеих последовательностей использовался коэффициент k , определяемый как:
k = О аЙЙ. /О комб , (1)
где Dadd., Dkom6. - изоэффективные дозы для аддитивного действия агентов (сумма простого сложения, теоретическая кривая выживаемости) и комбинированного воздействия (эксперименталь- ная кривая выживаемости) соответственно. Если Dадд../Dкомб.>1, тогда результат комбинированного применения агентов носит синергический характер, при Dadd./DkOM6 =1 - эффект аддитивен, и при Dadd../Dkom6.<1 - наблюдается антагонизм.
На рис. 1 представлен пример расчёта коэффициента к после последовательного действия гипертермии, уровень выживаемости после действия которой характеризуется точкой 2 на оси ординат, и УФ-света (кривая 1) на дрожжевые клетки с интервалом времени t между применяемыми агентами. В данном случае теоретическая кривая (4) аддитивного сложения эффектов лежит выше экспериментальной кривой выживания (3) после комбинированного воздействия, что свидетельствует о синергическом взаимодействии агентов и коэффициент к = 1,7.
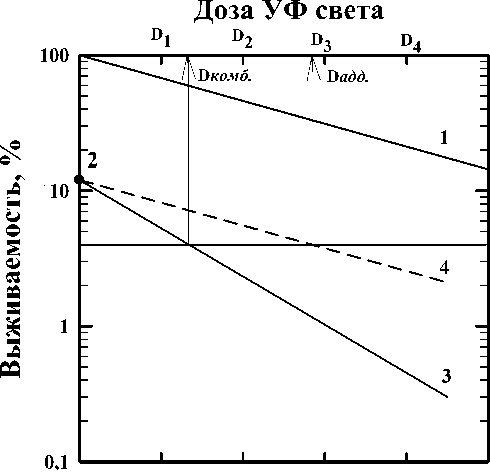
Рис. 1. Пример зависимости выживаемости клеток от дозы облучения УФ-светом для расчёта коэффициента к .
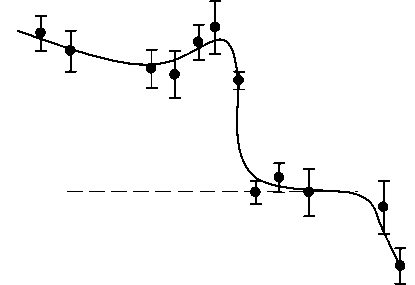
Результат исследования зависимости проявления эффекта ( к ) комбинированного последовательного действия гипертермии 55 °С и УФ-излучения на диплоидные дрожжевые клетки XS800 от фактора времени или временного интервала ( t ) между воздействиями температуры и УФ-света представлены на рис. 2.
Видно, что от 3 до 90 мин между воздействующими факторами наблюдался синергический эффект ( к >1), коэффициент к изменяется незначительно (1,40-1,56). Дальнейшее увеличение интервала времени приводило к резкому снижению синергического эффекта, и при t =2 ч взаимодействие факторов становится аддитивным ( к ~1,0), сохраняясь до t =5 ч. Дальнейшее увеличение времени между действием гипертермии и УФ-света приводит к антагонистическому эффекту ( к <1).
Далее в работе была исследована обратная последовательность воздействия на клетки изучаемых факторов: перед термическим воздействием клетки облучали УФ-светом в течение 1,5 мин, снижая выживаемость до 10%. Цитотоксический эффект воздействия 1,5-минутного УФ-света в данной работе изоэффективен воздействию гипертермии 55 °С в течение тех же 1,5 мин.
На рис. 3 представлена зависимость величины коэффициента k , свидетельствующего о характере взаимодействия УФ-света и гипертермии, от интервала времени между ними.
2,0
1,8
1,6
H я
s
1,4
s
1,2
к
1,0
0,8
0,6
0,4
Интервал времени между воздействиями, мин
Рис. 2. Зависи жду действием гипертермии и УФ-света.
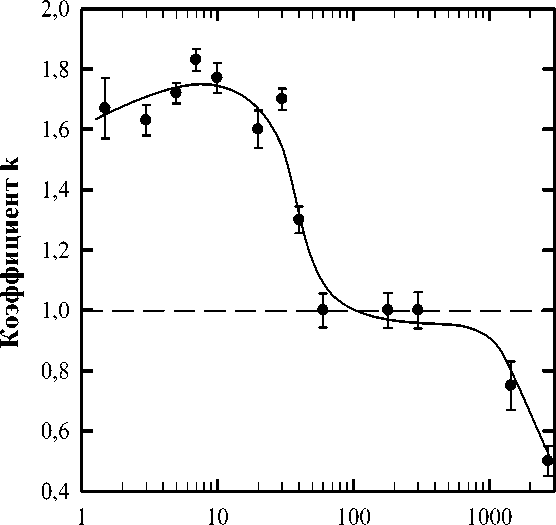
Интервал времени между воздействиями, мин
Рис. 3. З и между последовательным действием УФ-света и гипертермии.
Видно, что при изменении последовательности воздействий, когда на клетки сначала действовали УФ-излучением, а потом гипертермией, результат взаимодействия факторов также существенно зависит от интервала времени между ними. При t от 1,5 до 40 мин действие УФ-света и гипертермии характеризуется синергическим эффектом ( к =1,30-1,83). Дальнейшее увеличение интервала времени влечёт за собой резкое снижение величины синергизма до аддитивности, а затем взаимодействие УФ-излучения и гипертермии становится устойчиво антагонистическим.
Сравнение характера зависимостей, представленных на рис. 2 и 3, позволяет отметить отсутствие принципиального отличия между ними.
Как отмечалось выше, на кривых зависимости величины коэффициента к от интервала времени t , представленных на рис. 2 и 3, присутствуют три участка, характеризующих взаимодействие УФ-света и гипертермии при разных последовательностях их применения. Первый, когда к больше 1 - синергический. В основе анализа синергического действия факторов различной природы на биологические объекты лежит предположение, что синергизм обусловлен образованием дополнительных летальных повреждений за счёт взаимодействия субповреждений, образуемых каждым из агентов, участвующих в комбинации [5]. Величина синергизма больше при одновременном действии повреждающих агентов, независимо от их природы и объекта воздействия [5]. Интервал времени между воздействиями позволяет субповреждениям восстановиться, что уменьшает число летальных повреждений и, соответственно, приводит к снижению синергического эффекта или аддитивному сложению эффектов от отдельных воздействующих факторов. В нашем случае это разные последовательности действия гипертермии и УФ-света.
Далее следует участок кривой, свидетельствующий об аддитивности или простом сложении эффектов от гипертермии и УФ-света, независимо от применяемой последовательности. Последний участок кривых - резкий переход к антагонизму взаимодействия УФ-света и гипертермии по отношению друг к другу.
Заключение
В работе получены данные о влиянии фактора времени на конечный эффект последовательного действия УФ-света и гипертермии. Показано, что интервал времени между воздействующими факторами приводит не только к снижению синергического эффекта, но и к возникновению устойчивого антагонистического взаимодействия, независимо от последовательности применения УФ-света и температуры.
Механизмы возникновения синергических взаимодействий факторов различной природы на биологические объекты достаточно подробно описаны в литературе [5, 6]. В частности, причиной синергизма может быть возникновение дополнительных летальных повреждений за счёт взаимодействия субповреждений, вызванных каждым из используемых в комбинации факторов и не являющихся эффективными при их раздельном действии.
Объяснить возникновение антагонизма элиминацией субповреждений не представляется возможным. В современной литературе антагонистические эффекты при действии гипертермии объясняются высокой экспрессией белков теплового шока (БТШ) после действия повышенных температур [21-23]. БТШ активно участвуют в клеточных реакциях на гипертермию и другие цитотоксические воздействия. Основные молекулярные белки-шапероны - БТШ90, БТШ70 и БТШ27 - являются эндогенными супрессорами апоптоза и помогают клетке, подвернутой стрессу, реактивировать или деградировать денатурированные белки.
Можно предположить, что в случае комбинации УФ-света и гипертермии, по аналогии с комбинированным действием гипертермии и ионизирующего излучения, БТШ образуют комплексы с денатурированными белками. При одновременном действии гипертермии и другого фактора или при последовательном действии, но с минимальным интервалом воздействия, цитозольный пул шаперонов истощается быстрее, чем происходит экспрессия новых БТШ [21]. Возникает дефицит БТШ, который не способен обеспечить нейтрализацию денатурированных белков, образующихся при действии второго агента, поэтому происходит клеточная гибель (апоптоз), и результат взаимодействия определяется как синергетический [22].
Увеличение интервала между действием агентов позволяет цитозольному пулу БТШ восстановиться до нормальных значений. Также известно, что в клетках стрессовый фактор может спровоцировать индукцию дополнительных БТШ, которые действуют как протекторы для клеток, повышая их устойчивость к действию последующего агента [23]. С этой точки зрения становится объяснимым наблюдаемый эффект антагонизма при увеличении интервала времени более 20 ч при действии гипертермии и УФ-света независимо от последовательности в наших экспериментах.
В работе мы использовали коротковолновый УФ-свет. Модифицировали его действие гипертермией. Выше мы упоминали, что свечение Вавилова-Черенкова представляет широкий частотный спектр, в том числе и в ультрафиолетовой области. Следствием присутствия коротковолнового УФ-света при действии ионизирующего излучения высоких энергий является наличие фотореактивируемых повреждений у облучённых клеток. Если представлять ионизирующее излучение комбинированным действием ионизаций и возбуждений, и возбуждение как причину возникновения свечения Вавилова-Черенкова, тогда модификация эффекта ионизирующего излучения гипертермией может приводить к меньшим по сравнению с ожидаемыми результатам за счёт возможного антагонистического взаимодействия Уф-составляющей свечения Вавилова-Черенкова и гипертермии. Пока это теоретическое предположение. Однако учитывать такую возможность при практическом использовании комбинированного воздействия ионизирующего излучения и гипертермии имеет смысл. При этом действие химических модификаторов в присутствии УФ-света ещё предстоит исследовать.
Список литературы Эффекты комбинированного действия гипертермии и УФ-света на клетки дрожжей: фактор времени и последовательность воздействия
- Van den Tempel N., Horsman M.R., Kanaar R. Improving efficacy of hyperthermia in oncology by exploiting biological mechanisms //Int. J. Hyperthermia. 2016. V. 32, N 4. P. 446-454.
- Mantso T., Goussetis G., Franco, R., Botaitis S., Pappa A., Panayiotidis M. Effects of hyperthermia as a mitigation strategy in DNA damage-based cancer therapies //Semin. Cancer Biol. 2016. V. 37-38. P. 96-105.
- Dellinger T.H., Han E.S., Raoof M., Lee B., Wu X., Cho H., He T.F., Lee P., Razavi M., Liang W.S., Schmolze D., Priceman S.J., Lee S., Lin W.C., Lin J.F., Kebria M., Hakim A., Ruel N., Stewart D.B., Wang E.W., Rodriguez-Rodriguez L. Hyperthermic intraperitoneal chemotherapy-induced molecular changes in humans validate preclinical data in ovarian cancer //JCO Precis. Oncol. 2022. V. 6. DOI: 10.1200/PO.21.00239.
- Petin V.G., Kim J.K. Synergistic interaction and cell responses to environmental factors. New York: Nova Sciences Publisher, 2016. 337 p.
- Петин В.Г., Морозов И.И. Синергетика факторов окружающей среды. М.: Геос, 2015. 248 с.
- Петин В.Г., Белкина С.В., Жураковская Г.П. Математические модели и реакции клеток на облучение ионизирующими излучениями разного качества. М.: Геос, 2020. 263 с.
- Жураковская Г.П., Петин В.Г. Зависимость степени синергизма одновременного действия УФ-света и гипертермии на дрожжевые клетки от интенсивности УФ-света //Цитология. 1988 Т. 30, № 10. С. 1276-1280.
- Мясник М.Н., Скворцов В.Г., Соколов В.А. Фотобиологические аспекты радиационного поражения клеток. М: Энергоатомиздат, 1985. 152 с.
- Беспалов В.И. Взаимодействие ионизирующих излучений с веществом. Томск: Изд-во Томского политехнического университета, 2008. 369 с.
- Valkovic V. Radioactivity in the environment. Elsevier Science, 2019. 810 p.
- Alexander D.A., Tendler I.I., Bruza P., Cao X., Schaner P.E., Marshall B.S., Jarvis L.A., Gladstone D.J., Pogue B.W. Assessment of imaging Cherenkov and scintillation signals in head and neck radiotherapy //Phys. Med. Biol. 2019. V. 64, N 14. DOI: 10.1088/1361-6560/ab25a3.
- Black P.J., Velten C., Wang Y.F., Na Y.H., Wuu C.S. An investigation of clinical treatment field delivery verification using Cherenkov imaging: IMRT positioning shifts and field matching //Med. Phys. 2019. V. 46, N 1. P. 302-317.
- Desvaux E., Courteau A., Bellaye P.S., Guillemin M., Drouet C., Walker P., Collin B., Decreau R.A. Cherenkov luminescence imaging is a fast and relevant preclinical tool to assess tumour hypoxia in vivo //EJNMMI Res. 2018. V. 8, N 1. DOI: 10.1186/s13550-018-0464-7.
- Li Y., Liu H., Huang N., Wang Z., Zhang C. Using Cherenkov imaging to monitor the match line between photon and electron radiation therapy fields on biological tissue phantoms //J. Biomed. Opt. 2020. V. 25, N 12. DOI: 10.1117/1.JBO.25.12.125001.
- Mitchell G.S., Gill R.K., Boucher D.L., Li C., Cherry S.R. In vivo Cerenkov luminescence imaging: a new tool for molecular imaging //Philos. Trans. A Math. Phys. Eng. Sci. 2011. V. 369, N 1955. P. 4605-4619.
- Ruggiero A., Holland J.P., Lewis J.S., Grimm J. Cerenkov luminescence imaging of medical isotopes //J. Nucl. Med. 2010. V. 51, N 7. P. 1123-1130.
- Soter J.A., LaRochelle E., Byrd B.K., Tendler I.I., Gunn J.R., Meng B., Strawbridge R.R., Wirth D.J., Davis S.C., Gladstone D.J., Jarvis L.A., Pogue B.W. Tracking tumor radiotherapy response in vivo with Cherenkov-excited luminescence ink imaging //Phys. Med. Biol. 2020. V. 65, N 9. P. 095004. DOI: 10.1088/1361-6560/ab7d 16.
- Zhang R., Gladstone D.J., Jarvis L.A., Strawbridge R.R., Jack Hoopes P., Friedman O.D., Glaser A.K., Pogue B.W. Real-time in vivo Cherenkoscopy imaging during external beam radiation therapy //J. Biomed. Opt. 2013. V. 18, N 11. P. 110504. DOI: 10.1117/1 JBO.18.11.110504.
- Krohn J., Chen Y.C., Stabo-Eeg N.O., Hamre B. Cherenkov luminescence imaging for assessment of radioactive plaque position in brachytherapy of uveal melanoma: an in vivo feasibility study //Transl. Vis. Sci. Technol. 2020. V. 9, N 7. P. 1-10.
- Thorek D.L., Riedl C.C., Grimm J. Clinical Cerenkov luminescence imaging of (18)F-FDG //J. Nucl. Med. 2014. V. 55, N 1. P. 95-98.
- Кабаков А.Е., Анохин Ю.Н., Лебедева Т.В. Реакции нормальных и опухолевых клеток и тканей на гипертермию в сочетании с ионизирующей радиацией //Радиация и риск. 2018. Т. 27, № 4. С. 141-154.
- Кабаков А.Е., Мосина В.А., Хохлова А.В. Усиленная радиосенсибилизация опухолевых клеток с помощью сочетанного воздействия гипертермии и ингибиторов протеасом //Радиация и риск. 2020. Т. 29, № 4. С.118-125.
- Кабаков А.Е., Кудрявцев В.А., Хохлова А.В., Макарова Ю.М., Лебедева Т.В. Апоптоз в опухолевых клетках, подвергнутых сочетанному действию гипертермии и облучения: исследование молекулярных механизмов и мишеней //Радиация и риск. 2018 Т. 27, № 2. С. 62-75.


