Экологический фактор, изменяющий активность ферментов антиоксидантной системы - магнитное поле с частотой 66 кГц
Автор: Сергеева Е.Ю., Азанова А.В., Фефелова Ю.А., Сергеев Н.В., Титова М.С., Цугленок Н.В.
Журнал: Вестник Красноярского государственного аграрного университета @vestnik-kgau
Рубрика: Экология
Статья в выпуске: 10, 2013 года.
Бесплатный доступ
В результате исследований выявлено, что действие магнитного поля с частотой 66 кГц вызывает достоверное увеличение концентрации малонового диальдегида и снижение активности ферментов антиоксидантной системы в крови.
Магнитные поля, перекисное окисление липидов, малоновый диальдегид
Короткий адрес: https://sciup.org/14082707
IDR: 14082707 | УДК: 613.168:613.6-02:616.419-092.9
Ecological factor changing the activity of the antioxidative system enzymes - magnetic field with 66 kHz frequency
As a result of the conducted research it was revealed that the influence of magnetic field with 66 kHz frequency leads to the increase of concentration of MDA and decrease of the activity of the antioxidative system enzymes in the blood.
Текст научной статьи Экологический фактор, изменяющий активность ферментов антиоксидантной системы - магнитное поле с частотой 66 кГц
Методы исследования. В работе использовалась кровь добровольцев, взятая непосредственно перед экспериментом и стабилизированная гепарином. Принцип метода определения активности СОД основан на ингибировании реакции автоокисления адреналина в щелочной среде в присутствии СОД вследствие дисмутации супероксидных анион-радикалов. Об интенсивности автоокисления адреналина судят по динамическому нарастанию поглощения при длине волны 347 нм, обусловленному накоплением продукта окисления, опережающим по времени образование адренохрома с максимумом поглощения при 480 нм; определение активности КАТ выполняли электрофотоколориметрическим методом при длине волны 400 нм. Содержание малонового диальдегида определяли в реакции с тиобарбитуровой кислотой, включающей в себя инкубацию с тиобарбитуровой кислотой исследуемой пробы, экстракцию продуктов реакции бутанолом и спектрофотометрическое измерение их содержания [2]. В качестве источника промышленных магнитных полей использована установка высокочастотная для индукционного нагрева на базе генератора высокочастотного транзисторного ВГТ5-5/66 со следующими характеристиками: частота колебаний магнитного поля 66 кГц, напряженность магнитного поля в непосредственной близости к установке 500 А/м. Статистическая обработка результатов проведена с использованием пакета программ Statistica 6.
Результаты и выводы исследования. При действии магнитного поля с данными параметрами выявлено достоверное снижение активности супероксиддисмутазы (рис. 1).
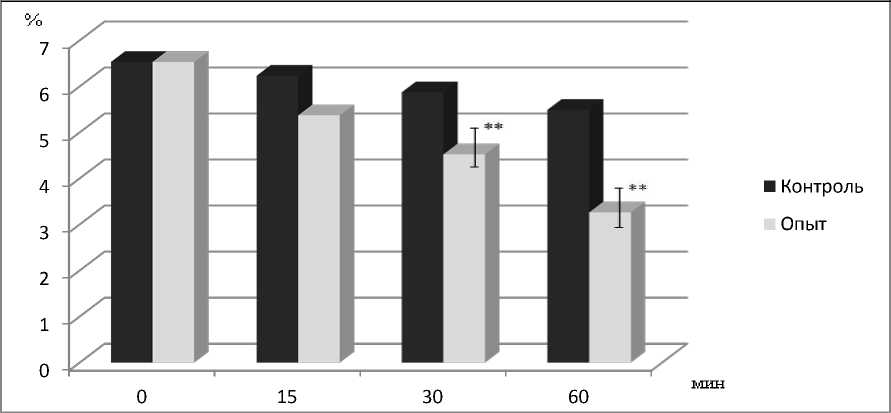
Рис. 1. Изменение активности СОД в крови при действии магнитных полей с частотой 66 кГц in vitro [25–75%], Ме
Здесь и далее **Р < 0,01
При этом воздействие магнитных полей в течение 30 минут приводило к снижению активности СОД в 1,3 раза. Воздействие же магнитных полей в течение 60 минут приводило к снижению активности СОД в 1,7 раза.
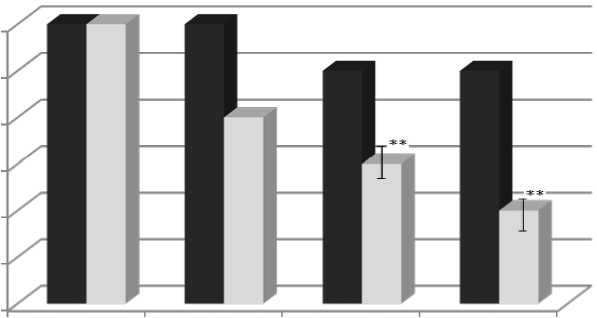
Действие магнитного поля с данными параметрами приводило к достоверному снижению активности каталазы (рис. 2).
%
0,06
0,05
0,04
0,03
0,02
0,01
0,00
30 60
Контроль
Опыт
Рис. 2. Изменение активности каталазы в крови при действии магнитных полей с частотой 66 кГц in vitro [25–75%], Ме
В экспериментах in vitro воздействие магнитных полей в течение 30 минут приводило к снижению активности каталазы в 1,6 раза. Воздействие же магнитных полей в течение 60 минут приводило к снижению активности каталазы в 2,5 раза.
При действии магнитного поля с данными параметрами выявлено достоверное увеличение продукции малонового диальдегида, отражающее выраженность окислительного стресса (табл.).
Изменение продукции МДА в крови при действии магнитных полей с частотой 66 кГц [25–75%], Ме
|
Время воздействия |
Контроль (ммоль/л) (n=27) |
Магнитные поля (n=27) |
|
0 минут |
1,22(1,22+1,23] |
1,22(1,22+1,23] |
|
15 минут |
1,35(1,33+1,35] |
2,56(2,53+2,56] |
|
30 минут |
2,16(2,13+2,16] |
5,86(5,83+5,87]** |
|
60 минут |
2,57(2,53+2,57] |
7,23(7,23+7,25]** |
Примечание: n – объем выборки.
При этом воздействие магнитных полей в течение 30 минут приводило к увеличению продукции малонового диальдегида в 2,7 раза. Воздействие же магнитных полей в течение 60 минут приводило к увеличению продукции малонового диальдегида в 2,8 раза.
Традиционно патогенез окислительного повреждения клеток рассматривался преимущественно с позиций мембрано- и генотоксичности свободных радикалов (перекисное окисление липидов (ПОЛ) и нарушение структуры ДНК), к повышению продукции которых может привести воздействие магнитных полей с используемыми параметрами. Регуляция содержания перекисей и свободных радикалов тканей обеспечивается различными ферментными системами и природными антиоксидантами. На стадии инициирования регуляция ПОЛ в клетке осуществляется посредством генерации супероксидных радикалов, влияния на активность СОД и каталазы, а также на уровень свободного железа. На стадии продолжения цепи изменяется уровень кислорода, микровязкости и содержания полиненасыщенных жирных кислот. На этапе разветвления цепи контроль за уровнем ПОЛ осуществляется за счет влияния на количество свободного железа, активность глутатионпероксидазы и уровень свободных тиолов. На стадии обрыва цепи возникают липофильные антиоксиданты и наблюдаются высокие концентрации свободного железа [1].
Известно, что важнейшим индикатором окислительно-восстановительного гомеостаза клетки является структурное и функциональное состояние клеточных белков, в том числе их термодинамическая и операционная стабильность. Большинство меж- и внутримолекулярных взаимодействий (связывание ионов, субстратов, кофакторов, лигандов, межбелковые и белок-липидные взаимодействия, конъюгация с углеводами, формирование всех видов связи и гидрофобные взаимодействия) напрямую зависят от редокс-статуса среды. В основе денатурационно-ренатурационных превращений и субстрат-ферментных взаимодействий лежит прежде всего тиол-дисульфидный обмен [1, 2]. Реакционная способность цистеиновых остатков белков зависит от присутствия окружающих их ароматических или электростатически заряженных молекул (преимущественно гистидина), а также общего редокс-потенциала системы - при преобладании окислительных валентностей формирование дисульфидных связей облегчено. Редокс-центры белковых молекул в физиологических условиях удалены от поверхности, поэтому белки могут рассматриваться в качестве своеобразного органического матрикса, движение электронов в котором осуществляется благодаря «скачкам» из одного центра в другой или по ковалентным и водородным связям. При этом дисульфидные анионы выступают в роли центров переноса электронов. Формирование дисульфидных связей, катализируемое протеиндисуль-фидизомеразой, обусловливает самоорганизацию белков клетки помимо изомеризации по пролину и ассоциации полипептидных цепей. При этом дисульфидные связи стаилизируют исходное состояние, но не определяют пространственную перестройку белковой молекулы [2]. Промежуточным на пути приобретения стабильной конформации при де- и ренатурационных процессах, сопровождающихся восстановлением дисульфидных связей, является этап формирования «расплавленной глобулы», имеющей объем, превышающий окончательный на 5-15 %, со сниженной степенью ригидности вторичной и третичной структур [1, 3]. Такие структуры способны, будучи локализованными против гидрофобной поверхности, приобретать четвертичную структуру, соответствующую исходной [1,4].
При окислительном стрессе денатурация белковых молекул клетки приводит к уменьшению периода их функционирования в результате повышения чувствительности к протеолитическим реакциям и процессам посттрансляционной модификации (фосфорилированию и рибозилированию); поддержание же частично денатурированных полипептидов в форме «расплавленной глобулы» является обязательным событием при синтезе новых пептидных цепей и их транспорте через клеточные мембраны, что создает основу эффективной регуляции метаболизма через альтерацию редокс-буферных компонентов клетки [1].
Известно, что окислительное повреждение мембран клеток (плазматической, лизосомальной, митохондриальной, ядерной) возникает вследствие окисления полиненасыщенных жирных кислот фосфолипидов, активации и деградации липидных радикалов, реорганизации двойных связей и деструкции липидов. Вследствие появления гидрофильной гидроперекисной группировки в полиненасыщенной жирной кислоте нарушается гидрофобность бислоя, диальдегиды выступают в роли поперечносшивающих бифункциональных реагентов, снижается молекулярная подвижность фосфолипидов, нарушаются липид-белковые взаимодействия, устраняется трансбислойная асимметрия липидов [1, 4].Сопутствующим процессом является деструктурирование мембранных белков – рецепторов, ферментов, ионных каналов, выступающих в роли окисляемых субстратов, особенно при наличии тиоловых групп. Последние, будучи окисленными, образуют высокомолекулярные белковые агрегаты и, таким образом, ответственны за пермеабилизацию мембран внутриклеточных органелл, в том числе митохондрий. В митохондриях протекание такого рода процессов непосредственно сопряжено с формированием свободных радикалов в дыхательной цепи, а также со связыванием ионов кальция с белками, облегчающим их окислительное повреждение. Модуляция тиолдисульфидного обмена в белках митохондриальных мембран лежит в основе повышения их ионной проницаемости [1, 3].
Выводы. Таким образом, мы можем предположить, что воздействие магнитного поля с используемыми параметрами индуцирует развитие окислительного стресса, что является результатом целого ряда взаимосвязанных процессов и реакций.


