Экспериментальное исследование биосовместимости противоспаечных мембран при околосердечной имплантации
Автор: Шишкова Дарья Кирилловна, Кудрявцева Юлия Александровна, Насонова Марина Владимировна, Ходыревская Юлия Ивановна, Бурков Николай Николаевич
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 1 т.32, 2017 года.
Бесплатный доступ
Проведен сравнительный анализ мембран на основе (поли(3-гидроксибутират-ко-3-гидроксивалерата) с поли(лактид-ко-гликолидом), изготовленных методом электроспиннинга, и коллагеновых мембран (КолГАРА) при имплантации на переднюю поверхность сердца крыс (Wistar). При исследовании физико-механических свойств было показано, что прочность коллагеновых мембран превышает таковую у мембран из искусственных полимеров, которые, в свою очередь, обладают большей способностью к деформациям. В течение всего периода наблюдения не было выявлено различий в сывороточных концентрациях провоспалительных цитокинов у животных, которым имплантировали полимерные либо коллагеновые мембраны, в сравнении с ложнооперированными животными. Мембраны из природных и искусственных полимеров не вызывали какой-либо системной специфической воспалительной реакции, что свидетельствует об их высокой биосовместимости.
Биодеградируемые полимеры, мембраны, колгара, поли(3-гидроксибутират-ко-3-гидроксивалерат), поли(лактид-ко-гликолид), электроспиннин
Короткий адрес: https://sciup.org/14920163
IDR: 14920163 | УДК: 615.461-77:577.11:621.31
Biocompatibility testing of natural and synthetic pericardial adhesion barriers
Here we performed a physico-mechanical and biocompatibility testing of pericardial adhesion barriers prepared from either blend of poly(3-hydroxybutyrate-co-3-hydroxyvalerate) with poly(lactide-co-glycolide) or collagen. Collagen adhesion barriers had higher durability while synthetic barriers were more prone to deformation. No significant differences in serum levels of pro-inflammatory cytokines (TNF-б, IL-1в, IL-6, and MCP-1) were found between rats with either collagen or synthetic adhesion barriers implanted to anterior pericardium compared to mock-treated rats. We conclude that both natural and synthetic pericardial adhesion barriers do not cause any systemic inflammation and have high biocompatibility.
Текст научной статьи Экспериментальное исследование биосовместимости противоспаечных мембран при околосердечной имплантации
В сердечной хирургии, в частности, при коррекции сложных врожденных пороков сердца, проводятся многоэтапные хирургические вмешательства, при этом важную роль играет профилактика образования послеоперационных спаек. Применение биодеградируемых про-тивоспаечных мембран может позволить предотвратить спаечный процесс, являющийся причиной массивного кровотечения, которое удлиняет время повторной операции, а также увеличивает частоту послеоперационных осложнений и летальность. Мы предположили, что биодеградируемые противоспаечные мембраны из поли(3-гидроксибутират-ко-3-гидроксивалерата) (PHBV) с поли(лактид-ко-гликолидом) (PLGA) в соотношении 70:30 с включением дексаметазона (ДМ) при имплантации будут способствовать равномерному выделению данного препарата в окружающие ткани, что позволит снизить воспалительную реакцию и уменьшить риск образования спаек.
Цель работы: оценить реакцию организма на ортотопическую имплантацию противоспаечных мембран.
Материал и методы
Для изготовления мембран использовали PHBV с молекулярной массой 330 кДа (Институт биохимии и физиологии микроорганизмов им. Г.К. Скрябина РАН, Пущино) и PLGA (Лаборатория биополимеров и биотехнологии химического факультета Томского государственного университета) в соотношении лактида к гликолиду 60:40. В качестве группы сравнения была взята рассасывающаяся противоспаечная коллагеновая мембрана Кол-ГАРА (Синтаколл ГмбХ, Германия), в состав которой входит ренатурированный лошадиный коллаген. Были описаны клинические случаи использования КолГАРА при операциях на органах брюшной полости и малого таза [1–3], но не встречались источники литературы, в которых описывались бы случаи использования данного материала в хирургии сердца. Мембраны изготавливали на установке для электроспиннинга Nanon-01А (MECC Inc., Япония) при напряжении 21 Кв и скорости подачи раствора 0,4 мл/ч. Экспериментальные образцы противо-спаечных мембран были представлены следующими группами: PHBV+PLGA, PHBV+PLGA+ДМ (концентрация ДМ составила 0,5 мг/мл), КолГАРА. Для включения ДМ во внутреннюю часть волокна использовали коаксиальную насадку.
Непосредственно перед имплантацией лабораторным животным образцы стерилизовали этиленоксидом при комнатной температуре. Все манипуляции проводили, соблюдая принципы гуманного обращения с животными, регламентированные требованиями Европейской конвенции (Страсбург, 1986).
Образцы мембран (n=28) размером 0,7x0,7 см имплантировали крысам-самцам линии Wistar весом 300– 350 г (одна мембрана на крысу). После введения в ингаляционный наркоз изофлураном (“E-Z Anesthesia”, E-Z Systems Corporation) в условиях чистой операционной проводили доступ к сердцу посредством левосторонней торакотомии с пересечением двух ребер. После выпол- нения перикардиотомии мембраны фиксировали нитью Prolene двумя узловыми швами (у верхушки и у основания сердца) по углам экспериментальных мембран на передней поверхности сердца. После этого грудную полость послойно ушивали нитью Лавсан 3/0. В качестве контрольной группы служили ложнооперированные животные (группа ЛО, n=12), которым в аналогичных условиях выполнялись все манипуляции за исключением подшивания матриксов. В качестве второй контрольной группы выступили здоровые интактные животные (n=5). Вывод животных из эксперимента после оперативного вмешательства проходил на временных точках 2 недели, 1 мес. и 2 мес. (по 3 животных из каждой группы на точку). У всех животных забиралась кровь с целью последующего определения моноцитарного хемоаттрактантного белка (МСР-1) и провоспалительных цитокинов TNF-α, IL-6 и IL-1β посредством иммуноферментного анализа. У всех животных биоптировали сердце с фиксированной на нем мембраной для макроскопического и гистологического изучения. Гистологические срезы готовили по стандартной методике, окрашивали гематоксилин-эозином и по Ван Гизону.
Результаты
Нами были поставлены следующие задачи:
– оценить специфичность воспалительной реакции на имплантацию противоспаечных мембран;
– сравнить противоспаечный эффект мембран из природных и искусственных полимеров;
– выяснить, снижает ли инкорпорирование ДМ в мембраны из искусственных полимеров воспалительную реакцию и препятствует ли образованию спаек.
Для этого было проведено макроскопическое исследование, а в сыворотке крови крыс во всех группах на всех временных точках были измерены концентрации провоспалительных цитокинов (MCP-1, TNF- α , IL-6 и IL-1 β ).
Во всех группах оперированных животных был выявлен спаечный процесс. В группе ложнооперированных животных спаечный процесс отмечался между грудной клеткой и шовным материалом на протяжении всего сро-
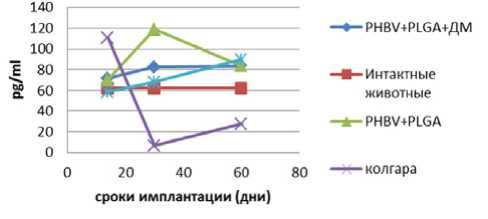
Риc. 1. Динамика MCP-1 противоспаечных мембран и групп сравнения
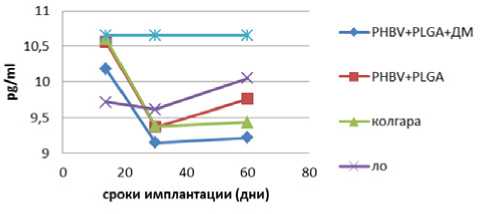
Рис. 2. Динамика TNF- α противоспаечных мембран и групп сравнения
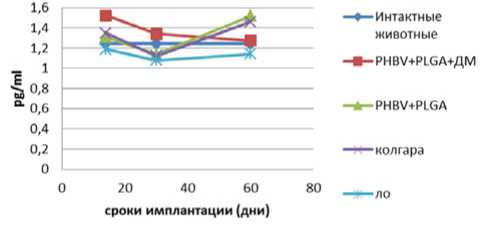
Рис. 3. Динамика IL-6 противоспаечных мембран и групп сравнения
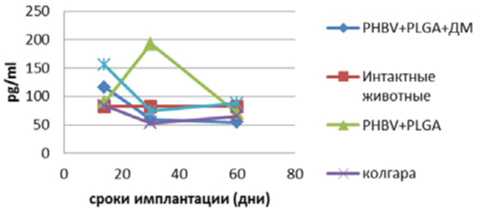
Рис. 4. Динамика IL-1 β противоспаечных мембран и групп сравнения
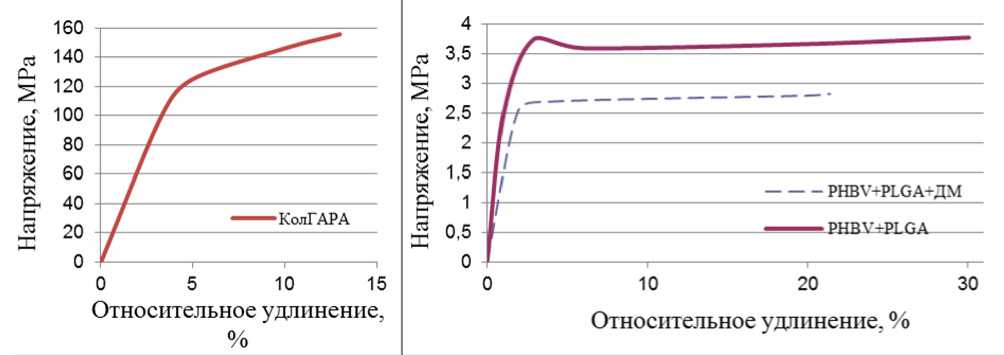
Рис. 5. Диаграмма растяжения противоспаечной коллагеновой мембраны КолГАРА и противоспаечных мембран PHBV+PLGA, PHBV+PLGA+ДМ
ка эксперимента. Наиболее интенсивный спаечный процесс отмечался в группе PHBV+PLGA: спустя 2 недели имплантации спайки визуализировались между внутренней стенкой грудины и нижним краем мембраны, а к 2 мес. имплантации спаечный процесс вокруг мембраны охватывал область перикарда и части легкого.
В группе PHBV+PLGA+ДМ спустя 2 недели после имплантации спаечный процесс был выражен слабее в сравнении с мембраной без добавления лекарственного вещества; к 1 мес. имплантации визуализировались некрупные спайки, мембрана была слегка припаяна к внутренней поверхности ребер, наблюдалась слабая деградация.
В группе КолГАРА к 2 неделям имплантации спаечный процесс наблюдался между внутренней поверхностью грудной клетки, плевры и шовным материалом; а к 2 мес. имплантации мембрана уже не визуализировалась.
Таким образом, мы предположили, что развитие спаечного процесса было обусловлено травматизацией грудной клетки и шовным материалом, а не имплантированными противоспаечными мембранами.
Моноцитарный хемоаттрактантный белок 1 (МСР-1) экспрессируется в основном макрофагами в ответ на широкий спектр таких цитокинов, как IL-6, TNF- α и IL-1 β , но может также секретироваться и другими клет-
Таблица
Физико-механические свойства противоспаечных мембран на основе PHBV+PLGA и мембраны КолГАРА
При сравнении сывороточных концентраций фактора некроза опухоли- α (TNF- α ) и провоспалительных ин-терлейкинов-1 β и -6, которые являются плейотропными молекулами с центральной ролью в реакциях воспаления и апоптоза [4, 5], статистически значимых различий между группами обнаружено не было (рис. 2–4).
При изучении механических свойств противоспаеч-ных мембран было обнаружено, что прочность экспериментальных образцов PHBV+PLGA и PHBV+PLGA+ДМ ниже прочности мембраны КолГАРА в 41,2 (р=0,04) и 55 (р<0,01) раз соответственно (таблица). Добавление дексаметазона как жидкой фазы в состав полимерного матрикса статистически незначимо снижает прочность, и в то же время повышает эластичность материала, увеличивая способность к растяжению. При этом эластичность мембраны PHBV+PLGA+ДМ статистически незначимо превышает эластичность КолГАРА в 1,6 раз.
Одной из характеристик упругих свойств является модуль Юнга, показывающий способность материала сопротивляться растяжению. С модулем Юнга линейно связан коэффициент жесткости, который является показателем конкретного отдельного образца, в то время как модуль Юнга характеризует весь материал в целом. Кол-ГАРА обладает большим модулем упругости, достоверно превышающим аналогичный показатель мембран PHBV+PLGA и PHBV+PLGA+ДМ в 6,37 (р=0,04) и 10,58 (р<0,01) раз соответственно.
Высокий предел прочности барьера КолГАРА при малом растяжении (рис. 5) дает большую жесткость в сравнении с полимерными мембранами и, соответственно, меньшую деформационную способность по сравнению с полимерными мембранами.
При рассмотрении зависимости “напряжение–удлинение” для групп противоспаечных мембран было отмечено, что упругие свойства коллагеновой мембраны Кол-ГАРА сохраняются до нагрузки порядка 100 МРа и относительного удлинения 3%, полимерных мембран, изготовленных методом электроспиннинга – до 2,5 МРа и 1,8% для PHBV+PLGA, 2,2 и 2,5% для PHBV+PLGA+ДМ, после чего идут пластические деформации и дальнейший разрыв образцов.
Выводы
Не было выявлено как специфического воспалительного ответа на имплантацию противоспаечных мембран, так и различий в выраженности иммунной реакции на мембраны из природных и искусственных полимеров, что свидетельствует об их высокой биосовместимости. Кроме того, показано, что инкорпорирование дексаметазона в противоспаечные мембраны из искусственных полимеров не снижает местную воспалительную реакцию. При исследовании физико-механических свойств показано, что прочностные свойства коллагеновых мембран превышают таковые у мембран из искусственных полимеров, которые в свою очередь обладают большей способностью к деформациям.
Список литературы Экспериментальное исследование биосовместимости противоспаечных мембран при околосердечной имплантации
- Силуянов С.В., Алиев С.Р. Первый опыт применения противоспаечной коллагеновой мембраны при операциях на органах брюшной полости и малого таза//Рос. мед. журн. -2015. -№ 13. -С. 789-795.
- Савельева И.В., Полянская И.Б., Красникова Е.Г. и др. К вопросу о профилактике спайкообразования при оперативных вмешательствах на органах малого таза//Рос. мед. журн. -2015. -№ 20. -С. 1233-1237.
- Gorskiy V.A., Sivkov A.S., Agapov M.A. et al. The first experience of using a single-layer intra-abdominal collagen plate//Khirurgiia (Mosk). -2015. -Vol. 5. -P. 59-61.
- Juhasz K., Buzas K., Duda E. Importance of reverse signaling of the TNF superfamily in immune regulation//Expert Rev. Clin. Immunol. -2013. -Vol. 9(4). -P. 335-348.
- Zelova H., Hosek J. TNF- signalling and inflammation: interactions between old acquaintances//Inflammation Res. -2013. -Vol. 62(7). -P. 641-651.


