Экспериментальное исследование деградируемых биополимеров нового класса для пластики костных дефектов и остеомиелитических полостей
Автор: Шишацкая Е.И., Винник Ю.С., Маркелова Н.Н., Шагеев А.А., Камендов И.В., Старосветский С.И., Хоржевский В.А., Назарьянц Ю.А., Шумилова А.А., Пахомова Р.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Экспериментальные и лабораторные исследования
Статья в выпуске: 6 (28), 2012 года.
Бесплатный доступ
В статье проанализированы остеопластические свойства полигидроксибутирата на лабораторных животных. Биодеградируемые объемные имплантаты и пломбировочный материал на основе полигидроксибутирата обладают выраженными остеопластическими свойствами, медленно деградируют in vivo, обеспечивая нормальное протекание репаративного остеогенеза.
Полимер 3-гидроксимасляной кислоты, пгб, гидроксиапатит, гап, тиенам, объемные имплантаты, пломбировочный материал, сегментарная остеотомия, хронический остеомиелит, костная пластика, реконструктивный остеогенез
Короткий адрес: https://sciup.org/142211062
IDR: 142211062 | УДК: 617-089.856:612.6.05
Текст научной статьи Экспериментальное исследование деградируемых биополимеров нового класса для пластики костных дефектов и остеомиелитических полостей
В настоящее время травматизм получил статус эпидемии [7]; до 30% в структуре хирургической патологии связано с получением травм различной тяжести и локализации. Несмотря на использование современных конструкций и технологий лечения, процент осложнений и неудовлетворительных результатов все еще остается высоким, до 37% [19].
В настоящее время для реконструкции костных дефектов в ортопедии, травматологии и хирургической стоматологии наиболее распространенными материалами с четко выраженной опорной функцией являются искусственные и натуральные кальций-фосфатные материалы (гидроксиапатит, ди- и трифосфат кальция) [13; 21; 24]. После установления способности коллагена стимулировать регенерацию костной ткани [6] начаты получение и исследование биокомпозиционных материалов, содержащих коллаген и гидроксиапатит. Для челюстно-лицевой хирургии и хирургической стоматологии за рубежом разработаны композиции типа «Alveloform» и «Bigraft», содержащие очищенный фибриллярный кожный коллаген и частицы гидроксиапатита. Серия гибридных материалов на основе кальцийфосфатов и коллагена создана в России, это «Гидроксиапол», КоллапАн®, «Росдент», «Полистом», «Индост» [4, 5]. Однако физико-механические характеристики этих препаратов (невысокие показатели прочности порядка 6,5 МПа и модуль Юнга около 2 ГПа) ограничивают применение материалов такого типа для заполнения крупных костных дефектов [21].
Среди подходов, направленных на улучшение механических свойств биоматериалов из гидроксиапатита (уменьшение жесткости, повышение эластичности), в последние годы сформировалось направление исследований, ориентированное на получение композитов ГАП с синтетическими полимерами (полиэтиленом, полисульфоном). Однако наполнение гидроксиапатита такими полимерами значительно снижает биосовместимость [26]. Новым решением проблемы может стать создание гибридных материалов на основе гидроксиапатита и биосовместимых полимеров, способных к биодеградации [16, 18].
Среди разрушаемых биополимеров особое место занимают полигидроксиалканоаты (ПГА) – полимеры гидроксипроизводных алкановых кислот, которые с конца 1980-х годов прошлого века активно изучают в качестве материала для хирургических элементов, тканевой инженерии и биоискусственных органов [22, 25]. ПГА представляют большой интерес для ортопедии в связи с их механической прочностью, высокой биосовместимостью и медленной биодеградацией [12, 15, 17]. В Институте биофизики СО РАН разработана технология получения ПГА различного состава; получено семейство экспериментальных полимерных изделий и конструкций биомедицинского назначения различного типа; для реконструктивного остеогенеза разработан композит из полимера гидроксимасляной кислоты (полигидроксибутирата, ПГБ) и гидроксиапатита (ГАП) с различным соотношением компонентов, исследованы физико-химические и физико-механические свойства [8]; in vivo показано, что композит ПГБ/ГАП обладает остекондуктивными свойствами и способствует образованию костной ткани в тесте эктопического костеообра-зования [9, 20].
Цель настоящей работы – исследование остеопластических свойств полигидроксибутирата на лабораторных животных на моделях сегментарной остеотомии и хронического остеомиелита.
Maтериалы и методы
Исследованы экспериментальные объемные имплантаты трех типов, изготовленные из собственно полигидроксибутирата (ПГБ), гибридного материала полигидроксибу-тират/гидроксиапатит (ПГА/ГАП) с содержанием ГАП 20% (фирмы ЗАО Полистом®, Москва), и материал сравнения – Bio-Oss® (препарат ксенокости фирмы Geistlich, Швейцария), а также пломбировочный материал, представляющий собой порошок ПГБ и смесь ПГБ с тиенамом.
Эксперимент для моделирования коcтной ткани (тест сегментарной остеотомии) проведен на половозрелых крысах-самках линии «Вистар» с исходной массой 200– 220 г(разводки питомникаИнститута цитологии игенетики СО РАН). Животных содержали в виварии на стандартном рационе, руководствуясь инструкцией «Использование животных в космической биологии и медицине» и «Правилами проведения работ с экспериментальными животными». Использовали 36 животных, которые были разделены на 3 группы (по 12 крыс в каждой): две экспериментальные
(имплантаты на основе ПГБ и ПГБ/ГАП) и группа сравнения. Область для формирования дефекта выбрана с учетом известных данных о том, что наиболее оптимальной моделью у крыс, позволяющей корректно оценить эффективность влияния на репаративный остеогенез имплантатов из различных материалов, является дефект метаэпифизарной зоны большеберцовой кости диаметром от 1,5 до 3,0 мм и глубиной от 1,0 до 3,5 мм [1–3]. Для формирования дефекта костной ткани у животных под ингаляционным наркозом в области эпифиза большеберцовой кости после обнажения мышелков и верхней трети провой голени с помощью остеотома диаметром 2,5 мм при постоянном охлаждении физиологическим раствором создавали дефекты диаметром 3,0 мм и глубиной 2–2,5 мм, которые заполняли сконструированными имплантатами. После этого проводили послойное ушивание послеоперационной раны. Исходная площадь экспериментальных имплантатов составила 26,28 мм2; объем – 39,42 мм3.
Хронический остеомиелит моделировали у кроликов-самцов породы «Шиншилла» 4–5-месячного возраста. Использовали 60 животных (3 группы по 20 животных): 2 – экспериментальные и контрольная. Под калипсол-дроперидоловым наркозом по переднемедиальной поверхности бедра животным проводили разрез кожи длиной 3 см. Мышцы тупо разводили и фиксировали. В области передней поверхности метадиафиза бедра выполняли остеотомию на протяжении 0,5 см, ограниченную отслойку надкостницы, вскрывали костномозговой канал; ложкой Фолькмана удаляли костный мозг. В образованный дефект имплантировали марлевую турунду с культурой золотистого стафилококка – 109 микробных тел Staphylococcus aureus . Рану послойно ушивали. Модель экспериментального остеомиелита формировали в течение 1 месяца; воспроизводимость модели – 100%; процесс был первично-хроническим.
Далее у животных с хроническим остеомиелитом производили пластику костных дефектов. Разрез кожи осуществляли с иссечением послеоперационных рубцов, свища и свищевых ходов. По ходу разреза вскрывали гнойные затеки, удаляли некротические ткани, секвестры. В процессе операции отбирали пробы для определения возбудителя и чувствительности к антибиотикам. Выполняли трепанацию кости на достаточном протяжении до видимой здоровой кости, с вскрытием костномозговых каналов. Образовавшаяся корытообразная костная полость и прилежащие костномозговые каналы тщательно обрабатывали ложкой Фолькмана. После удаления всех нежизнеспособных тканей, полость промывали раствором антисептиков (пливасепт, раствор хлоргексидина). Через контрапертурные разрезы в рану устанавливали ирригаторы для дренирования в области операции в послеопе- рационном периоде. Далее в костную полость заполняли полностью костнопластическими материалами на основе ПГБ и ксенотрансплантатом. Рану послойно ушивали наглухо. Дренажные трубки присоединяли к вакуумному устройству. В послеоперационном периоде для покоя проводили иммобилизацию конечности гипсовой лонгетой или артезом.
В послеоперационном периоде осуществляли динамическое наблюдение за состоянием животных (аппетит, двигательная активность, опороспособность оперированной конечности, состояние тканей в месте операции. Выведение животных из эксперимента для забора материала осуществлялся летальной дозой ингаляционного наркоза. Морфологические исследования выполнены общепринятыми методами. После декальцинации препаратов раствором «Трилона-Б» готовили гистологические срезы (толщиной 5–10 мкм), которые окрашивали гематоксилин-эозином. На аутопсии оценивали состояние окружающих мягких тканей, состояние надкостницы, кортикального слоя и костномозгового канала. В эксперименте с модельным остеомиелитом в области дефекта проводили бактериологический посев на среду Чистовича (желточно-солевой агар). Морфологические исследования проводили с применением поляризационного микроскопа в проходящем свете Axioskop 40 Pol. (Karl Zeiss) с цифровой фотокамерой AxioCam MRc-5. С использованием Image Analysis System «Carl Zeis» (Германия) проводили анализ изображений и морфометрические исследования срезов для костной ткани в месте дефекта, оценки состояния и динамику резорбции материала имплантатов. Определение остаточного содержания материала имплантатов в месте дефекта проводили модифицированным морфометрическим методом В.П. Яценко [10].
Статистическую обработку результатов осуществляли с помощью программы «MS Excel»; рассчитывали среднюю арифметическую величину и ее ошибки (М×m) и критерий Стьюдента (t) с определением достоверности различий (р). Критический уровень значимости р принимали меньшим или равным 0,05. Анализировали не менее 5-ти гистологических срезов препаратов, полученных от каждого животного; в ходе морфометрического анализа анализировали не менее 10 областей (10 полей зрения).

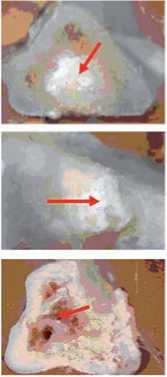
Рис. 1. Верхний ряд – фото пломбирочного порошка ПГБ (1), объемных пористых имплантатов (натуральные размеры) (2) и увеличенного х10 раз (3); нижний ряд – СЭМ изображения пористого имплантата из ПГБ
Результаты и обсуждение
На рис. 1 представлены фото и СЭМ изображения исследуемых имплантатов из ПГБ. На электронных снимках видна взаимосвязанная пористость, однако сама структура пор была несколько неравномерной. Размеры пор составили 100–200 мкм; пористость матриксов у композита ПГБ/ ГАП незначительно превышала пористость ПГБ (табл. 1).
Изученные характеристики имплантатов в общем близки, отмечены незначительные изменения плотности и краевого угла смачивания водой у композитных изделий. Плотность имплантатов из ПГБ составила 0,90 г/cм3 против 0,96 г/cм3 у ПГБ/ГAП.
Результаты исследования ПГБ на модели сегментарной остеотомии
Процесс репаративного остеогенеза в месте имплантации материалов разных типов исследован в течение 3-х месяцев. Все животные удовлетворительно перенесли оперативное вмешательство; значимых осложнений у животных в постоперационном периоде не выявлено. У всех животных раны зажили первичным натяжением. Через 7–8 дней животные могли нагружать оперированную конечность в полном объеме. На всех сроках наблюдения имплантаты
Таблица 1
Характеристики объемных имплантатов на основе ПГБ
|
Имплантат |
Характеристики |
||||
|
Пористость,% |
Плотность, г/см3 |
Контектный краевой угол смачивания водой, |
Поверхностное натяжение эрг/cм2) |
Свободная энергия межфазовой поверхности |
|
|
ПГБ |
72 |
0,90 |
72006I |
31,18 |
8,70 |
|
ПГБ/ГАП |
76 |
0,96 |
69012I |
33,56 |
7,50 |
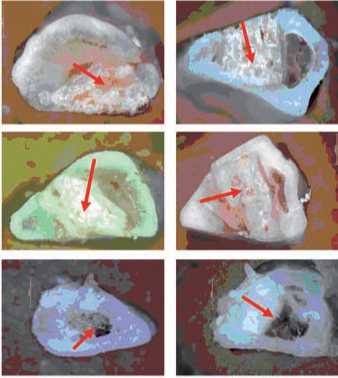
90 суток
Рис. 2. Поперечные спилы костей в области дефекта в динамике эксперимента; имплантаты: 1 - ПГБ, 2 – композит ПГБ/ГАП (наполнение полимера ГАП 20 % по массе), 3 – Bio-OSS® (показаны стрелками). Окраска гематоксилин-эозином, увеличение х25
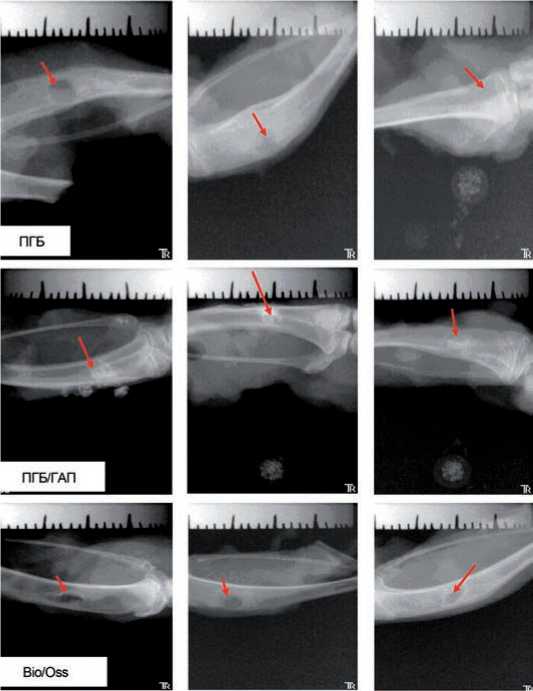
30 60 90 суток
Рис. 3. Данные рентгенологических исследований динамики восстановления модельного дефекта костной ткани при использовании различных имплантатов из ПГБ, ПГБ/ГАП и Bio-OSS®
всех типов находились в месте костного дефекта. Нагноения тканей в области имплантации и воспалительных реакций не отмечено.
По данным рентгенологических исследований зон лизиса, образования фиброзных капсул вокруг имплантатов всех типов не выявлено. Заживление костных дефектов у животных протекало по общим закономерностям, включая фазы посттравматических изменений тканевых элементов, регенерации и адаптивной ремодуляции. Заполнение модельного дефекта имплантатами, изготовленными из различных материалов, способствовало регенерации костного дефекта в разной степени. На рис. 2 представлены фрагменты костной ткани в месте закрытия модельного дефекта костной ткани исследуемыми имплантатами на разных сроках наблюдения, из которого следует, что при использовании Bio-Oss в отличие от экспериментальных групп животных с имплантатами из ПГБ и ПГБ/ГАП полного закрытия дефекта к концу наблюдения не произошло. Эти результаты подтверждены рентгенологически (рис. 3). На 60-е сутки у большинства животных опытной группы рентгенологическая картина характеризовалась восстановлением кортикальной пластинки и костно-мозгового канала, структура костной ткани полностью соответствовала нормальной. На 90 сутки у всех животных рентгенологически подтверждено восстановление анатомической структуры кости. В группе сравнения у животных на 90 сутки сохранялась неоднородность структуры регенерата, утолщение надкостницы, костно-мозговой канал не прослеживался.
Результаты гистологических исследований срезов тканей в местах модельных дефектов, заполненных имплантатами из различных материалов, представлены на рис. 4. Через 1 месяц в зоне дефекта при имплантации имплантата из полимера ПГБ на фоне активного образования костных пластинок и перестройки их в кортикальную кость, что подтверждалось наличием остеонов с четкими линиями цементации, зафиксированы значительное сокращение количества полимерного имплантата; фрагменты полимера на гистологических срезах составили около 60% от исходной площади. В отдельных участках исследуемых препаратов наблюдали слабовыраженное разрастание мезенхимальной ткани вокруг материала с пролиферацией остеобластов и образованием остеоидов. На этом сроке наблюдений наибольший прирост новообразованной костной массы определялся в области эндоста, что подтверждалось значительным увеличением количества, объема и степенью зрелости костных трабекул.
К окончанию эксперимента (3 месяца) в зоне имплантации ПГБ отмечено активное формирование новообразованной кости, имеющей зрелый характер, о чем свидетельствовало выраженное пластинчатое строение и формирование остеонов. В препаратах видны отдельные мелкие фрагменты разрушающегося полимера, которые не включились в
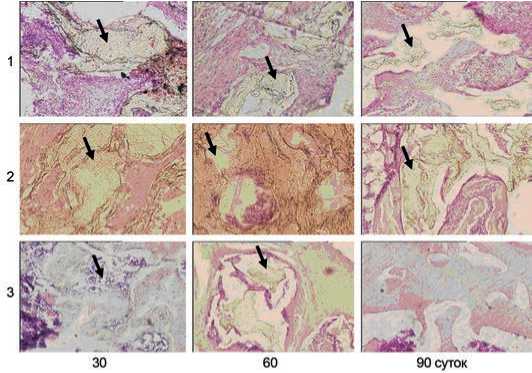
90 суток
Рис. 4. Регенераты в области имплантации 1 - ПГБ, 2 - ПГБ/ГАП, 3 - Bio-Oss® на разных сроках после операции. Стрелками обозначены остатки материалов имплантатов. Окраска гематоксилин-эозин, увеличение х100
состав остеогенной ткани и находились отдельно от нее в форме кластеров, площадь которых составила порядка 25% от исходной. Присутствие полимерного материала в препаратах на этом сроке после имплантации свидетельствует о низких скоростях его резорбции. Проявлений воспалительный реакций в месте контакта имплантата с нативной костью, формирования капсулы не отмечено.
При имплантирование в модельный дефект костной ткани образцов, изготовленных из композита ПГБ/ГАП, картина репаративного остеогенеза несколько отличалась от течения процесса при использовании чистого полимера. Через месяц масса остеогенной ткани заметно возросла, но строение костных пластин было хаотичным; система остеонов выражена в меньшей степени по сравнению с экспериментом, в котором использовали имплантаты из ПГБ, на том же сроке (рис. 4). На срезах отчетливо видны фрагменты полимера, не интегрированные в новообразованную костную ткань. Отмечено усиление продукции гемопоэтических клеток. Формирующаяся кортикальная кость с сохранением крупных лакун достаточно рыхлая, что позволяет предполагать о том, что ее биомеханические свойства значительно ниже, чем в группе животных с использованием полигидроксибутирата. Через три месяца зафиксирована практически полностью сформированная кортикальная костная ткань, содержащая систему остеонов, остеоцитов и остеокластов. Тем не менее, костные пластинки в отдельных участках гистологических препаратов имели не продольную, а хаотическую направленность.
По-прежнему в препаратах видны достаточно крупные фрагменты имплантатов, суммарная площадь, занимаемая остаточными фрагментами имплантата составляла до 40–45% от исходной, что практически в 2 раза выше этого показателя в случае использования имплантата, изготовленного только из ПГБ. При этом отмечено наличие фрагментов гидроксиапатита, отделенного от полимера слоем мезенхимальных клеток. Таким образом, резорбция композитного имплантата протекала значительно медленнее по сравнению с чистым ПГБ.
При использовании для заполнения модельного дефекта костной ткани препарата Bio-OSS® регенерация костного дефекта протекала на фоне более активной резорбции матриксов в сравнении с матриксами на основе ПГБ (рис.4). Через 1 месяц в препаратах представлена в основном компактная кость с четкими гаверсовыми системами. Костных пластинок (трабекул) мало, пролиферативная активность остеогенных клеток и остеобластов слабая. Периост утолщен за счет фиброзного слоя. Костно-мозговой канал широкий, заполнен костным мозгом. Спустя 3 месяца, картина остеогенеза, аналогична сроку 1 месяц, в препаратах зафиксирована компактная кость с широким костно-мозговым каналом, заполненным костным мозгом. Костных трабекул нет. Эндост выстлан остеогенными клетками. Периост фиброзирован. В целом, морфологические признаки репаративной регенерации костной ткани выражены слабее, а объем новообразованной кости меньше, чем при использовании имплантатов, изготовленных с использованием полигидроксибутирата.
Результаты исследования ПГА на животных с моделью хронического остеомиелита в хроническом эксперименте
В раннем послеоперационном периоде (до 3 суток) животные оставались вялыми, мало двигались, щадили оперированную конечность. Аппетит и двигательная активность кроликов восстанавливалась к 3–5 суткам, однако отсутствовала опора на больную конечность. На 5–12 сутки после операции у 19 животных выявлен отек мягких тканей в области операции, у 12 – локальная гиперемия кожи. В среднем на 16,5±3,2 сутки отек и гиперемия купировались. Опора на конечность появлялась на 6,22±1,72 сутки после операции. Операционные раны заживали в среднем на 11±1,32 сутки. Летальных случаев в послеоперационном периоде не наблюдали. При замещении костных полостей экспериментального остеомиелита пломбировочным материалом на основе ПГБ наблюдали достоверно более быстрое заживление послеоперационных кожных ран и восстановление опорных свойств оперированной конечности, по сравнению с контрольной группой. Так, в экспериментальных группах заживление операционной кожной раны произошло в среднем через 7,4±0,9 суток; купирование отека и гиперемии мягких тканей – через 8,75±0,96 суток; в контрольной группе – соответственно на 9,9±1,7 и 11,7±1,8 суток. Восстановление опороспособность оперированной конечности у экспериментальных животных получено на 4,28±0,9 сутки; в контрольной группе – на 5,56±1,2 сутки.
Таблица-2
|
Группы экспериментальных животных |
30-е сутки послеоперационного периода |
90-е сутки послеоперационного периода |
|
Контроль |
6,4 х107±110 в 1 г Staph. aureus 4,4 х107±110 в 1 г ассоциации грам (+) и (-) анаэробных микроорганизмов, E. сoli |
3,2х104±150 в 1 г Staphilococcus aureus 2,8х104±150 в 1 г ассоциации грам (+) и (-) анаэробных микроорганизмов, E. Coli |
|
ПГБ |
4,2 х104±150 в 1 г Staph. aureus 4 х104± 150 в 1 Ассоц. грам (+) и (-) анаэробных микроорганизмов, E. Coli |
– |
|
ПГБ/тиенам |
– |
– |
Анализ рентгенографических данных оперированных конечностей животных выявил следующее: на 15-е сутки после применения для пластики дефекта ПГБ и ПГБ/ тиенам в проекции костного дефекта определены участки просветления округлой формы с четкими границами с облачковидным затемнением в центре. На 90 сутки у всех экспериментальных животных рентгенологически подтверждалось восстановление анатомической структуры кости. В контрольной группе животных в эти сроки сохранялась неоднородность структуры регенерата и утолщение надкостницы..
Результаты микробиологических исследований проб материала из области дефекта представлены в табл. 2.
При исследовании микробного профиля контрольной группы на 30 и на 90 сутки высевались ассоциации микроорганизмов, среди которых доминировали (48,2%) Staphilococcus aureus, остальное – ассоциации грамполо-жительных и грамотрицательных анаэробных микроорганизмов, кишечная палочка. В экспериментальной группе с использованием ПГБ на 30 сутки высевались ассоциации микробов преимущественно (44,1%) Staphilococcus aureus и 55,9% ассоциации грамм положительных, грамм-отрицательных анаэробных микроорганизмов, E. сoli . На 90 сутки бактериоскопические посевы были отрицательными, то есть гидрофобный поропошок ПГБ подавлял инфекцию. В группе животных с использованием ПГБ/тиенам пробы биоматераилов при бактериоскопическом исследовании показали отсутствии роста микроорганизмов на более ранних сроках.
Восстановление анатомической структуры костной ткани наблюдали только в экспериментальных группах животных. В группе сравнения полноценного восстановления костной структуры не произошло. При гистологическом исследовании препаратов экспериментальных групп, в которых дефект заполняли порошком ПГБ и ПГБ/тиенам, на 15-е сутки дефект в центре был заполнен грубоволокнистой соединительной тканью с выраженной перифокальной пролиферацией капиллярного типа сосудов, очаговой лимфо-гистиоцитарной инфильтрацией. Преимущественно вокруг новообразованных сосудов отмечены очаги примитивного остеогенеза с формированием остеоидноподобных масс, а также костных балок с нарушенной архитектоникой, хаотичным расположением остеоцитов. Зона остеогенеза характеризовалась выраженной базофилией клеток и остеомукоида развивающейся костной ткани. В контрольной группе в эти сроки дефект был заполнен рыхлой соединительной тканью с участками грануляционной и фиброретикулярной ткани и остатками детрита. Отмечена выраженная лейкоцитарная инфильтрация регенерата, гиперемия кровеносных сосудов со стазом форменных элементов крови, периваскулярный отек, сосудистая сеть была слабо выражена.
В экспериментальных группах на 30-е сутки дефект уменьшался в размерах, был заполнен грубоволокнистой фиброзной, костной и хрящевой тканью. Вокруг сосудов вновь образующихся остеонов концентрически наслаивалось межклеточное вещество, формировались костные пластинки. По периферии дефекта, костная ткань была более зрелая, остеонно-балочного строения, расположение остеонов – нерегулярное, гаверсовы каналы различной ширины, полнокровны, периваскулярный отек отсутствовал. В контрольной группе дефект по периферии был заполнен незрелой костной тканью, в центре представлен грубоволокнистой рубцовой и хрящевой тканью. Васкуляризация регенерата и окружающей костной ткани слабая. Надкостница утолщена, инфильтрирована клетками макрофагального ряда.
На 90-е сутки во всех препаратах экспериментальных групп наблюдали признаки, указывающие на полное восстановление целостности костной структуры. Надкостница полностью моделирована, состояла из наружного и внутреннего слоев. Костная ткань различной степени зрелости, пластинчатого строения, расположение остеонов нерегулярное, увеличивалось количество зрелых фиброцитов и остеоцитов. Межуточное вещество становилось оптически более плотным и гомогенным. В группе контроля на 90-е сутки область дефекта определялась по сужению костной ткани в месте операции. Микроскопически в препаратах дефект заполнялся достаточно зрелой костной тканью, местами с прослойками хрящевой ткани. Преобладала плотная костная ткань с малочисленными остеонами, межклеточное вещество менее гомогенное и рыхлое. Клетки представлены в основном зрелыми фибробластами и остеоцитами, не наблюдалось базофилии клеток и межклеточного вещества. Кортикальная пластинка сужена, костная ткань более зрелая, клетки малочисленны, в межбалочных пространствах сосуды синусоидного типа, костно-мозговой канал либо резко сужен, либо закрыт замыкательной пластинкой.
Таким образом, в ходе эксперимента установлено, что при использовании для пластики костного дефекта, осложненного хроническим остеомиелитом, ПГБ купирование воспалительного процесса, реконструкция костных дефектов и восстановление функциональных свойств оперированных конечностей происходило значительно эффективнее, чем в контрольной группе животных (использован материал аллокости). Морфогенез репаративных процессов в экспериментальных полостях бедренных костей кроликов после пластики ПГБ характеризовался восстановлением анатомической и функциональной целостности костей уже к 60 суткам. При замещении костной полости аутотрансплантантом восстановления костной структуры не происходило.
Заключение
Полигидроксибутират и композиты ПГБ с ГАП виде объемных имплантатов обладают остеоиндуктивными свойствами, которые эффективны для восстановления дефектов костной ткани. Пломбировочный материал порошковообразного ПГБ и смеси ПГБ/тиенам пригоден для пластики костных полостей, инфицированных Staphylococcus aureus. Биодеградируемые имплантаты и пломбирочнвый материал на основе ПГБ обладают выраженными остеопластическими свойствами, медленно деградируют in vivo, обеспечивая нормальное протекание репаративного осте-генеза. Результаты позволяют рекомендовать ПГБ в качестве костнопластического материала для восстановления дефектов костной ткани.
Работа выполнена при поддержке Программы Президента РФ для молодых докторов наук (грант №260) и в рамках мега-проекта «Биотехнологии новых биоматериалов» по Постановлению Правительства России № 220 от 9 апреля 2010 года «О мерах по привлечению ведущих ученых в российские образовательные учреждения высшего профессионального образования» (договор № 11.G34.31.0013).
Список литературы Экспериментальное исследование деградируемых биополимеров нового класса для пластики костных дефектов и остеомиелитических полостей
- Шишацкая Е.И. Биосовместимые и функциональные свойства гибридного композита полигидроксибутират/гидроксиапатит//Вестн. трансплантологии и искусственных органов. 2006. № 3. С. 34-38.
- Шишацкая Е.И. и др. Структура и физико-химические свойства гибридного композита полигидроксибутират/гидроксиапатит//Перспективные материалы. 2005. № 1. С. 40-46.
- Шишацкая Е.И. Реакция тканей на имплантацию микрочастиц из резорбируемых полимеров при внутримышечном введении//Бюл. эксперим. биол. и мед. 2007. Т. 144, № 12. С. 635-639.
- Шишацкая Е.И., Камендов И.В., Старосветский С.И., Волова Т.Г. Исследование остеопластических свойств матриксов из резорбируемого полиэфира гидроксимасляной кислоты//Клеточная трансплантология и тканевая инженерия. 2008. Т. 3, № 4. С. 41-47.
- Caffee Н.Н., Hardt N.S., La Torre G. Detection of breast implant rupture with aspiration cytology//Plast. Reconstr. Surg. 1995. Vol. 95, № 7. P. 1145-149.
- Coskun S., Korkusuz F., hasirci v. Hydroxyapatite reinforced poly (3-hydroxybutyrate) and poly-3-hydroxybutyrate-co-3-hydroxyvalerate) based degradable composite bone plate//J. Biomat. Sci. Polymer. 2005. Vol. 16. P. 1485-1502.
- Ersek R.A., Beisang A.A. 3rd Bioplastique: a new textured copolymer microparticle promises permanence in soft-tissue augmentation//Plast. Reconstr. Surg. 1991. Vol. 87, № 4. P. 693-702.
- Greene W.B. et al. Electron probe microanalysis of silicon and the role of the macrophage in proximal (capsule) and distant sites in augmentation mammaplasty patients//Plast. Reconstr. Surg. 995. Vol. 95, № 3. P. 513-519.
- Hodgkinson, D.J. Buckled upper pole breast style 410 implant presenting as a manifestation of capsular contraction//Aesthetic. Plast. Surg. 1999. Vol. 23, № 4. P. 279-281.
- Kaiser W., Zazgornik J. Does silicone induce autoimmune diseases? Review of the literature and case reports//Z. Rheumatol. 1992. Bd. 51, № 1. S. 31-34.
- Miro-Mur F. et al. Medical-grade silicone induces release of proinflammatory cytokines in peripheral blood mononuclear cells without activating T cells//J. Biomed. Mater. Res. B Appl. Biomater. 2009. Vol. 90, № 2. P. 510-520.
- Raso D.S., greene w.B., harley R.A., maize J.C. Silicone deposition in reconstruction scars of women with silicone breast implants//J. Am. Acad. Dermatol. 1996. Vol. 35, № 1. P. 32-36.


